吉非替尼与化疗对晚期非小细胞肺癌患者的治疗效果
金春英
(丹东市中心医院肿瘤内科,辽宁 丹东 118000)
肺癌是临床常见的恶性肿瘤,而肺癌中又以晚期非小细胞肺癌(non-small-cell lung carcinoma,NSCLC)占比最高,其发病机制尚未明确,但多认为与吸烟、环境、既往肺部感染等因素有关[1]。临床治疗晚期NSCLC 以化疗为主,通过化疗能延缓病情进展,并对患者的免疫状态恢复有一定促进作用,然而化疗属于全身性治疗方法,在杀灭肿瘤细胞时会影响机体内其他正常细胞结构及功能,产生较多的不良反应。吉非替尼是用于治疗晚期非小细胞肺癌的分子靶向药物,其有效性、耐受性能较好的抑制肿瘤细胞生长[2]。本研究选取2018 年6 月至2019 年6 月本院收治的晚期非小细胞肺癌40 例作为研究对象,旨在探究吉非替尼与化疗治疗晚期非小细胞肺癌患者的临床疗效,现报道如下。
1 资料与方法
1.1 临床资料 选取2018年6月至2019年6月本院收治的40例晚期非小细胞肺癌患者作为研究对象,按患者就诊顺序奇偶性分为观察组与对照组,每组20例。对照组男11例,女9例;年龄50~76岁,平均(63.04±5.55)岁;疾病分期:Ⅲb期12例,Ⅳ期分别8例;病理类型:鳞癌9例,腺癌7例,腺鳞癌4例。观察组男10例,女10例;年龄50~77岁,平均(63.50±5.98)岁;疾病分期:Ⅲb期11例,Ⅳ期9例;病理类型:鳞癌6例,腺癌9例,腺鳞癌5例。两组临床资料比较差异无统计学意义,具有可比性。本研究已通过本院伦理委员会审核批准。
纳入标准:符合《中国常见恶性肿瘤诊治规范》[3]中非小细胞肺癌的诊断标准,且属于晚期;年龄≥50岁;临床分期为Ⅲb、Ⅳ期;患者预计生存期>3 个月;患者知情同意并签署知情同意书。排除标准:存在肝、肾功能异常者;对本研究药物过敏者;研究中途退出者。
1.2 方法 对照组采用GP(吉西他滨+顺铂)化疗方案治疗。第1、8天,给予患者1 000 mg/m2吉西他滨[齐鲁制药(海南)有限公司,国药准字H20113286]静脉滴注;第1、2、3 天,静脉滴注75 mg/m2顺铂(云南个旧生物药业有限公司,国药准字H53021740),21 d为1个治疗周期,连续治疗3个月。
观察组采用吉非替尼(阿斯利康制药有限公司,国药准字J20140142)口服治疗,每次250 mg,每天1 次,连续治疗3个月(1个疗程)。
1.3 观察指标 比较两组临床疗效、疾病控制率及治疗前、治疗3个月后外周血T淋巴细胞亚群成熟T淋巴细胞(CD3+)、诱导性T细胞/辅助性T细胞(CD4+)、抑制性T细胞/细胞毒性T 细胞(CD8+)与表皮生长因子受体(EGFR)水平,并随访6 个月;比较两组不良反应(骨髓抑制、消化道反应)发生率。
疗效判定标准:以世界卫生组织(WHO)制定的标准评估患者的治疗效果。完全缓解(CR):治疗后,患者肿瘤组织完全消失,≥4周无新病灶产生;部分缓解(PR):治疗后,患者肿瘤组织缩小>50%,≥4周无新病灶产生;稳定(SD):患者肿瘤组织缩小≤50%,或肿瘤组织增加<25%;进展(PD):患者肿瘤增加≥25%,或有新病灶出现[4]。总有效率=CR率+PR率;疾病控制率=CR率+PR率+SD率。
采用流式细胞技术检测患者外周血T 淋巴细胞亚群中CD3+、CD4+、CD8+水平,采用免疫吸附法检测EGFR水平,试剂盒购自上海希美化学有限公司,型号为96T,操作方法参照说明书。
1.4 统计学方法 采用SPSS 20.0统计学软件分析数据,计量资料以“”表示,采用t检验,计数资料以[n(%)]表示,采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效及疾病控制率比较 两组治疗总有效率比较差异无统计学意义;观察组疾病控制率为90.00%,明显高于对照组的60.00%,差异有统计学意义(P<0.05),见表1。

表1 两组临床疗效及疾病控制率比较[n(%)]Table 1 Comparison of clinical efficacy and disease control rate between the two groups[n(%)]
2.2 两组治疗前后外周血T淋巴细胞亚群及EGFR水平比较治疗前,两组CD3+、CD4+、CD8+及EGFR水平比较差异无统计学意义;治疗3个月后,观察组CD3+、CD4+水平均高于对照组,CD8+、EGFR水平均低于对照组(P<0.05),见表2。
表2 两组治疗前后外周血T淋巴细胞亚群及EGFR水平比较()Table 2 Comparison of peripheral blood T lymphocyte subsets and EGFR levels between the two groups before and after treatment()
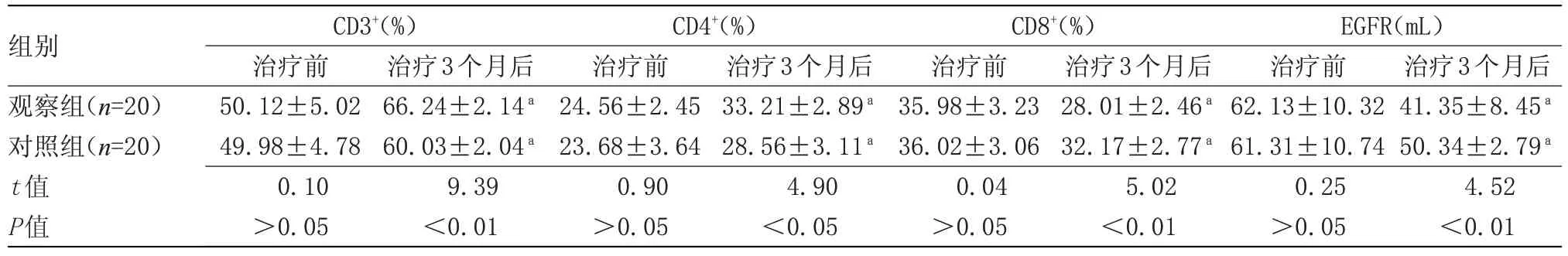
表2 两组治疗前后外周血T淋巴细胞亚群及EGFR水平比较()Table 2 Comparison of peripheral blood T lymphocyte subsets and EGFR levels between the two groups before and after treatment()
注:CD3+,成熟T淋巴细胞;CD4+,诱导性T细胞/辅助性T细胞;CD8+,抑制性T细胞/细胞毒性T细胞;EGFR,表皮生长因子受体。与本组治疗前比较,aP<0.05
组别观察组(n=20)对照组(n=20)t值P值治疗3个月后41.35±8.45a 50.34±2.79a 4.52<0.01 CD3+(%)治疗前50.12±5.02 49.98±4.78 0.10>0.05治疗3个月后66.24±2.14a 60.03±2.04a 9.39<0.01 CD4+(%)治疗前24.56±2.45 23.68±3.64 0.90>0.05治疗3个月后33.21±2.89a 28.56±3.11a 4.90<0.05 CD8+(%)治疗前35.98±3.23 36.02±3.06 0.04>0.05治疗3个月后28.01±2.46a 32.17±2.77a 5.02<0.01 EGFR(mL)治疗前62.13±10.32 61.31±10.74 0.25>0.05
2.3 两组不良反应发生率比较 两组不良反应发生率比较差异无统计学意义,见表3。

表3 两组不良反应发生率比较[n(%)]Table 3 Comparison of the incidence of adverse reactions between the two groups[n(%)]
3 讨论
早期NSCLC患者常有痰血、低热、胸部胀痛等症状表现,晚期则多表现为食欲下降、体质量减轻等,多数患者确诊时已发展至晚期[5]。晚期NSCLC 患者生存率低于早中期,且不宜行手术治疗,因此,临床多采用化疗延缓病情进展,以延长患者生存期[6]。
晚期NSCLC 患者行手术化疗、放疗,均能改善患者的生存质量,提高生存率。虽然化疗是治疗晚期NSCLC患者的常用方法,效果确切,但由于部分患者受疾病影响,机体的免疫力逐渐下降,单纯的化疗用药不仅会影响晚期NSCLC患者正常细胞的生长,还有可能使机体产生耐药性。吉非替尼是选择性的EGFR酪氨酸激酶抑制剂,可通过抑制肿瘤生长、转移及血管的生成促进肿瘤细胞凋亡。吉非替尼进入人体后,可迅速分布于组织内,对肿瘤病灶产生精确药效,且还能对正常的组织起到保护作用[7]。本研究结果显示,两组治疗总有效率比较差异无统计学意义;观察组疾病控制率为90.00%,明显高于对照组的60.00%,差异有统计学意义(P<0.05)。表明吉非替尼与化疗对晚期NSCLC 患者的效果确切。分析原因为,常规化疗属于全身性的治疗,易对体内正常的细胞产生影响,而吉非替尼具有较强的靶向作用,不会破坏正常细胞的生长。
CD3+、CD4+、CD8+均属于T淋巴细胞亚群指标,而T淋巴细胞属于免疫功能细胞,对清除肿瘤具有重要作用,其中CD3+、CD4+、CD8+检测有助于评估药物效果及预后。EGFR广泛分布于哺乳动物的上皮细胞、成纤维血细胞等细胞表面中,该指标在多个实体肿瘤中呈高表达的状态,与肿瘤细胞的增殖、血管生成、转移扩散等密切相关[8]。吉非替尼属于靶向治疗药物,能抑制络氨酸激酶的活性,并阻断肿瘤细胞中的EGFR信号传导,从而降低血管生长因子水平,抑制肿瘤血管生长,使肿瘤细胞凋亡[9]。患者受肿瘤细胞影响程度减轻,其机体免疫力能得到明显改善。本研究结果显示,治疗3个月后,观察组CD3+、CD4+水平均高于对照组,CD8+、EGFR水平均低于对照组(P<0.05)。表明吉非替尼能有效降低EGFR水平,改善患者的免疫功能。
本研究结果还显示,两组不良反应发生率比较差异无统计学意义,与李洋等[10]研究结果一致。表明吉非替尼治疗晚期NSCLC患者的用药安全性较高。
综上所述,吉非替尼与化疗对晚期NSCLC患者均有明显治疗效果,但吉非替尼能更好地改善患者免疫细胞水平,降低EGFR水平,有效控制疾病进展,安全可靠,值得临床推广应用。

