同型半胱氨酸及动态动脉硬化指数对高血压病人早期肾损害的影响
李 露,李 佳,王玉玲,申晓彧
2018年中国高血压防治指南[1]将血清同型半胱氨酸(homocysteine,Hcy)≥15 μmol/L列为预测高血压病人心血管预后的一项重要指标。Hcy增高会使血管疾病风险增加,也使大动脉的僵硬度增加,而动态动脉硬化指数(ambulatory arterial stiffness index,AASI)可作为反映全身血管僵硬度的指标。长期高血压引起肾血管受损,最终导致肾小动脉硬化,阻力增加,灌注降低,激活肾素-血管紧张素-醛固酮系统(RAAS),引发炎症反应,而肾脏又是Hcy的主要代谢场所,相互作用导致肾脏损害。同时Hcy也可导致内皮细胞功能受损,脂质沉积加速,促进动脉粥样硬化[2]。研究指出,血清胱抑素C (Cys-C)、血β2微球蛋白(β2-MG)能更灵敏地诊断早期肾损害[3],且β2-MG比肌酐、尿蛋白能更好地反映早期肾损害[4-5]。本研究探讨Hcy和AASI与早期肾损害的关系,以便及时预测高血压病人早期可能出现的靶器官损害,为临床诊断及治疗提供依据。
1 资料与方法
1.1 研究对象 入选原发性高血压病人120例作为试验组,同时收集30名同期体检健康人群作为对照组,年龄、性别等与试验组相匹配。
1.2 入选标准 ①既往未服用降压药,测量3次非同日血压收缩压均≥140 mmHg(1 mmHg=0.133 kPa)和(或)舒张压均≥90 mmHg;②血Hcy≤30 μmol/L,近半年无叶酸和维生素B12类药物服用史;③病史<5年。
1.3 排除标准 肾脏病变、心血管病变、内分泌相关疾病、脑部疾病、妊娠、药物等引起的继发性高血压病人。
1.4 分组 将120例原发性高血压病人依据Hcy水平分为4组,第1组:血Hcy为10.0~14.9 μmol/L,第2组血Hcy为15.0~19.9 μmol/L,第3组:血Hcy为20.0~24.9 μmol/L,第4组:血Hcy为25.0~30.0 μmol/L。另选取同期健康体检人群30名为对照组。
1.5 研究方法
1.5.1 收集相关病史及检查数据 采集入组病人及健康人群一般资料、相关病史,检测指标包括血清Hcy、总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、空腹血糖(FPG)、血清Cys-C、血清β2-MG等。
1.5.2 测量24 h动态血压 选择24 h动态血压监测仪,记录入选者24 h血压,测量期间嘱观察者正常活动,测量时尽可能取平卧位休息5 min,选取有效值达到80%以上的数据作为有效数据,舍弃无效数据(收缩压>260 mmHg或<70 mmHg;舒张压>150 mmHg,或<40 mmHg;脉压>90 mmHg,或<20 mmHg)。以收缩压和舒张压分别为自变量和因变量进行统计回归分析得一条回归直线,将直线斜率定义为β,AASI则可用1-β表示。
1.5.3 生化指标检查 嘱被测者前一日22:00后不进食,次日06:00抽取空腹静脉血检测,记录血清Hcy、TG、TC、LDL-C、HDL-C、FPG及血清Cys-C、β2-MG水平。
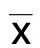
2 结 果
2.1 各组临床资料比较 各组性别比较差异无统计学意义(P>0.05),单因素方差分析显示FPG、TG、TC、LDL-C、HDL-C在各组间比较差异无统计学意义(P>0.05);年龄、收缩压、舒服张、平均动脉压(MAP)在各组间比较差异均有统计学意义(P<0.05)。详见表1。

表1 各组临床资料比较
2.2 各组病人AASI、Hcy、血清Cys-C、血β2-MG水平比较 采用LSD法对各组AASI、Hcy、血清Cys-C、血β2-MG进行两两比较,结果显示,第4组高于对照组、第1组、第2组和第3组,差异均有统计学意义(P<0.05);第3组高于对照组、第1组、第2组,差异均有统计学意义(P<0.05);第2组高于对照组、第1组,差异均有统计学意义(P<0.05);第1组高于对照组差异有统计学意义(P<0.05)。详见表2。
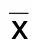
表2 各组间AASI、Hcy、血清Cys-C、血β2-MG水平比较 (±s)
2.3 AASI、血Hcy、血清Cys-C、血β2-MG相关性分析 Pearson相关性分析结果显示,AASI与血Hcy、AASI与血清Cys-C、AASI与血清β2-MG、血Hcy与血清Cys-C、血Hcy与血β2-MG之间均存在明显正相关(P<0.05)。详见表3。

表3 AASI、血Hcy、血清Cys-C、血β2-MG相关性分析
2.4 影响血清Cys-C、β2-MG的因素分析 多元逐步回归分析结果显示:β2-MG水平与Hcy含量、MAP呈线性关联;Cys-C水平与Hcy含量、MAP呈线性关联。详见表4。

表4 影响血清 Cys-C、β2-MG的因素分析
3 讨 论
高血压是动脉粥样硬化的重要危险因素,有研究表明,高血压病人的动脉结构和功能变化与血管内压力增高所致内皮功能异常有关[6-7]。而血流动力学改变是造成血管内皮损伤的初始因素。有学者研究了高血压病人的内壁剪切应力,结果显示低剪切应力可诱发动脉粥样硬化,高血压病人正是由此导致动脉的结构和功能较易发生改变[8]。血压持续处于较高水平,血管壁长期受压力刺激,血管内皮细胞损伤,炎症介质释放,血小板黏附聚集;缩血管因子与舒血管因子合成和释放失衡,长此以来导致血管管壁硬化。同时有研究指出血管钙化及脂质代谢紊乱会加速动脉硬化,尤其是在肾功能损害病人中更明显[9-11]。血管钙化与氧化应激和内质网应激有关,这两种应激反应促进NADPH氧化酶活性及过氧化氢水平升高,上调Runx2表达,促进血管钙化,影响肾脏血供[12-14],导致肾脏损害,参与脂质代谢的多种酶活性减低,引起TG和HDL-C的代谢紊乱[15],最终导致血管硬化。近年来,许多学者进行了关于Hcy对于心脑血管疾病影响的研究。大量研究显示,Hcy可导致动脉粥样硬化(AS),被认为是AS的独立危险因素[7]。抗氧化对氧酶1(PON1)活性、血浆Hcy和氧化低密度脂蛋白(ox-LDL)水平在试验组有明显变化,证明了AS进展加速与Hcy促进LDL-C和胆固醇氧化有关。随着研究的进展,又发现Hcy与肾损害有关。王宏伟等[16]收集了208例病人,抽取静脉血化验对比分析得到冠心病病人的血清Hcy水平与对照组相比明显偏高。有研究显示,Hcy为多种肾脏疾病独立危险因素[17]。有学者进行流行病学研究显示,慢性肾脏病的发展与Hcy水平呈正相关[18]。近期有研究显示,肾功能衰竭病人AS进展与Hcy水平升高有一定关系,更好地解释了Hcy与动脉粥样硬化及肾功能损害的关系。为了更好地研究三者之间的关系,近年来对早期肾损害的临床监测,以Cys-C、β2-MG用来评估肾功能。Betul等[19]比较了51例原发性高血压病人和29名健康受试者的血清CysC、β2-MG、肌酐、尿酸、尿素氮、白蛋白水平及24 h尿蛋白、白蛋白和肌酐水平,得出Cys-C、β2-MG对于评估早期肾损害更具优势。
综上所述,长期高血压状态会造成血管内皮受损,激活炎症反应,导致AS,而AS又与Hcy水平有一定关联,体内高水平Hcy会加速AS的进展速度,引起冠心病,肾脏作为人体重要器官,极易受到损害,若高血压病人同时合并血Hcy水平增高会加速肾脏损伤。

