新型冠状病毒肺炎康复者恢复期血浆采集和质量特征
李策生 ,谢勇 ,杨汇川 ,余鼎 ,侯继锋 ,袁明超 ,周东波 ,杜涛 ,吴晓 ,王丹 ,胡勇,喻剑虹,邓琨,王月,龚钦,周志军,彭焱,林连珍,韩韧,邢延涛,梁小龙,毛敏,梅宇,李陶敬,张勇,梁洪,董德梅,何彦林 ,,付道兴 ,杨晓明
1.国药集团武汉血液制品有限公司,湖北武汉430207;2.北京天坛生物制品股份有限公司,北京100024;3.中国生物技术股份有限公司,北京100029;4.中国食品药品检定研究院,北京102629;5.武汉血液中心,湖北武汉430030
世界卫生组织(WHO)官网(https://covid19.who.int /)统计数据显示,截至 2021 年 5 月 31 日,在世界范围内新型冠状病毒肺炎(Coronavirus Disease 2019,COVID-19)累计确诊170 051 718 例,累计死亡3 540 437 例。在2020 年疫情暴发之初,尚无有效治疗药物,康复者血浆治疗作为一种经验疗法,至今已有 130 年的历史,曾在 2003 年“非典”、2009 年甲型H1N1 流感、埃博拉病毒(Ebola virus,EBV)感染、中东呼吸综合征(Middle East respiratory syndrome,MERS)等疫情或重大传染病中作为经验疗法使用,有效治疗了重症患者[1-7]。但并未大规模使用,究其原因与血浆采集技术有一定的关系。单采浆技术使用一次性无菌密闭的单采血浆耗材,严格按照规程无菌操作,采集的血液经离心分离红细胞等有形成分还输至献浆员体内。但此种采集技术目前在我国主要在各血液制品生产企业下属的浆站规模使用,采集的血浆只对口供应国内血液制品企业。我国中心城市暂未规模化常规开展单采血浆工作。COVID-19 疫情暴发后,如何采集足够的康复者恢复期血浆用于COVID-19 患者的救治,成为一道难题。为了挽救患者生命,中国生物技术股份有限公司(简称中国生物)及其下属国药集团武汉血液制品有限公司等依托自身技术优势,于2020 年1 月即开始了康复者血浆采集计划预案的制定,获得政策许可后,迅速在全国18 个省设置了52 个血浆采集点,开展COVID-19 康复者恢复期血浆采集工作,并将采集的COVID-19 康复者恢复期血浆进行亚甲蓝病毒灭活,检测合格后用于临床救治,累计使近千人获益。目前我国关于COVID-19 康复者恢复期血浆的规模采集和病毒灭活血浆的质量特征鲜有报道。本文对截至2020 年3 月26 日中国生物在湖北省采集的COVID-19 康复者恢复期血浆捐献者基本情况及血浆的质量特征进行初步汇总和分析,现报道如下。
1 材料与方法
1.1 主要试剂及仪器 新型冠状病毒2019-nCoV核酸检测试剂盒、单管多重呼吸道病原体检测试剂盒和GNcycler-96s 多重病原微生物核酸检测仪均购自上海捷诺生物科技有限公司;新型冠状病毒IgG 抗体检测试剂盒购自武汉科源安博生物技术有限公司;HBsAg、HCV 抗体、HIV-1 / HIV-2 抗体检测试剂盒及HBV、HCV、HIV-1 核酸检测系统均购自北京万泰生物药业股份有限公司;梅毒螺旋体抗体诊断试剂盒购自上海科华生物工程股份有限公司;丙氨酸氨基转移酶检测试剂盒购自上海永华细胞和基因高技术有限公司及北京端瑞科技有限公司;抗A 抗B血型定型试剂(单克隆抗体)购自长春博德生物技术有限责任公司;抗D(IgM + IgG)血型定型试剂(单克隆抗体)购自宜美康生物制品有限公司;无菌检查用培养基购自北京三药科技有限公司;血液成分单采浆机分别购自重庆三大伟业制药有限公司(FLY / XJ-1和FLY / XJ-2)、四川南格尔生物医学股份有限公司(NGL-XJC 2000)和上海达华医疗器械有限公司(DHJ-1);医用血浆病毒灭活柜(ZBK-YBM-02)及一次性使用病毒灭活装置配套用亚甲蓝病毒灭活专用耗材(ZBKMB01)购自山东中保康医疗器具公司;GZR-IIA 高频热合机购自苏州市医用仪器厂;酶标仪购自美国MD 公司(SpectraMax Plus384);固相萃取系统购自美国Thermo 公司;GN-96S PCR 仪购自上海宏石医疗科技有限公司;UV-2550 紫外可见分光光度计购自日本岛津公司。
1.2 COVID-19 康复者恢复期血浆的采集及质量分析 登记捐献者基本信息,采用血液分离单采浆技术采集COVID-19 康复者恢复期血浆。制定血浆采集标准及抗重症急性呼吸综合征冠状病毒2(severe acute respiratory symptom coronavirus 2,SARS-CoV-2)灭活血浆质量标准,对亚甲蓝灭活前血浆进行外观、病毒标志物等检测;灭活后血浆进行外观、SARS-CoV-2抗体、SARS-CoV-2 核酸、亚甲蓝残留等检测,并分析检测结果。对捐献者采集过程和采集后随访发生的与单采浆相关不良事件进行记录,分析单采浆技术的安全性。统计在湖北省各地市州采集血浆情况,以血浆采集份数比地区确诊人数计算血浆采集率。
采集率(%)= 采集份数 / 确诊例数 × 100%
1.2.1 血浆捐献者入选标准 捐献者应为符合《新型冠状病毒肺炎诊疗方案》最新版中解除隔离和出院标准的COVID-19 康复者。年龄应不小于18周岁,不大于55 周岁,无经血传播疾病史,经临床医师评估符合献血标准者。两次采浆间隔期不少于14 d。
1.2.2 血浆采集 按照《血站技术操作规程(2019版)》要求,对捐献者进行知情告知捐献血浆的利弊,可能存在的风险。对捐献者进行医学检查。采用血液成分单采浆机采集200 ~400 mL / 次,具体采集量由捐献者意愿和临床医师评估确定。同时留取全血,通过正定法进行ABO / RhD 血型检测,血浆样品用于病原学和理化指标的检测。
1.2.3 抗SARS-CoV-2 灭活血浆的制备 COVID-19康复者恢复期血浆经亚甲蓝病毒灭活后,制备为抗SARS-CoV-2 灭活血浆,分装成 50、75、100 mL / 袋等规格。-20 ℃及以下贮存,-15 ℃及以下冰冻状态运输,如短期保存(24 h 内),则保存于 2 ~ 8 ℃。
1.2.4 抗SARS-CoV-2 灭活血浆的关键质量控制 参照国家标准[8]中全血及成分血质量要求,对灭活血浆进行亚甲蓝残留、2019-nCoV 核酸(RT-PCR 法)、乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)、艾滋病病毒(HIV)标志物(酶联免疫法与核酸检测法)、梅毒螺旋体(Treponema pallidum,TP)标志物(酶联免疫法)和抗2019-nCoV(RBD-IgG)抗体等检测。
2 结 果
2.1 单采浆技术的安全性 截至2020 年3 月26 日,中国生物在湖北省累计采集COVID-19 康复者恢复期血浆933 份,其中在武汉市累计采集462 份,在地市州累计采集471 份。采集过程顺利,未发生血浆采集相关严重不良事件。捐献者捐献血浆日期距离出院日期平均为18 d。采集后对捐献者进行至少1次回访,均未报道血浆采集相关严重不良事件。
2.2 湖北省地市州COVID-19 康复者恢复期血浆捐献区域分布 湖北省除武汉外14 个地市州,COVID-19 康复者恢复期血浆采集量前3 位依次为宜昌、十堰、襄阳,采集率前3 位分别为十堰、宜昌、襄阳。各地市州采集份数之和与武汉市采集份数相当。见图1 和图2。
2.3 COVID-19 康复者恢复期血浆捐献年龄和血型分布 捐献者平均年龄38 岁(n = 933),年龄分布见图3。
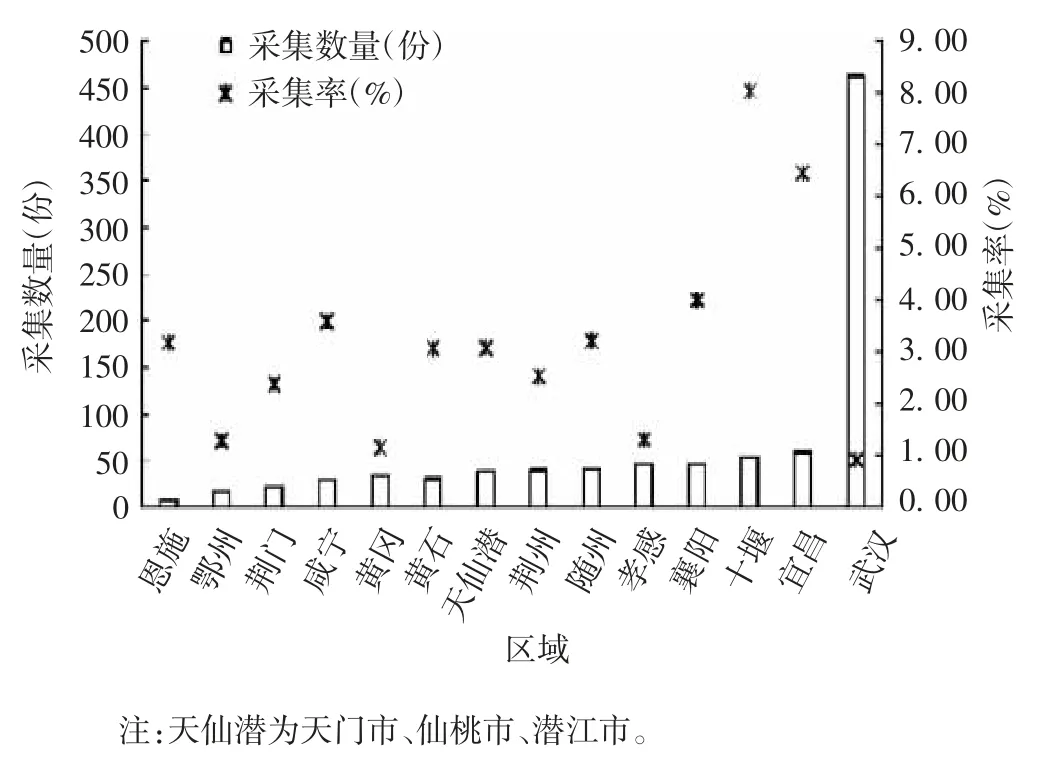
图1 湖北省各市COVID-19 康复者恢复期血浆采集量和采集率Fig.1 Quantity and rate of COVID-19 CP collection in cities of Hubei Province
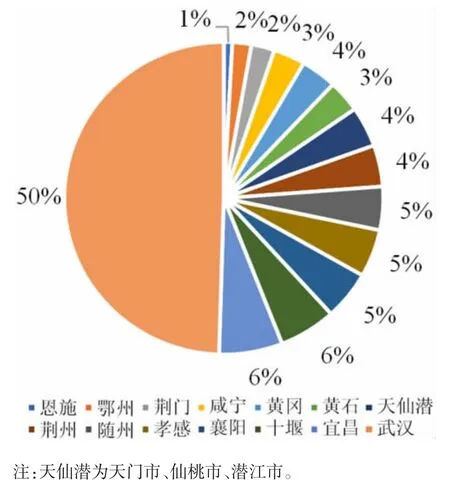
图2 湖北省各区域采集量比例Fig.2 Percentages of COVID-19 CP collected from various regions of Hubei Province
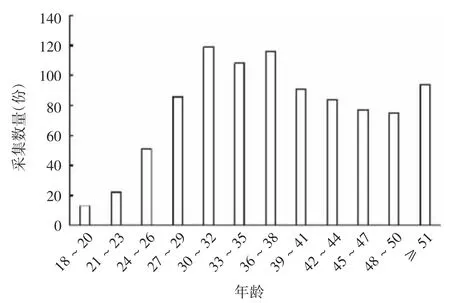
图3 COVID-19 康复者恢复期血浆捐献者年龄分布Fig.3 Age distribution of COVID-19 CP donors
2.4 抗SARS-CoV-2 灭活血浆ABO 血型结果 血型Rh 阳性:A、B、AB、O 型占比分别为 33.4%、29.2%、10%和27.2%;Rh 阴性:累计采集到Rh 阴性B 型血 1 份。
2.5 抗SARS-CoV-2 灭活血浆的关键质量指标
2.5.1 核酸 收集的933 份COVID-19 康复者恢复期血浆SARS-CoV-2 核酸检测结果均为阴性。
2.5.2 抗体 抗体效价低于1 ∶160 的占7.40%,其中SARS-CoV-2 抗体阴性血浆比例为5.04%,见表1。

表1 康复者血浆中抗SARS-CoV-2 抗体水平分布Tab.1 Distribution of antibody level against SARS-CoV-2 in COVID-19 CP
2.5.3 亚甲蓝残留 每份康复者血浆经亚甲蓝病毒灭活后,亚甲蓝残留为 0.03 ~ 0.04 μmol / L,远低于 0.3 μmol / L,符合要求。
2.5.4 经血传播感染性病原标志物 检测结果显示,累计23 份采集的康复者血浆病原标志物不合格,见表2。检测合格的血浆才可放行,以保证产品的安全性。

表2 病原标志物检测结果Tab.2 Detection result of virus markers
3 讨 论
由中国生物采集的933 份COVID-19 康复者恢复期血浆采集过程顺利,未发生严重不良事件。对每位献浆员进行至少1 次回访,目前未报道采血相关严重不良事件。表明单采浆技术安全可靠,未对人体产生不良影响。
武汉市累计确诊逾5 万人,但本研究中来自武汉市COVID-19 康复者恢复期血浆仅462 份。以血浆采集人次与地区确诊人数计算血浆采集率,武汉市低于湖北省的各地市州区域,分析原因主要与疫情期间武汉市居民自觉居家隔离,社区通行和道路通行受限等因素有关,导致武汉市采集率不高,但在武汉市采集的康复者血浆采集绝对数最高。本研究只统计了由中国生物采集的COVID-19 康复者恢复期血浆,由中国生物之外采集的血浆未纳入本研究统计,因此与其他来源报道数据可能有差异。
本研究中COVID-19 康复者恢复期血浆捐献者平均年龄为38 岁,由于捐献血浆有年龄限制,能够在出院两周后捐献血浆者多为轻型和普通型患者,身体一般状态良好,因此在此年龄段的人员数量最多,少有导致COVID-19 恶化风险的基础疾病,如糖尿病[9],与老年人相比,年轻人患 COVID-19 后有更高的生存率[10],身体状况更适合捐献血浆。
有文献报道,COVID-19 患者A 型血比例高于正常比例,A 型普遍易感,武汉市3 694 名正常人A、B、AB 和 O 型血分布分别为 32.16%、24.90%、9.10%和33.84%,武汉金银潭医院1 775 名COVID-19 患者 A、B、AB 和 O 型血分布分别为 37.75%、26.42%、10.03%和25.80%,COVID-19 患者中A 型血的比例显著高于正常人群(P <0.001)[11]。本研究收集COVID-19 康复者恢复期血浆 A 型、B、AB、O 型血占比分别为33.4%、29.2%、10%和27.2%,患病血型比例与捐献血浆比例不等同,可能与疾病严重程度、年龄、区域分布、宣传力度、捐献血浆便利程度等有关。本研究中累计仅采集到Rh 阴性B 型血COVID-19 康复者恢复期血浆1 份,主要原因为Rh 阴性血型稀缺所致。
采集的933 份COVID-19 康复者恢复期血浆SARS-CoV-2 核酸检测均为阴性,以其为原料经亚甲蓝光照灭活制备的抗SARS-CoV-2 灭活血浆亚甲蓝残留检测结果显示,均明显低于0.3 μmol / L,符合要求,亚甲蓝病毒灭活步骤使得安全性进一步得到保证。亚甲蓝光照灭活病毒的原理是血浆的亚甲蓝表面携带正电荷,与病毒核酸结合后可嵌入DNA/RNA中,与病毒核酸带负电荷的G-C 碱基对相结合。在有光照的条件下,亚甲蓝分子吸收光能后可激发产生单态分子氧,单态分子氧通过修饰鸟嘌呤碱基而影响核酸,使其产生缺口,引起核酸链的断裂或导致碱基位点丢失,从而达到灭活病毒的目的。大量数据表明,亚甲蓝光化学法能高效灭活血浆中的脂包膜病毒。亚甲蓝对冠状病毒的灭活效果明显[12]。
抗SARS-CoV-2 灭活血浆抗体阴性率为5.04%,阴性及滴度小于1 ∶80 合计占比7.40%。抗体水平可能与机体状态有关,症状轻微的年轻人和老年患者产生的抗体滴度是否低于青年人,抗体随时间的变化,以及抗体产生后能否保护机体免于再次感染[13],尚有待研究。
COVID-19 疫情暴发后,中国生物积极响应,率先提出康复者恢复期血浆疗法。并借助公司技术和资源优势,按照《单采血浆站技术操作规程(2011版)》和《血站技术操作规程2019 版》相关要求,调集人员和单采浆机等设备,在全国18 个省市自治区共设置52 个血浆捐献点,采用血液成分单采浆机进行康复者恢复期血浆采集,截至2020 年03 月26 日,全国共采集血浆1 000 余人次,其中武汉市采集的462人次血浆经亚甲蓝病毒灭活,并进行各种病原学等检测。检测合格的血浆用于临床救治,任一项目检测不合格的血浆均未用于临床,进一步保障了抗SARSCoV-2 灭活血浆在临床COVID-19 患者救治中使用的安全性。采集或制备的COVID-19 康复者恢复期血浆进行临床救治至今,尚无病毒安全性事件报道,不仅在本次疫情期间对于患者救治具有重大意义,更对今后可能面临的突发疫情防控措施的制定及疫情应对提供了经验。
COVID-19 疫情期间,COVID-19 康复者恢复期血浆和血液制品在疫情防控中发挥了重要作用,康复者恢复期血浆及静注人免疫球蛋白被列入COVID-19 重型、危重型及儿童 COVID-19 患者治疗方案[14]。中国生物在此次COVID-19 疫情期间,倡导康复者恢复期血浆采集生产的抗SARS-CoV-2 灭活血浆用于临床救治、临床研究和静注COVID-19 人免疫球蛋白的研发,累计使上千人获益。国外采用COVID-19康复者恢复期血浆也开展了多项临床研究[15-21]。由此可见,血液制品与疫苗一样,其供应直接关系到人民健康和国家安全。
疫情期间收到捐献血浆近万次咨询,成功捐献血浆比例在10% ~15%。民众对采集血浆的知识了解程度是影响是否捐献血浆决定的相关因素。疫情初期,医务工作者献浆比例较高,由于职业原因,医务工作者对于血浆的认识以及捐献血浆的知识了解和认可程度高于普通人群,提示对于血浆捐献的宣传政策和知识普及程度将影响捐献血浆的预期。来访咨询中,超过献浆年龄人员和疾病恢复期人员均有强烈的捐献血浆诉求。身体暂时不适合献浆的人员,在其身体状况恢复后,近3 / 4 再次联系,最终实现了捐献血浆。
在欧美,捐献血浆已成为一种生活方式。我国有规模庞大的潜在献浆员人群,提升普通群众对捐献血浆的意识,创造捐献血浆的条件,我国的血浆采集量可以预见会有显著提升。期望有积极的政策引导,合适的宣传方式让国人参与到献浆队伍中。
综上所述,单采血浆技术安全,在此次疫情中发挥了重要作用,采集的COVID-19 康复者恢复期血浆具有较高的抗体滴度,SARS-CoV-2 核酸检测结果为阴性,经病原学检测,合格的血浆用于临床救治。亚甲蓝灭活后,亚甲蓝残留均远低于0.3 μmol / L,符合要求。城市人群有捐献血浆需求,因此我们呼吁在中心城市建立规模化单采血浆技术平台及应急血浆采集制度,进行康复者血浆储备,增设浆站,发展血浆采集事业,开发血液制品,实现我国血浆和血液制品自给自足。

