阿柏西普联合玻璃体切除术治疗增殖型糖尿病视网膜病变临床观察
王智勇,王洪亚,马胜男,蔡永芹,周玮琰,刘丽萍1,
1山东大学附属省立医院,济南 250021;2德州市市立医院;3山东省第二人民医院(山东省耳鼻喉医院);4山东第一医科大学附属省立医院
增殖型糖尿病视网膜病变(PDR)是糖尿病最严重的眼科并发症,可引起患者视功能异常[1]。目前主要通过玻璃体切除术来去除PDR患者眼内的增殖膜及新生血管,但术中纤维血管膜引起的出血会导致手术难度增加,导致手术失败,并提高并发症发生率[2]。术前给予眼内注射抗血管内皮生长因子(VEGF)药物可降低PDR手术失败率及并发症发生率。阿柏西普眼内注射溶液是2018年被我国批准上市的一种抗VEGF药物,是一种重组融合蛋白。VEGF和促红细胞生成素(EPO)是已知的在PDR发生发展中起重要作用的促新生血管因子。对VEGF、EPO进行监测,可了解PDR患者视网膜血管内皮细胞增殖及新生血管的发展变化,这对患者病情进展和手术预后评估有重要价值。本研究用玻璃体腔注射阿柏西普来联合玻璃体切除术治疗PDR,并观察其治疗效果。
1 资料与方法
1.1 临床资料 选择2018年10月—2020年3月山东大学附属省立医院收治的PDR患者59例,随机分为观察组30例、对照组29组。观察组男14例、女16例,年龄(58±2)岁,DR分期:Ⅳ期16例、Ⅴ期10例、Ⅵ期4例,病程(15.40±0.98)年,空腹血糖(10.08±0.58)mmol/L,糖化血红蛋白(8.47±0.33)mmol/L;对照组男16例、女13例,年龄(55±2)岁,DR分期:Ⅳ期18例、Ⅴ期5例、Ⅵ期6例,病程(15.10±1.22)年,空腹血糖(8.54±0.56)mmol/L,糖化血红蛋白(9.00±0.34)mmol/L。两组上述资料比较差异均无统计学意义。根据PDR国际临床诊断标准筛选患者[3]。纳入标准:年龄>18岁、2型糖尿病、自愿参与研究、可进行定期随访;诊断明确同时有手术指征;手术当日空腹血糖≤8 mmol/L;无全身其他疾病。排除标准:1型糖尿病;有外伤史以及内眼手术史,有其他各类视网膜疾病;血糖控制不佳。本研究经山东大学附属省立医院医学伦理委员会批准;患者均签署知情同意书。
1.2 治疗方法 两组均行玻璃体切除手术治疗,行球后利多卡因麻醉后25 G玻璃体切除手术,手术开始先抽取玻璃体液0.5 mL后再打开内眼灌注,取出的玻璃体液离心后放-80℃冰箱保存。另外,观察组于术前3~5 d给予玻璃体腔注射阿柏西普。玻璃体腔注药术操作方法:注药术前3 d及术后1周给予可乐必妥眼液点术眼每日4次,每次1~2滴,预防感染。铺消毒铺巾,用爱尔凯因眼液表面麻醉患者眼球3次,自角巩膜缘后4 mm向玻璃体腔内注射阿柏西普(Bayer公司,德国)0.05 mL,按压注射部位30~60 s,观察有无出血、针孔渗漏等。
1.3 观察指标及方法
1.3.1 玻璃体腔内VEGF、EPO检测 采用ELISA实验。按照试剂盒说明书将标准品按照不同浓度配置好后加入孔中,样品孔中加入待测样本玻璃体。加入一抗、孵育、洗涤,再加入底物试剂A、B,于37℃恒温培养箱中孵育15 min,加入终止液。孵育10 min之内采用ELX808酶标仪测定各孔450 nm处光密度值,绘制标准曲线,计算样品浓度。
1.3.2 黄斑中心凹厚度(CMT)、最佳矫正视力(BCVA)检测 分别于术前及术后1周、1月,采用光学相干断层成像(OCT)检测黄斑中心凹厚度(CMT),采用ETDRS视力表检查最佳矫正视力(BCVA)。
1.3.3 手术并发症 采用裂隙灯显微镜、间接眼底镜、眼底照相、B超、眼压计等检测观察术后1个月医源性裂孔、玻璃体积血(二次出血)、前房积血(二次出血)及眼压升高(>25 mmHg)等并发症的发生情况。
1.4 统计学方法 采用SPSS22.0统计软件。符合正态分布计量资料用±s表示,比较采用t检验;计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组玻璃体腔内VEGF、EPO水平比较 观察组玻璃体腔内VEGF、EPO水平分别为(561.32±4.43)pg/mL、(463.18±55.17)U/L;对照组玻璃体腔内VEGF、EPO水平分别为(777.00±6.10)pg/mL、(717.06±90.05)U/L。与对照组比较,观察组玻璃体腔内VEGF、EPO水平低(P均<0.05)。
2.2 两组手术前后CMT、BCVA比较 术前,两组CMT、BCVA比较差异无统计学意义。术后1周、1月,两组CMT、BCVA低于术前,且观察组CMT、BCVA低于对照组(P均<0.05)。见表1。
2.3 两组并发症发生情况比较 观察组发生医源性裂孔1例、玻璃体积血1例、前房积血2例、眼压升高2例,并发症发生率为20%;对照组医源性裂孔3例、玻璃体积血2例、前房积血3例、眼压升高5例,并发症发生率为44%。观察组并发症发生率低于对照组(P<0.05)。
3 讨论
糖尿病视网膜病变作为一种严重的致盲性疾病,发病率越来越高,PDR作为糖尿病最严重的眼部并发症。研究表明,视网膜血管内皮细胞异常增生增殖和新血管的形成是PDR主要临床病理表现[4],同时伴随着新生血管的不断生长,最终形成纤维增殖膜牵拉视网膜,导致牵拉性或孔源性视网膜脱离[5],严重影响患者生存质量[6]。因此,找寻一种安全、行之有效的治疗方案有重要意义。
表1 两组手术前后CMT、BCVA比较(±s)
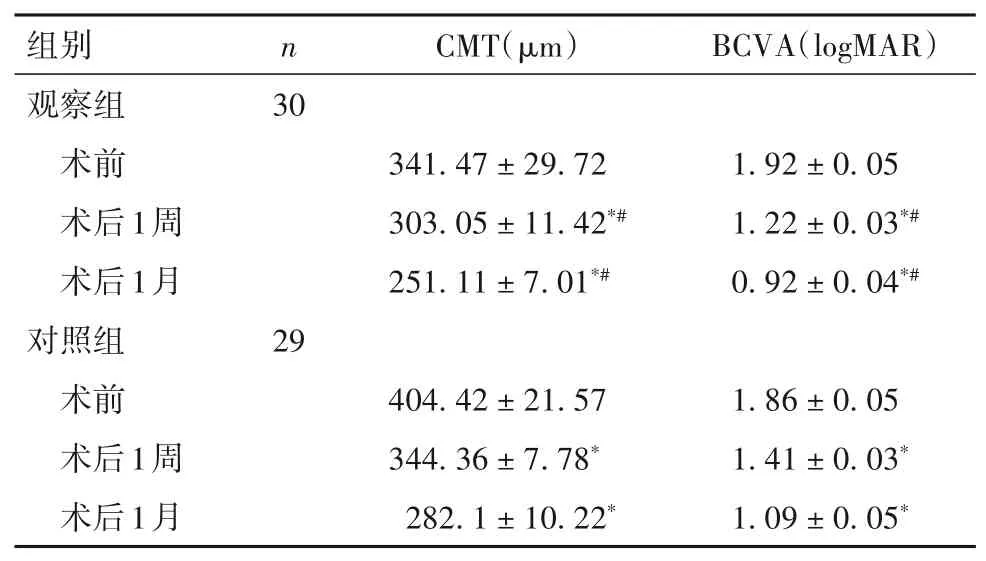
表1 两组手术前后CMT、BCVA比较(±s)
注:与本组术前相比,*P<0.05;与对照组同时点相比,#P<0.05。
?
目前临床主要通过玻璃体切除术去除PDR患者眼内的新生血管以及纤维增殖膜,来治疗脱离的视网膜[7]。但手术过程中眼内的新生血管膜易再次破裂导致出血,不仅影响术野,增加了手术难度及操作时间,同时还易引发术后玻璃体及前房的再次出血、孔源性视网膜脱离、眼压增高等相关并发症,从而影响手术效果。
VEGF作为目前已知的最重要的血管生成因子,在新生血管的病理生理形成过程中及PDR疾病的发生发展中起重要作用[8]。目前抗VEGF药物被广泛应用于PDR患者的玻璃体切除术前,以提高玻璃体切除手术的治疗效果[9],同时可减轻患者黄斑水肿,减少术中出血[10]。而EPO是一种糖蛋白细胞因子,缺氧可以刺激及促进其分泌。EPO在人视网膜组织中可以检测到。研究表明,EPO是一种能独立作用的促进新生血管形成的相关因子[11],PDR患者的眼内及体内EPO水平明显高于正常人群;同时发现玻璃体和血浆中EPO与PDR发生发展相关性也高于VEGF[12]。这些研究都表明玻璃体及体内EPO水平增加可能是PDR发生发展的原因。因此多数学者认为,在PDR发生发展中VEGF与EPO起重要作用[13]。
阿柏西普是一种是由人免疫球蛋白G1的Fc段与血管内皮生长因子受体胞外结构域相结合的一种重组融合蛋白,作为一种新颖的抗VEGF治疗药物,可与VEGF-A、VEGF-B以及胎盘生长因子(PIGF)紧密结合,从而产生足够的抗VEGF作用,达到消退新生血管,减少视网膜血管的渗漏以及抑制黄斑水肿的作用[14-15]。大量文献报道,在PDR的发生发展中VEGF和EPO联合起着重要作用,但是眼内注射阿柏西普后玻璃体腔内的VEGF和EPO因子的表达变化情况,目前尚未有相关的文献报道。
本研究中对照组行常规玻璃体切除术,观察组另外于术前3~5 d行玻璃体腔内注射阿柏西普[16]。结果显示,观察组玻璃体腔内VEGF、EPO水平较对照组低。可见,阿柏西普可降低玻璃体腔VEGF、EPO水平,从而抑制新生血管的形成。同时本研究发现,术后1周、1月两组CMT、BCVA均低于术前,且观察组CMT、BCVA低于对照组。观察组并发症发生率低于对照组,这与王萍等[17]的报道结果一致。这表明,阿柏西普联合玻璃体切除术能有效改善PDR患者CMT、BCVA,减少并发症的发生。这可能由于术前玻璃体内注射阿柏西普能有效抑制患者VEGF、EPO等血管生成因子的分泌,抑制血管新生,使视网膜新生血管不同程度的萎缩或消退,降低了术中清除玻璃体积血及剥除玻璃体视网膜增殖膜的难度,降低手术损伤风险。
综上所述,术前玻璃体腔注射阿柏西普并辅助玻璃体切割术治疗PDR能够显著降低患者玻璃体腔内VEGF、EPO水平,减轻黄斑水肿,提高患者术后视力,降低并发症发生率,是一种安全有效的治疗方案。

