早产儿早期低血糖的发生率及危险因素研究
赵艾菊,蔡莉君
(1.崇左市复退军人医院 儿科,广西 南宁530219;2.广西壮族自治区江滨医院 儿科,广西 南宁530021)
新生儿低血糖症是指新生儿的血糖低于所需要的血糖浓度。常发生于早产儿、小胎龄儿(small gestational age,SGA)、母亲糖尿病等疾病中。新生儿低血糖病因复杂,症状缺乏特异性,且大多数无症状,若未及时发现和妥善处理,将造成脑组织不可逆的损伤和智力低下[1]。研究发现足月儿血糖小于2.6 mmol/L时,临床上虽无症状却可引起神经系统不可逆性损伤[2]。
新生儿低血糖可以是一个独立的疾病,也可能是其他疾病的一个临床表现[3]。定义新生儿低血糖症仍具有挑战性,因为即使在非常低的葡萄糖浓度下,新生儿也可能保持无症状,另一方面,即使是轻微的低血糖症也可能出现症状。我国低血糖的诊断标准是血糖水平小于2.2 mmol/L[4]。
5%的健康婴儿会出现低血糖,早产儿的低血糖发生率更高[2]。胎儿直到妊娠36周后才开始缓慢地持续增加糖原,27周后才开始积累糖原,到分娩前糖原快速积累达到50 mg/g[5]。出生后,在足月婴儿出生后的前12 h内,血糖浓度降至最低3-3.3 mmol/L[6]。足月婴儿利用储存的糖原实现自给自足的稳态血糖水平[6]。相比之下,早产儿的糖原储备较低,消耗速度也更快,这使他们在出生后发生低血糖的风险更高[7]。关于早产婴儿出生后发生低血糖的发生率和潜在危险因素,目前的证据仍较少。本研究旨在探讨早产儿早期低血糖的发生率及危险因素。
1 材料与方法
前瞻性连续纳入2017年4月至2019年8月在崇左市复退军人医院分娩的小于37孕周的新生儿。排除有严重先天性异常或可能影响呼吸或通气条件的新生儿(如膈疝等)。
1.1 新生儿的资料采集
新生儿低血糖定义为血糖小于2.2 mmol/L[8]。新生儿体重依据全球胎儿体重和出生体重百分位数标准转化为百分位数[9]。SGA 定义为胎龄出生体重(BW)小于第10百分位数,大于胎龄儿(large for gestational age,LGA)是指出生体重在相同胎龄平均体重的第90百分位以上的婴儿。记录新生儿的结局,包括坏死性小肠结肠炎和脑室出血等。所有新生儿均按NICU方案常规喂养,低血糖按NICU方案治疗。新生儿在出生30 min内未开奶且未开始静脉输液前足跟采血0.03-0.05 ml,采用德国罗氏公司生产的微量血糖检测仪行快速血糖检测。
1.2 母亲的资料采集
孕产妇人口统计资料包括:(1)产前类固醇的给药;(2)产前接受硫酸镁(MgSO4)包括所有在出生前接受过MgSO4的母亲(以4 g的负荷剂量,30 min以上,然后以1 g/h的维持输注直至出生,24 h不超过25 g);(3)孕妇糖尿病包括妊娠前糖尿病和妊娠期糖尿病[4];(4)孕妇高血压包括妊娠前患有高血压病和妊娠期高血压。产妇年龄、伴随疾病、伴随用药通过患者病历收集。
1.3 统计学分析
使用SPSS 22.0软件进行统计学分析。符合正态分布的连续变量采用均数±标准差表示,采用独立样本t检验比较组间差异;计数资料采用频数(百分比)[n(%)]表达,视情况采用χ2检验或Fisher精确检验比较组间差异。不符合正态分布的数据使用中值(四分位数)[M(P25-P75)]表达,采用Mann-Whitney U检验法比较组间差异。单因素分析P<0.100的变量进入多因素Logistic回归模型考察早产儿发生低血糖的独立危险因素。检验水准α=0.05。
2 结果
2.1 早产儿发生低血糖单因素分析
共纳入175例小于37孕周妊娠的婴儿,低血糖发生率为33.7% (n=59)。低血糖组与正常血糖组比较,分娩方式、使用MgSO4人数、患有高血压人数组间差异有统计学意义(P<0.05),患有糖尿病的人数组间比较,P<0.10,上述参数均进入多元Logistic回归模型考察新生儿发生低血糖的独立危险因素,见表1。
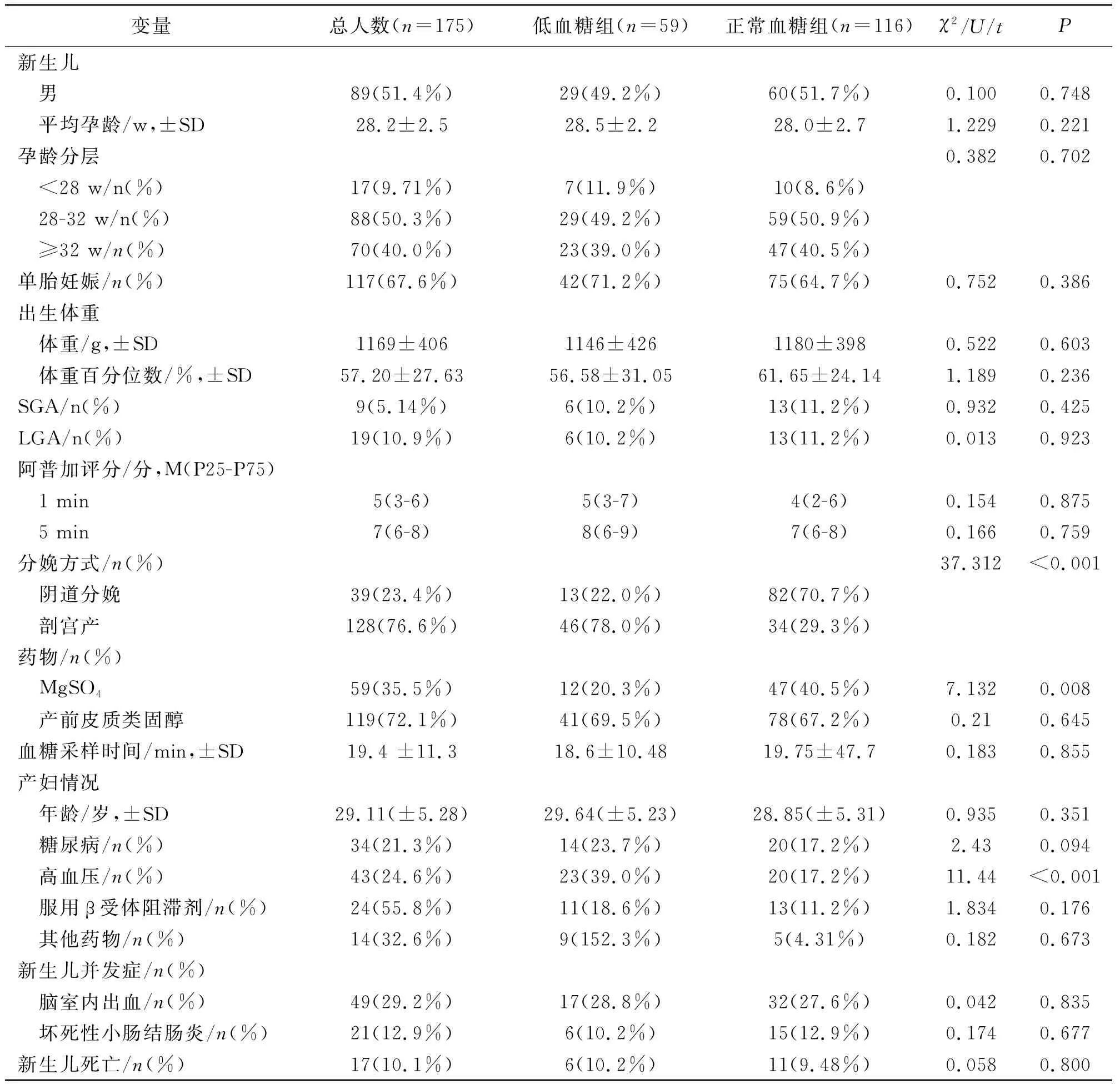
表1 早产儿发生低血糖单因素分析
2.2 早产儿发生低血糖的多因素分析Logistic回归分析
母亲高血压(是vs否: OR=2.40,95%CI=1.03-5.71)和糖尿病(是vs否:OR=1.87,95%CI=1.25-2.62)是早产新生儿发生低血糖的独立危险因素。而阴道分娩(否vs是:OR=3.63,95%CI=1.61-8.41)和产妇使用MgSO4(否vs是:OR=2.53,95%CI=1.23-5.50)是早产新生儿发生低血糖的保护因素。见表2。

表2 早产儿发生低血糖的多因素分析Logistic回归分析
3 讨论
本研究总体低血糖发生率为33.7%,这与文献报告的早产儿出生后第1天[10]内和大于35周的婴儿出生后1-48 h内[11]的数据相似。James等[10]报道在小于32周妊娠的婴儿中,总发病率为41%,但他们排除了母亲是糖尿病的婴儿。Singh等[11]报道,在出生后48 h内,怀孕35周的婴儿发病率为51%。最近的一项研究[12]表明,早产儿和极早产儿的血糖浓度最低值分别在70.5和60.9 min后。我们的血糖样本是在出生后19.4 min的平均年龄采集的,可能会错过低血糖的最低点,导致我们对发病率的低估。
本研究显示孕妇高血压导致新生儿低血糖的发生几率增加2.4倍。孕产妇高血压是新生儿低血糖的已知危险因素,可能反映了围产期应激、胎盘功能不全、SGA危险因素和早产危险因素的环境[13]。此外,孕妇使用β-受体阻滞剂是新生儿低血糖的已知危险因素[14]。β-受体阻滞剂作为一种降压药,在孕产妇高血压患者中使用率较高[15],这可能增加了新生儿低血糖的风险。
使用MgSO4是新生儿低血糖的保护因素。无论总剂量如何,产前MgSO4可降低早产婴儿脑瘫和脑出血的发生率[16]。在低血糖大鼠模型中,MgSO4可降低血脑屏障通透性,提高血糖浓度[17]。此外,MgSO4水平与胰岛素通路中的脂蛋白代谢和信号转导有关[18]。MgSO4通过降低大脑压力和血脑屏障通透性来降低葡萄糖在大脑中的利用[19]。结合MgSO4对适当的胰岛素调节和脂蛋白代谢的影响,我们推测MgSO4维持血糖的保护机制可能是多途径的。
本研究结果表明,阴道分娩可能对早产儿的低血糖有保护作用。妇女在阴道分娩过程中内源性类固醇的释放增加[20],这表明这些较高的循环内源性类固醇,在分娩过程中,可能会启动婴儿体内的糖异生作用。胎儿的这种糖异生环境可能对新生儿有保护作用。另一方面,由于麻醉需要,剖腹产前产妇禁食也可能加剧了新生儿低血糖的发生和发展[21]。
本研究中,产前使用皮质类固醇既不是危险因素,也不是保护性因素。但有研究显示,在妊娠34-36周时出生的晚期早产儿,产前使用类固醇会导致新生儿低血糖的风险增加[22]。在早产儿中使用倍他米松可以抑制母亲的促肾上腺皮质激素和皮质醇水平长达24 h[23],这可以解释为本研究中产前使用类固醇对新生儿低血糖没有保护作用。
众所周知,妊娠期糖尿病是早产新生儿低血糖的明确危险因素[24]。妊娠期糖尿病孕妇分娩后的新生儿20%-40%发生低血糖症状,且多发生在出生后1-2 h内[1],这与本研究结果相似。产妇高血糖症经过胎盘进人胎儿机体内,长期高血糖引起胰岛素增加以及胰腺过度刺激,引起β细胞增生,引发胎儿高胰岛素血症导致了新生儿低血糖的发生和发展。
本研究中,LGA和SGA新生儿没有增加低血糖的风险。然而,先前的研究表明这类新生儿有低血糖的风险[25]。SGA新生儿糖原和脂肪储备减少,胰岛素异常释放,导致新生儿低血糖的风险增加[26]。患有糖尿病的母亲更有可能产下LGA,而这类新生儿无论是早产还是足月时分娩,同样有可能发生新生儿低血糖[27]。LGA患儿没有表现出明显的低血糖风险,这可能是由于样本量较小,没有足够的统计学效能造成的。对更大样本量的新生儿的进一步研究可能会产生不同的结果。
本研究的一个局限是样本量较小,尤其是SGA新生儿,这可能影响了统计结果。本研究中所有病例都收集于同一家医院,发生在同一家医院内的16个月内,治疗方案相同。因此,治疗方法对不同新生儿血糖的影响较小。其次,因为考虑到开奶和静脉输液会影响血糖,我们采集血样的时间限定在新生儿出生后开奶和静脉输液前的0.5 h内采集的。而新生儿的血糖是动态变化的[12],仅选择这1个时间段采集血样,可能观察不到此时尚未发生低血糖而0.5 h后才发生低血糖的病例。
虽然早产儿出生后都会静脉输液治疗,连同开奶或鼻饲管喂养可能会改善低血糖状态。但是在进食和输液前及时检测患儿的血糖状态,有利于更及时地采取措施纠正患儿的低血糖状态,有效避免由此带来的损伤。未来的研究应检查母亲的血糖和胰岛素水平,新生儿胰岛素和血酮水平,以了解其潜在的调节机制。应对婴儿进行长期随访,了解新生儿低血糖对神经发育的长期影响。此外,对MgSO4与新生儿低血糖作用机制的研究可以为预防治疗的发展提供思路。

