BRCA2通过PI3K/AKT通路上调ATM抑制乳腺癌的增殖、迁移和侵袭
梅 楠,赵 妮,陈旭阳,阮稳稳,宜 烨,李春丽*
(1.西安交通大学第一附属医院 肿瘤内科,陕西 西安710061;2.商洛市中心医院 肿瘤内科,陕西 商洛726000;3.安康市人民医院 肿瘤内科,陕西 安康725000)
乳腺癌严重影响全球女性的身心健康,2018年,GLOBOCCAN[1]的数据统计发现,全球新诊断的女性乳腺癌病例几乎占女性癌症病例的25%,约210万,女性乳腺癌症死亡率占据女性癌症死亡率的15%,总计达630万。乳腺癌患者的存活率在不同的阶段有很大的差异,Ⅰ期、Ⅱ期和Ⅲ期的患者总体5年生存率在50%以上,而IV期患者的5年生存率只有27%[2]。因此,及时有效地预测治疗乳腺癌的效果,寻找更多的基因靶点和相应的突变位点,以便更全面、准确地指导肿瘤患者的个体化治疗是当务之急。
随着高通量测序技术的开展以及分子生物学在临床医学中的普遍应用,人们对乳腺癌易感基因及其突变在癌症发生、发展中的作用进行了广泛的研究。与乳腺癌密切相关的易感基因是BRCA家族基因(BRCA1和BRCA2),其通过调控细胞周期、基因转录和细胞凋亡等一系列生物学功能,参与保护和修复基因的共同通路,维持基因组完整性和稳定性,从而抑制肿瘤的发生和发展[3]。Kuchenbaecker团队通过前瞻性数据进行了基于BRCA1和BRCA2突变载体状态的癌症风险评估,在乳腺癌的风险评估中,发现BRCA基因突变的女性患乳腺癌的危险显著升高,BRCA1和BRCA2携带者在80岁时累积乳腺癌风险分别为72%和 69%[4]。PI3K/AKT是驱动细胞生长和存活的关键信号转导通路,在乳腺癌中经常被激活,抑制该通路还可以增加内分泌治疗乳腺癌效果[5]。ATM是常染色体隐性突变基因,属于PI3K蛋白家族成员,与乳腺癌的预后有较高相关性,其表达下调和缺失导致基因修复通路失调,作用于乳腺癌恶性发展的过程[6]。大量研究通过高通量测序技术,发现乳腺癌患者及其家族中BRCA2突变,比如杂合的c.5722_5723del突变[7]、c.8946_8947delAG突变[8]。BRCA2突变后,可能会通过PI3K/AKT通路干扰同源重组蛋白,比如ATM,导致DNA双链断裂修复功能障碍,最终促使乳腺癌的发生。目前,除了生物信息学技术的基因测序寻找的BRCA2突变外,还未发现相关细胞体内实验构建BRCA2过表达载体和突变载体,来分析BRCA2和同源重组蛋白共同作用乳腺癌发展过程。为进一步讨论BRCA2基因对乳腺癌生物学功能的影响,及其作用信号通路和相关机制,为后续BRCA2突变位点功能的分析和探索奠定基础,本实验构建BRCA2基因过表达载体并完成相关细胞实验,以期为乳腺癌的作用信号通路机制和分子精准治疗提供理论依据。
1 材料与方法
1.1 试剂和仪器设备
BT474细胞株(上海拜力公司),Lipofectamine
3000(invitrogen公司),CCK8试剂盒(七海生物公司),质粒提取试剂盒(天根),McCoy 5a培养基(Gibco公司),基质胶体和Transwell小室(Corning公司),1640培养基、胰酶、双抗(Hyclone公司),BRCA2兔多克隆抗体和ATM兔单克隆抗体(abcam公司),FBS(Gibco公司)。小离心机(1.5 ml)(大龙公司),离心机(15 ml)(湘仪公司),细胞培养箱(Thermo公司),水浴锅(国华),超净工作台(苏州净化公司),流式细胞仪(BD FACSCalibu公司),酶标仪(BIO-RAO公司),凝胶成像系统仪(ATTO公司)。
1.2 方法
1.2.1细胞培养
BT474细胞用1640 培养基(含10%胎牛血清、100 U/ml青霉素、100 μg/ml链霉素和10 μg/ml 胰岛素)于37℃、5% CO2细胞孵箱中培养。
1.2.2BRCA2过表达载体构建
从购买的cDNA-BRCA2克隆中扩增出目的片段,PCR扩增条件:预变性94℃,2 min 30 s;之后每个循环变性94℃,20 s;退火60 ℃,30 s;延伸68℃,1 min;共进行18个循环;68 ℃再延长5 min;15℃保存。琼脂糖凝胶电泳验证以上PCR产物,采用Qiagen胶回收试剂盒在凝胶成像系统下切胶回收目的片段。将上述回收纯化后的产物以及真核表达载体pCDNA3.1-coGFP进行Nhel和Xhol双酶切,37℃酶切30 min,酶切产物进行凝胶电泳,Qiagen胶回收后利用同源重组的方法,让酶切后的载体和扩增片段进行非依赖酶性连接。连接产物转化后挑取克隆进行菌液PCR,提取质粒,最后用Nhel和Xhol 双酶切进行鉴定。将回收得到的质粒样品以空载质粒pCDNA3.1-coGFP为对照,一起进行凝胶电泳,送公司测序。
1.2.3转染细胞系
将培养好的BT474细胞铺于24孔板,设置实验组(转染BRCA2基因过表达组)、空白细胞对照组(未转染组)和阴性对照组(空载体转染组),除空白细胞对照组,其它两组每个孔加入1.0 μg的质粒,细胞贴壁后用lipofect 3000转染试剂的方法进行转染。
1.2.4Western blot
将转染后的BT474细胞以及空白细胞对照组和空载体转染组用IP裂解液加1 %的PMSF蛋白酶抑制剂来裂解蛋白,测量蛋白浓度(BCA法);用12.5%聚丙烯酰胺凝胶电泳分离蛋白,100 V 转膜 1 h,经BRCA2、ATM、PALB2、Rad51抗体孵育后显色。
1.2.5免疫组化检测
选取一位病理诊断明确为“右侧乳腺浸润性导管癌”的女性患者的癌组织石蜡标本切片,采用SP法检测BRCA2和ATM蛋白的表达。在 HE 切片下选取合适的蜡块连续切片,约3 μm厚,脱蜡、乙醇脱水、修复抗原、过氧化氢、蒸馏水、PBS 缓冲液处理。分别在切片上加一抗BRCA2兔多克隆抗体(1∶200)和一抗ATM兔单克隆抗体(1∶100),过夜。DAB显色,自来水冲洗,复染脱水,透明封片,PBS作阴性对照。细胞核、细胞质和细胞膜中出现淡黄至棕黄色为阳性显色,根据细胞染色强度和阳性细胞比例确定BRCA2、ATM蛋白表达。
1.2.6CCK8法
pCDNA3.1(+)-copGFP-BRCA2质粒转染BT474细胞 24 h后,接种于96孔板(5×103个细胞/孔),设置3个复孔。记0 h(细胞贴壁时),分别在第48、72、96 h加入10 μl CCK-8,于37℃培养箱孵育1 h后,用酶标仪检测每孔在 450 nm 波长处的吸光度值(OD)。绘制细胞生长曲线(培养时间为横轴,OD取平均值为纵轴)。
1.2.7流式检测法
pCDNA3.1(+)-copGFP-BRCA2质粒转染BT474细胞 24 h后,接种于6孔板(5×105个细胞/孔),设置3个复孔,分别在第48、72、96 h收集转染的样品,测定凋亡率。
1.2.8细胞划痕实验
pCDNA3.1(+)-copGFP-BRCA2质粒转染BT474细胞 24 h后,接种于6孔板(5×105个细胞/孔),设置3个复孔,转染24 h后,对转染细胞划痕,拍照,记为0 h,继续培养,在转染48 h、72 h、96 h后,分别观察细胞生长迁移情况并拍照记录。
1.2.9Transwell实验
pCDNA3.1(+)-copGFP-BRCA2质粒转染BT474细胞 24 h后,接种于6孔板(5×105个细胞/孔),设置3个复孔,转染24 h后,每个小室中加入1×105个细胞;培养24 h后取出培养板;弃培养基,PBS清洗3次,4%多聚甲醛固定20 min;弃固定液,PBS清洗3次,0.1%结晶紫染色20 min,湿棉签擦去上层未发生迁移的细胞,PBS清洗3次后显微镜下拍照;细胞转染48 h、72 h、96 h后重复以上实验步骤。
1.3 统计学分析
2 结果
2.1 真核表达载体 pCDNA3.1(+)-copGFP-BRCA2的构建和鉴定
以购买的cDNA-BRCA2克隆出模板,PCR扩增人BRCA2的编码序列,扩增结果见图1和图2;产物以及真核表达载体pCDNA3.1-coGFP进行Nhel和Xhol双酶切,胶回收后利用同源重组的方法,进行非依赖酶性连接酶切后的载体和扩增片段。连接产物转化后挑取克隆进行菌液PCR,并选取阳性克隆再摇菌提取质粒,用Nhel和Xhol 双酶切鉴定,两次酶切结果分别如图3和图4。通过测序发现回收得到的质粒样品比空pCDNA3.1-coGFP对照高,可以确认构建好的质粒序列100%正确,因此确认构建成功。
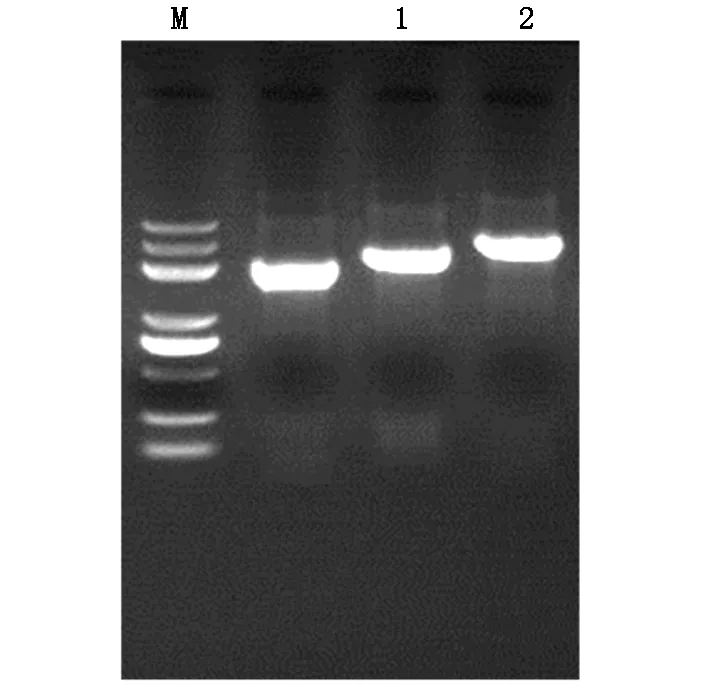
图1 BRCA2-I的两个分段
2.2 Western blotting 分别检测BRCA2蛋白及HR通路相关蛋白在BT474细胞中的表达

图2 BRCA2-II的两个分段
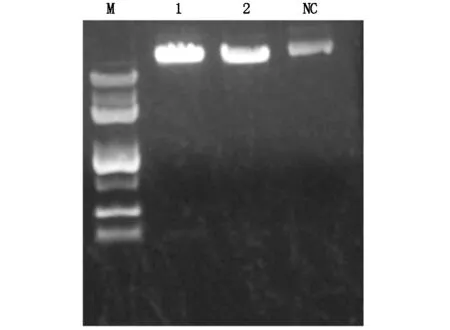
图3 pCDNA3.1-coGFP/NheI,XhoI酶切产物
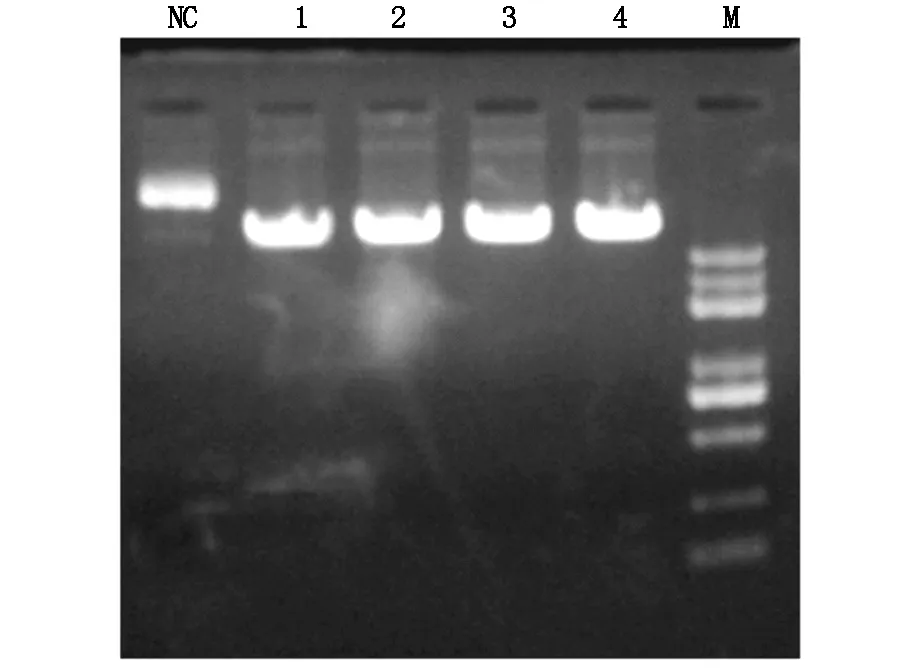
图4 pCDNA3.1-coGFP-BRCA2-II/NheI酶切产物
Western blot检测各组细胞中BRCA2、 ATM、PALB2和Rad51蛋白的表达。如图5结果显示,与空白细胞对照组和阴性细胞对照组比较,实验组细胞的BRCA2、ATM、PALB2和Rad51蛋白条带显现,其表达量显著上调(P<0.05)。
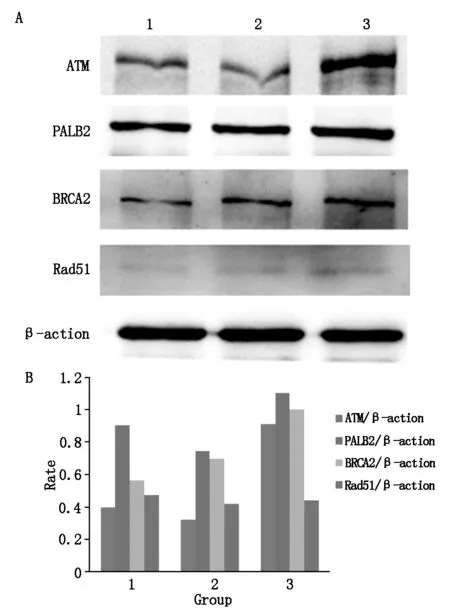
图5 乳腺肿瘤细胞中蛋白表达情况(A和B)
2.3 免疫组化检测人乳腺癌组织中BRCA2和ATM蛋白的表达
免疫组化结果如图6显示,BRCA2和ATM在乳腺癌组织中的阳性表达同时增加,表现为强阳性。
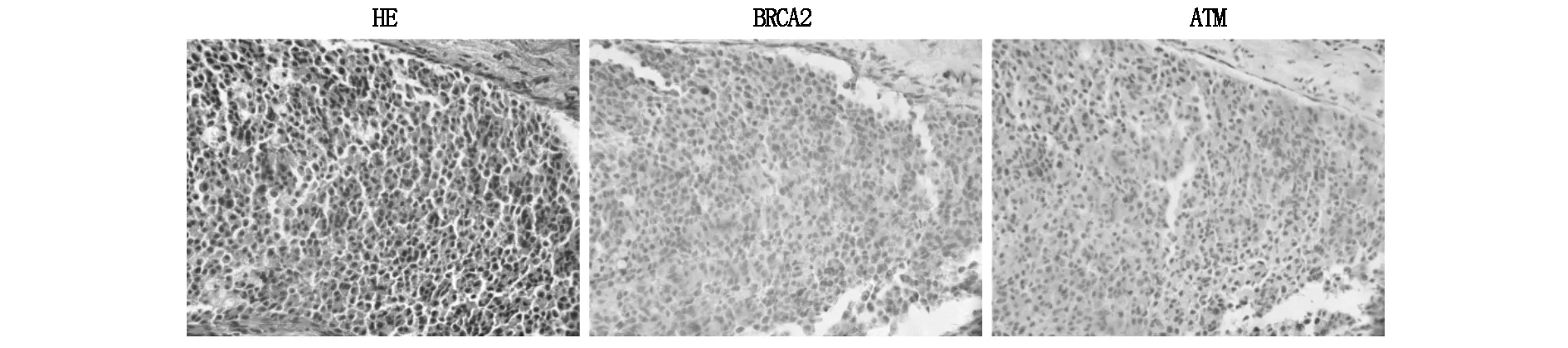
图6 BRCA2和ATM在乳腺癌组织的免疫组化(放大×400)
2.4 BRCA2基因过表达后BT474细胞的增殖凋亡情况
CCK8法检测BRCA2基因过表达组细胞系和空白细胞对照组以及空载体转染组细胞的生长增殖情况。在BT474细胞中,结果分别如图7所示,与对照组相比,BRCA2基因过表达实验组的细胞增殖能力降低,其生长速度显著低于相应的对照组(P<0.05),而空白细胞对照组和阴性对照组在不同时间的增殖速度相比,无明显差异(P>0.05),说明BRCA2基因可抑制BT474细胞的增殖。细胞凋亡情况的结果如图8所示,随着时间的延长,与对照组相比,BRCA2基因过表达细胞系凋亡率逐渐升高(P<0.05),说明BRCA2基因可促进BT474细胞的凋亡。

图7 BRCA2基因抑制乳腺肿瘤细胞增殖

图8 BRCA2基因促进乳腺肿瘤细胞凋亡
2.5 BRCA2基因过表达后BT474细胞的侵袭迁移情况
细胞划痕实验和Transwell实验分别检测BRCA2基因过表达后对肿瘤细胞迁移和侵袭的影响结果。将BRCA2过表达实验组及相应的对照组质粒分别转染BT474细胞系,待细胞贴壁后进行划痕实验,划痕48 h、72 h、96 h后,计算迁移距离。随着时间的延长,在BT474细胞中,BRCA2基因过表达组细胞系和空白细胞对照组以及空载体转染组细胞对比,迁移率降低,迁移能力下降(P<0.05),因此BRCA2基因抑制乳腺癌细胞的迁移(见图9)。Transwell检测细胞转染后侵袭能力的变化,结果表明,BRCA2基因可抑制乳腺肿瘤细胞侵袭(见图10)。

图9 BRCA2基因抑制乳腺肿瘤细胞迁移(A和B)

图10 BRCA2基因抑制乳腺肿瘤细胞侵袭
3 讨论
3.1 BRCA通路相关基因与DNA损伤修复密切相关
乳腺癌的发生不是一条简单的基因通路操纵,而是一个多步骤复杂通路参与的进程,初潮年龄、生育年龄、绝经年龄、母乳喂养、家族史、生殖因素、雌激素和生活方式都与此过程密切相关[9]。有研究分析表明,乳腺癌相关基因(BRCA1和BRCA2)的突变占家族性乳腺癌的20%-40%[10]。BRCA相关蛋白参与了重要的细胞功能,在调节DNA损伤如双链断裂修复、基因组稳定性、细胞周期进展的生物通路、转录调节、细胞生长、凋亡和参与DNA损伤的同源重组修复等方面发挥着重要作用,从而保护基因组,抑制肿瘤生长[11]。
DNA损伤修复是通过一系列复杂的信号事件和各种酶的活动来实现的,而同源重组修复通路是一种涉及大量蛋白质的DNA损伤反应途径,它们在非常精确的操作序列中相互作用,完成DNA的高保真修复[12]。在乳腺癌中,同源重组修复途径不仅涉及BRCA1/2的复杂协同作用,还涉及其它相关的DNA修复蛋白。一篇综述中阐述了乳腺癌常见的中、高外显率基因的大致种系频率,其中BRCA1、BRCA2、ATM、PALB2和Rad51在乳腺癌中的生殖系突变频率分别约为2%-3.7%,1%-2.8%,0.3%-1.1%,0.2%-1.3%和0.2%-0.49%[13]。ATM是DNA修复系统的核心组成部分,激活后可增强DNA双链断裂的同源重组修复通路,同时ATM中的致病种系变异,在DNA损伤反应和细胞周期检查点中起作用,导致乳腺癌风险的增加[14]。Rad51是DNA双链断裂修复中的关键蛋白,在侵袭性乳腺癌患者中,RAD51核表达的缺乏与较差的预后参数和较短的生存期有关[15]。PALB2截断变异会导致乳腺癌发病率升高,PALB2能够通过结合单链DNA与Rad51直接相互作用,使其成为同源重组介导修复的关键枢纽,因此PALB2的缺失导致BRCA2和RAD51加载到DNA双链断裂的位点功能受损[16]。目前都是相关综述或者基于单个基因研究的基础实验去讨论BRCA、ATM、PALB2、RAD51和同源重组的关系,暂时还没有发现通过体外实验将以上几者结合后再去进一步阐述它们的联系,但是本实验不仅验证BRCA2蛋白在乳腺癌BT474细胞中的表达,同时还研究了ATM、PALB2和Rad51蛋白在乳腺癌细胞中的表达情况。
3.2 PI3K/AKT信号通路在乳腺癌发生发展中的作用
PI3K/AKT作为一种细胞内信号通路,控制增殖、凋亡、血管生成、代谢和运动等多种细胞过程,是人类癌症细胞中最常见的失调信号通路之一,这条通路中最重要的靶向调控点是PI3K、AKT和mTOR[17]。PI3K/AKT通路的改变涉及多个基因,在乳腺肿瘤中,约20%-50%的乳腺癌发生PIK3CA突变,不超过5%的乳腺癌发生PTEN突变,约3%的TNBC发生AKT突变,激活此通路会导致癌细胞生长存活以及抗肿瘤治疗的耐药性[18]。PI3K/AKT/mTOR通路已被认为是乳腺癌的重要信号通路,其突变经常在乳腺癌中被发现,并与细胞转化、肿瘤发生、癌症进展和耐药性有关[19]。一项关于乳腺癌细胞的体外实验表明,乳腺癌中过表达MEG3通过PI3K/AKT通路下调miR-21,从而抑制乳腺肿瘤的发生[20]。在43%-70%的乳腺癌脑转移患者中,存在PI3K/AKT/mTOR通路的激活突变。Franziska等人在体内和体外的研究中发现,AKT抑制剂可降低PIK3CA突变型乳腺癌脑转移细胞的细胞活力,诱导细胞凋亡;其次,与PIK3CA野生型模型相比,显著抑制了PIK3CA突变肿瘤的生长,并显著改善了生存[21]。这进一步表明PI3K/AKT通路将会是一种有前景的治疗靶点。
乳腺癌常被分为以下4种亚型,LuminalA亚型、LuminalB亚型、HER2过表达亚型以及三阴性导管亚型[22]。在乳腺癌的治疗中,虽然激素治疗和HER2靶向治疗分别对ER+、HR+和HER2+的乳腺癌产生了较好的治疗效果,但是对于三阴性乳腺癌还没有确定的靶向药物。即使PARP抑制剂可应用于BRCA突变乳腺癌,但其在治疗三阴性乳腺癌中的价值仍需要进一步研究。转移性三阴性乳腺癌是乳腺癌症中预后最差的一种,目前认为免疫疗法、PARP抑制剂和PI3K/AKT通路靶向抑制剂可用于它的治疗,从而改善患者的生存率[23]。
3.3 BRCA2基因介导PI3K/AKT信号通路上调ATM基因抑制乳腺癌BT474细胞的增殖、迁移和侵袭
人类ATM基因编码的蛋白属于磷脂酰肌醇激酶样激酶(PI3KKs)家族,功能区是磷脂酰肌醇3激酶,主要参与 DNA损伤反应和细胞周期检查点通路。PI3K/AKT和p53通路是乳腺癌细胞中两个重要的调节通路,PI3K/AKT的激活和p53通路的抑制会促进癌细胞的增殖。当激活PI3K/AKT信号通路,此时AKT通过介导MDM2靶向抑制p53水平,促进乳腺癌发生[24]。ATM-Chk2通路对基因组稳定性至关重要,DNA损伤会导致ATM磷酸化,进而激活Chk2活化下游底物,如P53通路,因此其突变可能导致多种肿瘤易感性增加,其中就包括遗传性乳腺癌[25]。PI3K/AKT信号通路的活化可以加速细胞周期进程,会促使DNA损伤的细胞也进入有丝分裂,主要是因为PI3K/AKT可磷酸化DNA损伤检测点激酶CHK1的位点,从而使CHK1远离ATM,导致DNA损伤检测功能的降低,那么PI3K/AKT的去磷酸和失活可能会提高ATM的抑癌功能[26]。因此,我们认为ATM的表达和P53通路以及PI3K/AKT信号通路的变化密切相关,以此帮助调节细胞周期,维持细胞内基因组稳态。
PALB2也属于乳腺癌易感基因,最初被鉴定为一种与BRCA2互相作用的蛋白,随后也被证明与BRCA1相互作用,对BRCA基因组功能至关重要, 其单等位基因缺失突变会使患乳腺癌风险增加,而且这种风险可能与携带BRCA2突变患病风险重叠[27]。Rad51在乳腺癌细胞系中过表达,作用于损伤的单链DNA形成核蛋白丝,介导双链DNA之间的链间转移修复,Rad51蛋白和多种肿瘤抑制蛋白相互作用,包括p53、BRCA1和BRCA2[28]。ATM、PALB2、Rad51为同源重组修复通路相关蛋白,参与并协同BRCA2抑癌作用,共同维护基因组的稳定。当DNA受损时,可刺激ATM活化,此时同源重组修复通路被激活,各个细胞周期检测机制发挥作用使G1/S、S、G2/M期阻滞,开始DNA损伤修复,ATM使BRCA2的伙伴和定位者PALB2磷酸化,PALB2则通过其氨基和羧基末端独立地与BRCA1和BRCA2相互作用,促进RAD51核蛋白丝的稳定,而BRCA1相关环域蛋白1 (BARD1)与BRCA1形成稳定的异源二聚体,提高 BRCA1的活性,促进同源重组修复通路的激活[29]。有一些相关的细胞实验发现ATM、Rad51、PALB2影响乳腺癌细胞周期,比如青蒿琥酯通过激活ATM可以诱导乳腺癌细胞G2/M期的阻滞[30],Rad51的下调可以使乳腺癌细胞在G2/M期阻滞[31],而BRCA1、PALB2和BRCA2组成了BRCA1-PALB2-BRCA2轴,在检查点激活和检查点维护中都发挥重要作用,尤其是G2/M检查点[32]。大部分研究都是在单基因的细胞实验基础去观察这几个基因在肿瘤细胞的作用方式,还有一些综述在基因学方面分析它们的互相联系和在肿瘤细胞中的作用机制,很少有报道将以上几个基因结合起来,利用细胞和动物实验去更详细地验证它们的关系以及在乳腺癌细胞中的功能。在本实验中,免疫组化结果显示在人乳腺癌组织中,BRCA2和ATM蛋白表达同时升高,而且都呈强阳性表达。Western blot结果清楚地显示BRCA2过表达载体转染乳腺癌BT474细胞后,其表达量上升,而且ATM、PALB2、Rad51相关蛋白的条带也相应显现。与两个对照组相比,BRCA2表达量增加的同时,以上几个蛋白表达量也同时增加,说明本实验成功构建了BRCA2基因过表达的真核表达载体,也初步验证ATM、PALB2、Rad51和BRCA2蛋白共同参与同源重组修复通路。
在Yasir团队的一项实验中[33],通过体外模型,发现抑制PI3K通路可以降低三阴性乳腺癌细胞BRCA1/2的表达,同时获得PARP激活的产物蛋白,这表明抑制PI3K会损伤同源重组修复通路。在一项关于他莫昔芬耐药乳腺癌细胞的研究中[34],发现耐他莫昔芬的乳腺癌细胞中磷酸化AKT的表达明显高于对照组细胞,且BARD1/BRCA1表达上调,认为耐他莫昔芬的乳腺癌细胞对化疗产生耐药是因为PI3K/AKT通路激活导致BARD1和BRCA1上调,BARD1/BRCA1的降低会使他莫昔芬耐药的乳腺癌细胞对化疗药物重新敏感。因此,我们考虑PI3K/AKT信号通路和同源重组修复通路互相联系,互相影响,进一步推测PI3K/AKT信号通路和本实验研究的BRCA2目的基因有潜在作用通路。
为了验证ATM是否介导BRCA1的磷酸化,Li[35]等使用siRNA干扰的ATM和其抑制剂作用于人乳腺癌MCF-10A细胞,如预期猜想一样,在紫外线损伤的MCF-10A细胞中,siRNA干扰的ATM会显著降低细胞中BRCA1的磷酸化和p53的乙酰化,表明 ATM介导了人乳腺上皮细胞中DNA损伤引起的BRCA1磷酸化和p53功能。本实验在BRCA2基因过表达载体转染至乳腺肿瘤细胞后,使用CCK8和流式细胞仪,观察到了BRCA2抑制乳腺肿瘤细胞的生长、促进凋亡的现象,Transwell和愈合实验表明BRCA2基因抑制乳腺肿瘤细胞的迁移侵袭,进一步证明BRCA2对乳腺癌有抑制效应。鉴于BRCA2和BRCA1基因在同源重组修复通路中是协同作用,而且PI3K/AKT和ATM以及BRCA2在乳腺癌的发展和后续治疗中是互相影响的,因此我们推测,ATM基因可通过调控PI3K/AKT信号通路介导BRCA2的磷酸化,进一步影响人乳腺癌细胞的存活和凋亡。
综上所述,BRCA2 作为一种重要的抑癌基因,可抑制乳腺肿瘤细胞的增殖、迁移和侵袭。本研究通过构建 BRCA2基因过表达真核载体,发现 BRCA2 基因过表达后可同时上调ATM、Rad51、PALB2蛋白的表达,抑制乳腺肿瘤细胞的增殖并诱导其凋亡。本研究阐述了BRCA2基因和PI3K/AKT信号通路以及同源重组修复通路的关系,进一步探究ATM基因和BRCA2基因的互相作用机制,认为BRCA2基因通过PI3K/AKT通路上调ATM抑制乳腺癌的增殖、迁移和侵袭。今后,我们将进一步完成PI3K/AKT抑制剂处理乳腺癌细胞的实验,探究 BRCA2 基因突变后乳腺癌细胞增殖和凋亡的具体机制,以进一步确认BRCA2基因介导 PI3K/AKT 信号通路以及其他信号通路靶向ATM基因,在乳腺癌中发挥关键作用的过程。由此发现更多基因水平的药物靶点,进一步指导临床中BRCA2 相关性乳腺癌的诊断,达到精准有效的个体化靶向治疗。

