马钱苷元抗大鼠实验性心律失常的作用与机制预测
冯 群,李 欣,姚景春,肖 敏,赵 涛,张贵民*
(1.鲁南制药集团股份有限公司 新药安评中心,中药制药共性技术国家重点实验室,山东 临沂 276006;2.山东新时代药业有限公司,山东 临沂 273400)
心律失常(arrhythmia)是心血管疾病中重要的一组疾病,可单独发病或与其它心血管病伴随发生,具有较高的发病率和潜在的死亡危险[1]。心律失常通常是由于窦房结激动异常或激动产生于窦房结以外,激动的传导缓慢、阻滞或经异常通道传导,即心脏活动的起源和(或)传导障碍导致心脏搏动的频率和(或)节律异常[2]。其预后与心律失常的病因、诱因、演变趋势、是否导致严重血流动力障碍有关,可突然发作而致猝死,亦可持续累及心脏而致其衰竭。心律失常大多通过心电图确诊[3]。目前临床应用的抗心律失常药物已近50 余种,至今还没有统一的分类标准。大多数学者同意根据药物对心脏的不同作用原理将抗心律失常药物分为四类:钠通道阻滞药、β 肾上腺素受体阻断药、延长动作电位时程药、钙通道阻滞剂,以指导临床合理用药。长期服用抗心律失常药均有不同程度的副作用,严重的可引起室性心律失常或心脏传导阻滞而致命。目前抗心律失常的西医药物治疗研究已经进入瓶颈期,而某些国产中成药在治疗此疾病方面具有独特优势[4]。
作为山茱萸果实中的成分之一,马钱苷元也可以通过马钱苷的降解而得。山茱萸及其有效成分可通过脂质代谢、氧化应激、炎性因子和免疫调节等路径发挥神经保护、强心、肝脏和肾脏保护等药理作用[5-7]。现代药理学研究已经证明了山茱萸提取物及马钱苷抗心律失常作用的有效性[8],但马钱苷元的抗心律失常作用仍不明确。本实验建立2 种不同的心律失常大鼠模型,考察马钱苷元对心律失常大鼠的保护作用,利用分子对接技术探索马钱苷元与抗心律失常靶点的相互作用,为其开发提供依据。
1 材料与方法
1.1 材料
1.1.1 药物与试剂 马钱苷元(C11H16O5,CAS:29748-10-5),由山东新时代药业有限公司提供(97.51%);氯仿(分析纯,西陇科学股份有限公司);乌头碱(分析纯,南京泽朗植提技术有限公司);盐酸胺碘酮注射液[赛诺菲安万特(杭州)制药有限公司]。
1.1.2 实验动物 SPF 级SD 大鼠,体质量为180 ~220 g。购自济南朋悦实验动物繁育有限公司,动物使用许可证号:SYXK(鲁)20180008,大鼠入室后至少检疫3 d,区分性别饲养。研究中所有实验动物相关的操作严格按照国际实验室动物伦理行为准则“Guide for the Care and Use of Laboratory Animals”实施[9]。
1.1.3 主要仪器 Waters 2489 型高效液相色谱仪(美国Waters 公司);SP2006 型心电图分析系统(北京软隆科技有限责任公司);PL-2002 型电子天平(梅特勒-托利多)。
1.2 方法
1.2.1 氯仿诱发大鼠心律失常实验 取SD 大鼠40只,按照性别和体质量随机分为4 组,模型组、马钱苷元低、高剂量组、胺碘酮组,每组10 只,雌雄各半。模型组按照10 mL/kg 腹腔注射生理盐水,马钱苷元剂量组按照10 mL/kg 腹腔注射马钱苷元1 mg/kg、10 mg/kg,胺碘酮组按照5 mL/kg 静脉注射盐酸胺碘酮注射液20 mg/kg,连续给药3 d,1 次/d。末次给药30 min 后,将大鼠放入含有10 mL 氯仿棉球的倒置2 000 mL 烧杯中(每换1 只大鼠添加2 mL 氯仿),待呼吸停止后立即沿胸骨左缘剖开胸腔,观察心脏跳动节律,以确定是否发生室颤,记录室颤大鼠数,计算室颤发生率[10]。
1.2.2 乌头碱诱发大鼠心律失常实验 取SD 大鼠40 只,按照性别和体质量随机分为4 组,模型组、马钱苷元低、高剂量组、胺碘酮组,每组10 只,雌雄各半。模型组按照10 mL/kg 腹腔注射生理盐水,马钱苷元低、高剂量组按照10 mL/kg 分别腹腔注射马钱苷元1 mg/kg、10 mg/kg,胺碘酮组按照5 mL/kg静脉注射盐酸胺碘酮注射液20 mg/kg,各组大鼠连续给药3 d,1 次/d。末次给药30 min 后,以3%戊巴比妥钠按45 mg/kg 将大鼠麻醉后,仰卧固定于大鼠手术台上,以针形电极扎入四肢皮下,用SP 2006心电图分析系统检测Ⅱ导联心电图,心电图稳定后尾静脉快速注射乌头碱(20 g/kg),观察心电图变化,记录大鼠室早的出现及终止时间,计算大鼠室早潜伏期和持续时间[11]。
1.2.3 分子对接 从KEGG 数据库(https://www.kegg.jp/kegg/drug/)[12]中检索抗心律失常药物及其对应的靶点,共得到66 个药物和39 个靶点,根据药物分类和作用通路,分别选择SCN5A、ADRB1、KCNH2 和CACNA1C 作为受体,马钱苷元作为配体,并同已上市药物利多卡因(lidocaine)、普萘洛尔(propranolol)、胺碘酮(amiodarone)、维拉帕米(verapamil)比较与受体的结合能和结合位点。
下载上述配体/ 药物的mol2 格式文件,用Autodock Tool 软件打开该化合物,使其能量最小化并判定化合物的Root、选定可扭转的键,保存为*pdbqt格式文件。从PDB 数据库(https://www.rcsb.org/)[13]下载受体的PDB 格式文件,运用Pymol 软件移除靶蛋白中的配体和非蛋白分子(如水分子),再保存为PDB 格式文件。随后用Autodock Tool 软件打开的PDB 文件,加氢、计算电荷并“Assign AD4 type”给蛋白添加原子类型,将其保存为*pdbqt 格式文件[14]。运用Autodock vina 将配体/药物和受体进行对接。结合能小于0 说明配体与受体可以自发结合,目前对于活性分子的靶点筛选尚无统一标准,本实验对结合能进行排序,结合能排序靠前且数值绝对值越大,对接结果较好。
1.2.4 统计学方法 用SPSS 21.0 软件进行数据分析,计量资料用均数±标准差(±s)表示,多组间比较采用方差分析,两两比较采用t 检验。计数资料用例与百分数 [n(%)] 表示,采用χ2检验。以P <0.05为差异具有统计学意义。
2 结果与分析
2.1 马钱苷元对氯仿所致心律失常的影响
与模型组比较,马钱苷元高剂量组和胺碘酮组大鼠室颤率明显降低,差异具有统计学意义 (P <0.01),马钱苷元低剂量组大鼠室颤率无明显降低,见表1。表明马钱苷元高剂量组可以抗室颤。
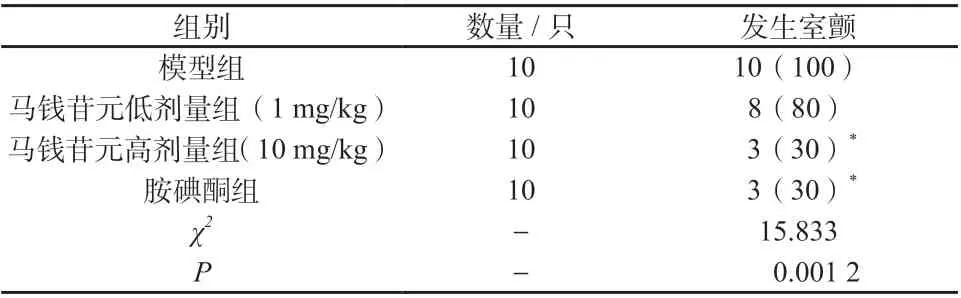
表1 各组大鼠室颤情况[n(%)]Tab. 1 Incidence comparation of ventricular fibrillation in each group[n(%)]
2.2 马钱苷元对乌头碱所致心律失常的影响
实验结果如表2 所示,静脉注射乌头碱后大鼠均可出现室性心律失常,与模型组相比,马钱苷元高剂量组和阳性药胺碘酮组大鼠出现心律失常的潜伏期明显延长(P <0.05),并有效缩短心律失常的持续时间(P <0.05)。结果表明,马钱苷元高剂量组大鼠对乌头碱诱发大鼠心律失常有较好的拮抗作用,低剂量组效果不明显。
表2 马钱苷元对乌头碱诱发大鼠心律失常潜伏期和持续时间的影响(±s,n = 10)Tab. 2 Influence of loganetin on incubation period and duration of arrhythmia induced by aconitine in rats(±s,n = 10)
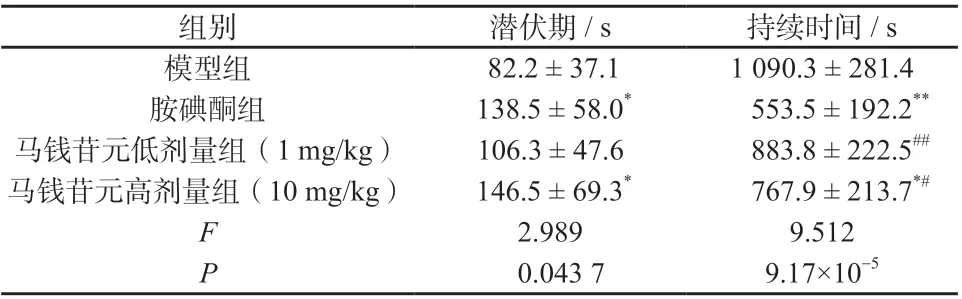
表2 马钱苷元对乌头碱诱发大鼠心律失常潜伏期和持续时间的影响(±s,n = 10)Tab. 2 Influence of loganetin on incubation period and duration of arrhythmia induced by aconitine in rats(±s,n = 10)
注:与模型组比较,*P <0.05,**P <0.01;与胺碘酮组比较,#P <0.05,##P <0.01
组别 潜伏期/ s 持续时间 / s模型组 82.2 ± 37.1 1 090.3 ± 281.4胺碘酮组 138.5 ± 58.0* 553.5 ± 192.2**马钱苷元低剂量组(1 mg/kg) 106.3 ± 47.6 883.8 ± 222.5##马钱苷元高剂量组(10 mg/kg) 146.5 ± 69.3* 767.9 ± 213.7*#F 2.989 9.512 0.043 7 9.17×10-5 P
2.3 分子对接
将马钱苷元和利多卡因(lidocaine)、普萘洛尔(propranolol)、胺碘酮(amiodarone)、维拉帕米(verapamil)与SCN5A、ADRB1、KCNH2 和CACNA1C 四个受体进行分子对接。配体与受体结合的构象越稳定能量越低,相互作用的可能性越大,结合能≤-1.2 kcal/mol 作为筛选标准,结合能≤-5.0 kcal/mol时则视为配体与受体有较好的活性[15]。
由图1 可知,马钱苷元和利多卡因、胺碘酮的结合能接近。马钱苷元和利多卡因均可与SCN5A 中93位丝氨酸(Ser)形成氢键(图2A 和2B);马钱苷元与KCNH2 中810 位天冬酰胺(Asn)和858 位异亮氨酸(Ile)形成氢键,胺碘酮与KCNH2 中810 位Asn 和854 位Ser 形成氢键(图2C 和2D)。结果表明马钱苷元与SCN5A 和KCNH2 均具有较好的结合能力,与前者的结合更稳定。
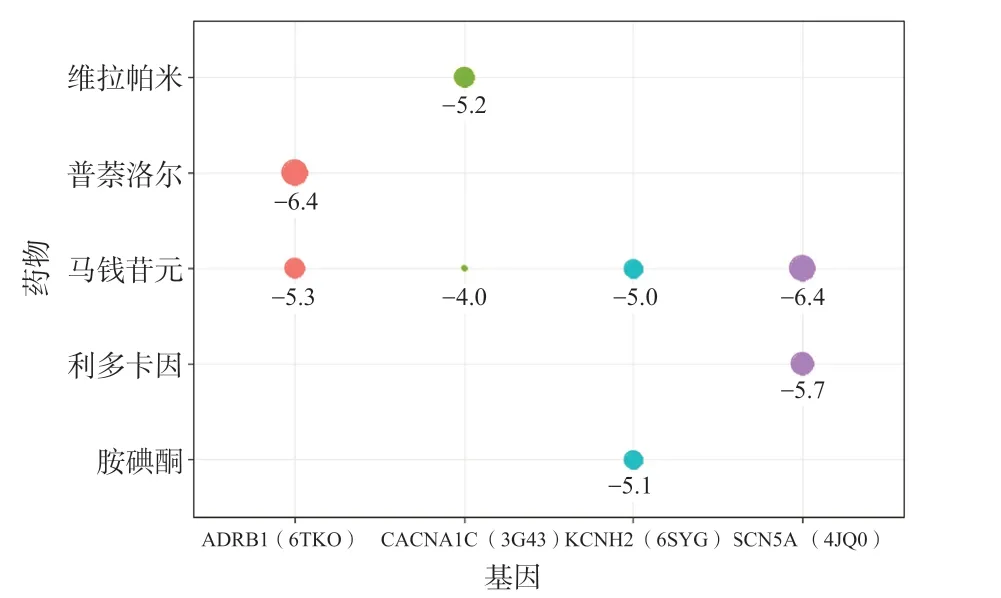
图1 分子对接结果气泡图Fig. 1 Bubble diagram of molecular docking

图2 药物与受体相互作用分析Fig. 2 The analysis of the interaction between drugs and receptors
3 讨论
从中医的角度来说,心律失常属于“心悸”“胸痹”“心痛”等范畴,多由于脏腑气血阴阳虚损、内伤七情、气滞血瘀交互作用致心失所养、心脉失畅而引起[16-17]。许多化学药品可诱导不同类型的心律失常,常用于制备快速性心律失常模型的药物有氯仿、乌头碱、氯化钡、哇巴因、异丙肾上腺素等[18]。氯仿作用于心肌细胞,使心室不应期不规则地延长、复极不均一性增加。其诱发室颤机制可能是刺激植物性神经及其递质释放或肾上腺髓质分泌大量儿茶酚胺,激活肾上腺素β 受体有关[19]。乌头碱诱发心律失常的机制较为复杂,可激活心肌细胞Na+通道,加速Na+离子内流,促使细胞膜去极化,形成一源或多源性异位节律而诱发心律失常[20]。本研究选择此两种模型作为基础探讨马钱苷元的抗心律失常作用。研究结果表明,马钱苷元高剂量(10 mg/kg)具有一定的抗心律失常作用,能明显降低氯仿所致大鼠的室颤发生率,对乌头碱所致大鼠室上性早搏也有预防作用,能延长室早潜伏期并缩短其持续时间,低剂量(1 mg/kg)时无明显作用。
目前已知心律失常相关基因有60 多个,单一基因的异常表达可引发多种心律失常,而同一种心律失常与多种基因相关[21]。本研究从已知的作用通路中分别选择SCN5A、 ADRB1、KCNH2、CACNA1C 作为分子对接的受体[22-26]。同时选择四类抗心律失常药物中的代表性药物(利多卡因、普萘洛尔、胺碘酮和维拉帕米)作为配体,与马钱苷元和受体对接的结果进行比较。发现马钱苷元与SCN5A、ADRB1 和KCNH2均有较好的结合能力,与SCN5A 的结合能最佳。SCN5A 基因编码的心脏Na+通道α 亚基(Nav1.5)是维持心肌细胞正常兴奋性不可或缺的关键蛋白[22-23]。马钱苷元可落入该蛋白“口袋”中,并通过1 位羟基与丝氨酸羟基形成的氢键,确保二者结合稳定。表明马钱苷元可能通过阻滞钠通道发挥抗心律失常作用。
4 结论
本研究通过药效学实验证明了马钱苷元抗心律失常的有效性,运用分子对接技术发现,马钱苷元与心律失常相关蛋白的结合位点和已上市药物相似,与Na+通道蛋白的结合能力最佳,为马钱苷元抗心律失常作用的开发提供了方向,但其作用机制还需进行进一步的实验验证。本课题组将针对心律失常不同作用通路的靶点继续进行定性和定量分析,以期验证马钱苷元抗心律失常的作用机制。

