量子化学计算法比较不同脂肪酸分子的反应活性位点
王淳纯,覃小丽,阚建全,刘 雄,索化夷,钟金锋
(西南大学食品科学学院,重庆 400715)
脂肪酸对人体有重要的生理功能,根据其碳链长度的不同可分为短链脂肪酸、中链脂肪酸、长链脂肪酸和超长链脂肪酸;根据其饱和度的不同可分为饱和脂肪酸、单不饱和脂肪酸以及多不饱和脂肪酸[1]。目前对于脂肪酸的研究主要集中在具体物质中脂肪酸的含量及其检测方法的分析,而对于脂肪酸的反应活性位点的研究还未涉及,脂肪酸反应活性位点预测可为揭示脂肪酸构效关系提供理论依据,同时对食品的油脂工业中关于脂肪酸的选择具有参考意义。
使用实验观测的方法很难对脂肪酸的反应活性位点进行精密预测,而量子化学计算对于反应活性位点的预测具有相当高的计算精度。量子化学可从微观角度,对稳定或不稳定的分子结构、性能及其结构与性能之间的关系,分子与分子之间的相互作用以及分子与分子之间的相互碰撞和反应等进行研究[2]。量子化学计算是根据量子化学理论,采用不同算法获得相应的量化参数,并以此解释或预测原子、分子和晶体的各种性质[3]。Soni等[4]利用量子化学计算对γ-油酸的结构和振动光谱进行了研究;Hassanzadeh等[5]使用量子化学计算法对橄榄中酚类化合物结构与抗氧化活性之间的关系进行了研究,并鉴定了橄榄中的抗氧化活性位点为C3—OH,均说明量子化学计算能够探究结构与活性的关系,并且已被广泛应用于食品研究领域中。密度泛函理论[6]是一种通过电子密度函数代替波函数作为基本量进行研究的一种量子力学方法,Gocen等[7]基于密度泛函理论在B3LYP/6-311++G(d,p)的理论水平上系统地研究了ω-6脂肪酸分子结构对量子化学描述符的影响,探讨了脂肪酸分子的熔点、能量等随链长及不饱和度的变化关系。脂肪酸的碳链长度和不饱和程度对脂肪酸的分子性质及生物活性有强烈影响[8],目前在脂肪酸与甘油的结合过程的研究中,对油脂合成机理的研究方法多采用对基因转录组的分析,而脂肪酸的反应活性位点预测对进一步揭示油脂合成途径以及对脂肪酸的选择具有指导意义。因此,为了进一步探究不同链长及不饱和度脂肪酸分子之间反应活性位点的区别,可采用量子化学计算方法进行研究,而目前还鲜见使用该方法对脂肪酸分子的不同结构对其反应活性位点的影响的相关研究。
Qin Xiaolin等[9]在对T1脂肪酶与脂肪酸特异性结合的研究中表明辛酸与T1脂肪酶结合的特异性常数最高,其值为1,而硬脂酸与T1脂肪酶结合的特异性常数最低,其值为0.08,阐述了不同脂肪酸与T1脂肪酶之间的结合活性。因此本研究选用6 种碳链长度以及不饱和度有差异的脂肪酸为研究对象,分别是辛酸(C8:0)、棕榈酸(C16:0)、硬脂酸(C18:0)、油酸(C18:1)、亚油酸(C18:2)、亚麻酸(C18:3),在密度泛函理论和量子化学计算的基础上对脂肪酸进行几何结构优化以及单点能计算,通过对定量分子表面分析预测6 种脂肪酸的反应活性位点,并比较不同链长及不同双键含量脂肪酸活性位点之间的差异,以期为脂肪酸与甘油结合过程的反应机理研究及脂肪酸的选择提供理论依据。
1 材料与方法
6 种脂肪酸的分子结构取自PubChem数据库,本实验所有对脂肪酸分子的结构优化及量子化学计算都在Gaussian 09[10]程序进行,GaussView 5.0.9用于结构可视化。通过构象搜索选取处于能量最低点的脂肪酸分子作为结构优化的初始结构,对初始结构的几何优化以及单点能的计算均采用m06-2x[11-12]理论方法,几何优化使用def2tzvp基组,单点能和溶剂效应的计算使用ma-def2tzvp基组。运用Multiwfn程序[13]对分子表面静电势[14]、平均局部离子化能(average local ionization energy,ALIE)[15]、前线分子轨道[16]以及简缩福井函数[17]进行计算,利用VMD可视化程序[18]作图,其中简缩福井函数的计算需要在自洽反映场和SMD隐式溶剂模型[19]下进行。
2 结果与分析
2.1 分子表面静电势分析

图1 优化结构图Fig. 1 Optimized fatty acid structure
由图1可知,6 种脂肪酸分子处于能量最低点时,碳链均处于弯曲状态,且不饱和脂肪酸均为顺式结构。对分子表面静电势进行分析可以得到分子表面的静电势极大值点和极小值点,图2表示出了脂肪酸分子表面静电势的极值点分布及其区域面积分布情况,表1列出了6 种脂肪酸分子的主要极值点大小,可以更好地对比不同链长及不饱和度的脂肪酸分子表面静电势极值点大小的异同,静电势极值点与以静电主导的弱相互作用强度有密切关系,可以初步预测出分子的反应活性位点。



图2 分子表面静电势分布图Fig. 2 Electrostatic potential distribution on the molecular surface
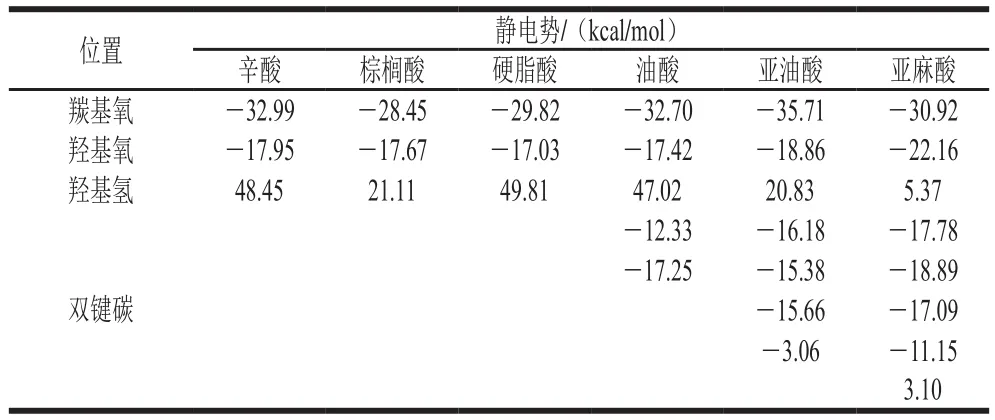
表1 6 种脂肪酸的极值点对比Table 1 Comparison of extremum points of six fatty acids
分子表面静电势图上颜色深浅反映静电势的强弱,红色区域表示静电势为正,蓝色区域表示静电势为负,橙色小球表示极大值点,青色小球表示极小值点,静电势值越负的地方所对应的原子越容易发生亲电反应,静电势值越正的地方所对应的原子越容易发生亲核反应[20]。由图2可知,脂肪酸分子的极小值点主要分布在分子中羧基基团中的氧原子及碳碳双键附近。其中静电势最小值点在羰基氧附近,6 种脂肪酸的静电势最小值分别为-32.99、-28.45、-29.82、-32.70、-35.71、-30.92 kcal/mol;其次是羟基氧,6 种脂肪酸中羟基氧的静电势值分别为-17.95、-17.67、-17.03、-17.42、-18.86、-22.16 kcal/mol,这是由于氧原子的电负性强于分子中的氢原子,所以使氧原子所含电子较多,从而呈现极小值点。对于不饱和脂肪酸而言,在每个双键附近均会出现极小值点,这些极小值点体现的是π电子云对静电势的负贡献。油酸含有一个双键,附近出现了2 个极小值点,其值分别为-17.25、-12.33 kcal/mol;亚油酸含有2 个双键,其中C12和C13之间的双键附近的一个极小值点较大,值为-3.06 kcal/mol,亚麻酸含有3 个双键,其中C15和C16之间的双键附近也有一个极小值点较大,这是因为这些极小值点靠近羟基氢,而羟基氢的正电性强,使其极小值点的值偏大。6 种脂肪酸分子的静电势极大值点在分子中主要分布于氢原子附近,因为氢原子电负性弱,致使周围所含电子较少。6 种脂肪酸的静电势最大值点除了亚麻酸均在羟基氢原子的附近,其中辛酸、硬脂酸和油酸的静电势最大值在48.43 kcal/mol左右,比其他极大值点都高出几倍,其次是羰基碳以及α-H附近有极大值点存在,可能是由于氧原子的电负性太强,吸电子能力强,从而使得羰基碳的静电势呈现正值。对于辛酸分子,其表面的H16附近没有极大值点出现,这可能是由于羟基氢的正电性太强,使其附近一大片分子表面上的静电势都较大,淹没了H16附近区域,因此H16较弱的正电性无法造成极大值点[2]。棕榈酸和亚油酸的静电势最大值点的值分别为21.11 kcal/mol和20.83 kcal/mol,而亚麻酸羟基氢的静电势值为5.37 kcal/mol和3.74 kcal/mol,其静电势最大值点在α-H附近,其值为15.18 kcal/mol,这是由于碳链的弯曲,羟基氢靠近碳碳双键,使得其静电势极大值点变小。根据图2中的分子表面静电势的区域分布面积图可知,分子表面的静电势正值区域以及接近0的区域占大部分面积,负值区域是由羧基氧的明显负电荷造成的。
从分子结构上看,部分电子由于诱导效应和共轭效应的影响到羧基中的羰基氧上,所以静电势为最小;类似地,羟基氢由于氧原子吸电子诱导效应及羰基吸电子共轭效应,使其静电势值为最大。Garzón等[21]在对香豆酸活性位点的研究中表明羟基易受到亲核试剂的进攻,这与本实验计算出羟基氢静电势值为最大值的结论吻合,赵雅静[2]在使用静电势方法对植物甾醇反应活性位点的研究中也表明羟基氢对应的极大值点是最大值点,其值为44.98 kcal/mol,该结论与本实验中观察脂肪酸的结果类似。
因此,根据分子表面静电势分析结果可知,脂肪酸分子羧基中的羰基氧和羟基氧附近负电荷集中,其中羰基氧静电势最小,容易被显正电性的亲电试剂进攻;羧基中的羟基氢、羰基碳以及α-H附近正电荷集中,其中除了亚麻酸,其他5 种脂肪酸皆是羟基氢静电势最大,容易被显负电性的亲核试剂进攻;且不饱和脂肪酸中,在每个双键附近也存在静电势极小值点。
2.2 ALIE分析

图3 6 种脂肪酸的ALIE分布图Fig. 3 Average local ionization energy of six fatty acids
由图3可知,ALIE可用于考察分子亲电反应位点以及分子活性,ALIE是指在一个分子体系内,在空间某一点移走一个电子所需要的平均能量[22],由于ALIE值描述的是对电子的约束能力,因此其只能用于分析亲电反应。图3中蓝色的点表示ALIE的极小值点,其值越小,该点附近的电子被束缚得越弱,电子活性越强,越容易发生亲电反应[23]。可以看出,对于饱和脂肪酸,最小值点均出现在羧基基团附近,辛酸、棕榈酸和硬脂酸的ALIE最小值分别是11.68、11.81、11.78 eV;对于不饱和脂肪酸,油酸和亚油酸的羧基基团附近会出现极小值点,其值分别为11.80 eV和11.56 eV,而亚麻酸的羧基基团附近无较小的极小值点,且亚油酸羧基基团附近的ALIE值与饱和脂肪酸相比有减小的趋势,但是不饱和脂肪酸的碳碳双键附近出现的极小值点更小,且每个双键附近会出现2 个极小值点,油酸双键附近的ALIE极小值点为9.14 eV和9.75 eV,亚油酸双键附近的ALIE极小值点为9.28、9.72、9.70 eV和10.00 eV,亚麻酸双键附近的ALIE值为9.23、9.05、9.19 eV和9.65 eV,由此可见亚麻酸由于碳链的弯曲,双键靠近羟基氢,使得其C12和C13之间的双键及C15和C16之间的双键均只出现一个极小值点。因此对于饱和脂肪酸,ALIE的最小值点在羧基基团附近;而对于不饱和脂肪酸,最小值点均在碳碳双键附近,说明碳碳双键附近的电子活性比羧基基团附近的电子活性更强,更容易发生亲电反应。
从整个分子体系看,综合分子表面静电势分析以及ALIE结果可知,对于饱和脂肪酸,羧基中的羰基氧和羟基氧附近负电荷集中,容易被显正电性的亲电试剂进攻,羧基中的羟基氢、羰基碳以及α-H附近正电荷集中,容易被显负电性的亲核试剂进攻;对于不饱和脂肪酸而言,与饱和脂肪酸所不同的是,碳碳双键比羧基基团更容易发生亲电反应。
2.3 前线分子轨道分析


图4 6 种脂肪酸的前线分子轨道结构图Fig. 4 Frontier molecular orbital of six fatty acids
如图4所示,其中蓝色和绿色表示轨道波函数的相位,绿色为正,蓝色为负。前线轨道包括最高已占轨道(highest occupied molecular orbital,HOMO)和最低未占轨道(lowest unoccupied molecular orbital,LUMO),其中HOMO对于电子束缚力较弱,具有给电子性质,EHOMO表示分子给电子的能力,其值越大代表分子给电子能力越强;LUMO对于电子的亲和力较强,具有电子接受体的性质,ELOMO表示分子吸电子能力,其值越小代表分子吸电子能力越强,且前线分子轨道能级差ΔE能垒值越小,则表征分子中电子越容易发生跃迁,反应活性就越强[24]。
由图4可以看出,辛酸的HOMO轨道主要分布在碳链和氧原子附近,表明该区域容易发生亲电反应,而LUMO轨道主要分布在羟基氢处,表明该区域容易发生亲核反应;棕榈酸的HOMO轨道主要分布在碳链以及羰基氧原子附近,LUMO轨道分布在羰基和羟基氧附近,而硬脂酸的的HOMO轨道主要分布在碳链附近,LUMO轨道主要分布在羟基处,表明该区域容易受到亲核试剂的攻击发生亲核反应。对于油酸,HOMO轨道出现在双键处,表明碳碳双键区域易发生亲电反应,LUMO轨道主要出现在羧基附近;对于亚油酸和亚麻酸,HOMO轨道均主要出现在双键附近,羧基基团附近无前线轨道,说明对于亚油酸和亚麻酸而言,亲电反应活性位点是双键。对比3 种不饱和脂肪酸可以看出,随着不饱和度的增加,前线分子轨道能级差ΔE能垒值越来越小,ΔE从8.062 eV逐渐减小至7.869 eV,说明对于链长相同的脂肪酸分子,不饱和度越大其反应活性越强。常瑞等[25]对N-羟乙酰神经氨酸分子的结构分析显示出LUMO轨道主要集中在羧基中的羰基区域;Zhao Gang等[26]对胶原蛋白氨基酸的轨道分析也表明LUMO轨道主要集中在羧基区域;Gocen等[7]在对长链不饱和脂肪酸结构与性质的研究中表明对于链长相同的脂肪酸,随着不饱和度的增加分子能隙有减小的趋势,与本实验的结论类似。
综上所述,对于饱和脂肪酸,其亲电反应活性位点是氧原子,其中辛酸和硬脂酸的亲核反应位点在羟基氢原子上;对于不饱和脂肪酸,油酸的亲电反应活性位点在碳碳双键,亲核反应活性位点在氧原子,随着双键数量的增多,不饱和脂肪酸的反应活性位点均在碳碳双键。
2.4 简缩福井函数分析

表2 6 种脂肪酸简缩福井函数值Table 2 Condensed Fukui function values of six fatty acids
简缩福井函数能对分子中的原子定量分析其亲电亲核反应活性,f-和f+可分别表征亲电活性和亲核活性,一个分子的反应活性位点上福井函数值越大,其越可能是相应类型反应的活性位点[27-28]。选用正己烷[29-30]作为溶剂,对6 种脂肪酸进行简缩福井函数计算,表2列出了6 种脂肪酸中一些主要原子的f-值和f+值。由表2可知,对于辛酸分子,羰基氧原子的f-值最大,其值为0.371 9,其次是羟基氧,其值为0.128 1,说明氧原子附近的负电荷集中,观察辛酸分子表面的f+值可知,f+的最大值0.402 7在羟基氢上,说明辛酸分子的亲核反应位点是羧基基团中的羟基氢,与分子表面静电势分析结论一致;对于棕榈酸和硬脂酸,可见其羧基基团附近的f-值都很小,说明对于饱和脂肪酸,随着碳链长度的增加,亲电反应活性逐渐降低,其中硬脂酸的羟基氢原子附近的f+值较大,这和前线分子轨道分析结论一致,说明硬脂酸的亲核反应位点在羟基氢原子上。对于不饱和脂肪酸而言,f-较大值均出现在碳碳双键附近,羧基基团附近的值均偏小,因此在不饱和脂肪酸中,双键的反应活性高于羧基基团,这和ALIE以及前线分子轨道分析的结论具有良好一致性。
3 结 论
本实验采用量子化学计算的方法对6 种脂肪酸分子的分子表面静电势、ALIE、前线分子轨道以及简缩福井函数进行分析从而预测其反应活性位点。静电势分析结果表明6 种脂肪酸分子表面的静电势最小值点主要位于羧基基团的羰基氧,最大值点除亚麻酸外均位于羟基氢,亚麻酸的最大值点位于α-H,不饱和脂肪酸每个双键附近也会出现静电势极小值点;ALIE分析结果表明饱和脂肪酸的最小值点出现在羧基基团附近,不饱和脂肪酸的最小值点出现在双键附近;前线分子轨道分析结果表明对于3 种饱和脂肪酸,HOMO轨道主要出现在碳链附近,LUMO轨道出现在羧基附近;对于油酸,HOMO出现在碳碳双键附近,LUMO出现在羧基;对于亚油酸和亚麻酸,HOMO均出现在双键附近,而羧基基团附近无前线轨道出现,且对于链长相同的脂肪酸而言,随着不饱和度的增加,前线分子轨道能级差ΔE能垒值越来越小;简缩福井函数分析结果可知,辛酸中氧原子的f-值较大,羟基氢附近的f+值较大,棕榈酸和硬脂酸的氧原子f-值均较小,其中硬脂酸的羟基氢附近的f+值较大,不饱和脂肪酸中,双键碳的f-值都比其他原子大。因此,结合4 个分析结果可知,辛酸的氧原子附近负电荷集中,易被亲电试剂进攻,其羟基氢附近正电荷集中,易被亲核试剂进攻,硬脂酸的羟基氢也易被亲核试剂进攻,而随着饱和脂肪酸链长的增加,棕榈酸和硬脂酸的羧基基团附近几乎不发生亲电反应;对于不饱和脂肪酸,其中的油酸的亲核反应活性位点在氧原子,亲电反应活性位点在碳碳双键,亚油酸和亚麻酸的反应活性位点均在碳碳双键,对于链长相同的脂肪酸分子而言,随着不饱和度的增加,脂肪酸的反应活性逐渐增强。本实验从微观结构层面比较了具有不同链长及不饱和度脂肪酸的反应活性位点之间的差异,可用于加深对不同脂肪酸的结构与性能关系的理解,也为食品油脂工业中关于脂肪酸的选择提供了理论依据。

