强化剂量阿托伐他汀对STEMI患者直接PCI术后对比剂肾病的预防效果评价
许官学,张巍,王正龙,马懿,马肃爽
(1.遵义医科大学附属医院心血管内科,贵州 遵义 563000;2.威海市中心医院心血管内科,山东 威海 264400)
急性ST段抬高型心肌梗死(acute ST segment elevation myocardial infarction,STEMI)为由冠状硬化斑块破裂形成闭塞性血栓引起的心血管意外事件,是威胁中老年人群生命安全的重要疾病,也是急诊患者的常见疾病之一。开通梗塞相关动脉(infarct related artery,IRA)的再灌注治疗是治疗STEMI的核心手段,主要包括溶栓治疗和经皮冠状动脉介入(percutaneous coronary intervention,PCI)治疗,其中在时间窗内行直接PCI已成为临床指南中推荐的STEMI患者开通IRA首选再灌注治疗方案[1]。但是,随着行急诊直接PCI治疗病例数量的不断增加,复杂的介入手术使术中对比剂特别是碘对比剂的使用量也不断增加,导致对比剂肾病(contrast induced nephropathy,CIN)的病例在临床越来越多见。关于CIN的报道在1954年首次出现, 其发病率为3%~10%[2],其它研究[3]报道了更高的发病率。目前,CIN已成为医源性肾功能损害的三大病因之一,不仅会延长住院时间、增加医疗费用、影响生活质量,而且会提升患者血液透析和死亡的风险[4]。由于CIN的发病机制不明确,故预防和治疗方案比较有限,充分水化和减少对比剂用量是目前CIN预防中获得证据支持最多的方法[5]。但针对慢性肾脏病、充血性心力衰竭等特殊患者人群,不恰当的水化反而会提升PCI术后肾功能损害风险[6]。因此,近年来临床一直致力于寻找更加有效的CIN预防方案,阿托伐他汀是其中研究较多的药物。然而,针对阿托伐他汀的用量、应用时机、应用方式及预防效果等方面,学术界仍然存在着严重分歧,至今未能达成标准化的用药方案,故本研究采用前瞻性随机对照的方法针对强化剂量阿托伐他汀对STEMI患者直接PCI术后CIN的预防效果进行了评价。现将结果报告如下。
1 资料与方法
1.1 一般资料
选取2016年1月至2018年12月在遵义医科大学附属医院心内科急诊行直接PCI治疗的300例STEMI患者作为研究对象,根据治疗方案不同分为研究组和对照组,每组各150例。本研究方案经医院医学伦理委员会审查通过,患者知情同意。纳入标准:(1)患者均符合中华医学会心血管病学分会制订的《急性ST段抬高型心肌梗死诊断和治疗指南(2015年更新)》中的STEMI诊断标准[7];(2)患者发病12 h内急诊行直接PCI治疗开通IRA;(3)临床资料完整,且术后住院时间长于3 d。 排除标准:(1)合并急性感染性疾病、恶性肿瘤、脑卒中、血液系统疾病及PCI术前已确诊原发性肝肾功能不全的患者;(2)具有PCI治疗禁忌、需要接受冠脉旁路移植术、造影剂过敏的患者;(3)入组前30 d内有他汀类药物应用史、对他汀类药物过敏或有应用禁忌的患者;(4)妊娠期或哺乳期患者。
1.2 方法
1.2.1 CIN诊断标准 参照欧洲泌尿系统放射学会(ESUR)对比剂安全委员会(CMSC)制定的《对比剂肾病指南》中的CIN标准[8]进行诊断:在除外血栓形成、缺血、肾毒性药物应用等其他影响肾功能原因的前提下,血管内注射对比剂3 d内出现血清肌酐(Scr)水平较基线水平升高超过25%或绝对值升高超过44 μmol/L。
1.2.2 治疗方法 患者入院后均急诊检查心肌酶、心肌标志物、肝肾功能、凝血功能等指标,做好PCI治疗准备,PCI治疗中选用的造影剂均为非离子等渗造影剂碘海醇,PCI治疗操作均根据中华医学会心血管病学分会介入心脏病学组、中国医师协会心血管内科医师分会制订的《中国经皮冠状动脉介入治疗指南(2016年更新)》[9]。研究组患者于PCI术前口服阿托伐他汀(辉瑞制药有限公司)80 mg,对照组患者术前不给予阿托伐他汀。两组患者术后均给予口服阿司匹林(拜耳医药保健有限公司)联合氯吡格雷(赛诺菲(杭州)制药有限公司)或替格瑞洛(AstraZeneca AB公司)进行双联抗血小板12个月,同时给予口服阿托伐他汀20 mg/d,连续3 d。
1.2.3 肾功能指标检测血清 CysC水平的检测采用免疫比浊法,Scr水平的检测采用酶法,BUN水平的检测采用尿素酶耦联法,Ccr根据体重、年龄及Scr水平进行计算,计算公式为:男性Ccr(mL/min)=[(140-年龄)×体重(kg)]/[72×Scr(mg/dL)],女性Ccr为按上述公式计算后结果乘以0.85。
1.3 观察指标
(1)基线资料:通过查阅住院病历和PCI手术记录对两组患者的年龄、性别、体重、吸烟史、合并基础疾病、造影剂用量、血管病变数目、左室射血分数(LVEF)、低密度脂蛋白胆固醇(LDL-C)及急救期间应用血管紧张素转化抑制剂/受体拮抗剂(ACEI/ARB)、利尿剂等基线资料进行调查和对比。(2)CIN发生率=CIN例数/总例数(×100%)。(3) 肾功能指标:术前即刻及术后3 d血清胱抑素C(CysC)、肌酐清除率(Ccr)、Scr及血尿素氮(BUN)水平。
1.4 统计学分析
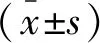
2 结果
2.1 两组患者基线资料比较
两组患者基线资料比较,差异无统计学意义(P>0.05)。见表1。
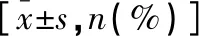
表1 两组患者基线资料的比较
LVEF:左心室射血分数;LDL-C:低密度脂蛋白C;ACEI:血管紧张素转化酶抑制剂;ARB:血管紧张素受体阻断剂。
2.2 两组患者CIN发生率的比较
研究组和对照组患者分别有9例(6%)和25例(16.67%)发生CIN,差异有统计学意义(χ2=8.492,P=0.004)。
2.3 两组患者PCI术前、后肾功能指标的比较
两组患者PCI术前各项肾功能指标比较,差异无统计学意义(P>0.05)。术后3 d,患者血清CysC、Scr、BUN水平较术前上升(P<0.05),且研究组低于对照组(P<0.05);Ccr水平较术前下降(P<0.05),且观察组高于对照组(P<0.05)。见表2。
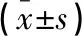
表2 两组患者PCI术前、后肾功能指标的比较
3 讨论
近年来,对CIN预防治疗方案进行了广泛的摸索,尼可地尔、重组人脑利钠肽、左卡尼汀、维生素C、曲美他嗪等多种药物得到了尝试性的临床应用,但其预防效果仍然无法得到有力的临床证据支持。
相对而言,阿托伐他汀的临床应用更加广泛,目前的主要问题是在应用方案和预防效果方面缺乏共识[10]。PCI术常规的阿托伐他汀治疗方案是术后3 d内连续应用10~20 mg/d的剂量,但是,研究发现合理调整阿托伐他汀的给药剂量和时间可能会提升对CIN的预防效果,有研究[11]报道称,应用40 mg/d阿托伐他汀在预防CIN方面的效果与水化治疗相当,在PCI围术期于常规水化基础上应用40 mg/d阿托伐他汀预防CIN的效果优于常规剂量应用阿托伐他汀。但也有学者通过临床研究[12]认为,40 mg/d阿托伐他汀仅在抗炎方面效果优于常规剂量,而在CIN预防方面并未增加临床受益,因此,学者开始分析和评价应用更高强化剂量阿托伐他汀预防CIN的可行性,有研究[13]报道,应用80 mg阿托伐他汀预防CIN的效果优于常规剂量,故有学者[14-15]提出了PCI术前24 h、术前2 h、术后连续3 d分别口服80 mg、80 mg、40 mg的方案和术前12 h、术前2 h、术后3 d分别口服80 mg、40 mg、40 mg的方案,均取得了较好的应用效果。本研究采用术前80 mg强化剂量应用联合术后3 d常规剂量应用的强化治疗方案,主要原因在于,虽然相关研究提示了高剂量阿托伐他汀可能具有更好的预防CIN效果,但更高级别的循证医学证据[16]认为,高剂量阿托伐他汀的预防性治疗仍需更多的研究来确定最佳预防性治疗方案。而且相关评价研究[17]结果也显示,对于PCI术前已应用大剂量阿托伐他汀的患者,围手术期再次追加阿托伐他汀用量并不能降低CIN发生率,故本研究仅在PCI术前单次强化了大剂量阿托伐他汀,并未在术前再次追加用药,也未调整术后用药剂量。
本研究发现,对于急诊行直接PCI治疗的STEMI患者术前应用强化剂量阿托伐他汀治疗,能够降低其CIN发生率,缓解血管内应用造影引起的肾功能损害,取得了较好的效果。虽然CIN的发病机制和阿托伐他汀预防CIN的确切机制尚未完全明确,但分析产生这一结果的原因[18-19],可能包括以下几方面:(1)阿托伐他汀对于应用对比剂患者的肾保护作用具有明显的剂量依赖性且与给药时间密切相关,通过PCI术前给予强化剂量阿托伐他汀,确保了PCI术中患者具有较高的阿托伐他汀血药水平,给药剂量和给药时间方案均优于常规的术后常规剂量方案,更加有效地发挥了阿托伐他汀的肾保护作用;(2)PCI术前短期强化阿托伐他汀,能够降低患者的血清C反应蛋白(CRP)、内皮素-1、白细胞介素(IL)-6、肿瘤坏死因子(TNF)-α水平和肾组织中的IL-1β、IL-6、IL-10、前列腺素E2、CRP、TNF-α水平,下调核转录因子κB表达,抑制转化生长因子(TGF)-β1/Smad2信号通路,从而发挥抗炎、保护血管内皮功能的效果;(3)急诊直接PCI术前应用阿托伐他汀,可通过提升患者机体的超氧化物歧化酶及一氧化氮合酶水平、减少丙二醛及氧化低密度脂蛋白等氧化产物堆积,缓解器官组织氧化应激损害,同时可对血脂代谢、脂质运载蛋白表达等发挥调节作用,进而降低血液黏度、稳定血液动力学指标,改善肾组织的血流灌注;(4)动物模型研究[20]结果显示,阿托伐他汀改善肾损伤的作用机制可能还包括上调腺苷酸活化蛋白激酶、沉默信息调节因子1表达等。总之,阿托伐他汀预防CIN的机制是较为复杂,还需要进一步的基础研究予以讨论和分析。
综上所述,对急诊行直接PCI的STEMI患者,采用术前强化剂量负荷联合术后常规剂量给药的阿托伐他汀治疗方案,可有效降低CIN的发生率,缓解血管内应用造影剂导致的肾功能损害。

