术前口腔管理对肝癌患者肝切除术后手术部位感染的影响①
李 静,徐 玲
(上海交通大学医学院附属新华医院崇明分院肝胆外科,上海202150)
肝细胞癌(Hepatocellular carcinoma,HCC)是最常见的肝脏恶性肿瘤,据估计,全世界每年约有70万人死于肝癌[1]。虽然肝硬化患者肝切除术后的死亡率高达10%~30%,但不断完善的手术方法和术后管理改善了患者的预后[2]。然而,肝癌肝切除术后并发症的高发生率仍然是一个未被解决的重要临床问题。特别是手术部位感染(surgical site infections,SSI)是一种危害严重且花费较高的并发症[3-4]。肝胰胆手术后SSI发生率为3.24%~7.04%,肝切除术后SSI发生率为3.1%~25.2%[5-6]。此外,在肝硬化或慢性肝功能障碍患者腹部外科手术后的细菌感染率为10%~30%[7]。
围手术期口腔管理对术后肺炎的预防作用已得到较多研究的证实[8-9]。口腔管理对预防SSI的作用,特别是口腔细菌转移后影响肠道菌群、通过血管和淋巴管转移侵袭远端器官等机制正受到越来越多的关注[10]。围手术期口腔管理也被证明可以减少结直肠癌和口腔癌患者的SSI[10-11]。本研究旨在通过回顾性分析探讨术前口腔管理对肝癌患者行肝切除术后SSI的影响。
1 资料与方法
1.1 研究对象 纳入2015年1月-2019年12月在上海交通大学医学院附属新华医院崇明分院肝胆外科进行肝癌肝切除术的334例患者的病例资料。排除标准:(1)并发糖尿病者;(2)急诊手术者;(3)血浆白蛋白<3.5 g/dL的患者;(4)同时进行结肠直肠切除或造口闭合等手术的患者。
1.2 引流和抗感染常规处理 在右侧膈下间隙或切除肝实质间隙置入1~2条闭合引流管。术后第3天或第4天确认无再出血或胆漏后拔除引流管。在术后2 d内,常规给予舒巴坦/氨苄青霉素(SBT/ABPC)预防感染。在皮肤切开前30 min内给予SBT/ABPC 1.5 g,术中每3小时给予相同剂量。
1.3 常规口腔管理内容 患者在肝切除术前2周接受牙科医生和护士进行的口腔管理干预。包括口腔自我管理指导、拔除感染的牙齿、清除牙斑、牙石和舌苔,清洁假牙。自我管理指导包括刷牙、用牙线清洁牙齿、刷舌头、假牙和漱口。这个口腔管理项目的目的主要是清除感染的牙齿和提高患者对菌斑控制的意识。
1.4 数据的采集 采集每例患者的资料,包括:(1)人口学和疾病一般情况资料(性别、年龄、吸烟史、饮酒、美国麻醉医师协会(ASA)身体状况分类、体重指数、类固醇治疗情况和肝脏其他疾病;(2)术前因素:Child-Pugh分级[12]、Karnofsky功能状态评分(Karnofsky performance status,KPS)[13]、Scheuer分级,吲哚菁绿15 min滞留率(ICG-15)、第1秒用力呼气量/用力呼气量百分比(FEV1.0/FCV%)、血红蛋白(Hb)、白蛋白;(3)术前干预:口腔管理、呼吸康复训练;(4)围手术期因素:痰、胆汁或腹水的细菌感染情况、切除范围、腹腔镜或开放性手术、失血、手术时间和输血;(5)术后因素:住院时间。
1.5 肝纤维化评分 采用Scheuer分级进行肝纤维化评分:0分:无汇管区纤维化扩大;1分:限局窦周及小叶内纤维化;2分:汇管区纤维化,纤维间隔形成,小叶结构保留;3分:纤维间隔伴小叶结构紊乱,无肝硬化;4分:早期肝硬化。
1.6 考察指标 SSI是根据2017年版美国疾病预防控制中心(CDC)手术部位感染预防指南[14]和2001年卫生部《医院感染诊断标准(试行)》[3]中手术部位感染的诊断标准,手术部位感染包括术后30 d内任何表浅切口感染、深部切口感染及器官腔隙感染。
1.7 统计学分析 采用SPSS 22.0软件进行统计分析。符合正态分布的连续变量采用-x±SD表达,采用独立样本t检验比较组间差异;计数资料采用频数(百分比)[n(%)]表示,采用χ2检验或Fisher精确检验比较组间差异,分析各变量与SSI的相关性。所有与SSI相关的变量都被引入到多元Logistic回归模型中,采用逐步向前方法剔除不符合模型的变量。P<0.05为差异具有统计学意义。
2 结果
2.1 纳入病例的一般情况 共纳入334例患者的病例资料,其中男性268例,女性66例,平均年龄(66.6±10.7)岁。其中肝细胞癌194例,转移性肝癌74例。
2.2 发生SSI的单因素分析 28例(8.4%)患者发生SSI,包括16例(4.8%)浅表SSI和12例(3.6%)器官/间隙SSI。在单因素分析中,缺乏术前口腔管理干预(P=0.005)和开放性手术(P=0.004)与发生SSI显著相关。发生SSI的患者住院时间明显长于无SSI患者(P<0.001)。见表1。
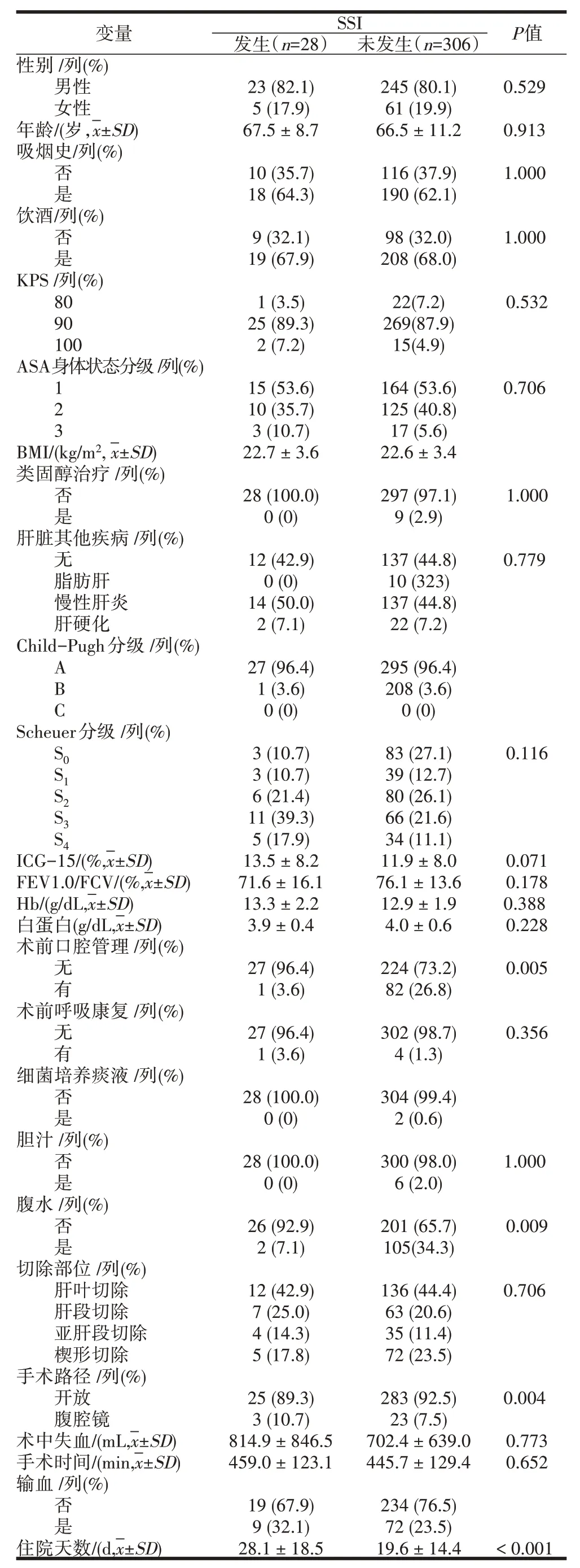
表1 发生SSI的单因素分析
2.3 发生SSI的多因素Logistic回归分析 采用逐步向前的Logistic回归模型结果显示,细菌性腹水感染(OR:13.72,P=0.014)、术前缺乏口腔管理(OR:10.17,P=0.035)、严重肝纤维化(OR:2.76,P=0.025)是患者术后发生SSI的独立危险因素。见表2。

表2发生SSI的多因素Logistic回归分析
3 讨论
据报道肝切除术后SSI的发生率为3.1%~25.2%[15-16],本组资料中SSI发生率为8.4%,与之前的研究较为接近。
口腔内的病原微生物可引起多器官感染,影响多种疾病。口腔微生物直接转移可导致吸入性肺炎或改变肠道菌群导致肠屏障功能障碍;血管内牙源性细菌、内毒素通过血管或淋巴管侵袭远端器官等,均可以导致术后并发症的发生和发展。通过口腔管理干预预防术后并发症已越来越受到重视。围手术期口腔干预对术后肺炎具有预防作用[8-9]。最新研究强调应在手术前预处理包括口腔在内的远端器官的感染性病变[17]。Hiroshi等[18]报道围手术期口腔管理降低了结直肠癌手术后的SSI风险,缩短了术后住院时间。本研究多因素Logistic结果显示,未接受术前口腔管理干预是术后发生SSI的独立危险因素。
据报道,肝切除术后SSI的多种危险因素包括血清天冬氨酸转氨酶水平、丙氨酸转氨酶水平、血小板计数、白蛋白、失血、输血、手术时间、疾病、Child-Pugh分级、ICG-15、外科手术、ASA得分、肝切除狭窄程度、腹水和肝纤维化程度等[16,19-20]。特别是晚期肝纤维化或肝硬化患者的术后SSI和并发症发生率更高[20]。在本研究中,严重的肝纤维化是术后SSI和并发症的显著危险因素。有研究推测肝硬化患者存在免疫防御机制不足,如网状内皮系统功能障碍、粒细胞功能障碍、补体浓度降低、细胞免疫功能改变等,这些免疫功能的下降可能是导致术后SSI的中间效应[21]。
肝脏切除术后常见的并发症是持续的胸腔积液和腹水,发生率为5%~56%[10,20]。本研究术后主要并发症为腹水(8.4%),与上述报道相似。术后腹水常发生在肝功能储备下降和术后住院时间延长的患者。据报道术后腹水患者腹腔内感染发生率为17.6%,而无术后腹水患者腹腔内感染率仅为4.8%[22];有感染腹水患者的伤口感染率为40.4%,无感染腹水患者的伤口感染率为25.0%,腹水中术后耐甲氧西林葡萄球菌感染是一种潜在的致命的医院并发症[19]。本研究结果表明,腹水细菌感染、术前缺乏口腔管理干预和严重肝纤维化是患者术后发生SSI的独立危险因素。这表明术前口腔管理可以降低接受肝切除术的HCC患者发生SSI的风险。
本研究受回顾性、非匹配的设计限制,不能对牙周病、龋病、口腔卫生等牙科因素进行分别检验。虽然通过多因素分析尽可能地降低混杂因素的影响,但不能完全排除偏倚。今后将考虑进行大规模的前瞻性队列研究,以评估术后SSI和并发症的预测因素。

