切割与射频对风湿性二尖瓣病变合并房颤的疗效
马杰 赵曙光 张文立 高伟年 于丁 陈子英
心脏瓣膜疾病尤其是二尖瓣病变,往往继发心房颤动、左心房血栓形成、栓子脱落可导致栓塞等并发症[1,2],有研究报道在二尖瓣手术中有40%~60%的患者可以合并心房颤动[3]。对于心房颤动的外科治疗,人们从未停止过对其探索,手术方式也经历了不断改进和完善。迷宫手术(Cox maze)是外科治疗心房颤动的公认术式[4],目前Cox maze术式经历了Ⅰ~Ⅳ型的不断改良, 其中以“切+缝”为基础的 Cox maze Ⅲ型手术治疗心房颤动的治愈率高达 90%以上,是公认的治疗心房颤动的金标准[5]。然而针对Cox maze Ⅲ型手术的耗时长及潜在心肌损伤以及因此诱发的炎症“风暴”研究甚少,目前射频消融Cox maze Ⅳ型手术已在国内外绝大部分心脏中心常规开展[6]。鉴于近年微创瓣膜手术下简化左侧射频消融(mini maze)治疗房颤取得了良好效果[7],本研究采用“切+缝”为主的方式开展简化左侧maze Ⅲ (SLM Ⅲ)型手术与射频Cox maze Ⅳ(CM Ⅳ) 型手术进行比较,重新评估SLM Ⅲ型手术的安全性及心肌损伤和炎性因子水平,为外科提供更多的治疗选择。
1 资料与方法
1.1 一般资料 选取2013年1月至2018年7月我院风湿性二尖瓣病变合并房颤的患者21例,术中二尖瓣置换手术同时实施了SLMⅢ型手术,同期1∶1筛选出临床资料较匹配23例患者行CMⅣ型手术,2组患者均经医院伦理委员会批准并签署患者知情同意书。入组标准:风湿性二尖瓣病变合并心房颤动,手术由同一术者完成。出组标准:联合瓣膜病变,合并冠心病,合并先天心心脏畸形,合并感染心内膜炎。依据 24 h动态心电图确诊心房颤动。阵发性心房颤动与持续性房颤的时间界限为7 d,心房颤动持续时间超过1年者定义为慢性持续性房颤。超声心动图检测二尖瓣狭窄或关闭不全程度、左心房内径(LAD)、左心室舒张末期内径(LVEDD)、左心室收缩末期内径(LVESD)、左心室射血分数(LVEF)。冠脉CTA及冠脉造影排除冠心病。见表1。
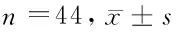
表1 2组患者临床资料一般资料
1.2 手术方法
1.2.1 SLM Ⅲ型手术:患者静吸复合麻醉,双腔气管插管。胸部正中切口。采用浅低温(32~34℃)体外循环下上下腔及升主动脉引流与灌注。20 min冷血顺行灌注行心肌保护1次。充分房间沟、上下腔静脉心包反折,上下腔及横窦套带便于牵拉显露。SLM Ⅲ型手术线路如下:于房间沟后方约1~2 cm切开左心房侧壁,向下延伸至距二尖瓣环2~3 cm,向上延伸切口至上腔静脉后方(线路1)。于距离二尖瓣环2~3 cm延伸做杯状切口至左心耳部(线路2)。湿纱布包裹牵拉心脏暴露并切除左心耳,切断mashall韧带,带毡片3-0prolene线褥式缝合对齐并固定切口位置(线路3),牵拉横窦套带做左心房顶至上腔静脉后方切口(线路4)。至此完成了包括双侧肺静脉及左心房后壁的左心房大部环形隔离,采用单极射频消融线路2至二尖瓣环之间的左心房峡部(线路5),应用3-0 prolene在牵拉暴露下连续缝合各切口,要求缝合均匀、抽紧缝线以防切口渗血。术毕常规于右心室表面安置心脏起搏导线。见图1。
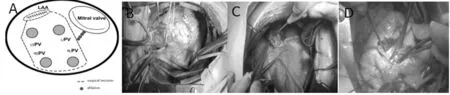
图1 SLM Ⅲ型手术示意图及操作步骤;LAA=左心耳;Mitral valve=二尖瓣;LSPV=左上肺静脉;LLPV=左下肺静脉;RSPV=右上肺静脉;RLPV=右下肺静脉;A SLM Ⅲ型手术示意图;B 心脏游离暴露; C 左心耳切除;D 缝闭切口
1.2.2 CM Ⅳ型手术:患者平卧位正中开胸,建立体外循环后阻断上下腔静脉,CM Ⅳ型手术分左右双侧心房操作,右侧心房消融及切口路线包括,垂直于右侧房室沟三尖瓣前叶瓣环2~3点位置做一斜切口,该切口距离瓣环约1.5 cm, 采用单极消融笔进行补充消融,该切口下端越过界嵴。应用双极射频消融钳分别消融上下腔静脉,切除右心耳,经心耳向斜切口的游离壁消融,距离切口约2 cm。经右心耳底部向三尖瓣环9∶00~10∶00双极消融,单极补充消融。左侧消融路线包括,游离并切开房间沟,游离下腔静脉心包反折,双极射频分别消融右侧及左侧肺静脉,消融左心耳基底部,经房间沟入路经左房峡部向二尖瓣后瓣环(p2-p3交界)消融,经房间沟入路向左侧做左心房峡部消融,与左侧肺静脉消融路线融合。经房间沟入路经左心房顶向左侧消融,与左侧左心耳消融路线融合[8]。
1.3 术后观察指标及随访
1.3.1 术后处理:术后常规重症监护及人工呼吸机辅助呼吸,持续监测心率,根据需要行心室起搏。根据血流动力学监测适当应用血管活性药物及胶体,所有患者术后均胺碘酮口服或静脉泵入控制心率及心律,如出现快速房性心律,微量泵静脉泵入胺碘酮 300~600 mg/d,进食后改口服200 mg,1~3次/d,口服3个月。此后根据复查心电图结果,对于转为正常窦性心律患者使用胺碘酮计量逐渐减少。恢复窦性心律或心率<60次/min时,停用胺碘酮;如出现严重心律过缓或结性心律时启用临时起搏器起搏,恢复窦性心律后停用。对于瓣膜修复或生物假体置换的患者,术后使用华法林抗凝6个月;对于机械瓣膜置换的患者, 终生使用华法林抗凝治疗。INR目标范围为2.0~2.5。
1.3.2 术后监测指标:术中体外循环(CPB)时间、主动脉阻断时间、心脏复跳及ICU监护期间心律情况,术后24 h心包纵膈引流量,开胸探查止血等并发症,呼吸机辅助时间,ICU停留时间,临时起搏情况,、胺碘酮应用情况、总住院时间。术后1~3个月分别对患者进行随访。随访内容包括体格检查、超声心动图和24 h Holter 监测。心房颤动复发定义为任何持续超过30 s的心房颤动或房性快速性心律失常发作,出现症状和(或)24 h Holter记录检测到。术后的不同时期采用放射免疫法测定血清IL-6及cTnI含量,由雅培AEROSET全自动生化分析仪测定。

2 结果
2.1 总体围术期情况 SLM Ⅲ组与CM Ⅳ组比较,CPB时间和主动脉阻断时间均明显增加,有统计学差异(P<0.01)。术后24 h引流液量、人工呼吸机辅助时间、ICU 监护时间、临时起搏及胺碘酮应用比例、并发症发生率差异无统计学意义(P>0.05)。44例患者均接受了二尖瓣置换同期行SLM Ⅲ或CM Ⅳ术,其中38例机械瓣置换,6例生物瓣置换。术后3例患者(6.9%)行二次开胸止血手术,出血原因均非迷宫切口所致。43例患者无术后死亡,发生低心排血量综合征5例(11.6%),发生肺炎4例(9.3%)。术后无患者早期卒中发生。27例患者(62.8%)在术后1周内需要临时起搏,出院时不需使用永久起搏器。见表2。

表2 围朮期及随访结果对比
2.2 2组窦性心律恢复率情况比较 窦性心律恢复率:SLM Ⅲ 组术后24 h为 61.9%,出院时窦性心律分别为 76.2%,3个月随访为81%。CM Ⅳ 组术后24 h为60.9%,出院时窦性心律分别为65.2%,3个月随访为73.9%。2组术后24 h窦性心律恢复率差异无统计学意义(P>0.05),出院时及术后3个月2组窦性心律恢复率差异均有统计学意义(P<0.05)。术后24 h未恢复窦性心律的患者中SLM Ⅲ组1例为阵发性房颤,4例为持续性房颤,3例为结性心律,CM Ⅳ组1例为阵发性房颤,3例为持续性房颤,5例为结性心律。3个月随访时SLM Ⅲ组有4例恢复窦性心律,CM Ⅳ组有3例恢复窦性心律。术后房颤患者均口服胺碘酮治疗,术后3个月内均无死亡病例。
2.3 2组术后cTnI含量比较 SLM Ⅲ组患者术后血清cTnI快速增长,术后24 h达到高峰,考虑与SLM Ⅲ术中大量左房壁心肌组织被切割有关,24 h后cTnI含量逐渐下降,至术后1周左右基本恢复正常。CM Ⅳ组患者术中采用射频热能消融心房壁组织,心房肌肉热损伤达到隔离效果,热损伤也造成了血清cTnI的升高,但明显低于SLM Ⅲ组血清cTnI含量,2组患者cTnI差异有统计学意义(P<0.01)。见图2,表3。
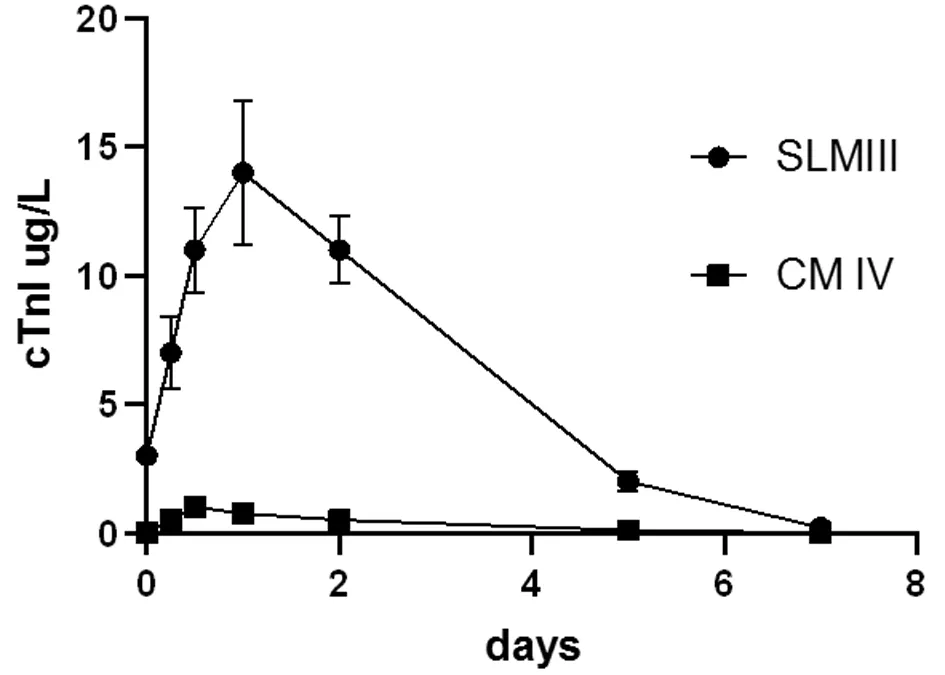
图2 2组患者术后血清cTnI变化图
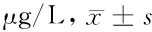
表3 2组患者术后不同时间点血清cTnI含量
2.4 2组术后血清IL-6含量对比 IL-6是反映机体炎症水平的重要因子,SLM Ⅲ较CM Ⅳ型手术需要较长的体外循环时间,SLM Ⅲ组主动脉平均阻断97.6 min,心肌及组织的灌注不良导致IL-6等炎性因子释放,术后早期(24 h)SLM Ⅲ组患者IL-6含量快速增长并达到高峰,随后逐步下降,术后1周SLM Ⅲ组患者血清IL-6含量依然维持在较高水平。CM Ⅳ组患者血清IL-6峰值浓度明显低于SLM Ⅲ组,在术后1周基本恢复正常水平,2组患者术后血清IL-6含量差异有统计学意义(P<0.05)。见图3,表4。
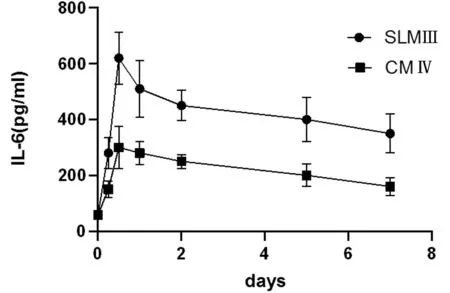
图3 2组患者术后血清IL-6变化图
表4 2组患者术后血清IL-6变化图
3 讨论
据统计外科收治的风湿性二尖瓣病变患者中合并房颤者占半数以上,风湿性病变是反复的风湿性炎症导致瓣膜增厚、钙化、交界黏连,从而导致瓣膜狭窄,进一步引起压力-容量超负荷相关的心房结构改变,产生异位起搏点和单向传导阻滞,并产生折返回路,从而导致心房颤动。如房颤未能有效治疗,可增加死亡率和并影响远期预后[9]。但目前外科医生实施的房颤治疗比例不容乐观,CM Ⅳ型手术繁杂的手术线路及低成功率伴高额费用成为推广外科房颤治疗的障碍,甚至有学者对无差别化采用CM Ⅳ的手术治疗房颤提出质疑[10]。对于以二尖瓣病变为基础的房颤,多合并左房的扩大及心房肌电生理的重构,及房颤维持最关键的折返性径路多存在于左肺静脉及左心房后壁[11]。鉴于此本研究采用SLM Ⅲ型手术来代替复杂的传统迷宫Ⅲ型手术,大幅减少手术操作难度及风险,以CM Ⅳ 型手术病例作为对照,探究SLM Ⅲ型手术的安全性、有效性及临床推广价值。
研究发现SLM Ⅲ较CM Ⅳ组在体外循环时间和主动脉阻断时间明显增加,主动脉阻断时间平均延长27 min,CPB时间平均延长44 min,然而在在现有体外循环转流水平和充分的心肌保护下,这一事件对患者术后并发症、呼吸机辅助时间、ICU 停留时间、24 h心包纵隔引流量、总住院时间等围朮期指标均无明显差异,说明SLM Ⅲ采用切+缝的方式来代替射频消融所付出的代价是可以接受的。CM Ⅳ手术中在消融钳钳夹时,常需钳夹6~8次,每次2 min,同样也消耗了较多的主动脉阻断时间。然而在房颤发生的最关键部位的左房部位CM Ⅳ的线路透壁性不及SLM Ⅲ手术。随着手术经验的积累,手术技巧的不断提高,这一术式对外科医生将不再具有难度,传统的认为“切+缝”的房颤迷宫手术“危险”的观点需改变。
通常认为SLM Ⅲ型手术切口多,加之体外循环时间长,造成机体炎症因子大量释放,本研究SLM Ⅲ组患者术后IL-6含量明显高于CM Ⅳ 组,而左侧心房组织的广泛切割,造成心房肌组织损伤,cTnI大量释放入血,因此SLM Ⅲ型手术较CM Ⅳ型手术损伤更重,对患者术后早期康复有一定影响,对凝血纤溶系统消耗大,24 h引流量必然大幅增加[12]。但研究发现2组24 h引流液量和二次止血发生率无统计学差异。我们认为术中严格的缝合技术是预防出血的关键。SLM Ⅲ的核心技术是心房的切开与缝合,本组的经验是充分游离上、下腔及横窦等部位的心包反折来牵拉暴露,左房壁切开部位解剖关系的准确对位及均匀严密的房壁全层缝合,薄弱处可垫以心包条加固。2组术后发生结性心律或各种形式的房室传导阻滞,甚至安装永久起搏器方面统计并无明显差异,但也有学者认为CM Ⅳ在右心房的操作经线过多导致其发生Ⅲ度房室传导阻滞及安装永久起搏器的概率高于单侧左心房消融[13-15]。
SLM Ⅲ组和CM Ⅳ 组术后窦性心律恢复率均超过60%, 且差异无统计学意义(P>0.05),在出院时及术后3个月随访发现,SLM Ⅲ组窦性恢复率高于和CM Ⅳ组,术后3个月,SLM Ⅲ组窦性恢复率可高达81%。分析SLM Ⅲ手术失败比例发现,4例患者均合并右心房明显增大,2例行三尖瓣成型手术,1例合并左房血栓,考虑风湿性二尖瓣病变随着疾病的病程发展,由单纯左心房扩大受损发展为双侧心房增大,进而右心房心肌电生理的重构形成右房折返性径路而参与房性心律失常的形成[16,17],因此对于该类患者单纯的左侧心房隔离已不能完全阻断房颤的发生。临床上对于实施SLM Ⅲ型手术在手术适应症和患者选择方面需严格把关。
迷宫手术以恢复正常窦性心律和左心房收缩功能为主要目标,本研究发现SLM Ⅲ组和CM Ⅳ 组患者均获得了超过80%的转窦律,这一结果与其他文献报道的70%~95%[18,19]相似,虽然窦性心律回复率尚令人满意,但并不是所有的窦性心律都可以伴随有效的左心房收缩,,本研究发现术后患者左心房收缩功能恢复并不理想,出院时2组患者经超声心动图判断具有左心房收缩功能的不足10%, 术后3个月随访该结果有所提升。有研究认为迷宫术后左心房收缩功能为一个动态提高的过程,直到术后1年后,窦性心律和左心房收缩共存的一致性才较好,这可能与心房壁肌肉重构过程有关[20,21]。需要注意的是本研究随访时间尚短,SLM Ⅲ型手术对左心房进行大量切割必然形成心房瘢痕组织,大量的瘢痕组织是否对左心房远期的射血功能形成影响仍待观察。
总之,SLM Ⅲ型手术与 CM Ⅳ 型手术比较,近期增加了体外循环时间和主动脉阻断时间,造成了机体炎性内环境的形成,但尚未发现围朮期不良事件,且窦性心律恢复率更高。因此,在严格把握适应症的前提下,SLM Ⅲ型手术是治疗风湿性二尖瓣病变伴发心房颤动的安全、经济且有效的方法。
——体外循环质量控制的基石

