腹盆腔多发性巨大胃肠道外间质瘤1 例
白文柯 江梓杰 黄婷 聂飚
患者 男,57 岁。因“发现左下腹包块进行性增大半年”于2019 年4 月10 日入住暨南大学附属第一医院。患者于半年前体检发现右下腹部包块,无不适,未引起重视;4 个月前就诊于深圳市人民医院,腹部CT检查提示腹部占位性病变,因无症状,患者仍未治疗;20 d 前无明显诱因下出现腹部膨隆,入院当天下午出现全身短暂性抽搐,持续数秒后自行缓解,无意识丧失,无肌肉疼痛,既往身体健康。查体:腹部膨隆,左下腹可触及固定球状包块,约15 cm×15 cm,质硬,与周围组织明显粘连,全腹无压痛和反跳痛。查血:Hb 122.6 g/L,乳酸脱氢酶280 U/L,凝血、肝肾功能、病毒全套、肿瘤指标均未见异常。肝胆胰脾彩超检查示第一肝门区及整个腹腔多发混合回声包块,性质待定。腹部CT 平扫示全腹多发肿块影,肝肾间隙及盆腔肿块较大,肿块压迫双侧输尿管造成肾积水,双侧腹股沟淋巴结肿大(图1)。进一步行全身正电子发射计算机断层显像(PET-CT)扫描提示大量腹水,腹膜、腹腔、盆腔多发结节,肿块与局部脏器(肝、脾、左肾及肾上腺、左侧输尿管、胃、肠管)分界不清,糖代谢增高,考虑恶性病变。遂在彩超引导下行腹腔肿块活检,病理检查见肿瘤细胞局部坏死,核分裂象12 个/50 HPF,符合高 度 恶 性 胃 肠 道 外 间 质 瘤(extra-gastrointestinal stromal tumor,EGIST)(图2)。免疫组织化学染色:CD34、CD117、discovered on GIST-1(DOG-1)、均呈弥漫强阳性,Ki-67(15%+),平滑肌肌动蛋白(SMA)、肌间线蛋白(Desmin)、高溶解性酸性蛋白(S-100)、神经嵴转录因子10、广谱细胞角蛋白均阴性。4 月18 日起患者口服甲磺酸伊马替尼片400 mg/d 进行靶向治疗,1 个月后腹部MRI 检查提示肿块较上次CT 检查结果缩小(图3a、b)。7月16 日复查腹部MRI 提示肿瘤直径与上一次变化甚小,未见肿瘤远处转移(图3c、d),增加甲磺酸伊马替尼片剂量至500 mg/d。9 月1 日复查腹部MRI 提示肿瘤大小同前,胸部增强CT 检查提示双肺散在多个直径约0.6 cm 结节状高密度影,考虑为转移瘤。截止至2020 年12 月患者继续靶向治疗,已随访18 个月,患者存活。
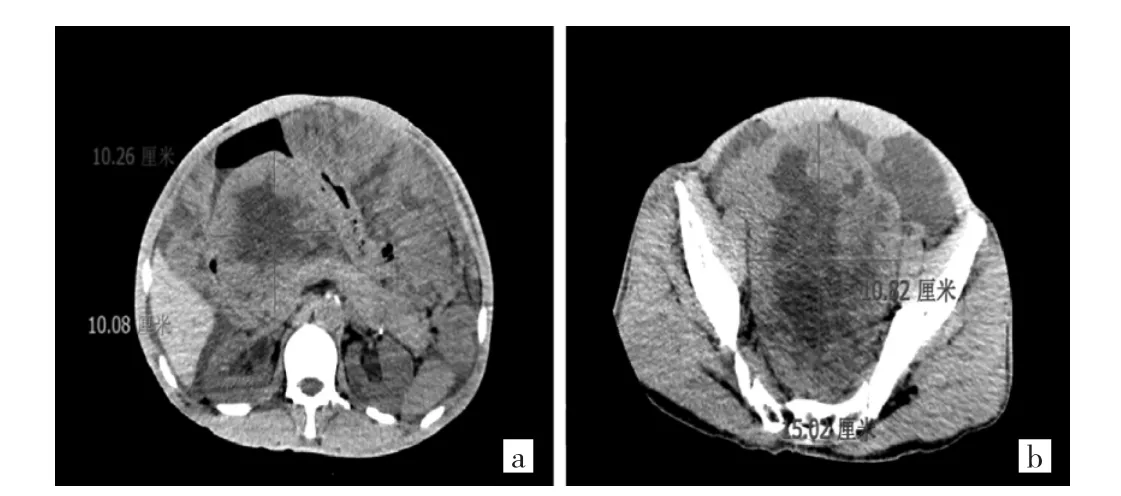
图1 2019 年4 月10 日腹部CT 平扫所示(a:腹腔肿瘤体积约10.26 cm×10.08 cm×9.68 cm;b:盆腔体积约10.82 cm×15.02 cm×13.02 cm,肿瘤内部囊变坏死,密度不均匀,局部与周围组织发生粘连)
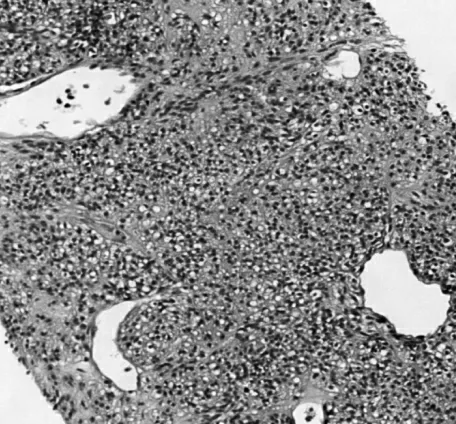
图2 2019 年4 月15 日病理检查所示(梭形细胞为主,短束状排列,可见梭形细胞与上皮样细胞相互移行区域,符合高度恶性胃肠道外间质瘤;HE 染色,×20)
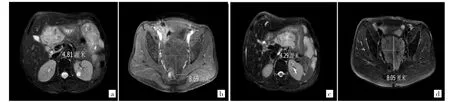
图3 腹部MRI 检查所示(a:2019 年5 月19 日患者靶向治疗1 个月后腹腔肿瘤体积缩小至7.79 cm×4.81 cm×9.32 cm,T2WI 呈高信号,肿瘤内部见不规则囊变区;b:盆腔肿瘤体积缩小至8.55 cm×8.69 cm×9.95 cm,增强扫描局部见间隔强化;c:2019 年7 月16 日患者靶向治疗中复查提示腹腔肿瘤较前相比,变化较小,体积约为8.25 cm×4.29 cm×10.15 cm;d:盆腔肿瘤体积约为8.29 cm×8.05 cm×9.75 cm)
讨论 胃肠间质瘤(gastrointestinal stromal tumor,GIST)是最常见的消化道间叶组织肿瘤[1],占胃肠道肿瘤的0.2%,我国发病率为1~2/10 万人。EGIST 是指出现于胃肠道以外的GIST,多见于网膜、腹腔、腹膜后,约占GIST 的10%[2]。EGIST 临床表现无特异性,肿瘤小者常无症状,由于EGIST 出现于胃肠道以外,肿瘤潜在生长空间大,绝大多数病灶直径超过10 cm,被称为巨大间质瘤,患者多表现为腹部包块、疼痛不适、转移瘤症状等[3]。本病例特点:(1)老年男性患者,慢性病程;(2)腹腔多发病灶,盆腔巨大间质瘤,无诉不适,查体左下腹触及与周围组织明显粘连的肿块;(3)多次复查肿瘤指标均未见异常,CT、MR、PET-CT 检查提示多发浸润性恶性肿瘤;(4)靶向治疗最初阶段肿瘤体积稍缩小,但在其后治疗过程中肿瘤增大并远处转移。经查阅文献,这种多发巨大肿块类型的EGIST 国内尚未见报道。
EGIST 的恶性程度与年龄、肿瘤体积、肿瘤坏死程度、核异型性、c-kit 基因或血小板源性生长因子受体 α 多肽(PDGFRA)基因突变、淋巴结受累和远处转移等相关[2,4]。EGIST 的确诊主要依据肿瘤位置、组织学及免疫组织化学检查,免疫表型CD117+、DOG-1+为诊断EGIST的主要标准[5],其他阳性抗原还有CD34(70%)、SMA(30%)、S-100(5%)、desmin(2%)、cytokeratin(2%)等[6-7],对于难以诊断的EGIST,应进一步行c-kit 和PDGFRA基因突变分子检测。腹盆腔EGIST 需与其他肿瘤进行鉴别:(1)脂肪肉瘤:不均质肿块,包膜不完整,常沿肝肾周间隙浸润性生长,坏死、囊变、出血,脂肪组织混杂的不均质实性密度是其常见的特征性表现,采用原位荧光杂交可区别脂肪肉瘤与EGIST;(2)平滑肌肉瘤:肿块巨大,中央常伴不规则坏死,出血及钙化少见,MRI 增强扫描呈明显环状强化,有浸润血管倾向,绝大多数不表达CD117 和CD34,而desmin 呈弥漫阳性;(3)纤维组织细胞瘤:多为良性,肿瘤较大者向周围浸润生长,血供丰富,有浸润与复发特性,质地硬,由单一的梭形细胞构成宽而粗的纤维束,desmin 和β-catenin 的表达较高,部分表达CD117,而CD34 和S-100 均阴性。
EGIST 作为一种特殊类型的GIST,与GIST 有着相似的形态学、免疫表型及分子遗传学特征[8],大多数临床医生根据GIST治疗原则进行治疗。GIST 遵循以手术切除后显微镜下无残留(R0)切除为主、分子靶向治疗为辅的治疗模式[9]。根据病理危险度分级和基因检测类型选择靶向药物,治疗前后应选择CT 或MR 作为评估治疗效果的手段,靶向药物疗效目前推荐Choi 评价标准。EGIST 的胃肠道及胃肠道外症状均不明显,很多病例在诊断时已为晚期,易经淋巴结或血液转移,本例患者肿瘤与临近多个重要器官粘连,考虑手术难以完整切除肿瘤[10],因此选择络氨酸激酶抑制剂甲磺酸伊马替尼一线治疗[11],期望肿瘤缩小后行R0 切除,据报道,c-kit 外显子11 突变者接受伊马替尼治疗疗效最佳[12];但是靶向治疗过程中发生肿瘤远处转移,预后较差,正考虑换用二线药物舒尼替尼(国内上市),原发c-kit 外显子9 突变和野生型GIST 患者接受舒尼替尼治疗的生存获益优于c-kit 外显子11 突变患者,继发性c-kit 外显子13、14 突变患者接受舒尼替尼治疗疗效优于继发性c-kit 外显子17、18 突变患者[13-15];或改用三线药物瑞戈非尼治疗,研究显示继发性c-kit 外显子17 突变患者接受瑞戈非尼治疗取得了较好的疗效[16-17];PDGFRA D842V 和D816V突变患者可能对使用伊马替尼、舒尼替尼与瑞戈非尼治疗原发性GIST 产生药物依赖性,或用PD-1 抗体试验性免疫治疗。
总之,腹盆腔多发性巨大EGIST 临床罕见,本例肿瘤发现时已是晚期,极易发生转移,生物学行为和预后较GIST 差,希望引起临床医师重视,早诊断、早治疗,同时严格随访,提高临床医师对多灶性EGIST 的认识。

