腹腔镜胰十二指肠切除术安全性及有效性初探
郑卫华,孟兴凯,任建军,乔建梁,靳君华,牛剑祥,王慧君,张俊晶,2
(1.内蒙古医科大学附属医院 肝胆外科,内蒙古 呼和浩特 010050;2.呼哈浩特市第一医院 肝胆外科,内蒙古 呼和浩特 010030)
腹腔镜胰十二指肠切除术(laparoscopic pancreatoduodenectomy,LPD)是应用腹腔镜技术完成或辅助完成的胰十二指肠切除手术,由于操作复杂、并发症多、病死率高,被誉为微创外科医师心目中的“珠峰”[1]。LPD最早由Gagner等[2]于1994 年报道,早期阶段只有个别地区、个别医师零星开展,随着新的腹腔镜仪器设备、手术器械研发,加之腹腔镜技术在其他领域如胃肠、泌尿外科以及妇科领域蓬勃发展,取得了较好的效果,推动了LPD技术发展,在大的胰腺外科中心甚至成为常规手术。
既往文献报道、手术演示都是渡过学习曲线后开展LPD的结果,对于从初始实施LPD术者来讲,更愿意看到第一例到渡过学习曲线的数据,为实施成熟稳定LPD提供借鉴。为此,本研究回顾性分析2017年1月至2019年12月内蒙古医科大学附属医院肝胆外科初期完成的15例LPD患者的围手术期临床资料,并与同期同一团队行开腹胰十二指肠切除术(open pancreaticoduodenectomy,OPD)的30例患者资料进行对比,报道如下。
1 资料和方法
1.1 一般资料
根据接受的手术方式,将患者分为两组,其中观察组为LPD组(15例),对照组为OPD组(30例)。
LPD组纳入标准和排除标准[3]。纳入标准:(1)体重指数(BMI)<28.0 kg/m2;(2)壶腹肿瘤、局限于十二指肠第二段的十二指肠肿瘤、胆总管下段肿瘤和胰头胰腺肿瘤;(3)由专业放射科医师和有经验的外科医师在术前放射学基础上仔细确定肿瘤的可切除性。排除标准[3]:肿瘤侵犯肠系膜上静脉、肠系膜上动脉,不可重建的肠系膜上静脉或门静脉闭塞、主动脉侵犯或包裹、既往有上腹部手术史、肿瘤延伸至钩突和严重的心肺合并症的患者被排除在LPD手术之外。
OPD组纳入标准和排除标准。纳入标准:(1)患者一般状况可,无心、肺、肾功能严重障碍,能够耐受手术;(2)肿瘤无远处转移,无血管侵犯。排除标准:(1)不能耐受手术者;(2)晚期肿瘤或恶病质者。所有患者均行腹部增强CT、MRI等影像学检查,对于十二指肠乳头病变加做十二指肠镜并活检;考虑胆总管下段、壶腹部以及胰头部病变加做超声胃镜检查。两组患者的术前资料详见表1。
1.2 手术方法
1.2.1 OPD。全身麻醉成功后,患者仰卧位,取右上腹部反L切口,腹腔探查。解剖胆囊三角,切除胆囊,于胆囊管开口上方横断肝总管,清扫肝门部及肝十二指肠韧带结缔组织及淋巴结,离断胃十二指肠动脉和胃右动脉。游离肝总动脉及其分支,清扫周围结缔组织和淋巴结。打开胃结肠韧带,在胃窦-体交界处切断胃体。Kocher法显露胰头十二指肠和下腔静脉,清扫相应区域淋巴结。显露肠系膜上静脉,在肠系膜上静脉左缘离断胰颈,显露主胰管,置入相应管径胰管支撑管。距离Treiz韧带远端10 cm处切断空肠。肠系膜上动脉右侧离断胰腺钩突系膜,完整切除标本。胰肠吻合口采用端侧套入式吻合,胰管支撑管外引流。距胰肠吻合口约10 cm处行肝总管空肠端侧吻合,距胆肠吻合口50 cm处行胃肠吻合,留置腹腔引流管,结束手术。
1.2.2 LPD。本技术通过我院伦理委员会审批[YJ(2018068)]。全麻成功后,取仰卧、“大字型”体位,扶镜手位于两腿之间,取脐下小切口置入戳卡作为观察孔,腹腔探查。另取平脐处腹直肌外侧缘、腋前线肋缘下2 cm处左右对称置入四个戳卡作为主刀和助手操作孔,主刀位于患者右侧。提起横结肠,依次显露十二指肠水平段、降段,向上直至肝脏脏面。向左暴露肠系膜上静脉,离断Henle干,向左掀起胰腺十二指肠清扫肠系膜上动脉根部结缔组织,探查第16组淋巴结情况。空肠起始处15 cm离断,十二指肠升段及部分空肠经肠系膜上血管后方由左移向右侧。打开胃十二指肠韧带,胃窦胃体结合部离断,沿肠系膜上静脉切断胰颈部,显露胰管,置入胰管内径匹配的聚乙烯管,可吸收线固定在胰管上。超声刀打开腹腔干血管鞘,依次裸露肝总动脉、肝固有动脉、胃十二指肠动脉,胃十二指肠动脉结扎、离断,继续裸露肝左动脉、肝右动脉,显露肝门部胆管,离断。提起十二指肠升段,依次离断空肠第一支血管、胰十二指肠下血管、钩突系膜,裸化门静脉,顺行切除胆囊后标本入袋。距残端约5 cm处空肠侧壁戳孔,
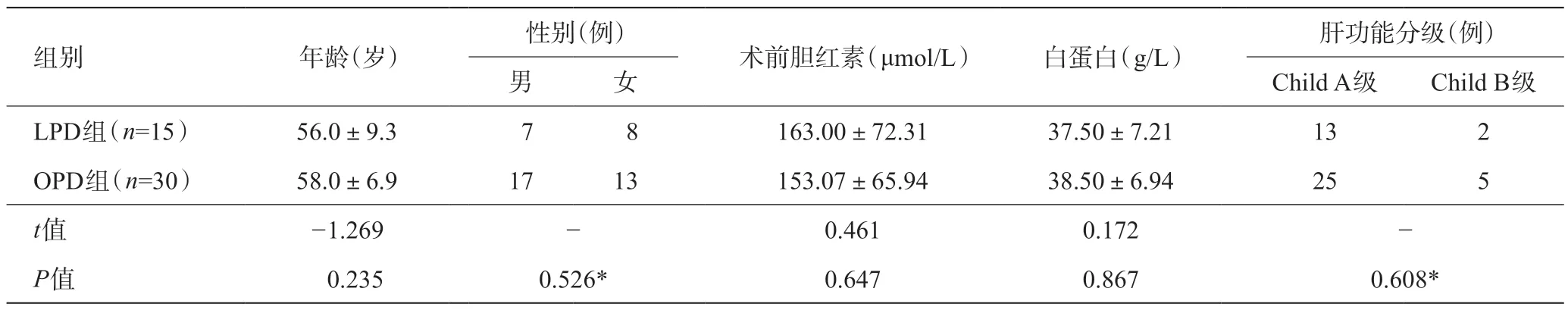
表1 两组患者术前资料的比较
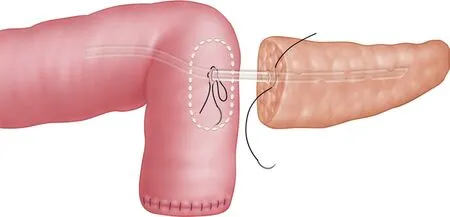
图1 固定胰管支撑管,空肠荷包缝合,胰管支撑管置入空肠
1.3 观察指标
观察两组患者的手术时间、术中失血量与输血量、术后入住ICU时间、术后排气时间、进食时间、术后住院时间等,以及并发症发生的情况(包括出血、感染、胆瘘、胰瘘、肠梗阻、死亡、胃排空障碍等)和术后切除肿瘤的病理情况等。
1.4 统计学分析
本研究利用SPSS 25.0对数据进行统计分析。当连续性变量服从正态分布时,采用(±s)表示,否则采用中位数(四分位数)表示;分类变量以例(百分比)表示。对于服从正态分布的连续性变量,组间比较采用两独立样本均数的t检验;对于不服从正态分布的连续性变量,组间比较采用秩和检验。当理论频数≥5时,二分类变量的组间比较采用χ2检验,否则采用Fisher精确概率检验。以P<0.05认为差异有统计学意义。
2 结果
2.1 两组术中情况对比
LPD组患者因患者肿瘤晚期、腹腔多发淋巴结荷包缝合,将胰管支撑管放入空肠内(图1),收紧荷包线并与胰管靠拢,胰腺断端与空肠侧壁采用“双U”法缝合(图2)。距离胰肠吻合口约10 cm处做肝总管空肠连续或间断吻合,距胆肠吻合口50 cm处行胃空肠吻合,于肝下及胰肠吻合口上方及后方处分别放置引流管,从戳卡孔引出固定,结束手术。转移中转开腹手术1 例,腔镜辅助2 例,其余为全腔镜胰十二指肠切除术。手术时间LPD组明显长于OPD组,但术中出血LPD组较OPD组少,差异均有统计学意义(P<0.05)。术中输血情况两组差异无统计学意义(P>0.05,表2)。
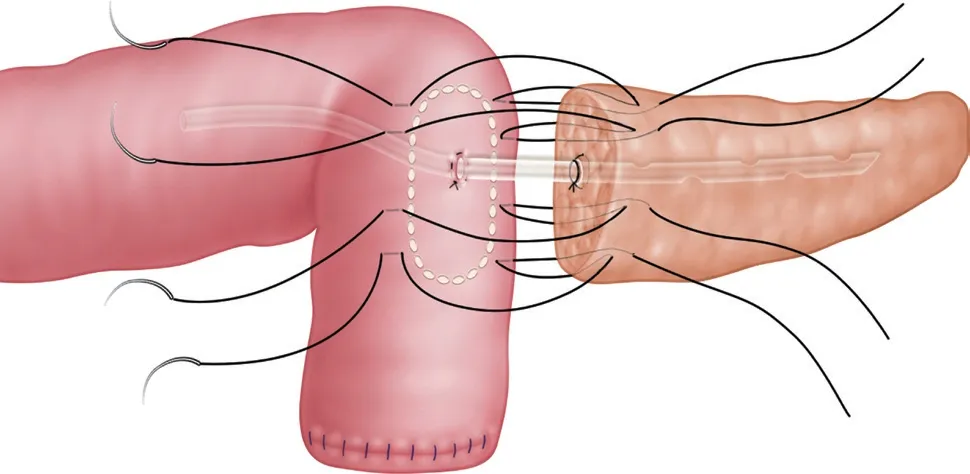
图2 胰腺断端与空肠侧壁双“U”缝合
2.2 两组术后情况对比
LPD组患者的排气较OPD组早,两者的差异有统计学意义(P<0.05,表2)。而两组的ICU监护时间、进食时间和术后住院时间的差异无统计学意义(P>0.05,表2)。
2.3 两组患者术后并发症的对比
LPD组和OPD组在出血、感染、胆瘘、肠梗阻、死亡、胰瘘、胃排空障碍等术后并发症并无统计学差异(P>0.05,表3)。
2.4 术后切除肿瘤的病理情况对比
两组患者的肿瘤类型、切除总淋巴结数、切缘阴性间的差异无统计学意义(P>0.05,表4)。LPD组肿瘤直径与OPD组的差异有统计学意义(P<0.05,表4)。
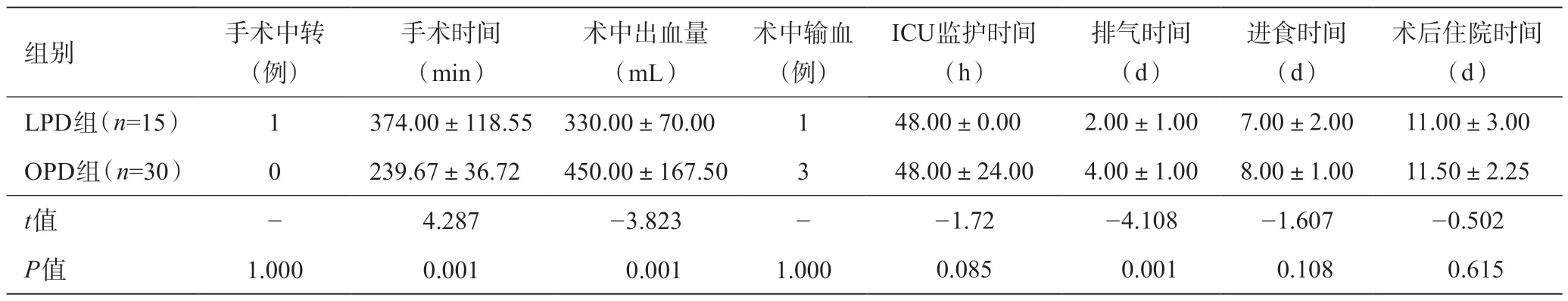
表2 两组患者术中和术后资料的比较

表3 两组患者术后并发症比较[例(%)]
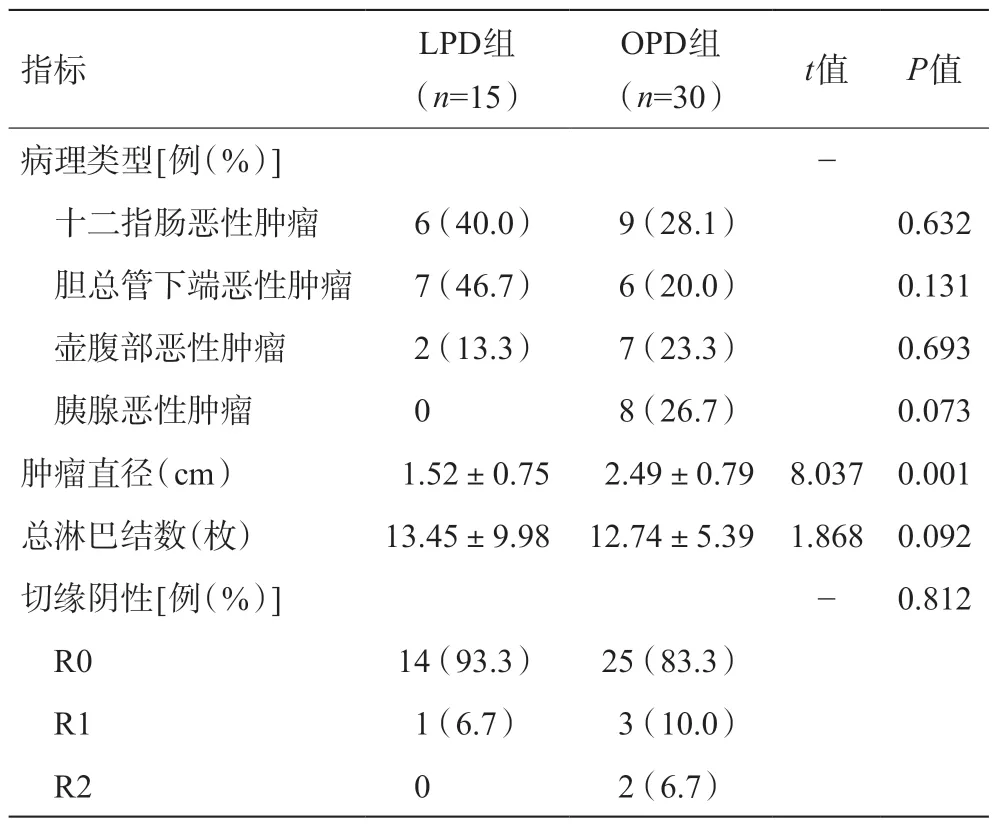
表4 两组术后切除肿瘤的病理情况对比
3 讨论
3.1 LPD手术方式
LPD主要分为以下三种类型[4]:(1)全腹腔镜胰十二指肠切除术;(2)腹腔镜辅助胰十二指肠切除术;(3)腹腔镜机器人联合手术。腹腔镜手术切除标本后再使用机器人手术系统进行消化道重建的联合手术有一定现实意义,机器人操作更精细,缝合较腹腔镜手术更有优势,更适合用于胰管、胆管直径细小的病例。虽然机器人手术系统设备昂贵,仪器尚未普及,但随着国产机器人的开发加之医保费用的调整,未来机器人技术必将大有可为[5]。笔者所在医院虽配置达芬奇机器人手术系统,但尚在调试阶段。腹腔镜辅助胰十二指肠切除术一般在开展初期采用,使重建易于完成;在后期阶段,技术成熟,大多采用全腔镜下胰十二指肠切除术。本研究中除1例探查肿瘤分期较晚实施中转开腹,2例采用腹腔镜辅助胰十二指肠切除术,其余均为全腹腔镜下胰十二指肠切除术。
3.2 LPD手术并发症
LPD是从OPD发展而来,其术后并发症与OPD术后并发症类别基本相同。本组患者无因手术本身死亡情况出现,OPD组因其他脏器损伤意外死亡1例。除围术期死亡外,其他主要并发症包括感染、出血、胰瘘、胆瘘、肠梗阻、胃排空障碍等。其中胰瘘是PD术后最严重的并发症,发生率为15%~25%[6]。由胰瘘导致的其他并发症会严重危及患者生命安全,应当极力避免,本研究中,因胰瘘而出现延迟性出血1 例,介入栓塞治愈,因此,多学科协作是围术期患者安全的重要保证。胰瘘的发生除了与技术是否熟练、操作是否细心、解剖是否轻柔有关外,胰腺质地、合并基础疾病等也是重要因素。除上述情况以外,在腔镜下选择一个适宜的胰肠重建方法也是关注的焦点,腔镜胰肠重建方法应具备两个特点:一是易于操作,二是与传统吻合方式相比胰瘘发生率一致或更低。胰腺重建按照吻合部位不同,可以分为胰胃重建和胰肠重建,胰肠重建更符合解剖生理需要,临床应用较广泛。胰肠重建大体可以分为套入式吻合和胰管对空肠黏膜吻合。不管哪种吻合方法,传统胰肠重建在腔镜实施难度较大,尤其对于初学者望而生畏。最近几年出现了很多腔镜下胰肠重建方法,有的甚至以姓氏命名,各有所长[7]。笔者所在团队在观摩录像与现场演示基础上,结合自身特点,改进胰管空肠黏膜吻合方式,即胰管置入支撑管,胰管侧与空肠黏膜侧荷包缝合并对拢,胰腺断端与上提空肠系膜缘对侧行双U字缝合。本研究结果显示,LPD组患者出现B级胰瘘3例,OPD组患者出现胰瘘7例,尽管两者术后胰瘘的发生率并无统计学意义(P>0.05),但对于初期开展LPD术者来讲,该术式易于操作,在尚未渡过学习曲线期间胰瘘发生率并无增加,值得推荐。除胰瘘外,LPD其他并发症发生率与OPD发生率一致,这与其他学者[8-10]的研究结果一致,说明两种手术的安全性是相当的,尤其在初期开展阶段精心准备实施也是安全可行的。
3.3 LPD手术优缺点
LPD与OPD在手术时间、术中出血上相比存在统计学差异,LPD手术时间较OPD组长(P<0.05)。国内外大的医疗中心[11-12]的回顾性分析显示:两组的手术时间相比差异无统计学意义(P>0.05)。本研究LPD组手术时间明显增加,可能与手术开展处于初期阶段有关。专家演示病例手术时间近乎与开腹一致,我们实施病例中,最早行LPD手术时间10 h左右,这与国内外早期或初次开展病例报告时间是一致的,经过病例积累和总结,后期阶段手术时间明显缩短。本研究LPD组术中出血情况要优于OPD组(P<0.05),可能与腔镜具有放大视野更容易辨清血管有关。术中出血是腹腔镜胰十二指肠切除术的术中常见危险并发症,也是导致腹腔镜中转开腹的常见原因,预防腹腔镜胰十二指肠切除术术中出血的关键是全面的术前评估和细致的术中操作[13]。本研究中两组患者ICU监护时间、进食时间和术后住院时间的差异无统计学意义(P>0.05),而吴祥虎等[9]的研究中LPD组患者入住ICU时间及住院时间更短(P<0.05),作者认为与腹腔镜技术创伤小、易恢复的优点有关。本组未出现上述效果,也与初期开展有关,围手术期护理较为保守,相信渡过学习曲线后,各项指标必好转于目前。本研究中两组患者肿瘤类型、总淋巴结数、切缘阴性的差异无统计学意义,但LPD组肿瘤直径与OPD组的差异有统计学意义(P<0.05,表5),这与初期开展,严格病例入组有关,胰腺癌患者未采用腹腔镜治疗,随着经验积累,腔镜技术应用指征逐渐扩大,而现有病例中OPD组有8 例胰腺肿瘤患者。金继宽等[14]通过对47例LPD组和61例OPD组对比分析,得出LPD组在清扫淋巴结总数上优于OPD组(P<0.05)。这与腹腔镜能提供放大、高清的术野和腔镜器械能在狭窄的空间灵活操作有关。本研究结果与上述不同,可能与研究样本量少有关。
3.4 LPD学习曲线
相比传统外科手术,腹腔镜手术由于其操作特殊性,需要临床前模拟箱训练、动物模拟操作[15],LPD的实施更要有其他临床复杂腔镜手术经历,即使这样,LPD开展需达到一定例数积累,才能够稳定实施。洪德飞等[16]认为至少须有30例才能渡过学习曲线,说明LPD的学习曲线较长。Gumbs等[17]对285例LPD的患者资料进行研究得出,LPD患者数越多,平均住院时间和手术时间会逐渐缩短。笔者所在团队开展第一例LPD手术时间长达10 h左右,后缩短到5 h左右。Wang等[12]和赵玉沛[18]都认为LPD的学习曲线分为三个阶段,渡过学习曲线后,LPD的短期临床效果可明显改善。本组病例有限,尚未渡过学习曲线,同时部分研究结果已经显示出腹腔镜优势,但部分研究结果与大的医疗中心相比还存在差距,相信随着病例数增加、经验积累,安全地渡过学习曲线后,腹腔镜技术优势必将全面客观展现。
总之,LPD虽然具有高难度,但经过手术观摩、专家指导,加之手术团队精诚合作、相关学科密切配合,初期开展LPD是安全的,近期效果明显。

