儿童自发性胆道穿孔诊治经验
陈巍,陈亚军,王晓曼,刘婷婷,张廷冲,王大勇
(国家儿童医学中心(北京)/首都医科大学附属北京儿童医院,北京 100045,1.普外科,2.超声科)
儿童自发性胆道穿孔(spontaneous perforation of the bile duct,SPBD)在临床上较为罕见。自1932年Dijkstra[1]首次报道以来,截止2016年外文文献仅有150例报道[2]。SPBD的确切病因仍不清楚,绝大多数为特发性病例。一部分患者合并胰胆管合流异常[3],或由于胆道结石[4]、闭锁[5]所致的胆总管远端的梗阻所致,一部分病例合并胆总管囊肿[6-7]。儿童SPBD临床症状缺乏特异性,也缺乏具有较高敏感性和特异性的实验室和影像学诊断方法。对儿童SPBD的治疗策略报道各不相同,从仅仅应用广谱抗生素的保守治疗[8],内镜下逆行胰胆管造影(endoscopic retrograde cholangiopancteatography,ERCP)[4],经皮引流[9-10]到手术治疗如胆肠重建手术等[11-13]。本研究通过回顾总结我院收治儿童SPBD的临床经验,分析儿童SPBD可能的病因、临床特点,探讨该疾病的诊断及治疗方法和疾病相关预后。
1 资料和方法
1.1 一般资料
将首都医科大学附属北京儿童医院2007年6月至2020年8月收治的以出院诊断为胆管穿孔(K83.202)患儿的病例资料纳入回顾性分析,本研究获得我院伦理委员会的批准。
纳入标准:(1)接受手术的患儿,术中发现胆汁样腹水或(和)术者直视下发现肝外胆道穿孔;(2)保守治疗的患儿,腹腔穿刺抽出胆汁样腹水;(3)年龄18岁以下。排除标准:(1)只有影像学诊断;(2)外伤、肿瘤及医源性因素(如手术损伤)所致胆道穿孔;(3)胃肠道的穿孔。
1.2 腹部超声
所有入组患儿入院时或入院后均常规行腹部超声检查。具有以下超声影像学表现可认为存在胆道穿孔:(1)直接征象:“洞征”(图1),即胆总管壁连续性中断,动态观察下可见胆总管内胆汁自此处溢出胆道;(2)间接征象:①胆总管扩张并管壁水肿、增厚并与周围组织粘连,同时存在游离腹水(图2A),②于胆总管周围粘连组织内发现胆道管腔外有胆石的影像(图2B)。
1.3 诊断性腹腔穿刺
部分入组患儿入院后接受诊断性腹腔穿刺。患儿取仰卧位,充分镇静、制动后,选择右下腹麦氏点为腹腔穿刺点。腹腔穿刺抽出黄绿色胆汁的患儿考虑为胆道穿孔。
1.4 治疗方法
1.4.1 保守治疗:对于症状轻微、病情无明显进展的患儿首先采用保守治疗。包括抗生素治疗、对症支持治疗和超声定位下腹腔穿刺置管引流。

图1 儿童SPBD腹部超声的直接征象,可见胆总管囊肿,囊肿壁连续性中断即“洞征”(线框箭头所指),考虑为穿孔部位,同时周围组织存在包裹粘连。
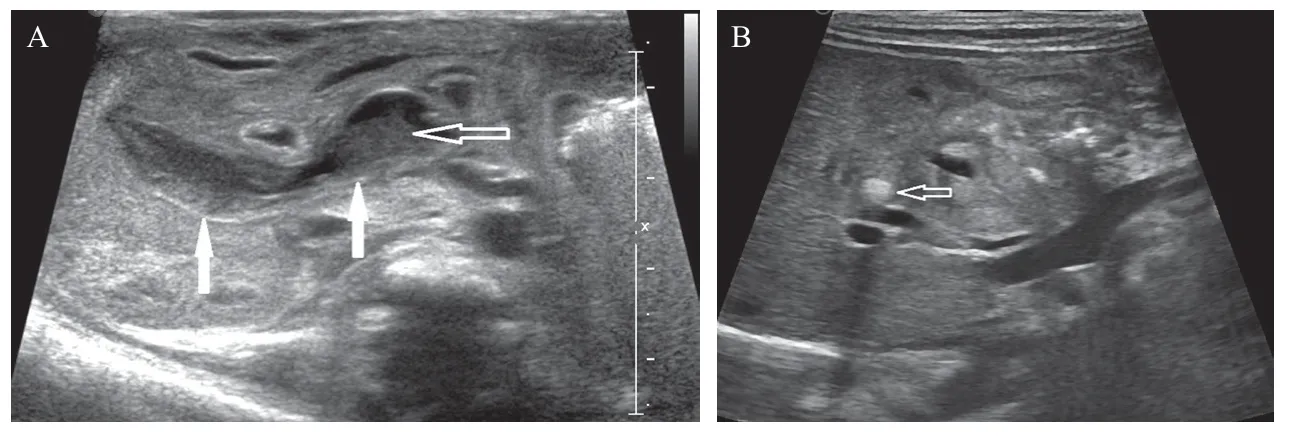
图2 儿童SPBD超声的间接征象
1.4.2 手术治疗:对于症状较重、病情持续进展、经保守治疗或初次手术治疗后症状仍无法缓解,病情继续进展的患儿,采用手术治疗或再次手术治疗。本研究中初次手术治疗(于我院)共采用了8种不同的手术方式:穿孔部位置管+腹腔引流、胆囊置管+腹腔引流、胆总管囊肿切开置管+腹腔引流、胆囊置管引流、胆总管切开引流、腹腔引流、穿孔修补+胆囊置管+腹腔引流、胆总管囊肿根治术。
1.5 统计学分析
采用SPSS 21.0进行统计学分析,计数资料采用率表示,组间比较采用χ2检验。计量资料符合正态分布采用(±s)表示,多组间比较采用方差分析,方差分析结果有统计学意义的基础上,两两组间对比采用LSD法;不符合正态分布采用M(P25,P75)表示,组间比较采用单因素Kruskal-Waliis秩和检验。以P<0.05为差异有统计学意义。
2 结果
2.1 SPBD患儿基本信息及临床表现
最终纳入36 例患儿中34 例为本院确诊,2 例为外院转入。其中男14例,女22例,男女比例为1:1.57。年龄分布:0~1岁8例,1~2岁12例,2~3岁7例,3~4岁3例,4~5岁3例,5~6岁2例,7~8岁1例。
胆道穿孔患儿临床表现缺乏特异性,本组患儿主要症状包括:腹痛或哭闹21例、呕吐22例、发热18例、腹胀13例、黄疸11例、腹泻4例、大便色浅3例。主要腹部体征包括:腹部膨隆22例、腹部压痛12例、局部肌紧张3例、全腹肌紧张15例。
2.2 诊断特征
本组36例患儿除外于外院手术并已确诊胆道穿孔2例,其余34例中15例初次超声检查提示存在胆道穿孔,6例行再次或多次超声检查后提示胆道穿孔。腹部超声的初次诊断敏感度为44.1%(15/34),再次或多次复查后的最终敏感度为61.8%(21/34)。
22例患儿接受诊断性腹腔穿刺,其中21例患者腹腔穿刺可抽出腹水(胆汁样腹水20例,血性1例)。腹腔穿刺为胆汁样腹水的患儿,后续手术均证实为胆道穿孔,诊断性腹腔穿刺液为胆汁样腹水诊断儿童SPBD的特异度为100%。
2.3 治疗结果
2.3.1 保守治疗:入院后在考虑SPBD诊断情况下选择保守治疗的患儿6例,其中2例在保守治疗7 d后症状加重,最终行手术治疗。详见表1。
2.3.2 手术治疗:32例患儿初次手术情况:30例(其中2例为在我院保守治疗失败患儿)于我院行初次手术,2例于外院行初次手术。在我院进行初次手术的30例患儿分别由15位不同年资的外科医师(从住院总医师至主任医师)实施手术。根据患儿术中情况共实施8种的术式,包括:穿孔部位置管+腹腔引流(8例)、胆囊置管+腹腔引流(13例)、胆总管囊肿切开置管+腹腔引流(3例)、胆囊置管引流(2例)、胆总管切开引流(1例)、腹腔引流(1例)、穿孔修补+胆囊置管+腹腔引流(1例)、胆总管囊肿根治术(1例)。初次手术治疗后,27例症状缓解,围手术期无并发症;3例术后症状仍无法缓解,行再次手术。

表1 保守治疗的SPBD患儿临床特点
将实施例数较多的3 种术式纳入分析,各组间患儿年龄,性别比及病史时间均无统计学差异(P>0.05),术后症状缓解时间无统计学差异(P>0.05),术后腹腔引流管拔管时间及术后出院时间存在统计学差异(P<0.05)。穿孔部位置管+腹腔引流术组术后腹腔引流管的拔管时间短于胆囊置管+腹腔引流术组(P<0.05),胆总管囊肿切开置管+腹腔引流术组和穿孔部位置管+腹腔引流组的术后住院时间短于胆囊置管+腹腔引流术组(P<0.05)。详见表2。
接受初次手术治疗后,4例患儿(初次手术我院3例,外院1例)因症状不缓解接受了二次手术治疗。术中发现,4例患儿腹腔内均存在大量游离或局限性包裹的胆汁,考虑为初次手术胆汁引流不充分所致,给与重新调整腹腔引流或增加胆道置管引流(手术方式见表3)后,4例患儿均症状缓解,出院。
在我院接受初次手术治疗的30 例患儿中,除2例(1例术前怀疑胆道闭锁,1例术前诊断胆总管囊肿)为择期手术中发现胆道穿孔外,其余28例均行急诊手术。手术探查过程中仅有17例(56.7%)可以明确穿孔部位,其中穿孔部位位于左右肝管汇合处1 例(3.3%),位于肝总管2例(6.7%),位于胆囊管与胆总管交界处11例(36.7%),位于胆总管3例(10.0%)。
2.4 随访结果
所有患儿均进行了门诊或(和)电话随访,随访1~11年。31例患儿因合并胆总管囊肿,行胆总管囊肿根治手术(其中2 例于外院手术),根治术距前次胆道穿孔引流手术或保守治疗时间间隔1~19个月。返我院行胆总管囊肿根治术的29 例患儿中,11 例(37.9%)术前行核磁共振胆管造影术(MRCP)检查,明确胰胆管合流异常5例,明确无胰胆管合流异常5例,1例未提及胰胆合流情况。根治手术方式均为胆总管囊肿切除+肝总管空肠Roux-en-Y吻合术,术后出现1例胆漏、1例胰漏,分别保守治疗2周和1个月出院。胆总管囊肿根治术后,患儿常规随访1年。
随访期间未发现合并胆总管囊肿的患儿5例,包括:1例因新生儿溶血造成肝外胆管结石并发胆道穿孔,随访中发现门静脉海绵样变并消化道出血,行Rex分流手术;1例随访期间黄疸不能消退,基因检查后明确为家族性胆汁淤积症,于术后1个月后行胆囊-空肠(间置)-横结肠(升结肠与横结肠交界处)分流术;其余3例术后随访3、5、11年,未发现胆道系统畸形或再发胆道系统疾病,生长发育良好。
3 讨论
儿童SPBD较为罕见。文献报道,儿童SPBD高发年龄为6个月[14]或1岁之内[15],而最小发病年龄为孕25周的胎儿[14]。本研究患儿的中位发病年龄为1.68岁,并且绝大多数病例为3岁以内的婴幼儿。国外大多数是个案报道,发病儿童的性别比鲜有提及,我国的荟萃研究[7]指出男女性别比为1:1.74,本研究中男女比为1:1.57,这可能与女孩有较男孩更高的儿童胆道系统发病率[16]有关。
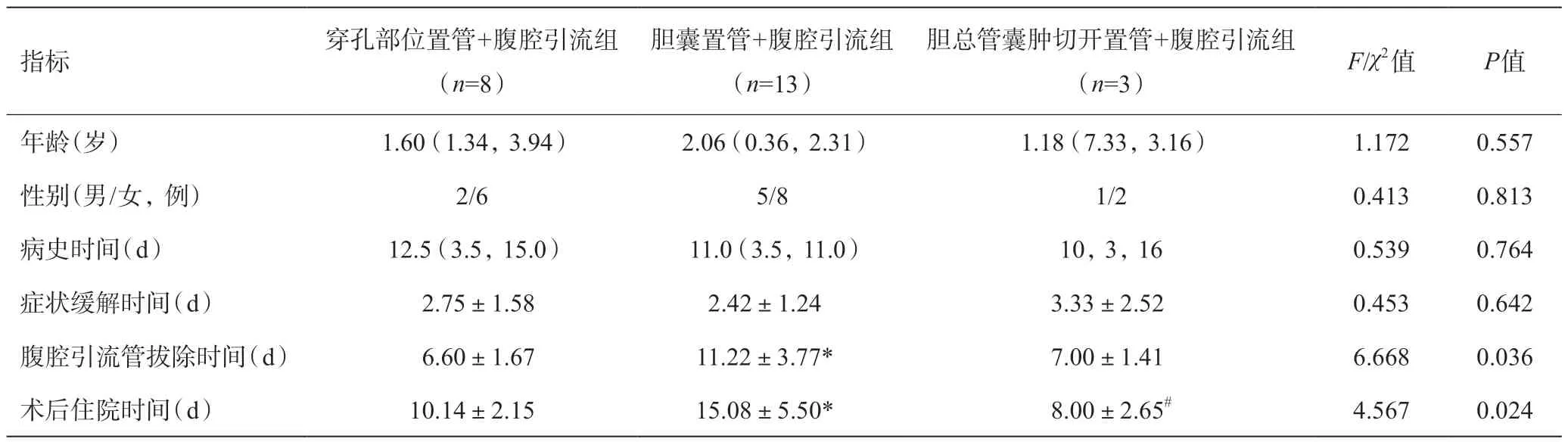
表2 SPBD三种主要手术方式的比较
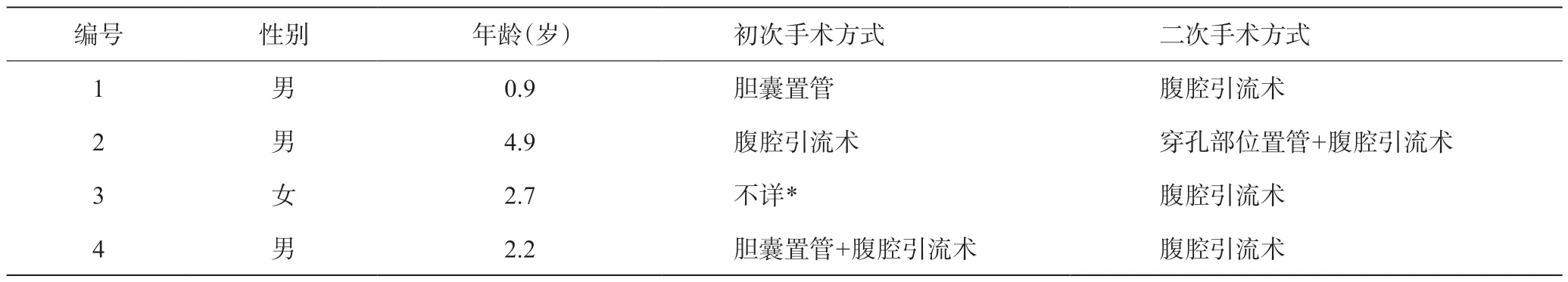
表3 接受二次手术治疗的患儿情况
SPBD的病因不清,胰胆合流异常被认为是儿童SPBD的一个重要病因。胰胆合流异常所致胰液逆行进入胆道,胰酶被激活破坏正常胆道壁层结构,与胆道压力的增加共同造成肝外胆道穿孔。日本Ohkawa等[17]和Yano等[18]分别报道了3例肝外胆道穿孔患儿均合并胰胆管合流异常和胆总管囊肿;伊朗Banani等[14]报道3 例儿童肝外胆道穿孔的病例虽然胆道造影未提示明确的胆总管囊肿,但均存在胆胰合流异常。国内荟萃分析发现320例儿童胆道穿孔患儿合并胆总管囊肿的占32.4%,合并胆胰合流异常的占28.4%[7]。本研究中明确存在胰胆管合流异常的患儿仅有5例(均为随访时MRCP证实),这可能与我们在一次引流术和二次胆总管囊肿根治术时,未行胆道造影,且随访中MRCP的实施比例较低(11/29)有关。
有亚洲学者认为儿童肝外胆道穿孔与胆总管囊肿有共同病因且相关性紧密[14],本研究也发现类似情况:36例SPBD患儿中31例(86.1%)合并胆总管囊肿。但另一项美国的研究报道了4例儿童肝外胆道穿孔的病例,并回顾了之前57篇肝外胆道穿孔的相关文献(包括94例胆道穿孔),只有2例明确合并胆总管囊肿[19]。这种差异可能与亚洲国家尤其是东亚国家胆总管囊肿发病率明显高于西方国家(胆总管囊肿在日本的发病率是西方国家发病率的100~150 倍)有关[16]。SPBD的穿孔最常见的部位为胆囊管与肝总管交接的部位,本研究中有36.7%的病例穿孔部位位于此处,而国内外大样本的报道此处穿孔所占比例分别为34.3%[7]和40.0%[19]。此解剖位置位于胆囊血供和胆总管血供的末梢,易发生局部缺血,因此容易出现穿孔[20]。
本组患儿SPBD的临床症状主要包括腹痛、呕吐、腹胀、发热、黄疸、大便色浅、腹泻,与国内外报道类似[7,19],症状并不具有特异性。普遍认为影像学检查在诊断儿童SPBD的作用有限。而我院腹部超声在SPBD的诊断上有较高的敏感度(61.8%),而且本研究中,再次或多次的超声检查可以提高诊断的敏感度。因此超声检查对临床医师诊断SPBD有着很高的参考价值。腹腔穿刺可作为诊断SPBD的重要方法。腹腔穿刺抽出胆汁样腹水可作为SPBD的临床确诊标准,国内外均有较多报道[7,19],本研究中腹腔穿刺的诊断特异度为100%(20/20),同样印证了上述结论。因此结合患儿病史及临床表现,在除外胃肠道穿孔的前提下,腹腔穿刺抽出胆汁样腹水可以明确SPBD的诊断。
国内外大多数报道认为,SPBD均需手术治疗。一部分原因是报道中的很多病例术前未明确SPBD诊断,必须通过手术探查来明确。而对于儿童SPBD的保守治疗,鲜有报道。Sahnoun等[21]和Malik等[10]报道了保守治疗SPBD成功的案例。而本组36例中有6例患儿初始选择保守治疗,2例因症状无缓解,最终选择手术治疗;4例患儿保守治疗成功。给予抗生素、对症治疗结合腹腔穿刺引流后,如果症状不能有效缓解,应积极手术干预。在手术方式的选择上,国内外文献都没有给出一种适合所有患儿的手术方式,很多手术方法都可以达到缓解症状、治愈疾病的效果。国内的报道[7]主要应用以下手术方法:T管引流+腹腔引流术(63.2%),单纯腹腔引流术(14.7%),胆囊造瘘+腹腔引流术(7.2%),胆道穿孔修补+腹腔引流术(6%)。我们的研究中由于实施手术的医师人数较多,各个患儿临床表现和术中所见不尽相同,因此也存在多种不同的手术方式。
本研究中实施例数相对较多的3 种术式均做到了对胆道系统的减压和对腹腔的充分引流。胆道系统的减压可以有效减少胆汁流入腹腔,减少胆汁对腹腔脏器和腹膜的刺激,还能有助于胆道穿孔部位的修复和愈合,缩短病程。而胆囊置管引流+腹腔引流术由于胆道内引流管位于胆囊内,胆道减压的效果可能弱于另两种术式,穿孔愈合的时间相对较长,增加了腹腔引流管拔除时间和术后住院时间。因此,我们推荐腹腔引流的同时进行胆道系统的引流。对于术中可以明确探查到穿孔部位的患儿可以经穿孔部位置入引流管引流,本研究中置入蕈伞状橡胶引流管,确切固定后不易脱出。对于术中未见明确穿孔部位的患儿,我们建议行胆囊置管引流,不推荐行胆总管切开置管引流。因为胆道穿孔患儿胆总管区域往往水肿较重,解剖关系不清,术中特意寻找胆总管行切开引流有可能造成不必要的副损伤;另外对胆总管区域的操作会增加局部粘连可能,对于合并胆总管囊肿需要再次行根治术的患儿,可能会增加再次手术解剖胆总管的难度。而4例患儿二次手术均由于胆汁引流不充分所致,仅调整了腹腔引流或增加了胆道内引流后,患儿症状均得到缓解,再次印证对于胆道穿孔的患儿腹腔内胆汁的充分引流及胆道系统的减压是手术治疗的关键。
合并胆总管囊肿的SPBD患儿在引流术后,胆总管囊肿的切除根治术是必须的。本研究中胆总管囊肿根治术距初次引流手术平均间隔4.52 个月,最短1个月,手术可行、效果满意。因此对于合并胆总管囊肿的胆道穿孔患儿,在进行引流术后1个月以上进行胆总管囊肿根治手术是安全可行的。对于不合并胆总管囊肿的胆道穿孔患儿,应长期随访,行腹部超声检查,观察胆道情况。本组胆道穿孔患儿总体预后良好,无死亡病例。绝大部分患儿长期随访无明显长期并发症出现,生长发育未见明确异常。
综上,儿童自发性胆道穿孔虽然总体发病率低,但在我国儿科临床中,尤其是在梗阻性黄疸的小婴儿和儿童急腹症中偶能遇到。由于临床表现缺乏特异性,因此基于病史和查体信息很难明确诊断。而腹部超声检查和诊断性腹腔穿刺目前是诊断儿童自发性胆道穿孔的主要手段。虽然部分病例可以通过保守治疗痊愈,但手术治疗尤其是联合胆道系统引流的腹腔引流术仍是诊断和治疗自发性胆道穿孔的重要手段。

