替吉奥阿帕替尼治疗晚期难治性卵巢癌的疗效对比及药物对HE4 CA125及CA199的影响
刘建婷,张荣生,邓天丽,侯松萍
(大理大学第一附属医院,云南 大理 671000)
卵巢癌(ovarian cancer,OC)是一种致死率较高的妇科恶性肿瘤,因其症状隐匿,导致多数患者就诊时已进入晚期,临床多使用手术、放化疗等方法来治疗OC,但其3年复发率仍然较高[1]。近年来研究[2]表明,血清肿瘤标志物糖类抗原125(carbohydrate antigen 125,CA125)、人附睾分泌蛋白4(human epididymis protein4,HE4)等在恶性肿瘤的早期诊断、病情监测中均有重要意义,且血清HE4、CA125异常表达与OC的发生及病情恶化存在密切相关。糖类抗原199(carbohydrate antigen 199,CA199)是类黏蛋白的糖类蛋白,已被证实可与CA125、HE4等联合诊断OC,弥补CA125单项检测的不足[3]。基于此,本文通过探讨分析医院收录的晚期OC患者相关资料,对比分析了替吉奥、甲磺酸阿帕替尼治疗晚期OC的疗效,并进一步探讨了两种治疗方案对上述因子水平的影响,以期为临床防治难治性OC提供新思路。现报告如下。
1 资料与方法
1.1一般资料:回顾性分析2018年4月至2019年9月本院收治的88例难治性OC患者资料,所有患者均经手术或病理活检确诊。按治疗方法不同将患者分为观察组以及对照组各44例,其中观察组年龄32岁~57岁,平均年龄为(44.52±12.16)岁;平均病程(27.75±9.28)个月;TNM分期:24例Ⅲ期,20例Ⅳ期。对照组年龄31岁~58岁,平均年龄为(45.07±13.54)岁;平均病程(27.64±9.18)个月;TNM分期:27例Ⅲ期,17例Ⅳ期。两组一般资料间差异无统计学意义(P>0.05)。本研究已经院伦理委员会审核批准[审批件(2018)伦审第(11)号]。纳入标准:①患者年龄31岁~58岁之间;②采用美国东部肿瘤协作组(ECOG)[4]体力状况评分患者体力状况在3分以内;③器官功能水平良好;④均已签署知情同意书。排除标准:①TNM分期<Ⅲ期者;②1个月内接受过抗肿瘤治疗者;③有高血压、糖尿病或严重心血管疾病者;④妊娠期或哺乳期妇女。
1.2方法:观察组患者口服500mg/次甲磺酸阿帕替尼(江苏恒瑞医药股份有限公司,国药准字H20140103)治疗,于饭后30min温水送服,1次/d。4周为一个疗程,若患者在治疗过程中出现病情恶化或不可耐受的不良反应,需立即停止服药。除此之外,如果患者出现了与甲磺酸阿帕替尼相关的III级或以上不良反应现象,则视情况决定减半药量或停止用药。对照组患者口服40mg/次的替吉奥胶囊(生产厂家:江苏恒瑞医药股份有限公司;规格:20mg/粒;批号:16110496),2次/d。21d为一个疗程,两组均接受至少2个疗程的化疗。
1.3观察指标:①采集所有患者空腹静脉血5mL,以3000r/min离心10min后分离新鲜血清0.5mL,-80℃冻存待检;HE4检测采用ELISA法测定,试剂盒购自北京热景生物技术有限公司。CA125、CA199采用电化学发光方法定量测定,试剂盒购自罗氏公司。严格按照实际和说明书执行操作。②治疗3个月后开始评价两组疗效。③按照WHO抗癌药毒性反应分度标准将不良反应分为非血液学不良反应[5]:乏力、腹泻、高血压、手足综合征、消化道出血、蛋白尿和血液学不良反应:血红蛋白浓度下降、血小板计数减少、白细胞计数减少、中性粒细胞比值降低。
1.4疗效评价标准:参考实体瘤疗效评价(Response Evaluation Criteria In Solid Tumour,RECIST)标准,对目标病灶的最长径进行测量,然后将所有最长径的和计算出来,并且将其与患者接受治疗前的最长径和进行比较。①完全缓解:患者所有的目标病灶全部消失;②部分缓解:相较于接受治疗前,患者接受治疗后目标病灶之和下降高于30%;③病变稳定:相较于治疗前,患者接受治疗后的病灶最长径之和位于减少30%至增加20%之间;④病变进展:相较于接受治疗前,患者病灶最长径之和增加20%以上。

2 结 果
2.1评估治疗后全体患者治疗效果:两组治疗疗效间差异有统计学意义(P<0.05);治疗后观察组总有效率50.00%,显著高于对照组的27.27%(P<0.05)。见表1。
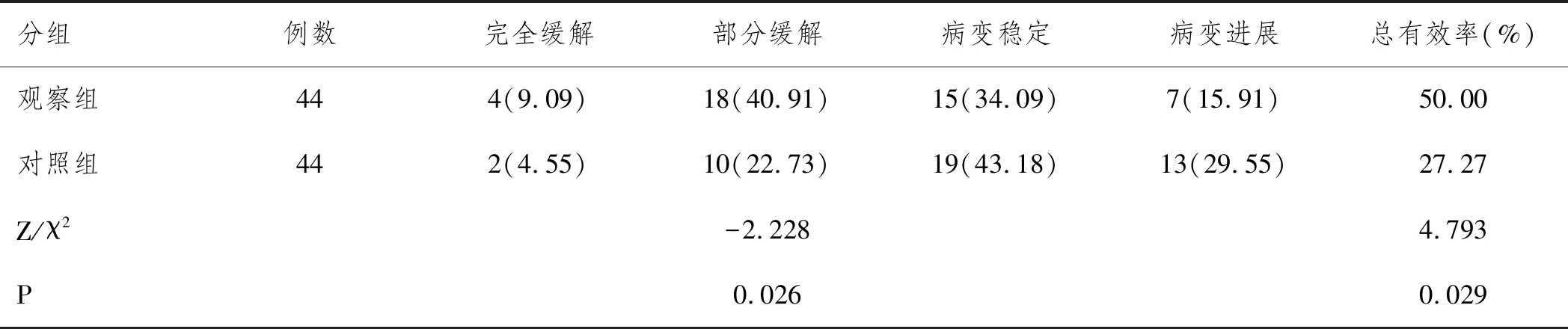
表1 评估治疗后全体患者治疗效果n(%)
2.2对比治疗前后全体患者血清肿瘤标志物变化情况:观察组治疗后HE4、CA125与CA199均较治疗前及对照组有明显降低(P<0.05);且两组治疗前后HE4、CA125及CA199差值间差异均有统计学意义(P<0.05)。见表2。
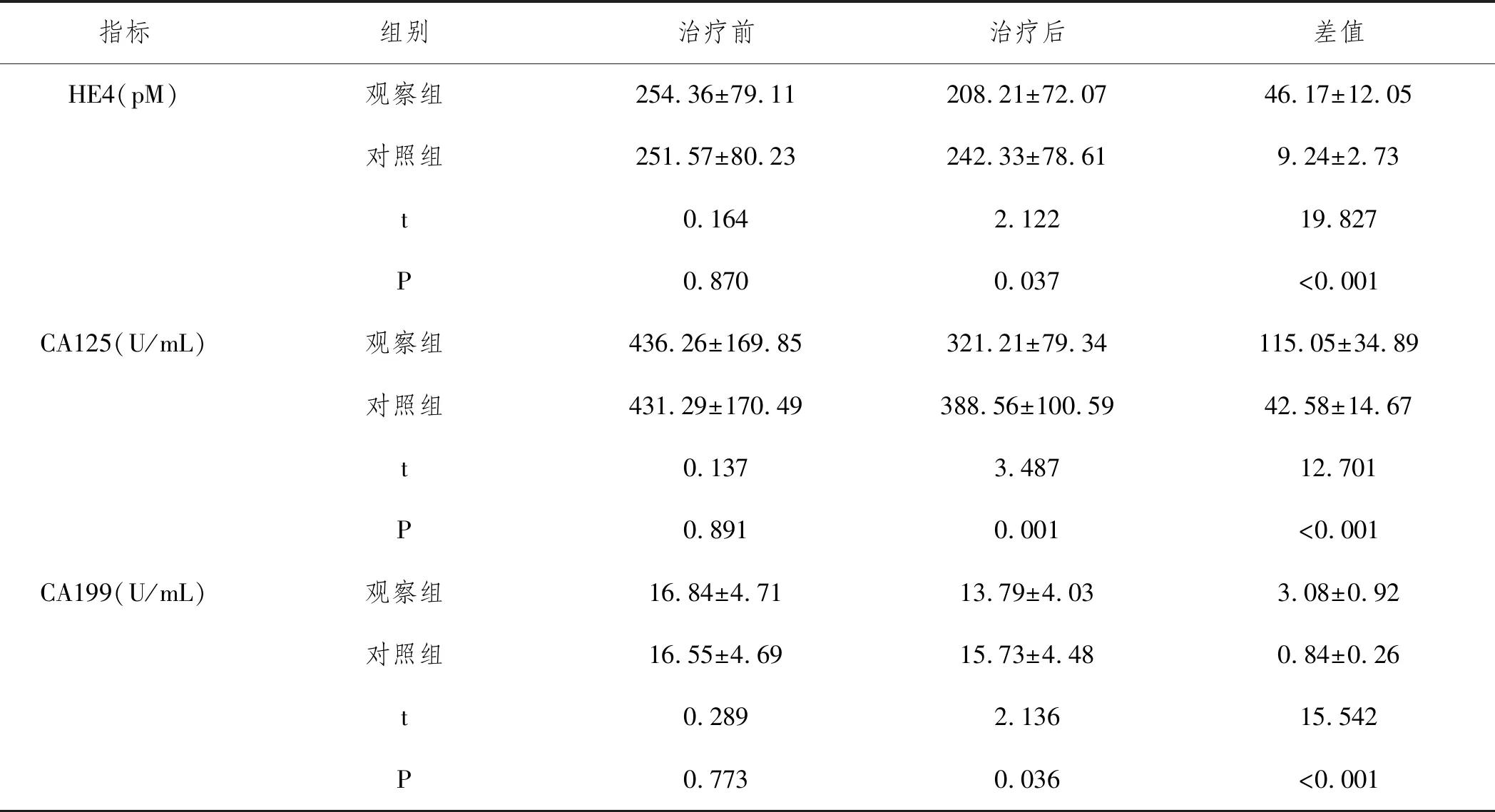
表2 治疗前后全体患者血清肿瘤标志物变化比较
2.3评估治疗后患者非血液学不良反应情况:治疗后观察组非血液学不良反应率52.27%,显著低于对照组的75.00%(P<0.05),见表3。

表3 评估治疗后患者非血液学不良反应情况n(%)
2.4评估治疗后患者血液学不良反应情况:治疗后观察组患者的血液学不良反应率36.36%,显著低于对照组的77.27%(P<0.05),见表4。

表4 评估治疗后患者血液学不良反应情况n(%)
3 讨 论
卵巢位于患者的盆腔深处,这使得OC早期无明显症状,流行病学表明:卵巢癌晚期患者的死亡率居世界妇科肿瘤之首[6]。手术与化疗联合的方法是如今治疗OC的主要方法,但是长期化疗也会对患者的身体造成无法修复的损害,因此患者预后往往较差。因此,尽早诊断OC,并给予对应的治疗方案是改善患者预后的关键。阿帕替尼是一种小分子抗血管生成靶向药物,可以与血管的内皮生长因子受体-2的酪氨酸激酶的ATP进行结合,以此来影响酪氨酸激酶激活过程,从而达到减少血管内皮生长因子中依赖内皮生长因子受体-2的数量的目的,以此来抑制肿瘤血管的生长[7]。国内研究结果表明,阿帕替尼治疗晚期卵巢癌均有不错的疗效[8]。
近年来医学发展迅速,肿瘤标志物已成为诊断、评估肿瘤疗效及预后的重要工具,其中HE4是一种新的血清肿瘤标志物,在卵巢癌患者的血清中含量极高,但是在人体其它良性肿瘤及正常组织中是不表达或者低表达,可作为临床诊断OC的敏感指标[9]。CAl25是上皮性卵巢癌传统的血清肿瘤标志物,但是对于卵巢癌的敏感性和特异性不高,早期诊断率低,而且在一些如子宫内膜异位症、卵巢良性肿瘤等妇科良性疾病中存在部分假阳性。CA199属于细胞膜上的糖脂质,其被广泛应用于消化道肿瘤的检测与诊断,研究表明,CA199能够有效弥补CA125在检测卵巢粘液性癌方面的不足,且上述指标均被证实与OC的发生发展存在密切相关[10]。本研究结果显示,两组HE4、CA125与CA199水平具有随时间变化趋势,且时间因素作用会因组别不同而有所差异,且观察组治疗后HE4、CA125与CA199均较治疗前及对照组有明显降低(P<0.05)。国内对胃癌患者的研究[11]也曾表明,阿帕替尼可明显降低患者血清中的CA199水平。考虑原因为患者在口服阿帕替尼后,这药物可迅速被肠道吸收,并且高度选择性的与内皮生长因子受体-2的ATP节点相结合,使得下游信号的传导受到阻断,明显抑制肿瘤组织新血管形成,发挥抗肿瘤的作用。
除此之外,阿帕替尼可以抑制PDGFR-β等酪氨酸激酶,抑制肿瘤细胞的增殖、迁移,并抑制Akt及ERK1/2的磷酸化,使细胞周期停滞于G2/M期,进而诱导肿瘤细胞的凋亡,且其甲磺酸阿帕替尼还能够促进介导免疫细胞攻击肿瘤,提高抗OC的效果。本次研究也表明,观察组总有效率为50.00%,较对照组有明显升高(P<0.05)。另有国内[12]等研究显示接受甲磺酸阿帕替尼治疗的晚期OC患者,客观有效率为33%~39.3%,略低于本研究结果,考虑与其研究样本的差异有关。本研究结果还发现,观察组血液不良反应率、非血液学不良反应率均显著低于对照组。提示阿帕替尼治疗的不良反应少,安全性较好。
综上所述,使用甲磺酸阿帕替尼进行治疗晚期难治性OC的疗效显著,不仅可显著降低患者血清内的CA125、HE4、CA199水平,且其药物毒副作用小,安全性佳,值得临床推广应用。但本研究尚存不足,如研究样本较小,未随访观察患者远期疗效及患者预后,需行进一步的大样本,远期随访研究。
——评《卵巢恶性肿瘤诊疗手册》

