呼伦湖水体悬浮颗粒物中有机质的赋存特征及来源解析
王雯雯, 郑丙辉, 郑朔方, 陈俊伊, 姜 霞, 王书航*
1.中国环境科学研究院, 湖泊水污染治理与生态修复技术国家工程实验室, 北京 100012 2.中国环境科学研究院, 国家环境保护湖泊污染控制重点实验室, 北京 100012 3.北京师范大学水科学研究院, 北京 100875
呼伦湖是我国第五大淡水湖,也是我国北方干旱-半干旱区面积最大的浅水湖泊[1-2]. 呼伦湖地处欧亚大陆腹地,流域跨中蒙两国,在调节区域气候、涵养水源、防止荒漠化、保护生物多样性以及维系呼伦贝尔草原生态平衡,乃至维护我国北方生态安全等方面发挥着不可替代的作用. 近年来,在水文气候条件变化及人类活动的双重影响下,呼伦湖水质常年处于GB 3838—2002《地表水环境质量标准》劣Ⅴ类水平,水体富营养化严重,夏季常有“水华”现象发生[3]. 呼伦湖水体中悬浮颗粒物的平均浓度为41.25 mgL,明显高于太湖(34.31 mgL)[4]、鄱阳湖(23.87 mgL)[5]、千岛湖(1.41 mgL)[6]、东湖(18.72 mgL)[7]、梁子湖(12.41 mgL)[7]及洪湖(10.98 mgL)[7]等我国大多数湖泊. 悬浮颗粒物的分布和赋存特征一方面可以影响太阳辐射在水中的传输和分布[8-9],对浮游藻类、沉水植物的生长繁殖造成影响;另一方面,悬浮颗粒物可与水体中的污染物相互作用成为其载体,在很大程度上决定着污染物在环境中的迁移转化及其归宿[10-13],而SPOM(suspended particulate organic matter,悬浮颗粒物中的有机质)的组成和性质对于营养盐、重金属离子和有机物等污染物的交换吸附具有重要作用.
SPOM是水体中有机质的重要存在形式[4,14],通常由碎屑、动物粪粒、浮游动植物细胞和细菌等构成,在全球碳循环中发挥着重要作用[15-17]. 研究[18]表明,在河口和海岸边缘沉积和埋藏的POC (particulate organic carbon, 颗粒态有机碳)占全球海洋碳汇的90%左右. SPOM不仅为水生异养细菌和浮游动物提供食物来源,也是溶解态有机物和营养盐的来源之一[19-20]. 作为潜在可以被生物利用的营养源,SPOM的迁移转化以及伴随的营养物质再生是浮游藻类营养盐快速供给的重要来源之一[4],对湖泊水体富营养化及其水环境质量具有深远影响. 呼伦湖水环境中有机质的研究多集中在沉积物中有机碳的分布、沉积、同位素特征及其环境指示意义[21-26],但对于水体中有机质的研究相对较少[27],尤其是SPOM相关的研究.
该研究综合利用连续提取法、δ13C (碳稳定同位素)、三维荧光光谱(three-dimensional excitation-emission matrix fluorescence spectra, 3D EEMs)结合平行因子分析技术(parallel factor analysis, PARAFAC)对呼伦湖水体中SPOM的赋存特征及其来源进行了系统研究,主要包括SPOM中有机碳的含量及组分、荧光特性、来源及相对贡献,以及SPOM的生物可利用性等,以期全面地了解呼伦湖水环境中有机质的赋存特征、生物化学特性,同时为呼伦湖的水环境和富营养化治理提供参考.
1 材料与方法
1.1 研究区域
呼伦湖(48.55°N~49.33°N、116.97°E~117.81°E),又名达赉湖[25]. 呼伦湖流域(包括哈拉哈河流域和海拉尔河流域)位于中国和蒙古国境内,面积达2.92×105km2,其中我国境内流域面积为1.08×105km2,占37%;蒙古国境内流域面积为1.84×105km2,占63%. 呼伦湖自然来水主要为克鲁伦河、乌尔逊河和海拉尔河,排水通道为新开河.
呼伦湖流域属中温型半干旱大陆性气候,具有中温带为主的寒暑剧变特点. 春季干旱多大风,夏季温凉短促,秋季降温急剧、霜冻早,冬季严寒而漫长[25]. 由于保护区大气透明度高,太阳辐射强度大,全年平均日照时数为 3 104.7 h. 流域多年年均降水量为264.3 mm,多集中在夏季,6—9月降水量占全年的80%~86%,多年平均蒸发量为 1 411 mm[28].
1.2 样品的采集与处理
该研究于2019年8月在研究区布设55个采样点进行悬浮颗粒物样品的采集,采样点分布如图1所示.
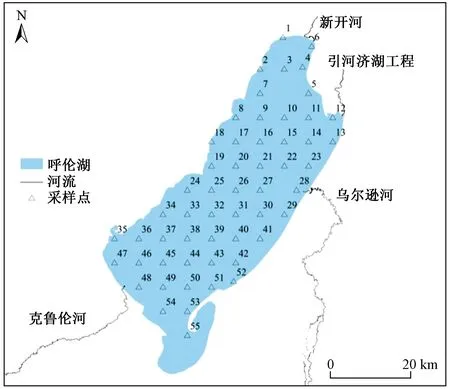
图1 呼伦湖采样点分布Fig.1 Distribution of sampling sites in Lake Hulun
用5 L有机玻璃采水器在各采样点采集距水面0.5 m的上覆水40 L于干净塑料桶内,运回野外实验站后用Whatman GFF玻璃纤维滤膜(450 ℃,灼烧3 h)过滤,将带有悬浮颗粒物的滤膜于-50 ℃真空冷冻干燥,将悬浮颗粒样品从滤膜上刮下并置于样品袋中保存备用.
1.3 样品分析测试方法
1.3.1悬浮颗粒物浓度的测定
上覆水中TSS (total suspended solids,总悬浮颗粒物)、OSS (organic suspended solids,有机悬浮颗粒物)和ISS (inorganic suspended solids,无机悬浮颗粒物)浓度采用重量法测定. 将GFC膜、瓷坩埚分别于105 ℃烘至恒质量,分别记为m1(g)、m2(g),过滤水样的体积记为V(mL),将滤有悬浮颗粒物的膜置于坩埚中,105 ℃烘干至恒质量,冷却后称量,记为m3(g). 将滤膜继续550 ℃加热6 h,冷却称量,记为m4(g),TSS、ISS和OSS浓度分别按式(1)(2)(3)计算:
[TSS]=(m3-m2-m1)V
(1)
[OSS]=(m3-m4)V
(2)
[ISS]=[TSS]-[OSS]
(3)
1.3.2TOC和TN浓度测定
样品的预处理:称取适量悬浮颗粒物样品置于100 mL离心管内,加入足量的3 molL HCl,充分反应去除碳酸盐,然后用超纯水洗至中性,冷冻干燥后研磨过100目( 0.15 mm )尼龙筛备用.
取适量处理后的悬浮颗粒物样品,用元素分析仪(elementar vario MACRO cube, Elementar Analysensysteme GmbH, 德国)测定TOC(total organic carbon,有机碳)和TN(total nitrogen,总氮)的浓度,并计算CN(TOC浓度与TN浓度的比值).
1.3.3有机质组分的连续提取
SPOM的赋存形态采用连续提取法测定:取1 g悬浮颗粒物干样,加入50 mL H2O置于25 ℃水浴振荡1 h后离心,上清液用0.45 μm滤膜过滤(下同),得到上清液A为WEOM (水提态有机质);用20 mL饱和NaCl清洗残渣A后,再加入50 mL NaOH (1 molL)-Na4P2O7(0.1 molL)混合溶液,并用0.1 molL HCl调节pH=13,25 ℃下振荡1 h后离心、过滤,得到上清液B和残渣B;残渣B用饱和NaCl清洗后于55 ℃烘干,得到HM (提取残渣). 取20 mL上清液B,用0.5 molL H2SO4调节pH为1.0~1.5,并在60 ℃下保持1.5 h,静止8 h后,离心、过滤,上清液为FA (富里酸),沉淀为HA (胡敏酸). WEOM、FA、HA含量均采用TOC分析仪(TOC-V, SHIMADZU, 日本) 测定,HM含量采用重铬酸钾氧化滴定法测定,SPOM含量为WEOM、FA、HA和HM含量之和,均以碳质量计,单位为gkg.
1.3.4δ13C的测定
选取部分点位的悬浮颗粒物样品测定δ13C值. 取适量预处理好的样品于石英管(预先在马弗炉850 ℃灼烧2 h)中,加入2~3 g CuO丝,在真空系统中抽真空后焊封,于马弗炉850 ℃灼烧5 h后在真空系统中纯化CO2,并在Finnigan MAT252同位素质谱仪上测定δ13C值,以美国南卡罗莱纳州白垩系Pee Dee组拟箭石化石(简称“PDB”)作为标准品,分析误差为±0.2‰.
δ13C=1 000‰×(RRs-1)
(4)
式中,R为样品的13C12C自然丰度比值,Rs为标准品的13C12C自然丰度比值.
1.3.5WEOM三维荧光光谱扫描及平行因子分析
取1.3.3节中WEOM的提取液A,使用紫外-可见分光光度计(D5000,美国哈希公司)测定样品的紫外-可见吸收光谱,扫描波长范围为200~800 nm,步长为1 nm,以超纯水为参比. 荧光光谱采用荧光分析仪(F-7000,Hitachi, 日本)进行分析,λEx(激发波长)扫描范围为200~450 nm,λEm(发射波长)扫描范围为250~600 nm,λEx和λEm增量均设为2 nm,狭缝宽度为10 nm,扫描速率为 12 000 nmmin. 三维荧光数据在进行平行因子分析之前需进行预处理,方法参考文献[29]. 在MATLAB软件中使用DOM Fluor工具箱运行PARAFAC模型对预处理后的三维荧光数据进行分析,通过核心一致性检测和裂半检测来验证PARAFAC建模的有效性,并确定最优荧光组分个数[30].
HIX (humification index,腐殖化指数)为λEx=254 nm时,λEm=436~480 nm的荧光峰值面积与λEm=300~344 nm的荧光峰值面积的比值[31].
1.4 SPOM来源的相对贡献率计算
采用端元混合模型[32-34]估算SPOM的PL(陆源贡献率)和PS(自生源贡献率). 利用δ13C和CN估算PL和PS,其计算公式分别参照文献[25][34]. 假设预处理后悬浮颗粒物样品TOC和TN含量分别为C和N,来自陆源与自生源的TOC和TN含量分别为CL、NL与CS、NS.
C=CL+CS
(5)
N=NL+NS
(6)
RL=CLNL
(7)
RS=CSNS
(8)
式中,RL和RS分别为陆源和自生源CN的端元值.
通过式(5)~(8)可以得出:
NL=(C-RS×N)(RL-RS)
(9)
NS=(C-RL×N)(RS-RL)
(10)
CL=RL(C-RS×N)(RL-RS)
(11)
CS=RS(C-RL×N)(RS-RL)
(12)
将端元值和实测的TOC和TN含量代入式(9)~(12),即可得到PL和PS.
PL=CLC
(13)
PS=CSC
(14)
δ13C=δ13CL×PL+δ13CS×PS
(15)
1=PL+PS
(16)
式中,δ13C为样品实测值,δ13CL为陆源有机质中δ13C端元值,δ13CS为自生源有机质中δ13C端元值. 一般而言,δ13CL和δ13CS由研究区实际情况决定,并非是固定的.
1.5 数据处理
所有分析均做3次平行,结果以3次样品分析的平均值表示(误差<5%). 采用Excel 2010、Origin 8.0、SPSS 17.0、ArcGIS 10.2和Surfer 14.0软件进行试验数据的统计检验、分析和绘图.
2 结果与讨论
2.1 呼伦湖水体悬浮颗粒物的分布
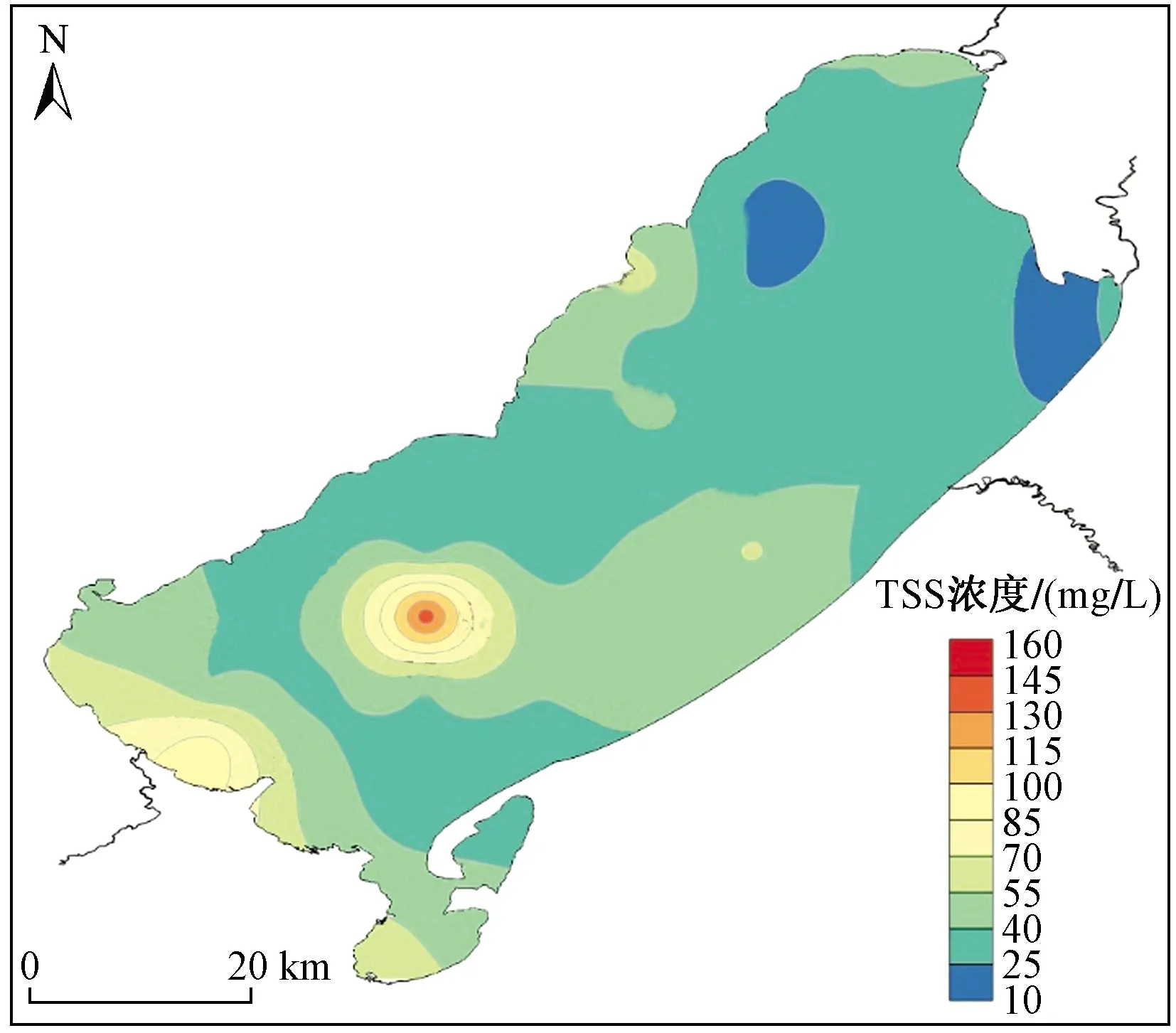
图2 呼伦湖水体中TSS浓度的空间分布Fig.2 Spatial distribution of the concentration of total suspended solids (TSS) in water of Lake Hulun
2.2 呼伦湖SPOM含量及组分特征
WEOM是SPOM中较为活跃的组分,是微生物生长的速效基质,其含量高低直接影响悬浮颗粒物上微生物的活性和微生物量[36]. HA具有溶于碱而不溶于酸的特点,颜色较深,为棕至暗褐色;而FA(又称黄腐酸)具有既溶于酸又溶于碱的特点,颜色浅黄[37]. HM是SPOM中最稳定的形态,具有酸碱不溶、难分解的特定[38]. 呼伦湖中SPOM的主要组分为HM(见图3),HM含量在6.91~22.3 gkg之间,占SPOM的43.6%~80.9%,平均值为61.2%,为SPOM的优势组分. FA和HA含量分别在1.7~5.6和1.8~5.4 gkg之间,分别占SPOM的18.0%和14.8%. WEOM含量最低,在0.45~2.3 gkg之间,占SPOM的6.0%.
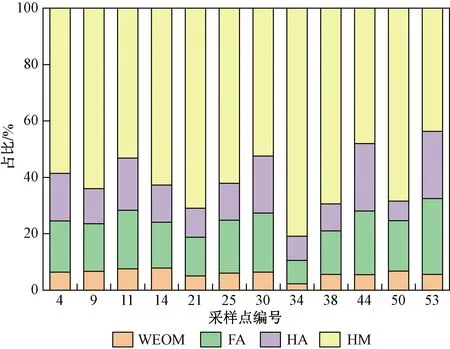
图3 呼伦湖SPOM组分的占比Fig.3 Proportions of the components in SPOM of Lake Hulun
2.3 呼伦湖悬浮颗粒物中WEOM的荧光组分分析
呼伦湖悬浮颗粒物中WEOM含有3个荧光组分,即C1(component 1,组分1)、C2(component 2,组分2)和C3(component 3,组分3)(见图4),主要反映类腐殖质和类蛋白质两类荧光峰. 其中C1组分的荧光峰对应的λEx和λEm分别为244和434 nm,反映的是陆源输入的类富里酸荧光峰[39-40];C2组分的荧光峰对应的λEx在272和368 nm处,λEm在480 nm附近,反映的是陆源输入的类腐殖酸荧光峰[41-42];C3组分的荧光峰对应的λEx在224和276 nm处,λEm在346 nm附近,反映的是生物降解源的类色氨酸荧光峰,主要与微生物和浮游植物的活动有关,也可能受到生物污水和工业废水等外源输入所携带的微生物影响[43-45].
WEOM的总荧光强度在1.69~4.68 R.U.之间,平均值为3.64 R.U.,其中C1组分和C2组分的荧光强度分别为0.67~1.88和0.61~1.63 R.U.,两个类腐殖质组分对SPOM总荧光强度的平均贡献率在61.3%~76.1%之间,平均值为70.4%,为呼伦湖水体中SPOM的主要荧光组分. 类色氨酸组分C3的荧光强度在0.40~1.53 R.U.之间,平均值为1.08 R.U.,对SPOM总荧光强度的贡献率为29.6%.
2.4 呼伦湖SPOM的来源解析
湖泊水体SPOM的来源主要包括陆源和自生源两大类. 自生源SPOM主要来自于水生植物、藻类和细菌等分泌、排泄物及其残体分解产物,以类蛋白物质为主;陆源SPOM主要来自土壤、陆地植物碎屑及人类活动,以类腐殖质物质为主[46-48]. 不同来源的有机质,其碳同位素和CN值具有各自的特征值,并且在物理混合中具有保守性质,据此可以有效辨析SPOM的来源.
根据光合作用途径的差异性,陆生植物可分为C3、C4和CAM三类. C3植物的δ13C分布在-37‰~-24‰之间,C4植物在-19‰~-9‰之间,CAM植物在-30‰~-10‰之间[49-50]. 根据水生植物与大气CO2的关系,可将水生植物简单分为漂浮植物和沉水植物,漂浮植物的δ13C与C3植物接近,介于-37‰~-24‰之间,挺水植物的δ13C值约在-30‰~-24‰之间[51]. 呼伦湖水体悬浮颗粒物中δ13C变化范围为-27.2‰~-26.2‰,平均值为-26.6‰,与呼伦湖周边草地(-25.96‰)、土壤(-26.04‰)及牲畜粪便(-26.13‰)的δ13C值[25]接近,表明呼伦湖水体SPOM可能以陆源输入为主.
2.5 呼伦湖SPOM的生物有效性分析
呼伦湖SPOM的主要组分是非可提取态的HM,HM占SPOM的61.2%;而溶解态的有机质组分(WEOM+FA+HA)仅占SPOM的38.8%. 其中,生物有效性最高的WEOM仅占SPOM的6%左右,并且WEOM的荧光组分主要以分子量相对较大的、难降解的类腐殖质为主,而分子量较小的、容易被生物降解的类色氨酸类物质所占比例最小. 一般来说,HIX值在4~10之间,说明有机质腐殖化程度较强,自生源组分的比例较小[31]. 呼伦湖WEOM的HIX值在4.09~7.40之间,平均值为6.09,WEOM表现出较强的腐殖化特征,这与荧光组分的调查结果一致. 因此综合SPOM的组分构成和荧光特性可以看出,SPOM的腐殖化程度较强,生物可利用性较低. 但自1960年以来,呼伦湖地区年均气温总体呈升高趋势,20世纪六七十年代年均气温为0.45 ℃,八九十年代年均气温升至1.44 ℃,2000年以来年均气温达到1.83 ℃[27],温度的升高有利于湖泊藻类的生长. 近年来,呼伦湖水华暴发已呈常态化,并且随着温度的升高,水华发生的面积增大、持续时间延长,浮游藻类在新陈代谢及腐解的过程中会向水体贡献大量类蛋白组分的有机质,导致自生源有机质含量的增加,进而导致SPOM生物可利用性有增强的趋势.

表1 呼伦湖SPOM陆源和自生源的相对贡献率
太湖与呼伦湖流域面积、水质和富营养化程度相当. 但太湖水体WEOM的荧光组分以类蛋白组分为主,类蛋白荧光组分占比的平均值为72.3%[4],显著高于呼伦湖(29.6%). 另外,太湖水体SPOM的HIX平均值为0.7[4],显著低于呼伦湖(6.09). 与呼伦湖相比,太湖频频暴发的蓝藻水华事件很可能与太湖水体中SPOM的生物可利用性较高有关. 因此,在未来呼伦湖水环境质量改善及富营养化防治工作中,应开展SPOM与溶解性有机质之间的动态转化过程、SPOM对水体营养盐的迁移转化和生物有效性的相关研究,进一步了解SPOM在呼伦湖水体富营养化中的重要意义.
3 结论
a) 呼伦湖上覆水中SPOM浓度(以TOC表示)在14.4~31.5 gkg之间,以HM为主,WEOM占的比例最小,HM和WEOM分别占SPOM总量的61.2%和6.0%.
b) 呼伦湖SPOM中WEOM含有1个类富里酸组分、1个类腐殖酸组分和1个类色氨酸组分共3个荧光组分,其中类腐殖质组分和类色氨酸组分占总荧光强度的比例分别为70.4%和29.6%.
d) 目前,呼伦湖中SPOM以难降解的腐殖质组分为主,腐殖化程度较强,生物可利用性较低. 但随着温度升高,预估自生源SPOM的贡献将增大,可能导致其生物可利用性升高,需引起高度重视.

