甘露聚糖肽注射液不良反应分析与用药安全*
黄师婧,胡 蝶,兰 瑛,徐 敏
(四川省成都市第三人民医院药学部,四川 成都 610000)
甘露聚糖肽为多糖类物质,是从正常人咽喉部分离的甲型溶血性链球菌株深层培养液中提取的一种生物反应修饰物[1],具有激活免疫细胞、提高机体免疫能力、刺激骨髓造血功能、升高白细胞水平等作用[2],临床主要用于恶性肿瘤放、化疗中改善免疫功能低下的辅助治疗[3]。甘露聚糖肽注射液引发的药品不良反应(ADR)多发生在初次使用,且发生迅速,严重者可导致过敏性休克,抢救不及时会危及生命[4-5]。为深入了解甘露聚糖肽注射液致ADR 的临床特点及影响因素,确保患者用药安全,本研究中通过文献检索并结合医院ADR 报告进行分析。现报道如下。
1 资料与方法
1.1 资料来源
通过国家药品ADR 监测系统,检索我院2011年1月1日至2019年12月31日上报的甘露聚糖肽注射液所致ADR,共15 例。以“甘露聚糖肽”“多抗甲素”“不良反应”“过敏”为关键词,检索中国期刊全文数据库(CNKI)和万方电子期刊数据库2011年1月1日至2019年12月31日纳入甘露聚糖肽注射液ADR 的个案报道,剔出综述性文献、回顾性群案报道及重要信息缺失的病例报道,共检索文献25 篇,纳入病例28 例。按报告类型,患者性别、年龄、原患疾病、过敏史、既往病史、用药情况,发生ADR 的时间及临床表现,以及处理措施和转归等相关信息进行筛查、统计,分析甘露聚糖肽注射液所致ADR 的特点和相关因素。
1.2 统计学处理
采用SPSS 23.0 统计学软件分析。计量资料行t 检验;分级数据行秩和检验;定性资料行卡方检验。其中,年龄用t 检验进行统计;本研究中,86.05%的患者均在首次使用甘露聚糖肽注射液后即出现ADR,后续未再继续用药,因此选择单次给药剂量采用秩和检验进行统计;性别、过敏史、既往哮喘病史等定性资料用χ2检验进行统计。P <0.05 为差异有统计学意义。
2 结果
2.1 报告数量与类型
共纳入病例43 例,包括本院15 例和文献报道28 例。ADR 类型根据严重程度分为一般ADR 和严重ADR 两类,参照《药品不良反应报告和监测管理办法》(卫生部令81 号)中对严重ADR 的定义,本研究中纳入的严重ADR 包括临床表现为过敏性休克、呼吸骤停、心跳骤停、意识丧失、呼之不应;处理措施除了一般的药物对症治疗和吸氧等常规护理外,还予以气管插管等有创抢救措施;ADR 转归为导致患者死亡、永久伤残或入住重症监护室等。胸闷、气促、心悸、恶心、皮疹、颜面水肿、局部麻木等症状相对较轻且未造成严重后果的纳入一般ADR。43 例ADR 中,严重ADR 占41.86%。详见表1。

表1 甘露聚糖肽注射液所致ADR 类型分布Tab.1 Types of ADR induced by Mannatide Injection
2.2 相关影响因素
患者性别与年龄:43 例ADR 患者中,男17 例(39.53%),女26 例(60.47%);年龄16 ~91 岁,50 岁以上占69.77%,平均(56.65±16.20)岁。详见表2 和表3。
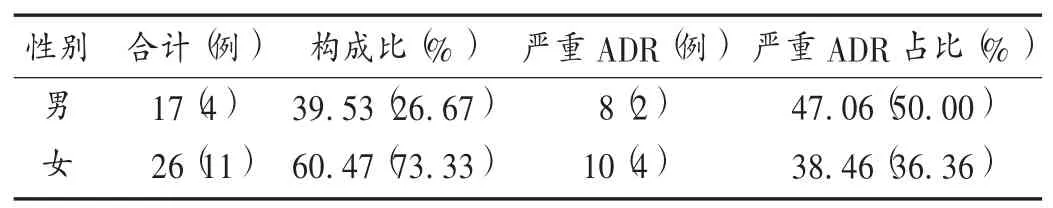
表2 甘露聚糖肽注射液所致ADR 患者的性别分布Tab.2 Distribution of gender in patients with ADR induced by Mannatide Injection
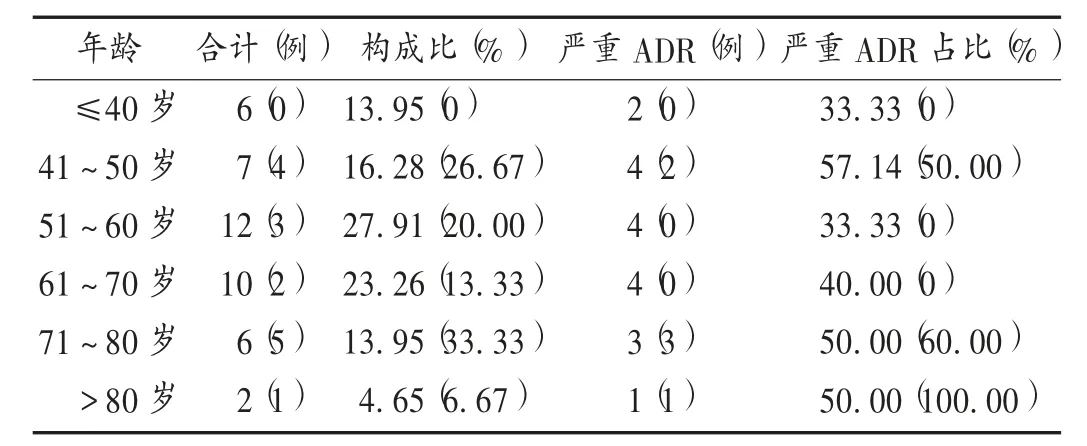
表3 甘露聚糖肽注射液所致ADR 患者的年龄分布Tab.3 Distribution of age in patients with ADR induced by Mannatide Injection
原患疾病:43 例ADR 患者中,患有恶性肿瘤32例,包括妇科肿瘤11 例,消化道肿瘤12 例,呼吸道肿瘤6 例,血液系统肿瘤2 例,头部肿瘤1 例;细菌病毒感染、结核等非肿瘤性疾病11 例。
过敏史及既往病史:8 例患者有青霉素等多种药物过敏史或多种食物、花粉等过敏史,其中6 例有青霉素过敏史,6 例有哮喘病史。详见表4。
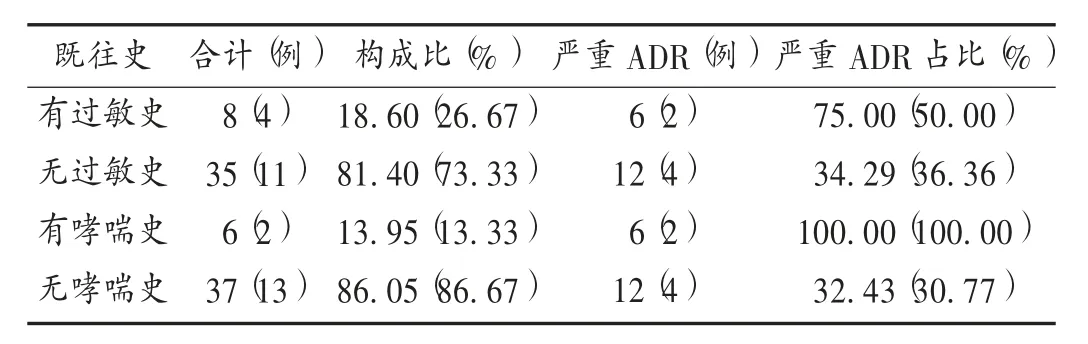
表4 患者过敏史及哮喘病史Tab.4 The allergy and asthma history of patients
用药情况:43 例ADR 患者所用药物共涉及2 个厂家产品,成都利尔药业有限公司27 例,国药一心制药有限公司8 例,另外8 例未注明生产厂家。给药途径除1 例采用肌肉注射外,其余均为静脉滴注;所用溶剂包括0.9%氯化钠注射液和5%葡萄糖注射液。详见表5 和表6。
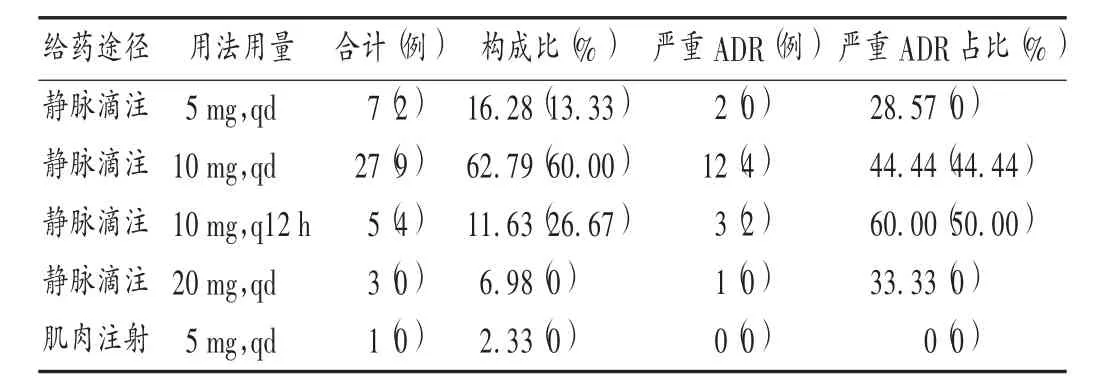
表5 甘露聚糖肽注射液用法用量Tab.5 Administration route and dosage of Mannatide Injection
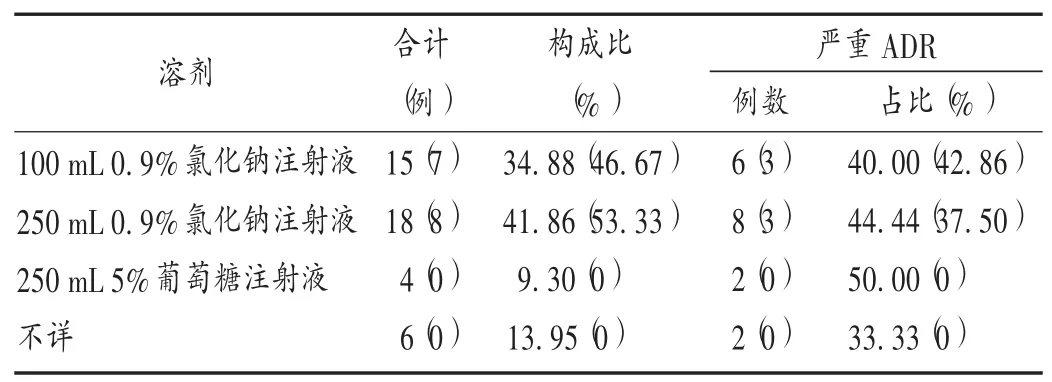
表6 甘露聚糖肽注射液溶剂使用情况Tab.6 Usage of Solvent for Mannatide Injection
2.3 临床特征
发生时间及严重程度:ADR 的发生时间主要集中在给药30 min 以内,共35 例(81.40%),其中严重ADR 17 例(48.57%),主要表现为呼吸困难、呼吸和心跳骤停、意识丧失等;给药30 min 后发生的ADR 8 例,仅1 例为严重ADR(发生在给药后47 min),其余7 例均为一般ADR。详见表7。
临床表现:甘露聚糖肽注射液所致ADR 以呼吸系统症状为主。43 例患者中,76.74%的患者出现呼吸系统症状,主要表现为呼吸骤停、呼吸困难、胸闷、气紧、气促、喘息等。其他ADR 大多是在出现呼吸系统症状的同时伴有其他系统/器官的损害,累及心血管系统、神经系统、消化系统、皮肤及全身反应等。详见表8。
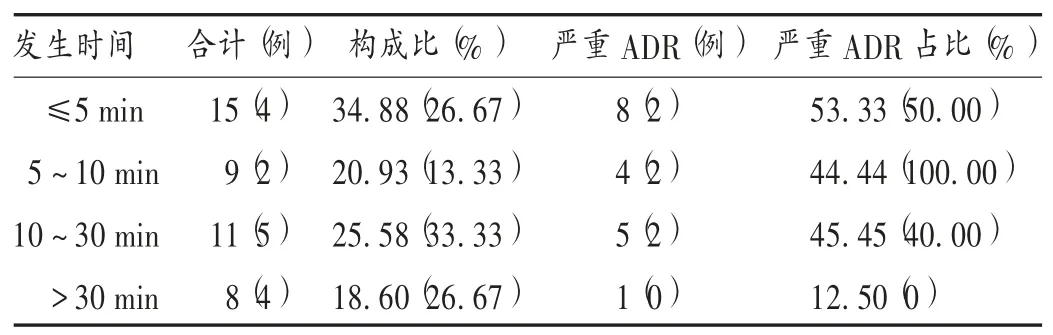
表7 甘露聚糖肽注射液ADR 发生时间及严重程度Tab.7 Occurrence time and severity of ADR induced by Mannatide Injection

表8 甘露聚糖肽注射液ADR 临床表现Tab.8 Clinical manifestations of ADR induced by Mannatide Injection
ADR 处理措施及转归:43 例患者中,13 例在药物抢救治疗的同时还予以气管插管等有创操作,28 例予以糖皮质激素、抗过敏等药物治疗及吸氧、心电监护等无创护理措施,另2 例仅停药观察,未予以特殊治疗。38 例经临床处理后均治愈或好转,4 例经抢救无效死亡,1 例呈植物状态。
2.4 严重ADR 相关因素分析
文献中有6 例所用溶剂不详,故仅对年龄、剂量、性别、过敏史及既往哮喘病史是否为引起严重ADR 的相关因素进行分析。结果表明,哮喘病史与严重ADR 的发生有显著相关性(P <0.05)。详见表9。

表9 甘露聚糖肽注射液致严重ADR 相关因素Tab.9 Related factors of severe ADR induced by Mannatide Injection
3 讨论
3.1 我院上报ADR 与文献报道ADR 比较
我院ADR 与文献报道ADR 在反应类型构成、甘露聚糖肽注射液用法用量、溶剂选择、ADR 发生时间和临床表现等方面基本一致。此外,我院上报的15 例ADR患者中,年龄均不小于40 岁,平均(62.87±15.66)岁;文献报道的28 例ADR 患者中,22 例年龄大于40 岁,平均(53.32±15.75)岁,略低于我院,但无显著差异(P =0.065)。文献报道的ADR 患者中,男13 例,女15例,男女比例较均衡,但我院上报的ADR 患者以女性为主,可能与我院患者原患疾病中乳腺癌、卵巢癌等妇科肿瘤占比较大有关。
3.2 ADR 临床特点
通过对纳入病例进行分析,甘露聚糖肽注射液致ADR 的发生与年龄呈正相关,发生ADR 人群的年龄主要集中在40 岁以上,50 ~70 岁年龄段占比最高。这可能是因为甘露聚糖肽注射液药品说明书规定的适应证为恶性肿瘤的辅助治疗。肿瘤为老年性疾病[6],且老年患者机体处于退化阶段,各器官功能有不同程度的衰退,代谢及排泄机能减弱,更易发生ADR[7-8]。本研究结果显示,甘露聚糖肽注射液所致ADR 发生迅速,大部分ADR 发生在首次给药后30 min 内。本研究中的43 例ADR 在首次给药后10 min 内发生的有24 例,且94.44%的严重ADR 均发生在首次给药后30 min 内。
3.3 严重ADR 相关因素分析
甘露聚糖肽注射液所致ADR 中,严重ADR 占比高,且发生迅速,反应重,甚至可导致患者死亡[9]。43 例患者中,6 例有哮喘病史的患者均出现严重ADR,其发生率为100.00%;无哮喘病史的37 例患者中,严重ADR 的发生率仅为32.43%。提示既往有哮喘病史是甘露聚糖肽注射液诱发严重ADR 的影响因素。因此,临床用药前应询问患者是否有哮喘病史,若有应禁用甘露聚糖肽注射液[10]。
本研究中,8 例具有青霉素等多种药物过敏史或多种食物、花粉等过敏史的患者中有6 例出现严重ADR(其中5 例有青霉素过敏史),严重ADR 发生率为75.00%;无过敏史的35 例患者中,严重ADR 发生率仅为34.29%(P =0.087)。虽然未得出过敏史与甘露聚糖肽注射液导致严重ADR 发生有显著相关性,但在临床应用中仍不能忽视过敏史这一因素,用药前需详细询问患者过敏史,尤其是青霉素类药物过敏史,对于有青霉素过敏史的患者应慎用[11-12]。
本研究结果表明,甘露聚糖肽注射液致严重ADR和一般ADR 患者的性别、年龄、单次给药剂量比较无显著差异(P >0.05)。由于本研究中纳入的病例数较少,虽进行了统计学分析,但仍不能排除有统计学偏移的可能性;且由于部分病例报告信息有缺失,溶剂种类、药液浓度、滴速等因素的影响尚未纳入分析,因此尚不能完全确定甘露聚糖肽注射液导致严重ADR 的因素,还需收集更多资料进一步研究。
3.4 ADR 致死亡病例分析
43 例患者中,4 例因ADR 导致死亡,年龄分别为38,52,62,77 岁,单次给药剂量均为10 mg。3 例在给药30 min 内出现呼吸和心跳骤停、神志不清、呼之不应,其中1 例同时具有菌类食物过敏史和哮喘病史,另2 例具有青霉素过敏史,提示哮喘病史或青霉素过敏史可能是导致患者出现致死性严重ADR 的危险因素。另1 例死亡患者于给药47 min 后出现寒战、高热、意识丧失、心跳骤停,该例患者无过敏史及哮喘病史,但初次给药时滴速较快,达到98 滴/分,提示滴速过快可能是引发致死性严重ADR 的危险因素,但病例数少,无法进行分析。
3.5 ADR 与临床不合理用药相关性分析
2003年4月11日,原国家食品药品监督管理局发布的《关于修订甘露聚糖肽注射剂说明书的通知》中规定,甘露聚糖肽注射剂的适应证为用于恶性肿瘤放、化疗中改善免疫功能低下的辅助治疗。43 例患者中,32 例恶性肿瘤患者具有用药指征,另11 例为非肿瘤性疾病,超说明书中规定的适应证,增加了用药安全风险。
甘露聚糖肽注射液的禁忌证为对本品过敏者、风湿性心脏病、支气管哮喘、气管炎患者禁用,高敏体质者禁用。本研究中6 例患者有哮喘病史,为甘露聚糖肽注射液的用药禁忌证,用药后均出现严重ADR,且有1 例患者最终抢救无效而死亡。
本研究中甘露聚糖肽注射液涉及2 个厂家的品种,成都利尔药业有限公司的药品说明书中用量为1 次5 ~10 mg,加入100 mL 0.9%氯化钠注射液静脉滴注,1日1 次;国药一心制药有限公司的药品说明书中用量为1 次10 ~20 mg,1日1 次或隔日1 次。不同厂家同一品种的药品说明书中单次给药剂量相差1 倍,易造成临床超剂量用药,建议厂家规范药品说明书用量,同时临床应严格按药品说明书中规定的剂量及溶剂进行配制。
3.6 临床安全应用及ADR 防范
本研究结果表明,甘露聚糖肽注射液所致ADR 多为速发型,且严重ADR 发生率高,可导致呼吸困难,甚至呼吸、心跳骤停,处理不及时可能出现休克甚至危及生命[13]。因此,建议甘露聚糖肽注射液仅在具备抢救条件的二级以上医疗机构内使用,临床医护人员应牢固树立防范ADR 的意识,用药过程中全程巡视,对于初次给药30 min 内者更需严密监护,一旦出现有关症状,应立即停药,及时采取相应抢救措施及对症治疗[14]。
临床使用应严格掌握适应证,仅用于恶性肿瘤放、化疗中改善免疫功能低下的辅助治疗。对于老年患者,更需谨慎用药,严格把控用药指征,强化用药规范[8]。严格按药品说明书给药,尽量从低剂量开始给药,控制滴速,初次用药时建议将滴速控制在40 滴/分以内,逐渐调至60 滴/分,并提醒患者及家属切勿擅自调节滴速,如有不适及时告知医护人员[14-15]。
使用甘露聚糖肽注射液前,应仔细询问患者既往病史及过敏史,尤其要高度关注是否有哮喘病史及青霉素类药物过敏史,甘露聚糖肽过敏、高敏体质及患有风湿性心脏病、支气管哮喘、气管炎的患者均禁用。虽然药品说明书未作皮肤过敏试验(简称皮试)要求,但《中国医师药师临床用药指南》中明确,初次使用甘露聚糖肽注射液的患者需皮试。皮试时,取本药注射液0.1 mL(约0.25 mg)作皮下注射,30 min 内观察红肿面积,如红肿面积在3 cm×3 cm 以上者则不宜使用[16]。
因此,临床用药应严格掌握适应证,树立ADR 的防范意识,按药品说明书谨慎用药;临床药师应严格审核甘露聚糖肽注射液的处方或医嘱,加强药学监护,密切监测患者用药期间的ADR,积极开展面向医护人员的ADR 宣传及合理用药教育;医院应进一步加强管控力度,将甘露聚糖肽注射液列入重点监控品种,定期开展专项点评工作[17],全方位切实保障患者的用药安全。

