运动康复对经皮冠状动脉介入术后急性冠状动脉综合征患者的效果
袁玮,聂姗,贾楠,郑志昌,王浩彦
1.首都医科大学附属北京友谊医院呼吸内科,北京市 100050;2.中国康复研究中心北京博爱医院心脏内科,北京市100068
目前急性冠状动脉综合征(acute coronary syndrome,ACS)的急性期治疗以药物治疗和再灌注治疗为主。当患者渡过ACS急性期后,防止心血管事件再发是二级预防的重要目标[1]。循证医学证据表明,以运动训练为核心的心脏康复治疗可有效预防心脏重塑,减少心脏症状[2],降低再住院率和死亡率[3-4]。国内外的临床指南也都推荐ACS患者在急性期常规治疗的同时,应早期开展以运动训练为基础的心脏康复[5-6]。但运动康复的参与率一直较低[7-8],受到医生、患者和费用等多重因素影响[9]。低参与率预示着大量患者失去进一步改善心脏功能和远期预后的潜在机会。因此,在运动康复前准确评价患者的心血管功能和心肺运动能力、制定个体化康复方案、预测康复疗效,对于运动康复治疗的开展具有重要意义[10]。
心脏超声和心肺运动试验(cardiopulmonary exercise testing,CPET)是目前公认的评价冠心病患者静态和运动心脏功能的主要方法[11-12]。本研究采用心脏超声和CPET 评估急性期接受经皮冠状动脉介入(percutaneous coronary intervention,PCI)治疗后ACS 患者进行运动康复的疗效,探讨何种类型的ACS患者能从运动康复中更多获益。
1 资料与方法
1.1 一般资料
采用队列研究方法,连续纳入2017 年12 月至2019 年7 月于首都医科大学附属北京友谊医院心脏中心接诊的ACS 患者共31 例,其中男性26 例,女性5例;年龄(56±11)岁;体质量指数(26.72±3.47) kg/m2;吸烟11 例,吸烟量中位数7 包年;并发高血压22 例;并发糖尿病11例;术后应用β受体阻滞剂20例。
诊断标准:所有患者均根据欧洲心脏病协会指南[1]临床诊断ACS。
纳入标准:①急性期接受PCI 治疗;②于PCI 术后接受常规药物治疗;③出院前根据临床表现、心电图、血清学检查和心脏超声评估,已处于临床稳定状态;④出院后规律应用冠心病二级预防药物;⑤于PCI术后4周完成基线期CPET测试;⑥出院后至入组前一直处于冠心病临床稳定状态。
排除标准:①明确诊断为非ACS 的心血管疾病,如单纯高血压、严重心脏瓣膜病、未控制的心力衰竭、肥厚型心肌病、扩张型心肌病、恶性心律失常、主动脉夹层;②并发其他系统慢性或严重疾病者,如严重肝肾疾病、慢性肺部疾病、急性肺栓塞、下肢静脉血栓、恶性肿瘤;③肢体残疾、瘫痪和运动协调能力异常等无法配合完成运动测试;④入组时正在参与其他研究。
剔除标准:中途自愿退出及失访。
根据患者PCI 术后出院前(基线期)的室壁运动功能,即是否存在节段性室壁运动异常分为节段性室壁运动异常组(异常组)和室壁运动正常组(正常组)。异常组均为男性,且更年轻(P<0.05)。两组其他资料比较无显著性差异(P>0.05)。见表1。
本研究获得北京友谊医院医学伦理委员会批准(No.2017-P2-013-01),所有参与该项研究的患者均于入组前签署知情同意书。
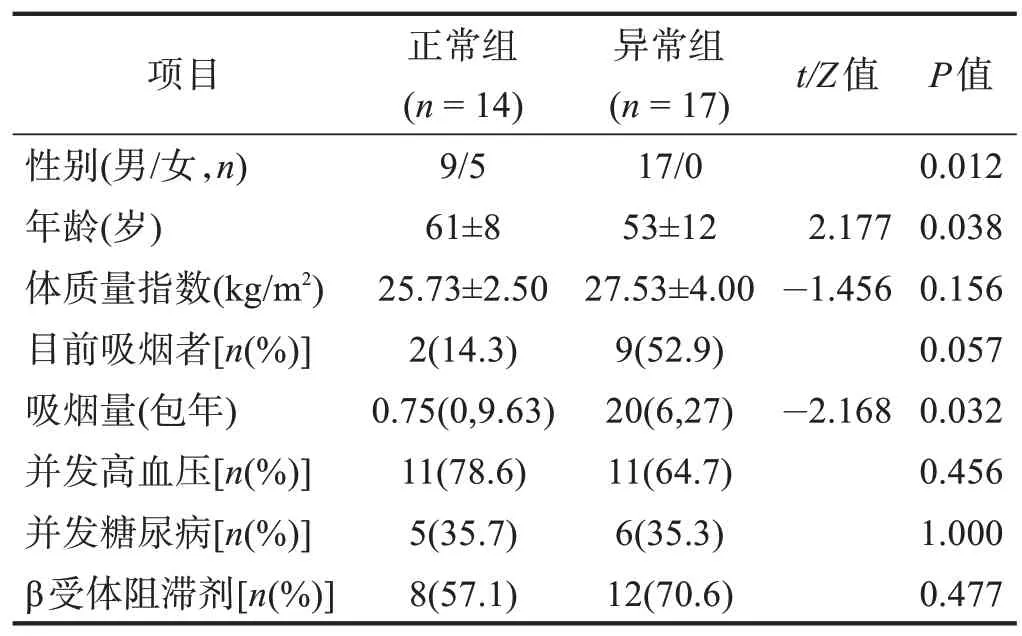
表1 两组一般临床资料比较
1.2 方法
所有患者于入组前完成心脏超声和CPET,根据上述基线期评估结果,制定个体化康复方案,进行为期3 个月的运动康复。3 个月后再次进行静态心脏超声和CPET 检查评估运动康复疗效。所有患者于入组及进行心脏负荷运动评估时均处于临床稳定状态,入组前没有规律运动史。
1.2.1个体化运动康复方案
根据《中国心脏康复与二级预防指南》[6],首先明确患者所有诊断、症状及治疗情况,通过患者调查表和冠心病危险因素调查表进行评估(包括现存疾病、临床表现、既往史、用药情况、治疗效果、吸烟情况、血脂水平、体质量指数、嗜酒、压力、衰弱状态、认知功能及心理相关问题和体力活动等),以期全面了解患者的一般状态和病情。
运动康复全程在康复科医师指导下于门诊完成。每次康复训练,先进行热身活动10 min;此后进行有氧运动30 min,依据患者基线期CPET 结果制定中等强度的个体化运动方案,采用功率自行车或跑台的方式,运动训练强度为基线期60%~70%的峰值摄氧量(peak oxygen uptake,pVO2),以基线期无氧阈时对应的心率水平作为运动过程中的适宜心率;最后进行放松活动10 min。每周1~2 次,共12 周[13]。此外,根据患者的基础状况进行有针对性的戒烟、风险因素控制和生活方式指导。运动康复计划的更多细节已在之前发表的文献中详述[13]。
运动过程中,对患者进行心电监测,并给予必要的指导。运动中或运动后出现以下情况,将暂停运动并重新评估患者状况,必要时调整运动训练方案[6]:①运动时感觉胸痛、呼吸困难、头晕;②运动时心率波动范围超过30 次/min;③运动时血压升高>200/100 mmHg,收缩压升高>30 mmHg 或下降10 mmHg以上;④运动时心电图监测ST 段下移≥0.1 mV 或上升≥0.2 mV;⑤运动时或运动后出现严重心律失常。
1.2.2CPET
CPET 由具备操作资质的专业医师和护士完成,实验仪器采用Master Screen CPX 心肺运动测试仪(德国JAEGER 公司)。患者于CPET 测试当日无需停用心血管药物(包括β 受体阻滞剂),测试前2 h 内避免吸烟及饮用咖啡因类饮品。根据美国胸科学会/美国胸科医师协会(American Thoracic Society/American College of Chest Physicians,ATS/ACCP)的心肺运动指南[14],CPET 采用连续负荷递增方案进行症状自限性踏车运动。患者坐于功率自行车上,连接12导联心电图,鼻夹夹鼻,口唇包绕咬口器并确认无漏气后开始测试。先静坐休息3 min,随后进行零负荷空踏热身至少1 min,此后进入负荷递增运动阶段,递增功率为10 W/min或20 W/min,使患者在8~10 min内达到症状自限的最大运动强度。测试全程踏车转速保持在55~65 r/min。负荷运动停止后继续监测恢复期心电图、血压和呼吸状况至少3 min,直至试验结束。
测试全程有心血管医师和康复科医师等专业人员在场,并备有急救药品和抢救设备,以确保患者安全。当出现下列情况之一时将提前终止试验[14-15]:①缺血性胸痛;②心电图出现ST段压低≥0.3 mV;③持续显著的心律失常,II°或III°传导阻滞;④收缩压或平均压下降>10 mmHg;⑤收缩压>250 mmHg 或舒张压>120 mmHg;⑥脉氧饱和度低于84%;⑦突然出现面色苍白、头晕、乏力、协调障碍、精神异常等无法继续测试或要求终止。
1.3 评估指标
1.3.1静态心脏功能评估
通过静态心脏超声测量左心室射血分数(left ventricular ejection fraction,LVEF)、左心室舒张末期内径(left ventricular end-diastolic volume,LVEDd)和左心室舒张早期/晚期血流峰值流速比值(early/late diastolic filling velocity ratio,E/A),并评估左心室室壁运动功能。以室壁运动积分指数(Wall Motion Score Index,WMSI)量化室壁运动异常的程度,根据美国心脏病协会(American Heart Association,AHA)的建议[16],采用17节段模型进行左心室分段,每个节段单独分析,根据其运动和收缩增厚的情况进行评分。分段评分标准如下:1 分,运动正常,心内膜运动幅度>5 mm,收缩期室壁增厚率>25%;2分,运动减低,心内膜运动2~5 mm,室壁增厚率<25%;3 分,运动消失(无运动),心内膜运动<2 mm,室壁增厚率消失;4分,反常运动(矛盾运动),包括室壁瘤形成,室壁变薄,向外膨出,矛盾运动,并有明显的转折点。

1.3.2运动心脏功能评估
通过CPET 测试,以连续呼吸法(breath-by-breath)测得摄氧量(oxygen uptake,VO2)、二氧化碳排出量(carbon dioxin production,VCO2)、分钟通气量(minute ventricular,VE)和最大运动负荷等指标。采用V-slope法计算无氧阈(anaerobic threshold,AT)。通过上述指标评价患者的运动耐量和运动状态下的心脏功能。观察CPET 恢复期心电图,通过负荷运动终止后每分钟心率恢复(heart rate recovery,HRR)评估患者自主神经协调能力。
1.4 统计学分析
采用SPSS 23.0 对数据进行统计学分析。对计量资料进行Shapiro-Wilk 正态性检验,符合正态分布以(±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验;非正态分布以M(Qu,Ql)表示,组间比较采用Mann-WhitneyU检验,组内比较采用Wilcoxon 秩和检验。计数资料以[n(%)]描述,采用χ2检验或Fisher确切概率检验。显著性水平α=0.05。
2 结果
正常组脱落3 例(男性1 例、女性2 例),异常组脱落5 例,均为男性。全程参与运动康复并于3 个月康复训练后再次接受心脏功能评估的患者共23例,其中正常组男性8例,女性3例;异常组12例,均为男性。上述脱落患者均为研究中途自愿退出。所有患者在研究期间均未发生心脏不良事件。
2.1 静态心脏功能
23 例患者运动康复训练前LVEF 均在正常范围(LVEF>50%)。与正常组相比,异常组运动康复前后LVEF 均较低(P<0.05),WMSI 均较高(P<0.05)。运动康复后异常组WMSI明显低于康复前(P<0.01)。其他指标均无显著性差异(P>0.05)。见表2。
2.2 运动心脏功能
运动康复前,正常组峰值摄氧量占预计值百分比(percentage of predicted value of peak oxygen uptake,pVO2pred)高于异常组(P<0.05);两组间其余运动心脏功能指标无显著性差异(P>0.05)。
运动康复后,正常组仅静息心率较康复前减慢(P<0.05),其余运动心脏功能指标较康复前均未见显著性变化(P>0.05);异常组最大运动负荷、pVO2、pVO2pred、峰值分钟通气量(peak minute ventricular,pVE)和运动终止后第3 分钟的心率恢复(the third minute heart rate recovery,HRR3)均较康复前提高(P<0.05),AT 存在改善趋势,峰值氧脉搏(oxygen pulse,O2pulse)和静息心率无显著性变化(P>0.05);异常组最大运动负荷、pVO2、pVE 和HRR3 均高于正常组(P<0.05)。见表3。
3 讨论
本研究显示,运动康复前室壁运动异常患者在康复后WMSI 明显降低,最大运动负荷、pVO2、pVO2pred、pVE 和HRR3 均提高,提示运动康复治疗可有效提高PCI术后仍存在室壁运动不良的ACS 患者的室壁运动能力、负荷运动耐量和心率调节能力,使该类患者的心脏功能、有氧代谢能力和自主神经协调性在心肌再灌注治疗后得到进一步的改善。
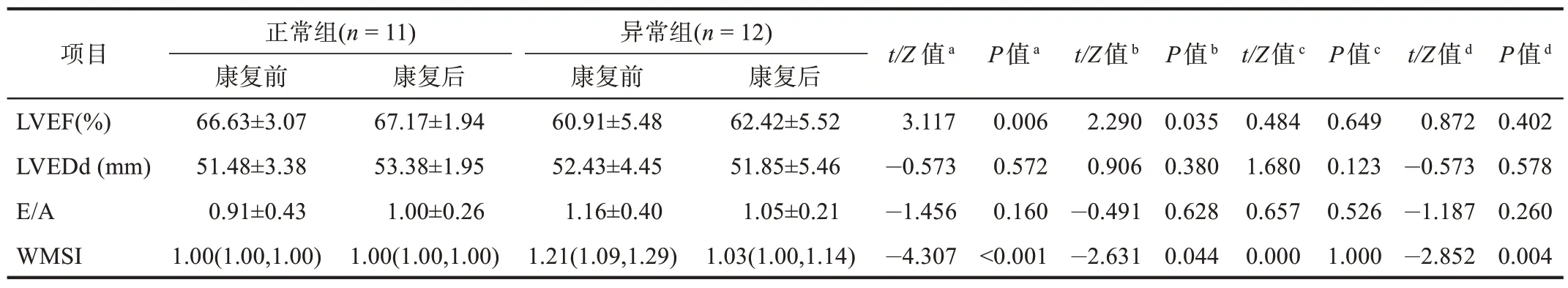
表2 运动康复前后静态心脏功能的变化
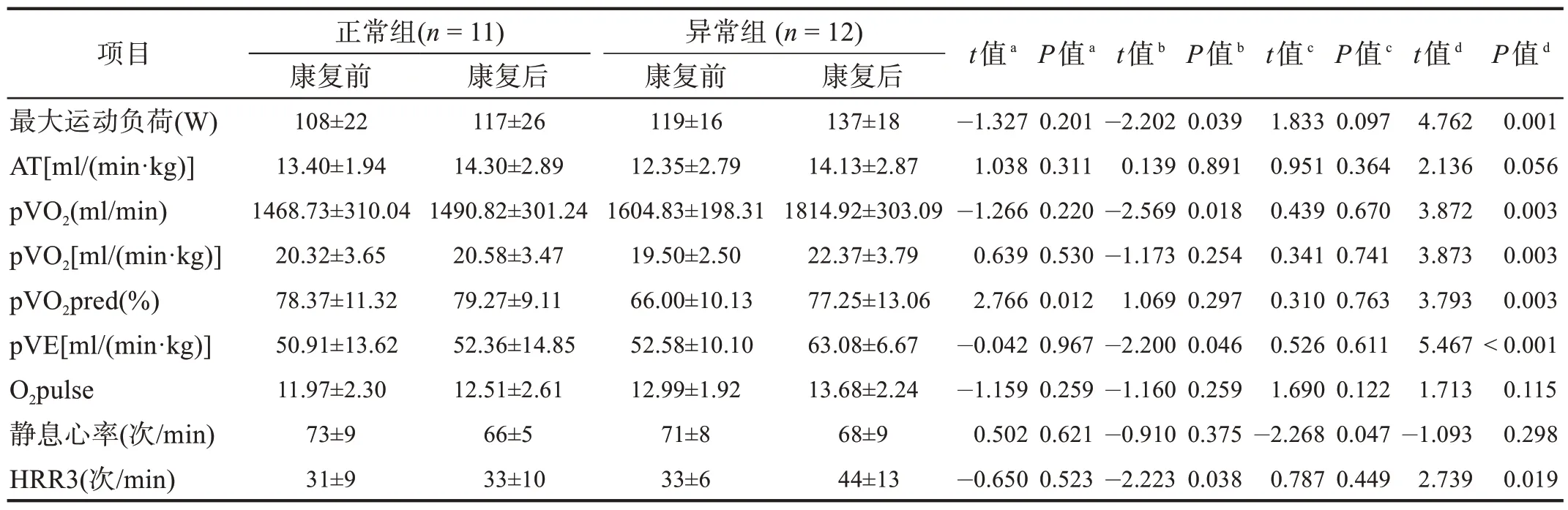
表3 运动康复前后的运动心脏功能的变化
既往大量研究证据表明,运动训练可降低梗死后心肌纤维化[17-18],以运动训练为核心的运动康复可减少患者的临床症状,提高运动耐量,降低急性心血管事件发生率和死亡率,有效改善患者生活质量及远期预后[2-4,19-21]。Giallauria 等[20]观察46 例经皮腔内冠脉成形术后残留低灌注的急性心肌梗死(acute myocardial infarction,AMI)患者,其中25 例早期开始运动康复治疗,6 个月后WMSI、室壁厚度积分指数、pVO2、O2pulse、VE/VCO2斜率等指标显著改善;而未进行运动康复的患者心肌灌注、左心室功能和心肺运动指标均无明显变化。提示AMI后早期开始运动康复可有效减少应激诱导的心肌灌注不足,改善左心室室壁运动和减少室壁增厚,提高运动能力。
近年来多项重要的临床指南均推荐ACS患者和进行冠脉血运重建(包括PCI 和冠脉搭桥术)的冠心病患者应早期进行以运动训练为核心的心脏康复治疗(I 级推荐)[22-23]。然而运动康复的参与率和完成率仍处于较低水平[7-8],主要原因包括非康复专业医生对特殊患者(如存在心肌再灌注不良、血管病变严重等)进行运动康复训练的安全性和有效性的认知偏差[24-26],以及患者对运动康复的必要性和获益认识不足[3,26]。本研究筛选期共有75 例患者符合入组标准,但最终仅有31 例患者同意入组。由于本研究是在ACS患者恢复早期开始的运动康复,为了增强患者对于运动训练安全性的信心、保持患者持续参与率,本研究的运动训练强度不高,运动康复频次较低,但仍有8 例未完成全部运动康复计划。然而,运动康复项目利用不足,可能使高危患者失去一项重要的治疗措施。因此,确定哪些患者将从运动康复中更多获益,对于运动康复治疗的有效实施非常重要。
本研究显示,PCI 术后基线期室壁运动异常患者的pVO2pred低于室壁运动正常患者,其余运动心脏功能指标无显著差异;但经过3 个月运动康复后,两组pVO2pred已无显著差异,而室壁运动异常患者最大运动负荷、pVO2、pVE 和HRR3 均明显优于室壁运动正常患者。运动康复后室壁运动异常患者最大运动负荷、pVO2、pVO2pred、pVE 和HRR3 均较康复前显著提高,而室壁运动正常患者上述指标在康复前后没有明显变化。提示血运重建后仍存在室壁运动不良的ACS 患者,从短期运动康复治疗中获益更多。Rosa等[27]研究也得出相似结论,其研究根据康复前ACS 患者LVEF 分组,结果显示LVEF 异常组(LVEF<50%)有55.9%康复后pVO2增加>10%,而LVEF正常组(LVEF≥50%)pVO2显著增加的患者比例为45.3%,虽然该比例差异不具有统计学意义,但也提示存在左室功能障碍的患者可能从运动康复计划中获益更多。
室壁运动异常患者康复疗效更佳,其原因可能与室壁运动异常区域的部分存活心肌在运动康复后被激活有关。存活心肌(包括顿逸心肌和冬眠心肌)常出现在缺血区域内,可发生于不稳定型心绞痛和急性心肌梗死早期再灌注后,表现为心肌收缩功能低下及局部室壁运动异常[28]。已有多项研究证实[29-31],运动训练可激活血管内皮生长因子信号通路,触发微血管生成,尤其使心梗瘢痕边缘区的微血管密度增高,增加心肌血流灌注,激发存活心肌的功能恢复,减弱左室病理性重塑,并改善左心室整体收缩能力[32]。既往还有研究发现[33],运动训练可通过增加内皮祖细胞(endothelial progenitor cells,EPCs)来改善左心室重构,EPCs 参与急性心肌梗死后受损组织区域的血管生成。本研究中室壁运动异常患者在PCI 术后仍存在节段性室壁运动异常,较室壁运动正常患者存在更明显的缺血坏死;且室壁运动异常患者基线期pVO2pred要明显低于室壁运动正常患者,患者基础运动能力较差,但康复疗效更佳,这可能是由于该组患者存在更多顿逸和/或冬眠心肌,运动训练使这类存活心肌的收缩功能得到改善和恢复,在介入治疗后进一步挽救了缺血坏死心肌,提高左心室功能,从而更显著改善患者的运动耐量。
本研究的所有患者基线LVEF 均在正常范围(LVEF>50%),运动康复后LVEF 无明显变化,但WMSI 较基线时下降,伴随最大运动负荷、有氧代谢能力的提高。提示对于保留射血分数的ACS 患者,WMSI 在反映其心肌供血和运动心肺功能的变化方面,比LVEF 更为敏感和准确。WMSI 是基于左心室各节段的室壁厚度和心内膜偏移程度进行评分,分值越高代表室壁运动能力越差[16]。WMSI可由心脏超声、心脏核磁、心肌核素等无创性检查获得,它可提示ACS 患者的远期不良心血管事件[34-35]。Eek 等[36]针对61 例非ST 抬高型心肌梗死(non-ST-segment-elevation myocardial infarction,NSTEMI)患者的研究还提示,WMSI 可反映NSTEMI 患者血管重建前的心肌梗死面积,尤其对于最终梗死面积≥12%的患者,其应用价值优于LVEF。而心肌坏死面积对于患者的死亡率和主要不良心血管事件发生率具有重要的预测作用[37-38]。心脏超声是目前临床实践中快速、易行并且可床旁完成的无创性检查,WMSI 作为可由该项无创性检查获得的心功能指标,对心肌损伤的检测比LVEF更敏感,在评价ACS 患者的心脏功能方面具有重要的临床意义。
本研究也存在一定局限性。本研究中室壁运动正常患者的静息心率在康复后明显减慢,提示心率储备能力提高;但其他运动心肺功能指标无明显改善,可能与本研究样本量较小有关,也可能由于本研究中运动康复频率相对较低[6,22]所致。对于再灌注治疗后心肌收缩功能较好的患者,可能需要更高频率、高强度或更长周期的运动康复方案,才能更明显获益。此外,作为一项单中心观察性研究,本研究样本量较小,随访时间有限,未能体现运动康复前后的室壁运动能力、心肺运动耐量对于远期预后的影响。ACS 急性期血运重建对冠脉病变改善的程度与运动康复的疗效之间的关系,也有待后续研究进一步探索。
综上所述,急性期接受PCI 治疗后存在室壁运动异常的ACS 患者,在病情恢复期接受运动康复治疗,更易获得心脏功能和运动耐量的进一步改善。WMSI在反映保留射血分数的ACS患者的心脏功能改善方面具有重要意义。
利益冲突声明:所有作者声明不存在利益冲突。

