电针对骶上脊髓损伤后逼尿肌亢进大鼠逼尿肌中环腺苷酸和蛋白激酶A含量及肌球蛋白轻链激酶磷酸化的影响
艾坤,许明,刘琼,邓石峰,刘继生,祁芳,易细芹,瞿启睿,张泓
湖南中医药大学,湖南长沙市410208
神经源性膀胱是一类由于神经系统病变导致膀胱和尿道功能障碍,进而产生一系列下尿路症状的疾病总称。脊髓损伤是导致神经源性膀胱发生的主要原因之一[1]。
骶上节段损伤是脊髓损伤最常见的类型,占全部脊髓损伤患者的80%以上[2]。因骶上节段横断性损伤,同时骶髓排尿中枢的反射弧保存完整,高位排尿中枢对骶髓排尿中枢的抑制作用消失,骶髓排尿中枢反射活动增加,逼尿肌反射亢进,出现无抑制性收缩,膀胱内压增高,这是导致膀胱功能障碍的主要原因。临床上,抑制逼尿肌收缩的一些药物被证实可有效改善骶上脊髓损伤所致的膀胱功能障碍,缓解其症状[3]。
临床及实验研究证实[8-9],电针干预骶上脊髓损伤后神经源性膀胱,可增大膀胱最大容量,降低膀胱内压,改善膀胱的顺应性。且因电针具有操作简便、无明显副作用及费用低廉等独特优势,目前已在临床广泛应用于该病的治疗。近年来关于该领域的机制研究越来越多,大部分针灸作用机制的研究主要集中在脊髓及周围神经通路上,选取逼尿肌作为研究靶点的较少。
逼尿肌由平滑肌细胞构成,平滑肌收缩是一种钙依赖的过程,胞浆内游离Ca2+浓度增高,可使肌球蛋白轻链激酶(myosin light chain kinase,MLCK)活化,引起平滑肌收缩[4]。目前研究认为,平滑肌细胞的舒张主要与细胞内环腺苷酸(cyclic adenosine monophosphate,cAMP)的作用密切相关,其下游蛋白激酶A(protein kinase A,PKA)可使MLCK磷酸化(p-MLCK)而失去活性,影响MLCK 和Ca2+-钙调蛋白(calmodulin,CaM)复合物的亲和力,使其对钙离子失敏,引起平滑肌舒张[5-7]。
本实验观察脊髓T10水平损伤大鼠脊髓休克期后,经电针干预,逼尿肌内cAMP、PKA 含量及p-MLCK水平的变化情况。
1 材料与方法
1.1 实验动物
健康SPF 级Sprague-Dawley 雌性大鼠60 只,体质量200~230 g,月龄2~3个月,购自湖南斯莱克实验动物有限责任公司,动物许可证号SCXK(湘)2013-0004。所有动物分笼饲养于湖南中医药大学实验动物中心,饲养温度24~26°C、湿度50%~70%,适应性喂养1 周后进行实验,使用许可证号SYXK(湘)2013-0005。动物实验过程获得湖南中医药大学动物伦理委员会批准,所有实验动物按照国家科技部《关于善待实验动物的指导性意见》予以护理及使用。
1.2 主要试剂和仪器
水合氯醛,产品批号20131031:国药集团化学试剂有限公司。青霉素钠,产品批号15050401-2:哈药集团。橡皮生肌膏,产品批号20150413:湖南中医药大学第一附属医院自制药。Tris、APS、SDS、TEMED、Tween-20、丙烯酰胺、甘氨酸、甲叉双丙烯酰胺、丽春红、大鼠cAMP、PKA 酶联免疫试剂盒:美国SIGMA公司。HRP羊抗鼠IgG、HRP羊抗鼠IgG:美国PROTEINTECH 公司。RIPA 裂解液:北京普利莱基因技术有限公司。SuperECL Plus 超敏发光液:美国THERMO PIERCE 公司。显影液、定影液:中国WELLBIOLOGY公司。p-MLCK抗体:英国ABCAM 公司。无水乙醇、二甲苯、苏木素染液、中性树胶等试剂均系国产分析纯,所有实验用水均为DEPC处理过的无菌双蒸水。
WZ-50C6微量注射泵:浙江史密斯医学仪器有限公司。MP150-WSW 多通道生理记录仪:美国BIOPAC 公司。SDZ-V 型华佗牌电针治疗仪:苏州医疗用品厂有限公司。TGL-18R 台式冷冻离心机:深圳黑马公司。QL-901 旋涡混合器:江苏其林贝尔公司。164-5050 电泳仪:美国BIO-RAD 公司。DYCZ-24EN电泳槽、DYCZ-40A 转膜仪:北京六一生物科技有限公司。PW-812 全自动酶标洗板机、MB-530 多功能酶标分析仪:深圳汇松科技发展有限公司。
1.3 动物分组
动物分组采用二次随机法,60只大鼠按随机数字表抽取12 只作为空白组,12 只作为假手术组。空白组不予造模,假手术组仅于相应部位做皮肤和肌肉切开处理,不切断脊髓。剩余36只采用脊髓横断法制作神经源性膀胱模型,经后肢运动功能及膀胱排尿情况评价确定成功的神经源性膀胱模型大鼠二次随机抽取12只作为模型组、12只作为电针组。
1.4 方法
1.4.1手术方法
大鼠术前24 h 禁食不禁水,于术前2 h 腹腔注射青霉素钠20 万U,预防感染。10%水合氯醛300 mg/kg 腹腔麻醉后,大鼠以俯卧位捆绑于鼠板上固定备皮,采用Hassan Shaker脊髓横断法基础上加以改良制作骶上脊髓损伤模型[10]。脊髓横断部位以浮肋连接的T13椎骨作为骨性标志向上定位T8椎骨以定位脊髓T10节段。确定手术部位后做标记并消毒皮肤,以标记点为中心行背正中切口,长约3 cm,依次切开表皮和皮下筋膜,使用玻璃分针钝性分离两侧竖脊肌,充分暴露棘突和椎板。用显微咬骨器从尾侧向头侧咬除T8椎板直至两侧椎弓根,充分暴露脊髓,用牙科钩沿横断椎间隙横向小幅度钩出脊髓,手术刀切断脊髓后反复刮扫以确定脊髓完全横断,确定无神经纤维残留。由内向外逐层缝合。手术过程严格无菌操作,术后观察大鼠的生命体征是否平稳。
1.4.2术后护理
手术后置于电热毯上保温,使肛温维持37 ℃以上。术后伤口及周围碘伏消毒,每天3 次;术后48 h内每12 h 腹腔注射青霉素钠20 万U,48 h 后每24 h 注射青霉素钠20万U,直至术后第7天;7 d后若有大鼠出现血尿、脓尿时,每24 小时腹腔注射青霉素钠20万U,直至尿液澄清。大鼠单笼饲养,每日总饮水量<30 ml,防止因膀胱大量尿潴留导致肾脏及膀胱壁损伤。每8小时(早、中、晚)用Crede法对大鼠进行人工辅助排尿,注意手法和力度,密切观察大鼠的生命体征,防止损伤膀胱。50%乙醇溶液擦拭大鼠的身体(腹部及双下肢)以防止压疮,有压疮形成的用橡皮生肌膏涂抹以促进伤口愈合。因手术后大鼠下肢感觉缺失,为防止其自噬,在其下肢涂上苦苹果喷雾剂。
1.4.3成模及剔除标准
术后第12 天对模型大鼠脊髓横断情况进行BBB(Basso-Beattie-Bresnahan)运动评分。将动物放入开口盆,轻敲盆壁,使其爬行,观察动物的臀、膝、踝关节行走、躯干运动及其协调情况。满分21 分。0 分为无可见双后肢活动;分数增加,大鼠躯干及双后肢运动功能逐渐改善;21分为持续性掌面移动、持续性协调步态、足趾持续抓地、尾巴翘起、躯干稳定、活动过程中身体与主动爪位置始终平行。两人采用单盲法对评价结果分别进行记录。
成模标准:①前肢行走时后肢处于拖动状态,BBB 评分为0 分;②手术麻醉及脊髓休克期,出现潴留,需手法辅助排尿;脊髓休克期过后逼尿肌出现无抑制性收缩,膀胱胀大不明显,且大鼠下腹部及笼内垫料潮湿。
剔除标准:出现双后肢自主运动,脊髓休克期后大量尿潴留或自主排尿、自噬或死亡的情况。
1.5 腧穴与电针
参照“十五”国家规划统编教材《实验针灸学》大鼠标准穴位图谱定位,并模拟人体腧穴骨度分寸法量取次髎、中极、三阴交。
电针组于造模后第19 天[9]开始电针干预,每天1次,共7 次。大鼠仰卧位固定于鼠板上,用30 号1 寸针,直刺中极和三阴交(三阴交左右两穴隔日交替进行),深5 mm,接SDZ-V 型电针治疗仪(华佗牌),疏密波10/50 Hz、电流0.1 mA,强度以肢体轻颤并耐受为度,留针20 min。随后将大鼠俯卧位固定,直刺次髎15 mm (次髎左右两穴隔日交替进行)和大鼠尾根部,重复以上操作。
1.6 标本采集与处理
电针治疗结束后各组行尿流动力学检查,后将动物断颈处死,取逼尿肌组织,4 ℃生理盐水漂净,滤纸吸干,-80 ℃冰箱冻存待用。
1.7 指标检测
1.7.1组织病理学观察
肉眼观察膀胱的大体情况,如大小、膀胱壁厚薄;检查上尿路情况。将逼尿肌组织放入4%多聚甲醛中固定48 h,常规脱水、石蜡包埋,间断连续切片,厚4 μm,HE 染色后在光镜下观察逼尿肌的组织形态学改变。
1.7.2尿流动力学检测
大鼠10%水合氯醛350 mg/kg 腹腔注射麻醉。取仰卧位固定,轻压腹部,排净膀胱内尿液,会阴部用络合碘消毒。将F3 导尿管经三通管与微量灌注泵及MP150 多通道生理记录仪连接,排净仪器和管内空气,在示波模式下标定零点。石蜡油棉球润滑F3 导尿管前端,将其经尿道缓慢插入膀胱并用胶带固定。待压力曲线稳定后,记录此时膀胱内压。然后100 μl/min 膀胱灌注温生理盐水(25~35 ℃),同步记录膀胱压力曲线变化及灌注液首次自尿道口漏出时的灌注时间;继续灌注直至出现4~5 个稳定波形,完成尿流动力学检测。导尿管进入膀胱的起始压力为膀胱基础压,膀胱最大容量为尿道口首次流出液体时的灌注容积,此时压力为漏尿点压力,膀胱顺应性为膀胱容量的变化与压力变化的比值。
1.7.3ELISA法检测逼尿肌cAMP、PKA蛋白含量
取逼尿肌组织1×1×1 cm,切片后,加入0.1 mol/L冰冷磷酸盐缓冲盐水(phosphate buffered saline,PBS),混合比例1∶9。冰上10 000 r/min 离心,取上清液,-80 ℃储存备用。采用ELISA 试剂盒检测样本cAMP、PKA水平。
1.7.4Western blotting法检测逼尿肌p-MLCK水平
剪取逼尿肌组织250 mg,RIPA 裂解提取组织总蛋白;配制BCA 工作液测量蛋白浓度;进行电泳,当溴酚蓝电泳到达胶底,结束电泳;分别切胶p-MLCK (211 kDa)、β-actin (42 kDa)进行转模;采用脱脂奶粉封闭1 h;分别加入p-MLCK (1∶1000)和β-actin(1∶4000)一抗,4 ℃下孵育过夜;1×TBST洗3次,每次15 min;采用1×TBST 稀释HRP(1∶3000)标记的二抗,孵育45~60 min;1×TBST洗3次,每次15 min;ECL 显色曝光。采用BIO-RAD 凝胶成像系统拍照,以QuantityOne 软件分析p-MLCK 和内参β-actin 蛋白的灰度值,以两者灰度比值作为p-MLCK 的相对表达水平。
1.8 统计学分析
采用SPSS 25.0 统计软件进行数据处理。计量资料符合正态分布,以(±s)表示,多组间均数比较,如满足正态性及方差齐性则采用单因素方差分析,方差不齐采用Tamhane's T2 多重比较;不满足正态性则采用非参数检验。显著性水平α=0.05。
2 结果
2.1 一般情况
空白组和假手术组一般情况良好。模型组术后后肢完全瘫痪,随意运动丧失,呈拖动爬行;膀胱胀大且有尿潴留,需手法辅助排尿;术后第19天,大部分模型大鼠渡过脊髓休克期,表现为尿失禁,膀胱无胀大,无需手法排尿,会阴部及笼内垫料保持经常性潮湿。大鼠饮食量较前减少,体质量有所下降。经过电针治疗后,电针组尿失禁症状有所好转,会阴部及笼内垫料潮湿程度减轻,饮食量增加,但后肢运动功能无明显改善。
2.2 逼尿肌组织形态学改变
2.2.1肉眼观察
与空白组和假手术组比较,模型组和电针组膀胱体积增大,膀胱壁粗糙、增厚,部分大鼠的输尿管出现明显扩张,肾盂有少量积水,尤以模型组明显。
2.2.2光镜下观察
空白组和假手术组膀胱组织的移行上皮细胞整齐紧密排列,固有膜完整,无炎性细胞浸润及组织水肿;肌纤维束排列层次较清晰,肌间隙充满弹性纤维,无增生及纤维化改变。
模型组膀胱组织的移行上皮细胞排列紊乱,固有膜被破坏,细胞间隙明显增大,同时伴有大量单核细胞浸润,组织水肿明显,部分区域伴有微血管破裂出血改变,肌纤维排列层次欠清晰,结缔组织增生明显,呈纤维化趋势。
与模型组比较,电针组逼尿肌组织的炎症反应程度有所好转,单核细胞浸润数量减少,组织的水肿程度有所减轻。见图1。
2.3 尿流动力学
与空白组和假手术组比较,模型组膀胱基础压和漏尿点压均明显升高(P<0.01),而膀胱最大容量和膀胱顺应性均明显降低(P<0.01)。与模型组比较,电针组膀胱最大容量、膀胱顺应性均明显增加(P<0.01),膀胱基础压和漏尿点压均降低(P<0.05)。见表1。
2.4 逼尿肌内cAMP、PKA含量
与空白组和假手术组比较,模型组逼尿肌内cAMP 和PKA 含量明显降低(P<0.01)。与模型组比较,电针组逼尿肌内cAMP 和PKA 含量增加(P<0.05)。见表2。
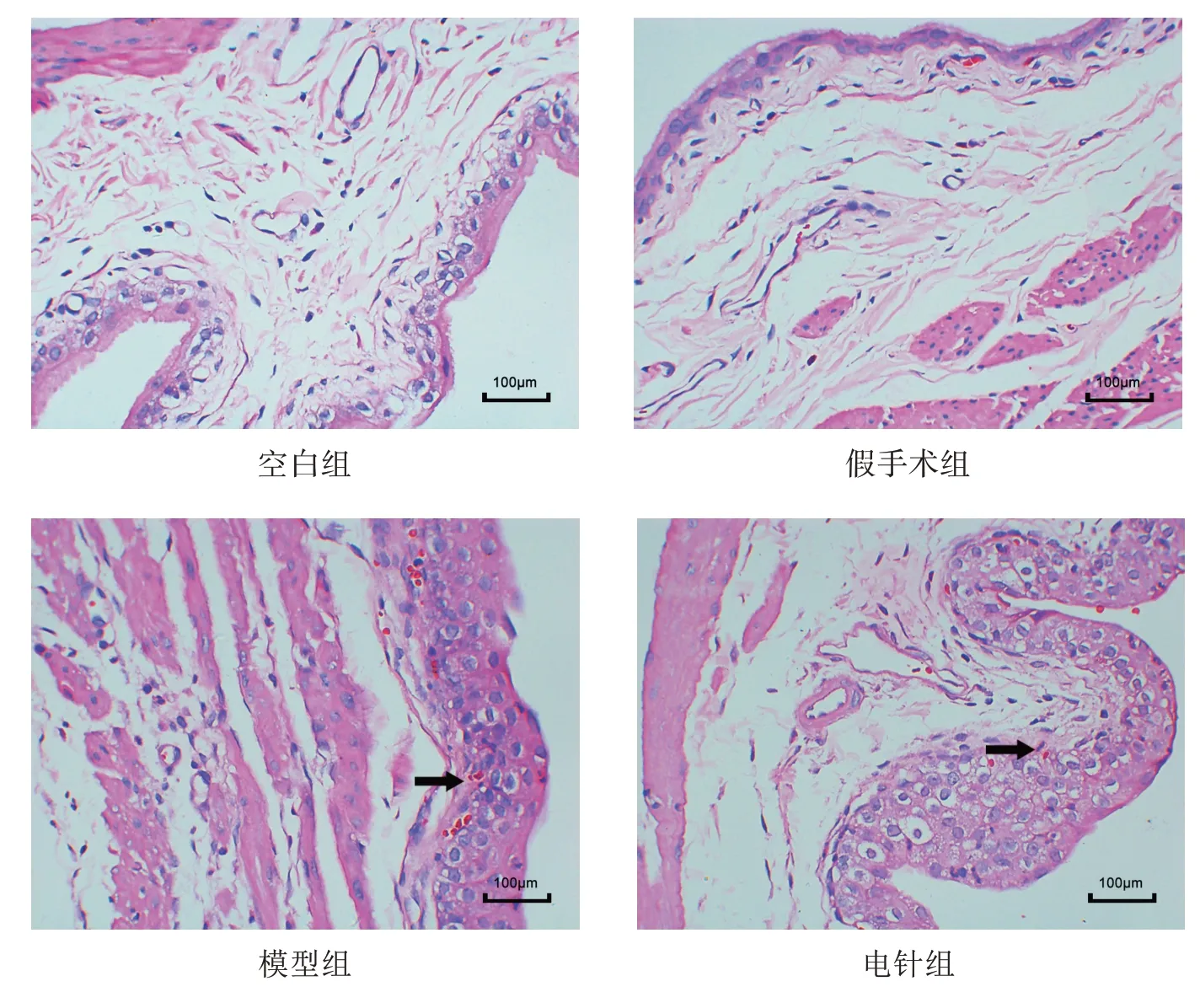
图1 各组逼尿肌组织形态学情况(光镜,×400)
2.5 逼尿肌内p-MLCK表达
与空白组和假手术组比较,模型组逼尿肌内p-MLCK 表达明显降低(P<0.01)。与模型组比较,电针组逼尿肌内p-MLCK 表达升高(P<0.05)。见表3、图2。
3 讨论
针对骶上脊髓损伤后逼尿肌反射亢进,抑制逼尿肌收缩是有效的治疗手段,如给予巴氯芬[13],或逼尿肌局部注射A 型肉毒毒素[3,14]、毒蕈碱受体拮抗剂[15]均可有效抑制膀胱过度收缩,改善膀胱症状。
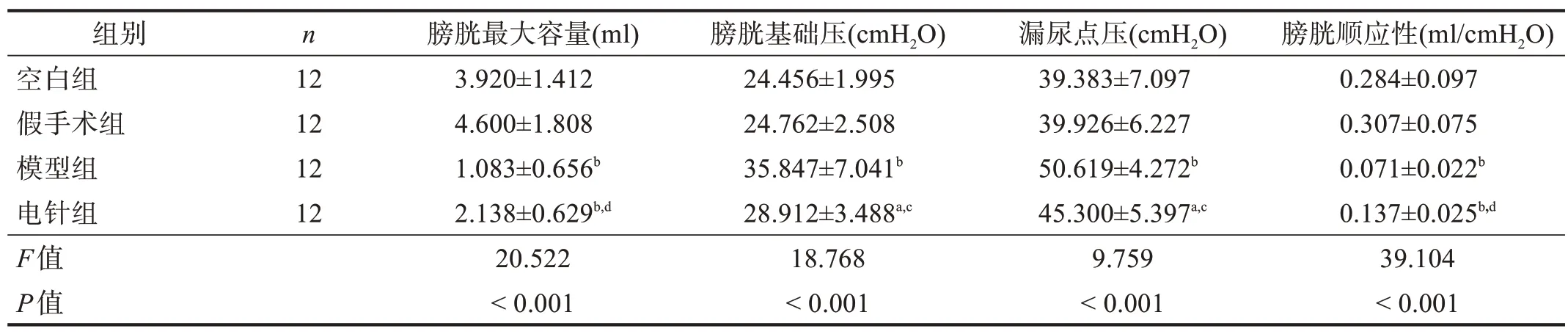
表1 各组大鼠膀胱尿流动力学指标比较
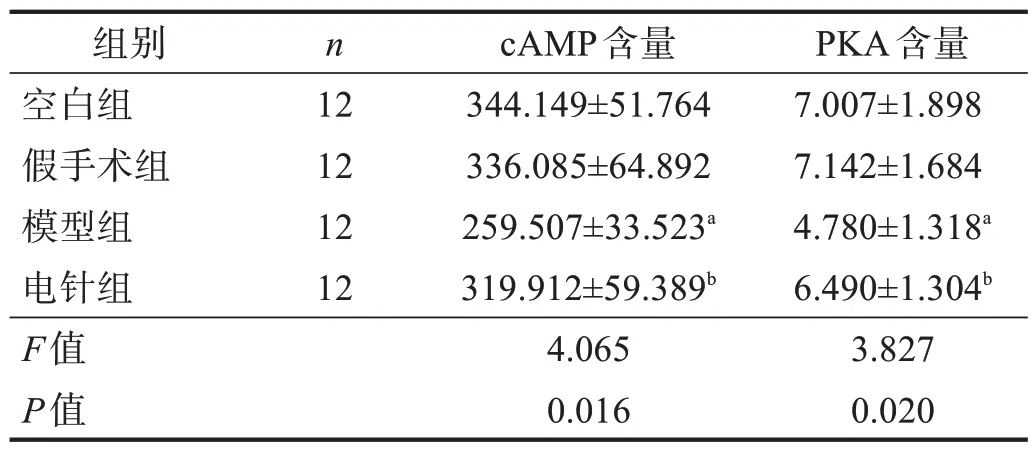
表2 各组逼尿肌cAMP含量比较(pg/ml)
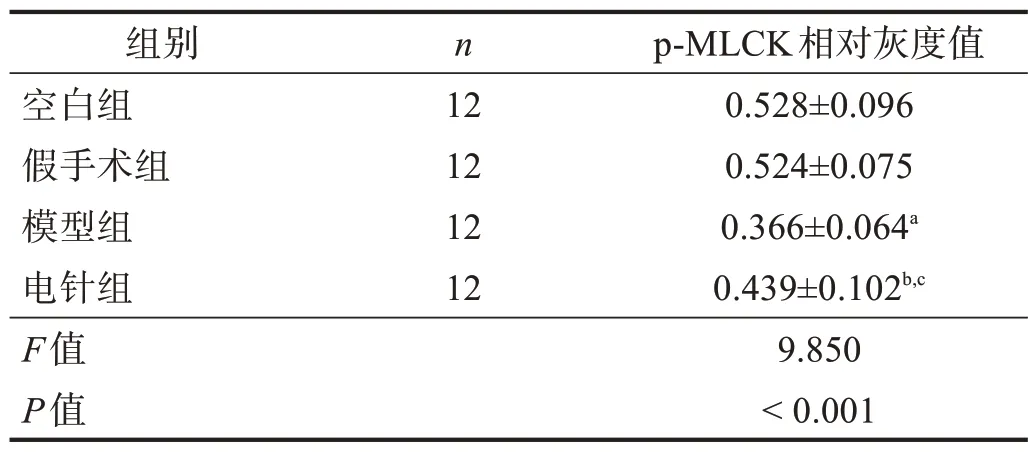
表3 各组逼尿肌内p-MLCK相对灰度值比较
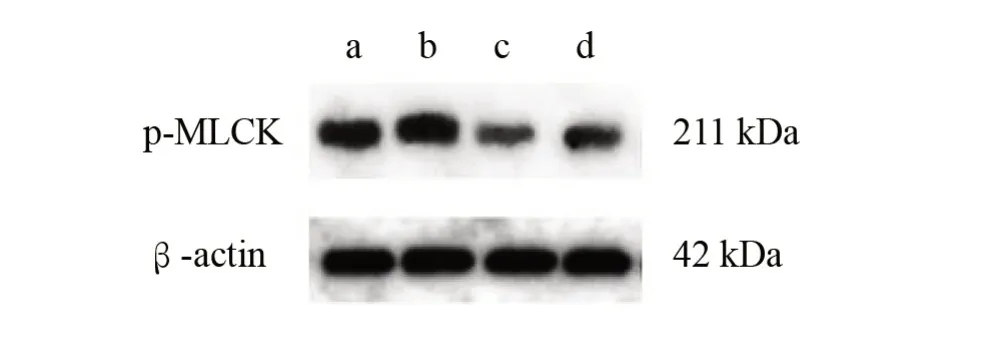
图2 各组逼尿肌内p-MLCK蛋白表达(Western blotting)
前期研究发现[9],T10水平横断损伤的大鼠,脊髓休克期后经电针干预,可增大膀胱最大容量,降低膀胱内压,改善膀胱的顺应性。已有研究证实[5-7],cAMP 及其激酶PKA 在平滑肌舒张的生理过程中起着非常重要的作用。cAMP 通过激活其激酶PKA,可使MLCK 磷酸化而失去活性,引起平滑肌舒张。本研究发现,T10水平脊髓横断损伤大鼠脊髓休克期后经电针干预,大鼠逼尿肌cAMP和PKA 含量明显升高,膀胱尿流动力学参数得到明显改善。表明cAMP/PKA 信号通路可能是电针治疗逼尿肌亢进型神经源性膀胱的重要分子信号途径。
骶上脊髓损伤后的逼尿肌反射亢进型膀胱在临床上根据括约肌是否协同既可表现为尿失禁,又可表现为尿潴留,属中医学“遗溺”“癃闭”范畴。中国古代医集中有关针灸治疗该病的记载颇多。程洁等[16]基于数据挖掘探讨针灸治疗脊髓损伤尿潴留的临床选穴规律,发现中极、次髎、三阴交是治疗该病最常用穴位。中极与膀胱体表投射区接近,由T12~L1脊髓节段支配,与支配膀胱的交感节后纤维盆神经、腹下神经和阴部神经的脊髓节段部分重叠。穴下为交感支配膀胱的传出神经分支髂腹下神经,针刺中极可能对膀胱及尿道内括约肌的交感支配产生影响[17-18]。次髎位于S2后孔内,位于S2神经肌支下方。S2~S4前角细胞是排尿的调节中枢,膀胱副交感神经节通过节后纤维支配逼尿肌和膀胱括约肌。骶神经调节对非梗阻性尿潴留患者有效[19-20]。电针刺激次髎可能直接影响S2神经根,引起膀胱节律性收缩,松弛膀胱肌肉,从而有利于自主排尿和自主排尿反射的重建[21]。三阴交下有来自于L4~S3神经根的胫神经通过,深刺该穴可通过反射弧传到脊髓后根,调节骶髓排尿中枢,调节膀胱的顺应性[22]。
电针对神经源性膀胱有很好的疗效。王彦彬等[23]利用S3神经电针治疗脊髓损伤后逼尿肌反射亢进,患者排尿次数、漏尿次数、充盈末期逼尿肌压减少。刘春茹等[24]认为电针联合膀胱功能训练能显著改善脊髓损伤后逼尿肌反射亢进型神经源性膀胱患者的临床症状,其机制与抑制逼尿肌的反应亢进,促进逼尿肌与尿道外括约肌的协调性活动,提高膀胱顺应性有关。电针结合膀胱功能训练可以明显改善骶上脊髓损伤患者的膀胱功能,与对照组比较,治疗组膀胱容量、膀胱顺应性显著增加,残余尿量、膀胱压力、直肠压力、逼尿肌压力显著降低[25]。本项目组临床研究亦发现[8],电针联合膀胱综合训练治疗骶上脊髓损伤后神经源性膀胱(逼尿肌反射亢进型)患者,治疗4 周后,观察组24 h 自主排尿次数、充盈期逼尿肌压力、残余尿量及生活质量精简问卷评分均明显低于对照组水平,而最大膀胱测压容积及最大尿流率均明显高于对照组水平。本研究使用T10脊髓横断后逼尿肌反射亢进型神经源性膀胱大鼠模型再次验证了临床研究的发现。相较于模型组,电针组膀胱最大容量、膀胱顺应性均显著增加,膀胱基础压、漏尿点压均明显降低,表明电针次髎、中极、三阴交等穴可有效降低模型大鼠的膀胱内压,提高膀胱顺应性,增加膀胱容量。
逼尿肌的收缩是一种钙和ATP 依赖的过程[4],胞浆内游离Ca2+浓度增高,形成Ca2+与CaM 复合物,结合MLCK后使MLCK活化,引起其下游肌球蛋白轻链(myosin light chain,MLC)的磷酸化水平增高,MLC 磷酸化过程分解足够的ATP,将化学能转变为机械能,从而引起平滑肌收缩。
cAMP 与平滑肌舒张之间存在密切联系,这一作用是通过其底物PKA 实现的。有研究发现[5-7,26],cAMP 通过PKA 使MLCK 磷酸化,从而影响与Ca2+-CaM 复合物的亲和力,使其对Ca2+失敏,降低其下游MLC 磷酸化水平,引起平滑肌舒张。此外,cAMP 促进平滑肌舒张的作用可能与肌球蛋白轻链磷酸酶(myosin light chain phosphotase,MLCP)有 关[27]。cAMP 的底物PKA 可使MLCP 的调节亚基MYPT1 等发生磷酸化,进而激活MLCP。活化的MLCP可使MLC去磷酸化,使ATP 分解减少,导致平滑肌舒张。另外,cAMP 还促使K+通道磷酸化,使细胞膜超极化,从而间接抑制膜上的L 型电压依赖性钙通道(L-type voltage-dependent calcium channel,L-VOC)的活动,阻止胞外Ca2+进入肌细胞内,降低胞浆内Ca2+离子浓度[28]。以上研究表明,cAMP/PKA 信号通路在调节平滑肌舒张中起着非常重要的作用。结合尿流动力学指标,我们观察到模型组逼尿肌cAMP、PKA 含量较空白组明显降低,这说明cAMP、PKA 参与调控逼尿肌收缩活动。而电针组cAMP、PKA 含量较模型组明显增加,这表明cAMP、PKA 可能是电针发挥抑制逼尿肌收缩作用的关键信号途径。
MLCK 是一个公认的调节平滑肌收缩信号通路上的关键蛋白。MLCK 可被PKA 磷酸化[6,26]。本研究显示,相较于空白组,模型组p-MLCK 水平明显降低,反映出骶上脊髓损伤后,逼尿肌反射性收缩活动明显增加,与尿流动力学指标表现一致。相较于模型组,电针组p-MLCK 水平明显增加。电针可以促进MLCK磷酸化使其失活,从而抑制逼尿肌反射性收缩,促进其舒张,同样与尿流动力学指标一致。同时p-MLCK水平与cAMP、PKA 含量变化一致。说明电针对p-MLCK 水平的调节可能是通过调节cAMP/PKA 信号通路实现的。
目前,我们尚未发现从cAMP/PKA 信号通路角度研究电针促进逼尿肌舒张的机制研究,本研究首次发现电针可通过cAMP/PKA 信号通路调节p-MLCK 水平,改善骶上脊髓损伤后神经源性膀胱的逼尿肌无抑制性收缩状态,改善膀胱功能,为针灸治疗逼尿肌反射亢进型膀胱提供一定的证据支持。
确定cAMP/PKA 信号通路在电针治疗骶上脊髓损伤后逼尿肌反射亢进型膀胱的作用机制,有待通过设置其信号通路上关键蛋白的阻断剂或激动剂展开进一步研究。另外,K+通道及MLCP可能是cAMP/PKA 信号通路调节平滑肌舒张信号通路的中间环节,针灸是否可通过cAMP/PKA调节K+通道及MLCP发挥促进逼尿肌舒张的作用有待进一步研究。
利益冲突声明:所有作者声明不存在利益冲突。

