肝硬化患者APRI与门静脉压力的相关性分析
左晨艳 孙连芹 刘澄 杨威 程文芳
门脉高压(portal hypertension, PH)是各种原因导致门静脉血流受阻和(或)血流量增加的结果,是肝硬化失代偿期(食管静脉曲张、腹水等)的直接原因,与高死亡率密切相关[1]。2003年,天冬氨酸氨基转移酶/血小板比值指数(APRI)被认为是慢性丙型肝炎患者显著肝纤维化和肝硬化的一个良好的无创评估指标[2]。随后,APRI被认为也可用于诊断其他病因的显著肝纤维化和肝硬化[3,4],但尚未得到充分研究。APRI能否作为门脉高压的无创测量工具尚不清楚,因此,本研究旨在探讨肝硬化门脉高压患者APRI与门静脉压力(PVP)的相关性,并探索APRI对门脉高压的无创诊断价值。
资料与方法
一、一般资料
选取2015年8月至2019年6月于南京医科大学第一附属医院介入科行经颈静脉肝内门体静脉分流术(TIPS)介入治疗的54名肝硬化PH患者为研究对象。纳入标准:①有症状、体征或检查依据的18至75岁肝硬化患者;②血清胆红素<5 mg/dL、Child评分≤12分,③无慢加急性肝功能衰竭的证据[5]。排除标准如下:①肝性脑病;②自发性细菌性腹膜炎;③肾功能衰竭(血清肌酐>2 mg/dL);④天冬氨酸氨基转移酶(AST)>5倍正常值上限(ULN);⑤任何恶性肿瘤;⑥门脉高压手术史或经颈静脉肝内门体分流术史;⑦潜在的严重心脏、呼吸或精神疾病;⑧伴随使用β受体阻滞剂、硝酸盐或任何其他预防静脉曲张出血的药物。
二、研究方法
每一个被纳入的患者都要通过详细的临床病史采集和全面的体格检查进行评估,确定肝硬化的病因。通过内镜检查明确是否存在食管静脉曲张,并询问静脉曲张出血史。完成血常规、肝肾功能和腹部超声检查,肝硬化严重程度根据Child评分进行分类。对每位患者进行APRI评估和PVP测量。
(一)天冬氨酸氨基转移酶/血小板比值指数 计算APRI时使用血清AST和血小板计数,两者在入院时和PVP测量之前同时获得。根据Wai等[2]2003年提出的公式计算APRI:(AST/AST的ULN)×100/血小板计数。我们实验室里AST的ULN是40 IU/L。
(二)门静脉压力的测量 TIPS手术过程中,门静脉穿刺成功后,在行球囊扩张前,沿导丝引入10F专用穿刺钢针鞘管系统至门静脉主干进行压力测定,以腋中线为零点,应用玻璃管水柱压力表测量。
三、统计学分析
采用SPSS 20.0软件进行统计学分析,使用双变量Spearman相关系数评价APRI与PVP的相关性,P<0.05为差异有统计学意义。绘制了受试者操作特征曲线(ROC),以研究APRI预测高门静脉压(PVP>30 cmH2O)的性能。通过计算约登指数,得到了预测高门静脉压的APRI最佳截断值。在截断值的基础上,计算了APRI预测高门静脉压的敏感度、特异性、阳性预测值(PPV)、阴性预测值(NPV)和准确率。
结 果
一、患者信息
共纳入54名肝硬化门脉高压患者,中位年龄为56岁(范围26~74岁),大部分为男性(64.8%)。肝硬化病因中病毒性30例(55.6%),酒精性3例(5.6%),隐源性和其他21例(38.9%)。大多数(85.2%)患者有食管静脉曲张,68.5%有静脉曲张出血史。Child评分中位数为7分(范围5~10分),其中Child A级17例,Child B级31例,Child C级6例。33例(61.1%)患者出现腹水。PVP中位数为40 cmH2O(范围16~61 cmH2O)。APRI中位数为1.255(范围0.08~4.72)。
二、APRI与PVP的相关性
APRI与PVP显著相关(Spearman相关系数r=0.356;P=0.008)。PVP≤30 cmH2O组和PVP>30 cmH2O组的APRI中位数显著不同,分别为0.40(范围0.08~1.27)和1.48(范围0.68~4.72);P=0.006。
三、门脉高压的预测(PVP>30 cmH2O)
绘制ROC曲线研究APRI预测高门静脉压(PVP>30 cmH2O)的性能时,曲线下面积为0.881(95%置信区间:0.756~1.000;图1)。尤登指数最大值为0.644,相当于APRI的截断值为0.81。APRI≥0.81在预测PVP>30 cmH2O时的敏感度为78.7%,特异性为85.7%,PPV为97.4%,NPV为37.5%,诊断准确率为79.6%。
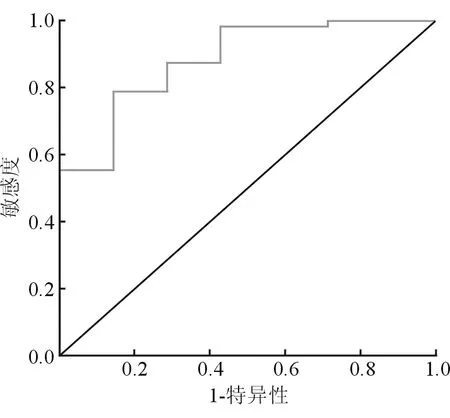
图1 PVP>30 cmH2O时APRI水平的ROC曲线
四、APRI与其他参数的关系
APRI评分与各种并发症和肝硬化严重程度的关系如表1所示。有食管静脉曲张出血史的患者中位APRI为1.51,明显高于无出血者(中位数为0.78,P=0.002)。同样地,有腹水的患者APRI高于无腹水的患者(P< 0.001)。APRI与Child评分之间存在显著的相关性(r=0.678;P< 0.001),Child A、B、C分级之间的APRI值具有统计学差异(A级与B级:P=0.01;A级与C级:P< 0.001;B级与C级:P=0.027),随着Child A、B、C分级的增加,APRI也逐渐升高(P< 0.001)。
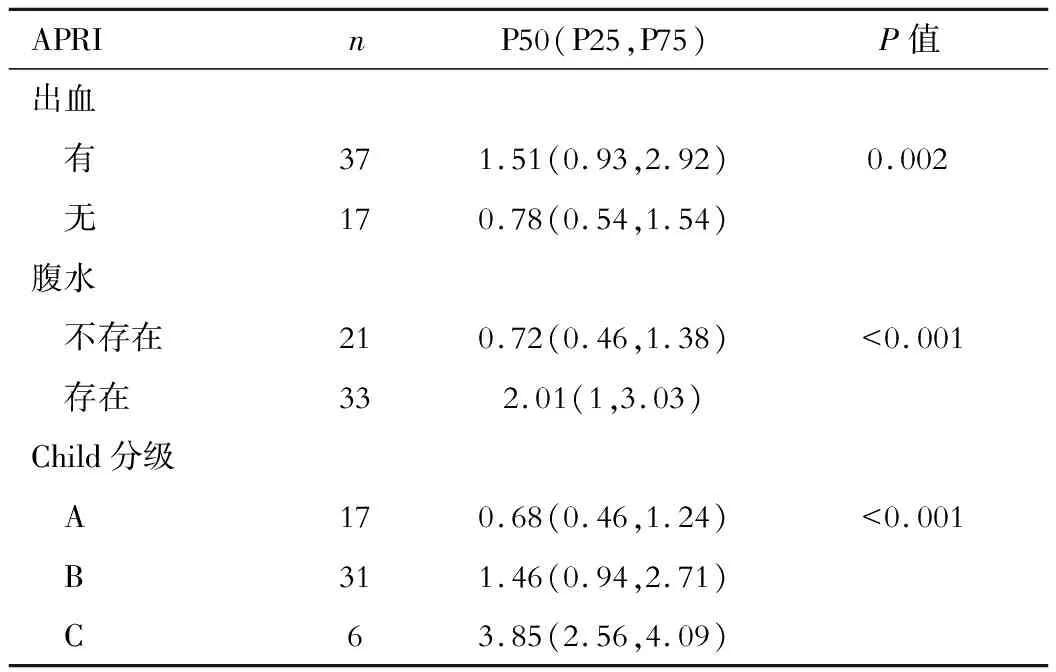
表1 APRI评分与肝硬化各种并发症及严重程度的关系
讨 论
门脉高压的发展是慢性肝病的常见后果,可导致食管静脉曲张、腹水等并发症的发生,与高死亡率密切相关。目前用于门脉高压的无创诊断技术有血清学标志物、弹性成像技术、超声检查、脾硬度测量、磁共振和计算机断层扫描等[6]。其中,血清指标APRI被认为是肝纤维化的无创预测指标,易于在临床进行推广,具有简单、无创、低成本等优点。与此同时,APRI还基于健全的发病机制。随着肝纤维化的进展和门静脉压力的升高,脾大和脾功能亢进使血小板的聚集和破坏增加[7]。此外,肝细胞产生的血小板生成素减少,因此血小板产生减少[8-9]。肝纤维化的进展降低了AST的清除率,导致血清AST水平升高[10]。此外,晚期肝病可能与线粒体损伤有关。与丙氨酸氨基转移酶(ALT)相比,AST在线粒体和细胞质中的释放更为显著[2,11-12]。
尽管目前已有多个关于APRI评估肝纤维化的研究,但APRI与门脉高压相关的研究甚少。在Verma等人的一项研究中[13],发现肝静脉压力梯度(HVPG)与APRI显著相关(r=0.365;P=0.001)。APRI预测门脉高压(HVPG>12 mmHg)的AUROC为0.716(95%CI:0.574~0.858)。APRI≥1.09在预测HVPG>12 mmHg时的敏感度为66%,特异性为73%,阳性预测值为85%,诊断准确率为68%。Kirnake等人[14]的研究也证实了APRI≥0.876对预测重度门脉高压(HVPG>12 mmHg)具有较好的准确性,且高APRI也与肝硬化的严重程度及其并发症相关。本研究通过直接测门静脉压力发现,在54例不同病因学的肝硬化患者中,APRI与PVP有很好的相关性。APRI≥0.81在预测高门静脉压力(PVP>30 cmH2O)时的敏感度为78.7%,特异性为85.7%,PPV为97.4%,NPV为37.5%,诊断准确率为79.6%,进一步证实了APRI对门脉高压的无创诊断价值。除了APRI与PVP之间存在一定的相关性之外,我们还发现APRI与肝硬化各种并发症(如静脉曲张出血、腹水)之间存在显著的相关。国内一项研究通过比较不同程度食管静脉曲张分级和APRI的相关性发现,APRI可用来预测肝硬化食管静脉曲张[15]。因此,APRI不仅与门静脉压力密切相关,也与肝硬化及门脉高压的预后有关。
APRI的一个重要局限是,除了慢性肝炎和肝硬化外,任何引起AST值升高的原因都会导致APRI错误地升高,比如各种急性肝炎或慢加急性肝功能衰竭。在我们的研究中,我们排除了血清胆红素≥5 mg/dL和AST>5倍ULN的患者。使用APRI时要注意的另一个问题是,APRI并不意味着取代HVPG、PVP、消化内镜等标准检查对门脉高压的评估。它的最佳用途是对门脉高压(PVP>30 cmH2O)作一个简单的床边预测,并优先给这些患者进行进一步的检查。由于APRI≥0.81的PPV为97.4%,因此大多数患者的门静脉压力都很高,可以紧急接受进一步的检查并服用降低门静脉压力的药物。我们研究的第三个重要局限是病因混杂且样本量小。由于肝硬化的病因可能对APRI值有重大影响,因此必须进行进一步的研究,以获得酒精、病毒和隐源性等个别病因的特异性截断值。
综上,本研究发现肝硬化患者的APRI和门静脉压力之间呈正相关。APRI≥0.81对预测门脉高压(PVP>30 cmH2O)具有可接受的准确性,可作为门脉高压无创诊断的血清标志物,但仍需要大样本的临床观察和验证。

