脑梗死后致华勒变性1例报告
张博浩,陈蕾
作者单位:天津市环湖医院神经内科,天津300350
1 病例介绍
患者,男性,72 岁,主因“头晕3 天、言语不清伴左下肢抖动2 天”于2020年7月6日收住神经内科。患者于入院前3 天无明显诱因出现头晕,自觉立位、坐位时明显,卧位稍好转,与转头方向无关,呈头部昏沉感,无言语异常,无肢体活动异常,无头痛,无恶心呕吐,无意识障碍及抽搐发作,无耳鸣及耳聋,无视物成双,未予在意。2 天前无明显诱因出现言语不清,吐字略含糊,交流略困难,语言理解正常,语言表达正常,伴伸舌左偏,伴左下肢不自主抖动,伴串联步态不能完成,头晕性质同前、程度较前加重,余症状同前,为求进一步诊治,就诊于我院急诊,查头CT 示脑桥腔隙灶,脑萎缩,脑白质脱髓鞘改变。头MR 示双侧桥臂T2WI稍高信号,考虑变性改变,脑桥、双侧基底节区腔隙灶伴软化灶,脑白质脱髓鞘改变,脑萎缩。胸CT 示右肺上叶支气管扩张,双肺纹理增多,双侧胸壁增厚,甲状腺左叶低密度影。新冠肺炎核酸检查阴性。给予输液及口服药物治疗(阿司匹林100 mg、阿托伐他汀20 mg、丁苯肽0.2 g、川芎嗪0.12 g、依达拉奉30 mg),治疗后症状较前稍好转,为求进一步诊治收入院。发病后精神、睡眠、饮食可,无发热,进食水无呛咳,二便无失禁。既往高血压8年,最高达150/100 mmHg,目前未服用药物降压,平素血压130/80 mmHg;否认糖尿病、冠心病、脑血管病史。有吸烟和饮酒30 余年,已戒10 余年。
入院查体:体温36.5℃,心率72 次/分,呼吸18次/分,血压143/89 mmHg。神清,记忆力、计算力、定向力正常,轻度构音障碍,双瞳孔等大等圆,伸舌左偏,四肢肌力V 级,肌张力正常,双侧肱二头肌反射(++),双侧肱三头肌反射(++),双侧桡骨膜反射(++),左侧膝腱反射(+++),右侧膝腱反射(++),双侧跟腱反射(+),左侧踝阵挛(+),左侧Chaddock(+),双侧掌颌反射(+),左面部及左上肢浅痛觉减退,双侧指鼻试验、跟膝胫试验欠稳准,轮替动作笨拙,左侧明显,Romberg 征(-),串联步态不能完成。血常规:淋巴细胞胞百分比19.2%,PCT、CRP 未见明显异常。入院血糖5.4 mmol/L。生化全项:总胆红素35.41 μmol/L,直接胆红素5.7 μmol/L,间接胆红素29.71 μmol/L,人血浆脂蛋白磷脂酶238.52 ng/mL;血液三项:维生素B12 168.5 ng/mL,叶酸0.957 ng/mL,血钾3.4 mmol/L;血常规、凝血功能、甲功全项、免疫全项、肾功能、尿酸、血脂属正常范围。颈部血管超声:颈动脉硬化,多发附壁斑块。TCD:血流频谱欠佳。神经肌电图:上下肢未见神经源性或肌源性损害。
入院诊断:①脑梗死(脑桥中部);②双侧桥臂异常信号(变性可能性大);③高血压病2 级(极高危)。
诊疗经过:阿司匹林100 mg/次,一日1 次(抗血小板聚集),阿托伐他汀20 mg/次,睡前服,一日1 次(调脂稳定斑块),氯化钾0.5g/次,一日2 次,口服(补钾);甲钴胺500 μg/次,一日3 次口服(补充B 族维生素);胞磷胆碱0.2 g/次,一日3 次,口服(营养神经);天麻素0.6 g/次,一日1 次,静脉滴注(止晕)、血栓通500 mg/次,一日1 次,静脉滴注(改善脑循环)等治疗,连续治疗7 天后患者头晕、语言功能较前有改善。出院后1 个月随访该患者恢复状态良好,双侧肢体共济失调症状明显好转。
2 讨 论
华勒变性指神经元胞体或近端轴突损伤后,锥体束失去了原本由锥体细胞与轴突的联系带来的营养来源,即发生Wallerian’s 变性。常伴随脑损伤后顺行性远侧神经元纤维束变性出现[1]。原发性脑损伤通常位于大脑半球的一侧,致病原因包括各类脑血管病、脑外伤、脑部占位性病变、脑白质病等,其中以脑梗死为最常见病因。
锥体束包括皮质脑桥束、皮质延髓束、皮质脊髓束等神经纤维,经内囊、桥脑基底部、大脑脚、延髓锥体、脊髓,最终下行止于脑干脑神经运动核和脊髓前角运动细胞。华勒变性以皮质脊髓束最常见[2]。本例患者为皮质脑桥小脑束损伤发病为特点,相对少见,具体特征是以脑桥基底部为原发脑梗死病灶,引发的缺血性脑卒中后双侧桥臂小脑中脚华勒变性[3]。
为了弄清单侧脑桥基底部损伤如何引发双侧小脑中脚纤维发生华勒变性,就需要从脑干神经解剖基础开启研究。事实上,脑桥基底部除了布满纵行的锥体束纤维以外,横还有横向走行的苔醉纤维为主要结构。苔藓纤维由单侧神经元发出,穿越对侧经基底部外缘向后连接小脑中脚,再由小脑白质放射至小脑皮质,继而完成大脑皮质-皮质脑桥束-脑桥基底核-小脑之间的神经元传递[4]。
华勒变性病理过程分为两部分:轴突变性和髓鞘变性。华勒变性被Kuhn 等[5]依据颅脑损伤的病理改变阶段分为4 期,病理过程对应相关核磁影像学表现特点:第1 期:4 周内,轴索退化退变,伴轻微生物化学变化,在影像上难以显示信号异常。第2 期:4~10 周,髓鞘蛋白破坏,髓鞘脂质完整,变性组织亲水性下降,表现为T1WI 上低信号,T2WI 低信号。第3 期:10~14 周,髓鞘脂质破坏,神经胶质增生,变性组织亲水性增加,表现为T1WI 上低信号,T2WI 高信号。第4 期:数月-数年,受累区域萎缩,其中以脑干病侧缩小最为突出,也可在第3 期呈现T2WI 高信号征象[6]。锥体束的异常信号在颅脑核磁主要表达的是髓鞘变性阶段:髓磷脂将由髓鞘前期溶解成的椭圆形的颗粒分解为简单的脂类,其产物中性脂肪最后被吞噬细胞吞噬。
结合本病历中病人的脑部核磁影像学特点,逐层逐序列深入分析脑干出现的异常信号:①脑桥中部偏右斑片样DWI 高信号,ADC 略低信号,FLAIR 及T2WI 略高信号。(图1-a、b、c、d)考虑急性脑梗死灶不除外;结合临床症状头晕伴言语不清,影像学检查能解释,但是患者出现的双侧共济检查欠稳准,仍存疑,尚需更多依据。②脑桥中部偏右后卵圆形长T1长T2信号,DWI低信号,ADC 高信号,最大径20 mm。(图1-a、b、c、d)考虑为陈旧性病灶,软化灶形成,非出血性。③双侧桥臂斜行片状略长T1、长T2 信号影,DWI 稍高信号,ADC 稍高信号,FLAIR 稍高信号。(图2-a、b、c、d)根据核磁特点分析,不除外神经元华勒变性,考虑由脑桥卵圆形陈旧病灶引发,给出了患者双侧共济检查欠稳准最合理的解释。④脑桥腹侧多发(2 个小点状)GRE低信号影(图1-a、b、c、d),考虑陈旧性微出血。
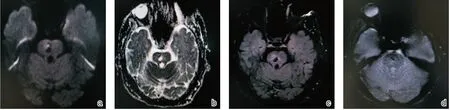
图1
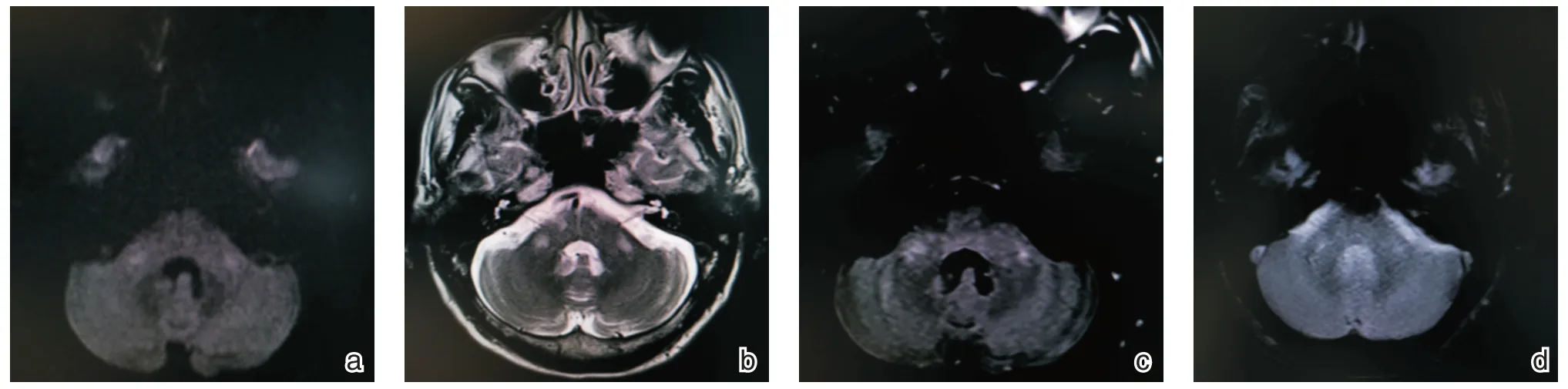
图2
华勒变性临床表现主要为明显的神经系统锥体束征,其变性的严重性与受损部位和受损大小有关,以脑梗死为例,病变部位越远离皮层锥体细胞,其变性程度越轻。病变范围越小,所累及锥体束越少时,变性轻。本例患者脑桥陈旧性梗死灶,部位远离皮层锥体细胞,范围较小,故临床症状较轻。锥体束变性与临床锥体束功能恢复密切相关,存在变性的患者功能恢复不佳,不存在变性的患者恢复较好;变性程度越重,出现时间越早,预后越差[7]。本例患者出院后1月余随访,步态不稳共济失调较住院时明显改善。
脑核磁DWI 高信号往往被认为是急性缺血性卒中细胞膜通透性增加以及细胞水肿的影像学表现。脑梗死引发神经纤维华勒变性时轴突内能量依赖的轴浆转运过程停止,导致细胞内水弥散下降。可见,DWI 出现高信号并不能除外华勒变性,常在第1 期[8]。
华勒变性目前无统一的诊断标准,可参考研究脑梗死华勒变性采用的标准:①梗死部位与继发华勒变性部位有着密切神经纤维联系,但是引起华勒变性的原发病变多位于大脑中动脉供血区,而锥体束走行区中内囊是由大脑前动脉分支供血,脑干则是椎一基底动脉系统供血,二者之间供血区并未完全重叠,显然不能用脑缺血的一元论来解释。②病程不同阶段的相应MRI表现[9]。
针对本例还有诸多需要完善之处,应该增加研究的病例总数,将来还可以逐步引入磁共振弥散张量成像DTI[10],这种通过高科技影像学手段,将神经纤维束继发变性的走行过程量化、可视化,以便完成进一步前瞻性探究,对神经变性引发患者神经功能的损伤修复,会起到极具价值的指导意义。

