纤维素/氧化纤维素/南极磷虾蛋白复合抗菌纤维的制备与表征
马 跃, 郭 静,2, 殷聚辉, 赵 秒,2, 宫玉梅,2
(1. 大连工业大学 纺织与材料工程学院, 辽宁 大连 116034;2. 辽宁省功能纤维及复合材料工程技术中心, 辽宁 大连 116034)
纤维素(C)作为一种丰富的天然高分子,具有可再生、可降解、无毒、无环境污染等特性[1-2]。虽然纤维素分子间和分子内结构中存在大量的氢键[3-5],但近年来已研发出N-甲基吗啉-N-氧化物[6]、离子液体[7-8]、碱金属氢氧化物[9-10]等多种溶剂来溶解纤维素,使其能够作为聚合物中的增强元素,改善材料的性能,拓宽其应用范围。马博谋等[11]制备了角蛋白/纤维素复合膜,该膜具有良好的表面润湿性,同时角蛋白的加入使复合膜的热稳定性略有增加,断裂强度提高近1倍。Silva等[12]制备的胶原蛋白和纤维素复合薄膜,具有良好的力学性能及较高的细胞黏附性和增殖性,可模仿软组织(动脉)并允许干细胞定向。
南极磷虾[13]数量巨大,且蛋白质含量非常丰富(虾粉中含有近70%蛋白质),但因其含氟量大而多数只作为鱼饲料使用[14]。为实现南极磷虾的高值利用,课题组开展了一系列的研究工作,如:研究了海藻酸钠(SA)与南极磷虾蛋白(AKP)的原料配比[15]、氢键相互作用[16]以及钠盐种类[17]对SA/AKP复合纤维的影响;还尝试将壳聚糖(CS)与AKP复合[18]、纤维素(C)与AKP复合[19],发现AKP可作为氢键的供体和受体[20]与天然大分子制成纤维。其中AKP与纤维素(C)的复合研究中,探讨了凝固浴组分H2SO4和Na2SO4二者的共混比对复合纤维性能的影响。另外,Kim等[21]制备了一种二醛纤维素(DAC)交联的纤维素-壳聚糖泡沫(CCLBD),发现DAC的交联可提高壳聚糖的稳定性和去除有害染料的能力。
基于以上分析,本文将ZnSO4和KAl(SO4)2分别加入至含有H2SO4/Na2SO4的凝固浴中,以探究不同盐的添加对C/AKP复合纤维成形的影响;同时,将DAC加入到C/AKP复合溶液中,并将2种溶液分别在H2SO4/Na2SO4/ZnSO4和H2SO4/Na2SO4/ KAl(SO4)2凝固浴中进行纺丝,以探究DAC的加入对C/AKP复合纤维成形的影响,并对所制备的复合纤维的热性能、降解性、抑菌性等进行表征。
1 实验部分
1.1 实验原料
纤维素(C),平均聚合度为 550,新疆光大山河化工科技有限公司;氧化纤维素(DAC)、南极磷虾蛋白(AKP),实验室自制[22-23];高碘酸钠、硫酸锌、硫酸铝钾,国药集团化学试剂有限公司;氢氧化钠、尿素、硫酸、无水硫酸钠,天津市科密欧化学试剂有限公司;模拟体液(SBF),青岛捷世康科技有限公司;细菌,北京赛尔瑞成生命科学技术有限公司。
1.2 复合纤维的制备
将7 g氢氧化钠和12 g尿素加入至81 g水中,充分溶解后得到均一溶液,并将其作为溶剂;将1 g磷虾蛋白(AKP)、1 g 氧化纤维素(DAC)和3 g 纤维素(C)依次加入溶剂中,低温溶解制备C/DAC/AKP(质量比为3∶1∶1)纺丝原液,同时以同样的方法制备C/AKP纺丝原液。然后用自制小型纺丝机以5 mm/min的速度将上述复合溶液分别挤入10%H2SO4/12%Na2SO4/10%ZnSO4凝固浴(1)和10%H2SO4/12%Na2SO4/10%KAl(SO4)2凝固浴(2)中,最后经1.2倍拉伸比牵伸后,洗涤干燥得到复合纤维,制备得到的4种复合纤维分别记为C/DAC/AKP-1、C/DAC/AKP-2、C/AKP-1和C/AKP-2。
1.3 性能测试
化学结构测试:采用Spectrum-One B型红外光谱仪(美国PE公司),利用溴化钾压片法测试原料及复合纤维的化学结构,波数范围为4 500~400 cm-1。
热性能测试:采用Q600型热重分析仪(美国TA公司)测试复合纤维的热性能。测试条件:温度范围为30~700 ℃,N2气氛,升温速率为10 ℃/min。
微观结构测试:先对纤维进行喷金处理,然后采用JSM-6460LV型扫描电子显微镜(日本电子公司)对纤维的表面形貌进行分析,加速电压为5 kV。
体外降解测试:将等质量的复合纤维分别浸泡在等体积的模拟体液(pH=7.4)中,并置于37 ℃恒温培养箱,分别浸泡2、5、10、15、20、30 d后用去离子水和酒精多次浸泡水洗,晾干后称量,计算复合纤维的质量损失率。
结晶性能测试:采用S-4800型 X射线衍射仪(日本电子公司)对复合纤维的结晶性能进行测试,测试条件为:铜靶,管电压40 kV,管电流30 mA,2θ范围10°~70°,扫描速度5(°)/min。
抑菌性能测试:采用琼脂平皿扩散法测定纤维的抗菌性能。分别将大肠杆菌和金黄色葡萄球菌的细菌悬浮液均匀分散在固体培养基中;再将等质量的纤维试样置于培养基中,于37 ℃培养箱中恒温培养24 h,观察复合纤维周围是否存在抑菌圈,以评估复合纤维的抗菌性能。
2 结果与讨论
2.1 化学结构分析
图1示出原料C、DAC、AKP和DAC/AKP的红外光谱,图 2示出C/AKP和C/DAC/AKP复合纤维的红外光谱。由图1中C的红外曲线可知,1 050 cm-1处为C—C拉伸振动峰,2 925 cm-1处为C—H拉伸振动峰,3 435 cm-1处的宽带主要是O—H拉伸振动峰。AKP的典型吸收峰位于1 641 cm-1和1 538 cm-1处,分别为酰胺Ⅰ带和酰胺Ⅱ带吸收峰。从DAC的红外曲线可以看出,在1 733 cm-1处出现了1个新的醛基吸收峰。这是由于高碘酸钠氧化纤维素,将纤维素大分子葡萄糖环的C2—C3键拆分,并将2个羟基氧化为醛基,得到二醛纤维素。DAC与AKP结合后,醛基吸收带减弱,在1 653 cm-1处出现新的吸收带,表明亚胺键的形成[24]。
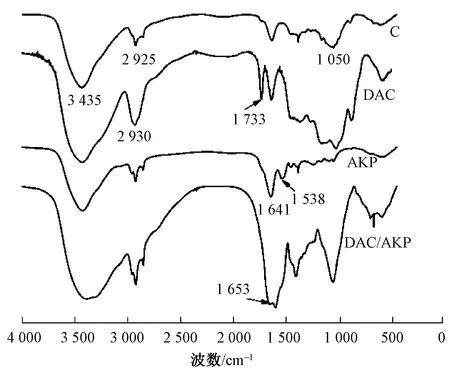
图1 C、DAC、AKP和DAC/AKP的红外光谱图Fig.1 Infrared spectra of C, DAC, AKP and DAC/AKP

图2 C/DAC/AKP和C/AKP复合纤维的红外光谱图Fig.2 Infrared spectrum of C/DAC/AKP and C/AKP composite fibers
由图2中C/DAC/AKP-1和C/DAC/AKP-2复合纤维的红外曲线可知,1 733 cm-1处的醛基吸收峰消失[25],说明DAC与AKP发生了反应。另外,羟基带吸收峰位置发生波动,这可能是由于C、DAC、AKP间分子相互作用的结果。
为进一步研究纤维的分子氢键作用,在Origin 9.1中将复合纤维在3 800~3 000 cm-1范围内的曲线用高斯分峰拟合[16,26],得到各氢键类型子峰的分布强度,并计算各子峰的峰面积和氢键比例[19,27],结果如表1所示。

表1 不同凝固浴制备的C/DAC/AKP和C/AKP复合纤维氢键拟合结果Tab.1 Hydrogen bonds fitting results of C/DAC/AKP and C/AKP composite fibers prepared in different coagulation baths
在同一凝固浴下发现,加入DAC的C/DAC/AKP-1与C/AKP-1相比,复合纤维中分子内氢键的比例从74.55%下降到63.27%,在分子内氢键中OH…OH氢键所占的比例大,说明分子内氢键中OH…OH占主要作用;而分子间氢键比例从24.26%升高到32.96%,升高了8.7%,且各种类型的分子间氢键的比例由大到小排列为OH…醚O、OH…π、OH…N。在不同凝固浴下发现,凝固浴中含有KAl(SO4)2时所制备的复合纤维的分子间氢键比例均高于凝固浴中含有ZnSO4的复合纤维,这是因为阳离子和分子之间的结合强度取决于所涉及阳离子的理化特性[28],其电荷密度越高,相互作用越强,而Al3+比Zn2+的电荷密度高,Al3+与分子的相互作用强,从而使复合纤维内分子氢键含量提高。
2.2 热稳定性分析
图3示出C/DAC/AKP和C/AKP复合纤维的热稳定性曲线。可以看出,复合纤维的质量损失主要分为2个阶段:1)在95~180 ℃之间的质量损失率为8%,这是由于结合水的蒸发所致;2)在260~360 ℃时的质量损失率最高,约为40%,主要是由于大分子骨架开裂所致。然而由图3(b)发现,C/DAC/AKP-1复合纤维的最大热分解温度(330 ℃)高于C/AKP-1复合纤维(307 ℃),这是由于DAC的加入使体系的分子间氢键增加,从而使体系的热稳定性提高。另外还可看出,凝固浴中含有KAl(SO4)2的复合纤维的热分解温度较高(如C/DAC/AKP-2为334 ℃,大于C/DAC/AKP-1的330 ℃),这是由于该凝固浴组分所制备的复合纤维结构致密,从而使其热稳定性提高。
2.3 复合纤维形貌分析

图3 C/DAC/AKP和C/AKP复合纤维的热稳定性曲线Fig.3 Thermal stability curve of C/DAC/AKP and C/AKP composite fibers.(a)TG curves;(b)Thermogravimetry curves
C/DAC/AKP和C/AKP复合纤维的表面形貌如图4所示。可以看出,在相同的拉伸和干燥条件下,纤维表面轴向分布的沟槽结构具有明显不同的深度。这是由于复合溶液与凝固浴之间的化学反应以及湿法纺丝过程中从表面到内部的双重扩散造成的。当复合溶液进入凝固浴时,硫酸和硫酸锌或硫酸铝钾迁移到纤维表面,并与尿素、氢氧化钠等发生多重反应,即硫酸与氢氧化钠的中和反应;硫酸和尿素形成硫酸脲,硫酸钠、硫酸锌、硫酸铝钾进入纤维,导致复合纤维脱水等。这些反应会破坏溶解平衡,将复合纤维从溶液中分离出来并产生凝胶化。另外,硫酸钠、硫酸锌、硫酸铝钾和硫酸的同离子效应能有效降低凝固浴中氢离子的浓度,降低中和反应速率,减缓纤维成形过程,也正是由于这些反应,才使得复合纤维表面存在不同深度的沟槽。而对比C/DAC/AKP复合纤维和C/AKP复合纤维的表面形貌发现,DAC的加入对复合纤维的形貌影响不大,从侧面也反映了DAC与C和AKP相容性好。

图4 C/DAC/AKP和C/AKP复合纤维的表面形貌(×200)Fig.4 Surface morphology of C/DAC/AKP and C/AKP composite fibers(×200)
2.4 复合纤维体液吸附降解性能分析
C/DAC/AKP和C/AKP复合纤维的模拟体液(SBF)降解实验结果如图5所示。可知,复合纤维发生降解的本质就是在SBF的作用下,其分子中D-葡萄糖的β-1,4糖苷键断裂,使大分子转变为小分子的过程[29]。由图5可以看出,在同一凝固浴下C/DAC/AKP复合纤维的降解率较C/AKP复合纤维的高,这是由于DAC的加入使复合体系含有更多的羟基,降低了表面反应势垒,简化了降解进程[30],从而使降解率提高;而在不同凝固浴中,含有铝离子的复合纤维相对于含有锌离子的复合纤维降解率低,这可能是由于铝离子的半径小,使体系的结构紧凑性相对高一些,因此对复合纤维进行了结晶性能测试,结果如图6所示。采用Jade6.5软件计算发现,C/DAC/AKP-2的结晶度(78.46%)高于C/DAC/AKP-1的结晶度(76.51%),即含Al3+的复合纤维的结晶度稍高。同时C/AKP-2的结晶度为79.65%,也高于C/DAC/AKP-2复合纤维,而降解主要是发生在纤维的无定形区域,因此C/AKP-2复合纤维降解率最低。
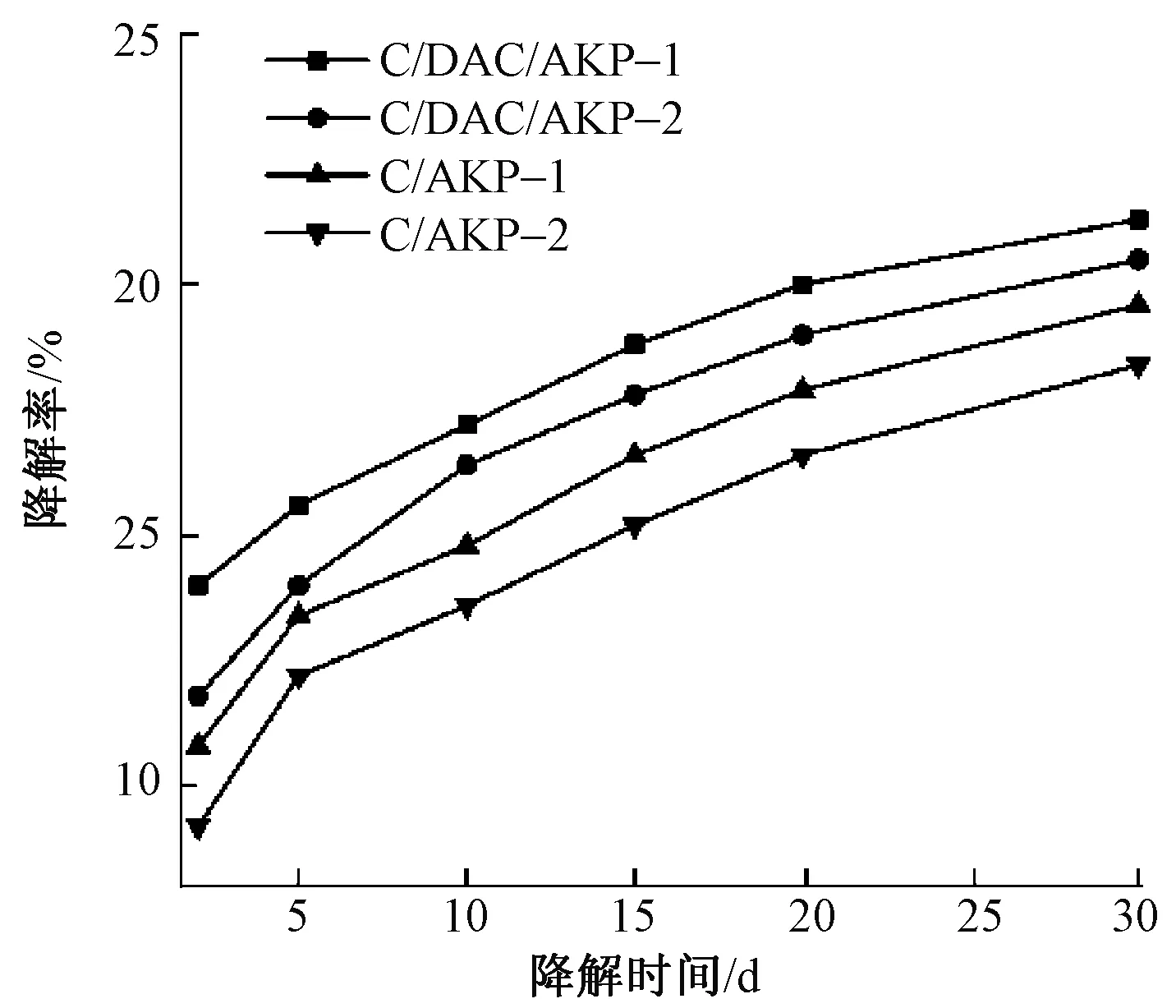
图5 C/DAC/AKP及C/AKP复合纤维的降解率Fig.5 Degradation rate of C/DAC/AKP and C/AKP composite fibers

图6 C/DAC/AKP及C/AKP复合纤维的结晶曲线Fig.6 Crystallization curves of C/DAC/AKP and C/AKP composite fibers
2.5 复合纤维抑菌性能分析
图7为复合纤维的抑菌效果图。可以看出,在复合纤维周围可检测到明显的抑制区,这意味着复合纤维有较强的抑菌作用。而C/DAC/AKP和C/AKP复合纤维的抑菌效果差别较小,说明DAC对纤维的抑菌性能影响不大。对比不同凝固浴下制备的复合纤维发现,2种复合纤维均具有良好的抑菌效果,这可能是因为纤维中含有的锌[24]抑菌,且硫酸铝钾也具有抑菌性[31-32]。为进一步验证该分析结果,采用能谱仪(EDS)测试了复合纤维上的元素分布,结果如图8、9所示。

图7 C/DAC/AKP和C/AKP复合纤维的抗菌效果图Fig.7 Antibacterial effect of C/DAC/AKP and C/AKP composite fibers. (a)Escherichia coli;(b)Staphylococcus aureus
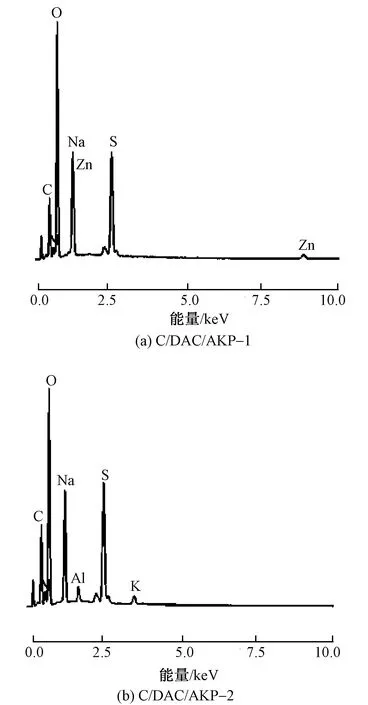
图8 C/DAC/AKP复合纤维的EDS能谱图Fig.8 EDS spectra of C/DAC/AKP composite fibers
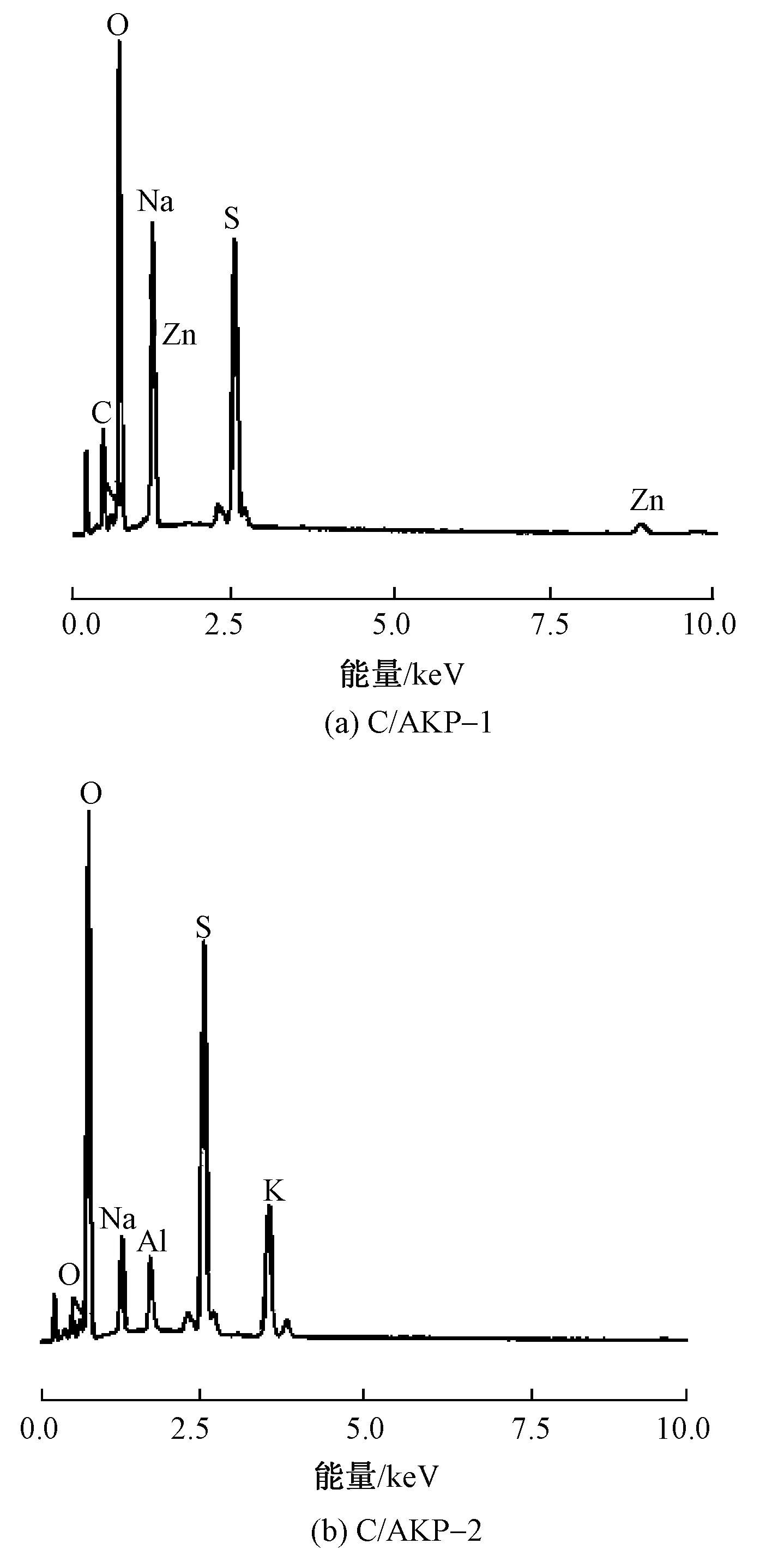
图9 C/AKP复合纤维的EDS能谱Fig.9 EDS spectra of C/AKP composite fibers
从图8、9可以看出,纤维中确实存在锌离子、铝离子,进一步证明了凝固中的硫酸锌和硫酸铝钾的添加使得复合纤维具有良好的抑菌性。
3 结 论
本文采用湿法纺丝工艺以H2SO4/Na2SO4/ZnSO4和H2SO4/Na2SO4/KAl(SO4)2为凝固浴,成功制备了纤维素/氧化纤维素/南极磷虾蛋白(C/DAC/AKP)和纤维素/南极磷虾蛋白(C/AKP)复合纤维。研究发现,C/DAC/AKP复合纤维的分子间氢键比例比C/AKP纤维的高8.7%,热分解温度也由307 ℃提高到330 ℃;C/DAC/AKP纤维的结晶度低于C/AKP纤维,降解速率高于C/AKP纤维;在H2SO4/Na2SO4/KAl(SO4)2凝固浴中制备的复合纤维的分子间氢键含量、热稳定性和结晶度均有所上升,形成的C/AKP和C/DAC/AKP复合纤维对大肠杆菌和金黄色葡萄球菌均具有良好的抗菌效果,说明其在生物材料方面具有潜在的应用价值。

