介入治疗真性红细胞增多症合并急性下肢动脉血栓形成1例
满新贺,丁 旭,李力宏,杨永久
真性红细胞增多症(polycythemia vera,PV)是一种慢性骨髓增生性肿瘤,其造血干细胞过度增殖,在分化或成熟过程中以红细胞增生为主要特点,发病中位年龄为65岁[1],年发病率为(0.4~2.8)/10万,中位生存期为14年[2],有向骨髓纤维化及急性白血病转化可能性[3]。血栓形成是PV的主要临床表现及死亡原因,也是最重要的预后因素。有研究报道,PV患者血栓发生率可达12%~40%[2, 4]。影响PV患者血栓形成的最重要因素是高龄和既往血栓形成史[5]。PV合并动脉血栓以脑血管和冠状动脉血栓形成多见,合并下肢动脉血栓形成临床罕见。笔者对我院收治的1例PV继发下肢动脉血栓形成患者的临床特点、影像学特征及治疗过程进行总结。
1 临床资料
1.1 病例介绍 患者,男,62岁,于2018-06-05入院,主诉1周前左下肢突发疼痛伴发凉,并伴有间歇性跛行,距离可达100 m,未发现明显破溃。既往史:无房颤,否认高血压、糖尿病、冠心病、脑血管病史、吸烟史。入院查体:生命体征平稳,心肺腹查体未见明显异常;双侧股动脉、右侧腘动脉、胫后动脉、足背动脉搏动可及,左侧腘动脉、胫后动脉、足背动脉未触及。入院后查血常规:血红蛋白(HGB)206 g/L,红细胞计数(RBC)6.23×109/L,血细胞比容(HCT)0.592;D-二聚体(D-dimer)1090 ng/ml。踝肱指数(ankle brachial index,ABI)左侧足背动脉未测出,左侧胫后动脉ABI 0.45,右侧足背动脉ABI 1.11,右侧胫后动脉ABI 1.32。影像学检查:下肢动脉CT血管成像示下肢动脉硬化改变、左侧股浅动脉长段闭塞(图1)。骨髓细胞学检查及基因检测:骨髓细胞学检查示骨髓增生活跃,粒系54.5%,红系36%,粒∶红=1.51∶1.00;粒系各阶段比例及形态大致正常。红系各阶段比例及形态正常。基因检测:样本JAK2基因V617F突变型:阳性。诊断为红细胞增多症。
1.2 方法 患者入院立即给予低分子肝素抗凝(6000 U,12 h/次,皮下注射);在明确PV诊断后给予羟基脲(0.5 g,2次/d,口服)降红细胞治疗;股动脉病变采取介入治疗,给予血栓抽吸、球囊扩张治疗(图2)。术后1周出院,出院后规律应用利伐沙班(20 mg,1次/d,口服)抗凝治疗,应用羟基脲(0.5 g,2次/d,口服)降红细胞治疗。
A.主髂动脉轻度钙化,左侧股浅动脉自开口未见明显显影;B.股浅动脉远端通过股深动脉侧枝显影,右侧股浅动脉及腘动脉未见明显异常;C.左侧腘动脉、胫前、胫后、腓动脉流出道良好,右侧腘动脉、胫前、胫后动脉流出道良好,右侧腓动脉未见明显显影
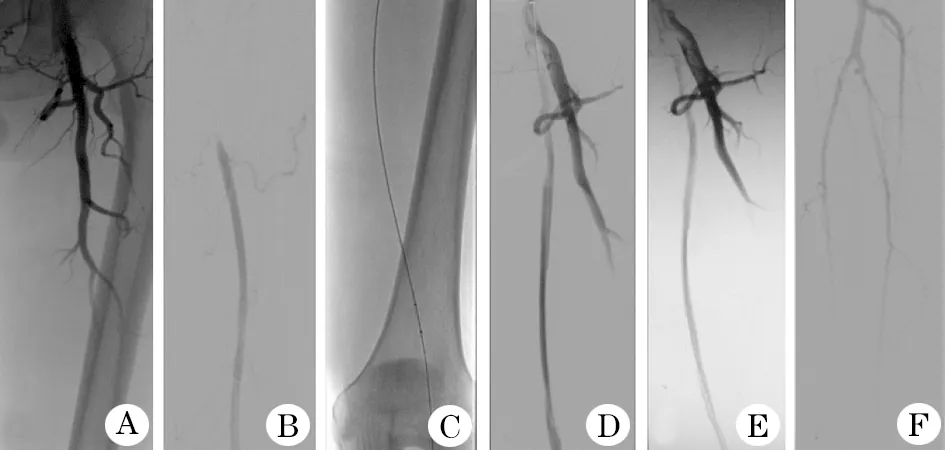
图2 真性红细胞增多症合并下肢动脉血栓患者股动脉介入治疗过程
A.股浅动脉自开口未见显影;B.通过股深动脉侧支,股浅动脉远端动脉显影;C. 导丝通过病变,ANGIOJET吸栓导管抽吸血栓;D.吸栓后再次造影可见:股浅动脉显影、股浅动脉近端可见明显狭窄、远端可见影响血流的夹层;E.给予球囊扩张,造影可见股动脉流出道良好;F.造影可见膝下动脉流出道良好,未见明显狭窄及闭塞病变
1.3 监测指标 出院后每个月门诊复查随访,行下肢动脉查体、下肢动脉ABI检查、血常规、凝血常规。随访时间12个月。
1.4 结果 术后下肢疼痛症状明显好转,术后1 d至术后12个月ABI均得到明显改善(表1);术后1~12个月HGB及HCT恢复至正常水平;术后12个月未再出现血栓事件及出血事件。
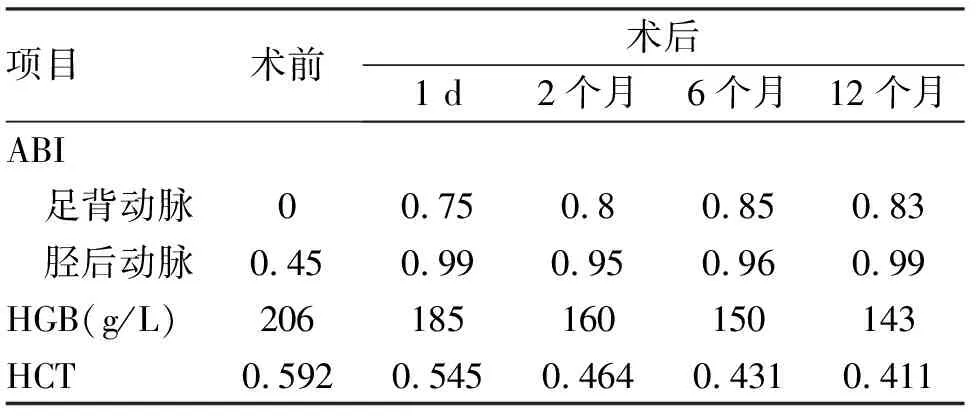
表1 真性红细胞增多症合并下肢动脉血栓患者术前及术后ABI、HGB、HCT变化
2 讨 论
PV的临床进展与是否发生血栓并发症有关,与无PV病史的血栓形成患者相比,合并PV的血栓形成患者死亡风险更高[6]。研究显示,PV合并血栓以脑梗死最为多见[7],目前,PV合并下肢动脉血栓形成的发病情况、治疗预后等缺乏临床共识,临床报道较为罕见。本文通过回顾1例PV合并下肢动脉血栓形成的治疗过程进行经验总结,以期为临床治疗提供参考。
高龄和既往血栓病史是血栓形成事件最主要的预测因素[8]。另外,HCT和白细胞增多也是PV患者血栓形成的相关危险因素[9]。其次,RBC升高、JAK2V617F基因突变、血液细胞(血小板、白细胞和内皮细胞)活化也与血栓形成事件的风险增加有关[7]。高血压病史、吸烟史、糖尿病病史、高脂血症、肥胖等因素也是增加PV患者发生血栓的危险因素[10]。根据以上风险因素,PV合并血栓形成风险程度可分为三级:年龄<40岁、既往无血栓事件为低危组;年龄40~60岁、既往无血栓事件、存在心血管危险因素(吸烟史、高血压病史、高胆固醇血症、糖尿病病史)为中危组;满足年龄>60岁、既往有血栓事件其中一项者为高危组[4]。临床上根据不同风险分级制定不同治疗方案,低危组和中危组治疗主要采用阿司匹林;高危组在阿司匹林或口服抗凝药合并放血治疗的基础上,联合羟基脲或干扰素α等降细胞治疗[4,11]。
对PV合并血栓形成,临床上多采用非手术治疗。既往有报道通过多次吸栓、球囊扩张或置入支架等介入治疗可以获得较好的治疗效果,并可作为一种有效的治疗手段[12]。但蔡伟等[13]研究发现,过早或过多的介入手术治疗有可能增加PV患者血栓复发风险。本例患者PV合并下肢动脉血栓形成诊断明确,风险分级为高危组,治疗上对患者患侧下肢动脉采用血栓抽吸及球囊扩张的介入治疗,同时联合规律利伐沙班抗凝、羟基脲降细胞治疗。术后患者下肢缺血症状明显缓解,术后2、6、12个月随访患者下肢无明显不适,无再发动脉血栓形成。对于PV合并血栓形成的治疗,抗凝是治疗过程中关键环节,在规律复查随访过程中应尽可能延长抗凝时间,同时定期评估出血风险。Parasuraman等[14]报道,HCT水平与PV患者血栓形成有较强的相关性,研究结果显示将PV患者的HCT控制在<45%,对预防血栓的发生有重要作用。因此,本文病例除定期复查下肢动脉查体、下肢动脉ABI检查、HGB等情况外,对患者HCT水平进行了重点随访和监测。
总之,PV合并下肢动脉血栓形成临床少见,多种因素均参与PV患者血栓形成过程中,临床上需重视PV患者血栓发生前的预防。对于PV合并下肢动脉血栓形成,应根据血栓风险分级选择不同的治疗策略,在充分评估患者血栓复发风险、抗凝或抗血小板治疗的出血风险后,根据个体化情况决定是否选择血栓抽吸、球囊扩张及支架成形术等介入治疗,使患者获得最佳的治疗效果,取得更好的临床预后。

