IgG4相关自身免疫性胰腺炎的诊治:5例报道并文献复习
闫斌斌,李鹏飞,张立达,杨玉秀,李 健
河南省人民医院,郑州大学人民医院,河南大学临床医学院消化内科,华中阜外医院消化内科,河南 郑州 450000
IgG4相关性疾病是一个新的独立疾病,临床表现多种多样,日本曾统计发病率为(0.28~1.08)/100 000,我国缺乏相应的数据,可浸润胰腺、胆管、唾液腺、颌下腺等多种器官,出现器官弥漫性肿胀或局部肿块形成,病理可见IgG4阳性浆细胞为主的淋巴细胞浸润、闭塞性静脉炎、组织纤维化等,血清IgG4升高[1]。IgG4相关自身免疫性胰腺炎(IgG4-related autoimmune pancreatitis,IgG4-AIP)病例数占同期慢性胰腺炎患者总数的3.6%~9.7%,自身免疫性胰腺炎(autoimmune pancreatitis,AIP)多表现为胰头肿大等,极易误诊[2]。现将我院收治的5例IgG4-AIP综合报道如下。
1 资料与方法
1.1 一般资料我院2019年1月1日至2019年12月1日收治的经病理确诊为IgG4-AIP的患者共5例,男4例,女1例,年龄50~66岁。
1.2 纳入及排除标准
1.2.1 纳入标准:(1)影像学检查:胰腺弥漫性或局限性增大,胰胆管弥漫性或局限性狭窄;(2)实验室检查:血清IgG4升高,大于正常上限值的2倍;(3)病理组织学检查:胰腺纤维化和淋巴细胞、浆细胞浸润,IgG4阳性细胞>10个/高倍视野[3]。
1.2.2 排除标准:(1)IgG4小于正常上限值的2倍;(2)病理组织学未见大量IgG4阳性细胞;(3)合并胰腺癌或其他肿瘤;(4)合并结缔组织病。
2 结果
2.1 临床表现腹痛5例,梗阻性黄疸3例,体质量减轻3例,合并腹膜后纤维化1例,合并颌下腺病变1例,合并胆管病变1例,局灶性胰头肿大3例,胰腺弥漫性肿大2例。经超声内镜引导下细针穿刺吸取术(EUS-FNA)诊断3例,外科手术探查术后病理诊断2例(见表1)。
2.2 辅助检查结果本组病例IgG4均大于正常上限值的2倍;CA19-9明显升高2例,轻度升高2例,正常1例;5例病理学检查均见浆细胞浸润,胰腺纤维组织增生,IgG4阳性细胞表达(见表2)。
2.3 治疗与随访5例患者均采用糖皮质激素治疗,口服醋酸泼尼松起始剂量(30~40) mg/d,2周后每周递减5 mg,1个月后复查所有患者腹痛明显缓解,肝功能正常,IgG4、CA19-9明显下降,CT提示胰腺缩小。目前随访4个月,5例患者未见复发。其中1例患者的详细诊疗过程如图1~11所示。

表1 5例患者临床资料Tab 1 Clinical data of 5 cases patients
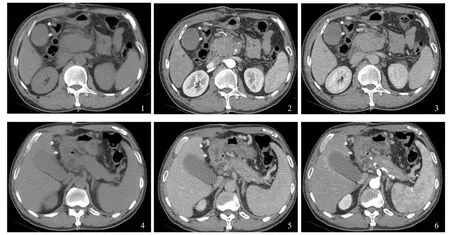
图1~6 治疗前增强CT:胰腺弥漫性肿胀,胰头为著,胰腺密度减低,增强扫描见强化降低 Fig 1-6 Enhanced CT before treatment: diffuse enlargement of the pancreas, especially the head of the pancreas,

图7~9 治疗后增强CT:胰腺形态尚可,体积较前缩小 Fig 7-9 Enhanced CT after treatment: the shape of the pancreas was moderate and the volume was smaller than before
3 讨论
AIP最早于1991年由川口和他的同事首次发现,胰腺组织术后病理学表现为淋巴浆细胞性硬化性胰腺炎[4]。1995年,由Yoshida等提出AIP的概念[5]。近年来AIP有两种类型[6],1型AIP是IgG4相关性疾病的胰腺表现,又称淋巴浆细胞硬化性胰腺炎,IgG4是唯一的血清学标志物[7],多见于50岁以上男性[8];2型AIP,又称特发性导管中心性胰腺炎,IgG4抗体阴性,在东亚地区极为罕见,多见于年轻患者,同炎症性肠病有一定关系[9]。本文所述5例患者均为IgG4-AIP,即1型AIP。
发病机制目前尚不清楚,可能与下列因素有关:(1)免疫因素:本研究中IgG4均升高,且大于正常上限值的2倍,根据患者常伴有γ-球蛋白、IgG升高、浆细胞浸润,激素治疗反应良好,推测与自身免疫相关。但有研究表明,IgG4诊断AIP的阳性率为74%[10],但IgG4仍被认为是最有价值的标准之一[7],此外胰腺分泌胰蛋白酶抑制剂(topancreatic secretory trypsin inhibitor,PSTI)[11]、抗淀粉酶α-2A[12]、热休克蛋白10(heat shock protein 10, HSP10)[13]等被发现在AIP发生中起一定的作用。(2)遗传因素:目前已有研究认为,AIP发病与遗传因素有关,

表2 5例患者治疗前后IgG4、CA19-9的比较Tab 2 Comparison of IgG4 and CA19-9 in 5 patients before and after treatment
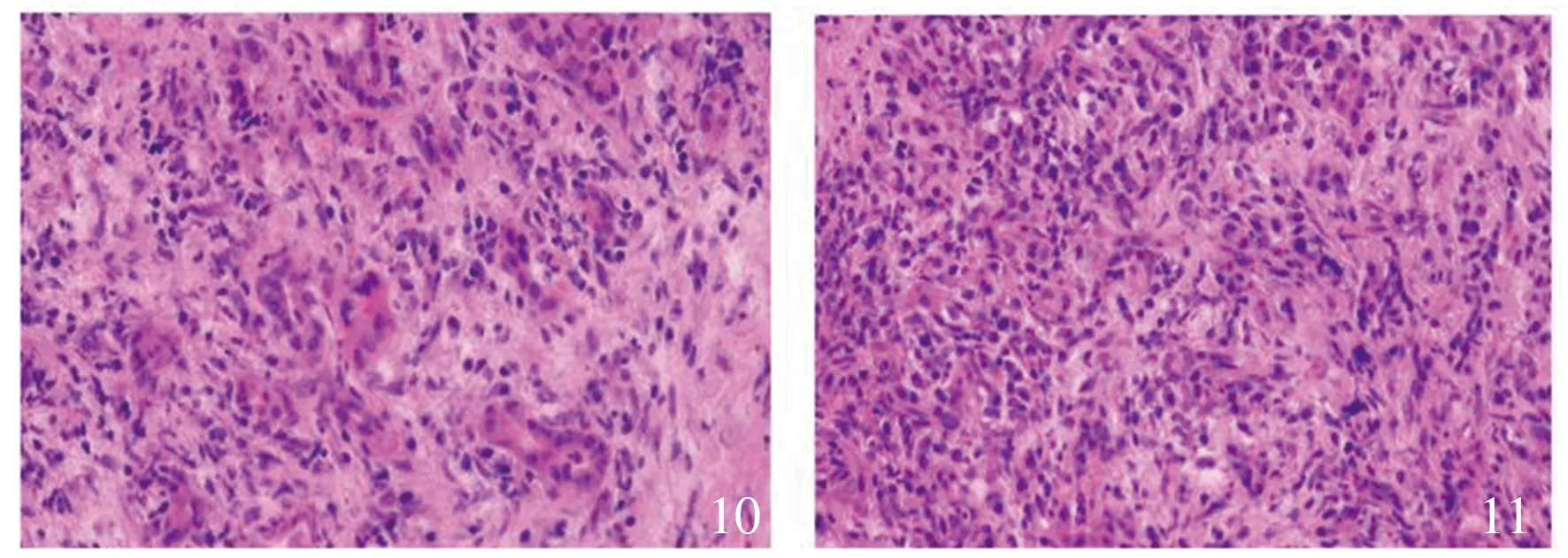
图10~11 IgG4表达升高,阳性细胞最密集处约
且有研究认为不仅与基因HLA相关,非HLA基因同样可能起着某种作用[14]。(3)特异质反应:Torre等[15]发现,AIP患者中有相当比例长期过敏,且发现外周血嗜酸性粒细胞增多,血清IgE升高。因此,提出过敏机制参与了疾病的发生。
IgG4-AIP影像学表现:彩超检查仅能提示胰腺体积增大,AIP根据病变范围可分为弥漫性和局灶性,弥漫性AIP的CT/MRI特征性表现为胰腺弥漫性肿胀,呈腊肠样改变,局灶性肿块多位于胰头,有时同胰腺癌鉴别较为困难[16]。PET-CT有助于检测病变器官的代谢活动,但不能区分病情。但影像学的检查有助于疾病的分期和监测,评估治疗效果。
IgG4-AIP组织病理学:胰腺导管周围有大量的淋巴细胞/浆细胞浸润和纤维化,大量IgG4阳性的淋巴细胞浸润,闭塞性静脉炎。组织标本的获取目前面临巨大挑战,常用的方法有EUS-FNA、手术切除标本。EUS-FNA创伤小,特异性高,但灵敏性较低。本组患者仅有3例术前通过EUS-FNA得以确诊,阳性率更高的穿刺方法有待进一步研究。
本病最重要的是与恶性肿瘤的鉴别,有时十分困难,胰腺癌患者中约10%的病例出现IgG4升高,而AIP中CA19-9同样会升高[17],本组患者中有4例CA19-9升高。一项纳入115例经病理证实为胰腺癌患者,对其进行血清IgG4水平检测,14例患者血浆IgG4水平>135 mg/dl,其中2例患者血清IgG4水平高于正常上限的2倍,1例患者符合组织学诊断标准的AIP同时存在PC[18]。提示我们有时区分胰腺癌和AIP是困难的,胰腺的靶向活检应是首选方法。
由于IgG4-AIP对激素治疗敏感,目前的治疗以口服激素为主。我国指南[19]推荐:口服泼尼松(30~40) mg/d,或按照0.6 mg·kg-1·d-1为起始剂量,治疗2~4周后,如效果较好可逐渐减量,以每1~2周减少5 mg,最终以5 mg/d剂量维持或停药。目前我国缺乏足够的流行病学依据,对于激素起始剂量及是否需要维持治疗仍存在一定的分歧。IgG4-AIP初始缓解后存在复发可能,对于复发患者首选再次给予激素治疗,有效患者需延长用药时间及维持治疗。对于激素无效的患者,利妥昔单抗是首选[20],另外其他免疫抑制剂也可选用。一般不需手术治疗,仅在以下情况需手术治疗:(1)诊断不明,特别是同胰腺癌鉴别困难时;(2)内科治疗无效或胆道梗阻需长期留置胆道支架者。本研究中2例手术患者均为不能明确诊断,术前不能排除胰腺癌。
综上所述,IgG4-AIP相对发病率低,目前对疾病的发病机制、诊断、鉴别诊断及治疗等方面存在认识不足及一定分歧,因此,需要临床医师充分提高对本病的认识,不断学习探索,总结经验,从而避免误诊误治,同时为患者提供更加安全、科学、有效的治疗方案。

