局部晚期非小细胞肺癌容积弧形调强放疗与固定野动态调强放疗剂量学对比*
刘楚基,吴秋梅,张 云,陈 敏
湛江中心人民医院,广东 湛江 524031
非小细胞肺癌是肺癌常见类型之一,约占肺癌总发病率的80%以上,其中局部晚期非小细胞肺癌约占1/3,此类患者已无法实施手术切除,需行放射治疗以延长生存期[1]。固定野动态调强放疗(IMRT)建立在三维适形放疗技术基础上,能使靶区照射剂量提高的同时,使周围器官的照射剂量减少,但其存在投照时间较长、机器跳数过多等不足[2]。容积弧形调强放疗(VMAT)是利用可变机架转速、可变剂量率和连续运动的多叶准直器等达到优化剂量分布的目的,属于新型的旋转固定野强调反射治疗手段,逐渐被应用于局部晚期非小细胞肺癌治疗。为此,本研究选取于2017年6月—2019年8月间就诊于湛江中心人民医院的84例局部晚期非小细胞肺癌患者作为研究对象,旨在分析局部晚期非小细胞肺癌VMAT与IMRT剂量学差异,研究如下。
1 资料与方法
1.1 基本资料
选取于2017 年6 月—2019 年8 月间就诊于湛江中心人民医院的84 例局部晚期非小细胞肺癌患者作为研究对象。研究经医院医学伦理委员会批准。将入组患者按随机数字表法分为两组,每组各42 例。试验组,男31 例,女11例;年龄34~72 岁,平均年龄(56.21±6.32)岁;腺癌17例,鳞状细胞癌25 例;周围型肺癌24 例,中央型肺癌18例。对照组,男28 例,女14 例;年龄31~73 岁,平均年龄(56.15±6.27)岁;腺癌15例,鳞状细胞癌27例;周围型肺癌29 例,中央型肺癌13 例。比较两组基本资料,差异无统计学意义(P>0.05)。
1.2 入选标准
(1)纳入标准:经病理学和MRI 等影像学检查确诊为局部晚期非小细胞肺癌肺癌者;患者或家属签署知情同意书;临床分期为Ⅲa/Ⅲb 期患者;入组前均未行放化疗治疗者。(2)排除标准:预计生存时间<3个月者;Ⅲ~Ⅳ级心功能不全者;精神异常者;肝、肾等重要器官严重不全者;不耐受放射治疗者。
1.3 方法
取仰卧位,交叉双手置于头顶,用体膜固定体位。在患者静止状态下用64 排螺旋CT 实施扫描,扫描范围:第6 颈椎~第2 胸椎,层厚5 mm。按照扫描获取的图像勾画靶区。临床靶区鳞癌需外放6 mm,腺癌外放8 mm。将短径>10 mm 的纵膈淋巴结划入大体肿瘤靶体积(肿瘤临床灶,包括转移淋巴结和原发灶),并向外扩张0.8 cm 左右,将其作为临床靶体积。分别于肺窗上、纵膈窗上对肺内病变、纵膈病变勾画。危及器官:食管、双肺、心脏、脊髓。以美国瓦里安Trilogy直线加速器6MV X射线、瓦里安治疗计划系统实施治疗计划设计,由同一个临床医生确定临床靶区和大体肿瘤体积,其中将临床靶区沿三维方向外放5~8 mm 作为计划靶区,对其给定处方剂量60 Gy/30次。试验组行VMAT:使用共面双弧旋转调强技术设计计划,准直器角度为10°~30°,机架旋转角度:顺时针和逆时 针 角 度 分 别 为181°~179°、179°~181°。对 照 组 行IMRT:共设计7 个照射野,机架角度为260°、210°、0°、310°、100°、50°、150°。机架50°和260°射野的准直器为0°,其他为90°。两组剂量率为600 MU/min,治疗床均为0°,使用约束条件实施逆向优化。
1.4 观察指标
(1)比较两组适形指数、不均匀指数和计划靶区平均剂量、最小与最大剂量。(2)比较两组危及器官评估指标:心脏V30、食管V60 和食管V50 及平均剂量、肺V5、肺V10、肺V20、肺V50、脊髓最大剂量等。
1.5 统计学方法
数据采用SPSS 21.0 软件进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用t 检验;计数资料以例数和百分比(%)表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组计划靶区最小剂量、最大剂量、平均剂量和适形指数、不均匀指数比较
两组计划靶区最小剂量、最大剂量、平均剂量和不均匀指数比较,差异无统计学意义(P>0.05);试验组适形指数高于对照组,差异有统计学意义(P<0.05),见表1。
2.2 两组危及器官评估指标比较
两组心脏V30、食管V60 和食管V50 及平均剂量、肺V5、肺V10、肺V20、肺V50、脊髓最大剂量比较,差异无统计学意义(P>0.05),见表2。
表1 两组计划靶区最小剂量、最大剂量、平均剂量和适形指数、不均匀指数比较(±s)

表1 两组计划靶区最小剂量、最大剂量、平均剂量和适形指数、不均匀指数比较(±s)
组别试验组(n=42)对照组(n=42)t P计划靶区最小剂量(cGy)4 527.65±421.65 4 509.44±420.59 0.198 0.843计划靶区最大剂量(cGy)6 540.36±330.65 6 547.65±333.54 0.101 0.920计划靶区平均剂量(cGy)6 088.74±440.75 6 059.32±429.61 0.310 0.758适形指数0.74±0.17 0.61±0.15 3.716 0.004不均匀指数1.11±0.04 1.08±0.11 1.661 0.101
表2 两组危及器官评估指标比较(±s)
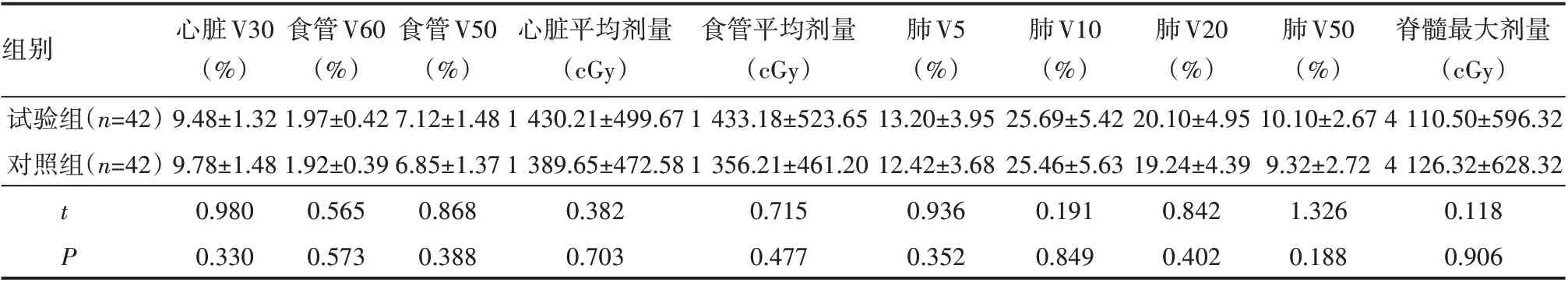
表2 两组危及器官评估指标比较(±s)
组别试验组(n=42)对照组(n=42)t P心脏V30(%)9.48±1.32 9.78±1.48 0.980 0.330食管V60(%)1.97±0.42 1.92±0.39 0.565 0.573食管V50(%)7.12±1.48 6.85±1.37 0.868 0.388心脏平均剂量(cGy)1 430.21±499.67 1 389.65±472.58 0.382 0.703食管平均剂量(cGy)1 433.18±523.65 1 356.21±461.20 0.715 0.477肺V5(%)13.20±3.95 12.42±3.68 0.936 0.352肺V10(%)25.69±5.42 25.46±5.63 0.191 0.849肺V20(%)20.10±4.95 19.24±4.39 0.842 0.402肺V50(%)10.10±2.67 9.32±2.72 1.326 0.188脊髓最大剂量(cGy)4 110.50±596.32 4 126.32±628.32 0.118 0.906
3 讨论
因非小细胞肺癌早期缺乏典型性临床表现,多数患者确诊时已发展为晚期,错失手术治疗最佳时间,预后较差。对于局部晚期非小细胞肺癌患者,放射治疗为常用手段,适当放疗剂量能使肿瘤局部控制率提高,使患者生存期延长,但易出现放射性损伤风险成倍增加,限制放射剂量的选择[3]。常规放疗计划中,不良反应发生率会随着照射野范围增大而增加,患者耐受性较差,导致治疗依从性下降,若行精准放疗,能控制病灶与靶区体积的近似适形,在达到靶区剂量增加的同时,使正常组织受照剂量减少[4]。
IMRT 是一种新型放疗技术,集逆向优化治疗计划设计软件、精密两维和三维剂量验证设备、新型高精尖加速器于一身,经提高肿瘤靶区适形度,使照射剂量增加,并减少正常组织受照剂量和体积,而改善患者病情[5]。但治疗耗时相对较长,可能会降低相对生物效应,并可造成治疗总因体位变化、器官蠕动等改变靶区风险增加,使治疗精度下降。此外,因肺癌靶区形态不规则,并与肺组织相互重叠,会加大IMRT 计划设计难度,影响射野角度的选择。本研究中,试验组适形指数高于对照组;两组计划靶区最小剂量、最大剂量、平均剂量和不均匀指数、心脏V30、食管V60 和食管V50 及平均剂量、肺V5、肺V10、肺V20、肺V50、脊髓最大剂量等比较无明显差异,提示VMAT 与IMRT 治疗效果相当,均可使靶区适形度提升,降低正常器官、组织的受照剂量,提高患者的耐受性,但VMAT 有更好的适应度。VMAT 可经CT 对肿瘤病灶和邻近正常组织、器官进行实时监控,便于医生监测、了解各组织、器官位置在治疗期间的变化,利于医生实施放射线跟踪肿瘤和调整剂量,实现精准放射[6]。VMAT 克服了日常摆位误差、呼吸运动、器官蠕动等因素改变治疗靶区,对放射剂量进行实时调整,可避免正常器官、组织受损,减少放射因素的毒副反应,具有反应速度快、精准、操作便捷、灵活等优点。
综上所述,VMAT 与IMRT 治疗局部晚期非小细胞肺癌均可满足临床治疗需要,其中VMAT 适形指数更好,可优先选择VMAT方案治疗局部晚期非小细胞肺癌。

