蒙特卡罗模拟评价中国成人患者的利奈唑胺给药方案
陈杏凯,张海霞
南京大学医学院附属鼓楼医院药学部,南京210008
近年来耐药的革兰阳性菌感染越来越成为临床需要重视的问题,其与皮肤感染、肺炎和菌血症都有关,引起的感染死亡率高[1]。当前的专家共识推荐利奈唑胺用于耐药革兰阳性菌的治疗[2]。利奈唑胺为第一个恶唑烷酮类的合成抗生素,通过作用于细菌70S 复合物,终止蛋白合成,从而起到抗菌作用[3]。与万古霉素等糖肽类抗生素相比,利奈唑胺[4]临床疗效差异大,传统的临床给药方案大多依赖临床医生经验与药敏结果,往往难以达到预期治疗效果。当前通常采用药物浓度监测方法 (therapeutic drug monitoring,TDM)作剂量调整,但鉴于有研究报道其谷浓度在同样剂量下差异达到10~20 倍[5],即如何进行调整仍是一个难题。
本研究将抗菌药物的药动/药效理论与革兰阳性菌监测结果相结合,拟通过蒙特卡罗模拟优化利奈唑胺给药方案,以期能为临床合理使用利奈唑胺提供参考。
1 材料与方法
1.1 药动学参数
中国成人患者利奈唑胺的药代动力学参数由以中国成人患者为研究对象的公开发表的文献得出:V 为(42.92±24.40)L;CL 为(10.20±4.28)L·h-1;t1/2为(3.27±2.1)h,其中CL 为表观清除率,V 为表观分布容积,t1/2为半衰期[6]。
1.2 药效学模型
利奈唑胺是一种具有持续抗生素后效应的时间依赖性抗生素[7],为保证临床使用利奈唑胺的有效性,根据相关文献报道将利奈唑胺的PK/PD 指数定为AUC0~24h/MIC≥100 或100%f T>MIC[8,9],当两者出现结果不一致时,则优先考虑AUC0~24h/MIC 所得结果。其中AUC0~24h为每日血药浓度曲线下面积,MIC 为最低抑菌浓度,公式为:AUC0~24h=Dose/CL。
Dose 为24 h 给药剂量;f T>MIC 指游离药物浓度高于最低抑菌浓度时间占给药间隔时间的比例,计算公式为:f T>MIC=(ln (Dose×f/V)-ln(MIC))/(CL×τ/V)×100%。
f 为游离药物百分数,利奈唑胺为0.69,τ 为给药间隔。
1.3 革兰阳性菌监测报告MIC
利奈唑胺对各种革兰阳性菌的药敏试验与耐药监测数据来自于2017~2018 年中国细菌耐药监测报告[10]。该研究对来自全国19 家三甲医院共2422 株革兰阳性菌进行MIC 测定,来源包括血标本、分泌物、痰标本、尿标本和引流液等,由中心实验室统一用平皿/肉汤二倍稀释法测定,其MIC 值分布见表1。
1.4 蒙特卡罗模拟
根据“1.2”项下的公式分别计算对于不同给药方案 (600 mg q24h,1200 mg q24h;600 mg q12h,900 mg q12h) 时利奈唑胺对不同MIC 值菌属的药效学目标达标概率(probability of target attainment,PTA);并采用美国Oracle 公司Crystal ball 软件(V11.1.2.4.000)进行蒙特卡罗模拟,其中假设药动学参数符合对数正态分布,MIC 值服从自定义分布,运行计算5000 次,置信区间为95%,计算对MIC 群体达到某一目标累计反应分数(Cumulative fraction of response,CFR),其公式为:
其中PTAi 为不同MIC 值所对应的PTA,Fi 为不同MIC 值的分布相对概率,其表示各MIC 水平下细菌数百分率与相应达标概率值乘积之和。
PTA 和CFR 均是概率的百分数,通过比较它们的大小来评价抗生素给药方案,通常以≥90%评价方案是否合理[11]。当知道患者所染菌MIC 值时采用PTA作为评价指标,不知时采用CFR 作为评价指标。
2 结果
2.1 不同利奈唑胺给药方案的PTA 值
中国成人患者采用不同利奈唑胺给药方案后药效学指标AUC0~24h/MIC≥100 和100%f T>MIC 的计算结果分别见图1 和图2。
利奈唑胺的所有给药方案随MIC 值的增大,其PTA 均下降。对于药效学指标AUC0~24h/MIC≥100,当MIC≤0.5 mg·L-1时,当前所有给药方案都能达到PTA≥90%,当MIC 为1 mg·L-1时,只有600 mg q24h 不能够达到目标,当MIC 为2 mg·L-1时,只有900 mg q12h 能够达到目标,当MIC≥4 mg·L-1时,当前所有给药方案都不能达到目标。对于药效学指标100%f T>MIC,当MIC≤2 mg·L-1时,当前所有给药方案只有600 mg q12h 和900 mg q12h 能达到PTA≥90%,当MIC≥4 mg·L-1时,当前所有给药方案都不能达到目标。
2.2 不同利奈唑胺给药方案后计算不同革兰阳性菌的CFR 值
不同利奈唑胺给药方案后,根据药效学指标AUC0~24h/MIC≥100 和100%f T>MIC,计算金黄色葡萄球菌、表皮葡萄球菌、粪肠球菌、屎肠球菌和肺炎链球菌的CFR 值,见表2 和表3。
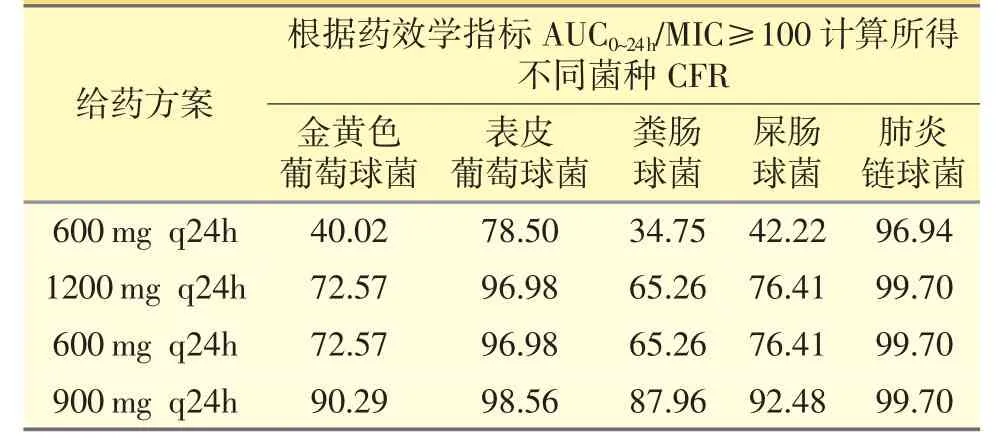
表2 不同利奈唑胺给药方案后根据药效学指标AUC0~24h/MIC≥100 计算所得不同菌种CFR
针对金黄色葡萄球菌,对于药效学指标AUC0~24h/MIC≥100 和100%fT>MIC,都只有900mg q12h 能够达标;针对表皮葡萄球菌,对于药效学指标AUC0~24h/MIC ≥100,1200 mg q24h、600 mg q12h 和900 mg q12h 能够达标,而对于药效学指标100%f T>MIC,600 mg q12h 和900 mg q12h 能够达标;针对粪肠球菌,只有对于药效学指标100%f T>MIC 时900 mg q12h 能够达标;对于屎肠球菌,无论是药效学指标AUC0~24h/MIC≥100 还是100%fT>MIC,都只有900 mg q12h 能够达标;针对肺炎链球菌,对于药效学指标AUC0~24h/MIC≥100,所有方案都能够达标,而对于药效学指标100%f T >MIC,600 mg q12h 和900 mg q12h 能够达标。

表3 不同利奈唑胺给药方案后根据药效学指标100%f T>MIC 计算所得不同菌种CFR
3 讨论
抗菌药物作为我国临床使用最广泛的一类药物,其使用量约占所有临床用药的30%~50%。当前对于如何合理使用抗菌药物,国家相关部门已经实施了数年的专项整治活动,进行细菌耐药监测是其中的一个重点环节。根据2017~2018 年中国细菌耐药监测报告显示,我国甲氧西林耐药金黄色葡萄球菌和甲氧西林耐药表皮葡萄球菌检出率分别为33.2%和85.7%[11],说明临床耐药的革兰阳性菌形势依然严峻,其给于临床抗感染治疗带来了极大的挑战。本研究使用蒙特卡罗模拟技术并结合细菌耐药监测报告的相关数据,探讨了不同利奈唑胺给药方案下临床不同MIC 值革兰阳性菌的临床达标率,为中国成人患者的利奈唑胺合理使用提供一些参考依据。
根据2017~2018 年中国细菌耐药监测报告数据,肺炎链球菌和表皮葡萄球菌对利奈唑胺MIC50、MIC90分别为0.5、0.5 mg·L-1和0.5、1 mg·L-1。根据本研究结果显示,临床目前最常用治疗方案600 mg q12h 和900 mg q12h 对于不同药效学指标其PTA和CFR 值均能够达到90%以上、且结果差异小,表明对于肺炎链球菌和表皮葡萄球菌引起的感染患者,利奈唑胺600 mg q12h 的给药方案仍然选用。针对金黄色葡萄球菌、粪肠球菌和屎肠球菌,其对利奈唑胺MIC50、MIC90都为2 mg·L-1,其与欧洲药敏试验委员会(EUCAST)[12]研究中关于利奈唑胺的PK/PD 转折点为2 mg·L-1相一致。不管是对于药效学指标AUC0~24h/MIC≥100,还是100%f T>MIC,都只有900 mg q12h 方案的PTA 和CFR 值基本能够达到90%以上。表明当前利奈唑胺600 mg q12h 的给药方案仍然可以使用;但有一些可能需要结合MIC 值进行调整、优化治疗。
本研究的蒙特卡洛模拟结果显示,给药剂量对PTA 的影响大于给药间隔的影响。因此,对于利奈唑胺的给药方案而言,如果临床抗菌疗效欠佳(例如PTA 较小),应优先考虑调整药物剂量,如由600mg q12h 提高为900 mg q12h,其次才考虑缩短给药间隔或延长静脉滴注的时间,这与之前Cai Y 等[6]所做的研究一致。
蒙特卡罗模拟是一种采用不同统计取样方法来提供定量问题近似解决方案的随机模拟方法[13],其能够通过计算机软件部分替代实际的实验,从而节约了大量的时间与金钱成本。该方法在抗菌药物的药动学和药效学中的应用越来越广泛,如王小庆等[14]和李永兵等[15]分别使用该方法对美罗培南在CRKP 感染者和硫酸依替米星在大肠埃希菌感染患者中的给药方案进行了优化研究。本研究也采取了这一方法,根据药物在人体内的PK 参数与MIC值,以各种PK/PD 参数为目标值,模拟出“临床患者”的达标概率,给出临床建议。当然该方法只是软件模拟结果,还需要得到临床实践的检验。
综上所述,本研究基于蒙特卡罗模拟方法与PK/PD 理论,对利奈唑胺在中国成人患者中的不同给药方案进行了评价,当前的临床给药方案基本能够达到临床疗效。当然本研究仅是基于单一药物的蒙特卡罗模拟,临床使用时还需要充分考虑患者具体生理、病理、合并用药等情况,这样才能够得到比较满意的个体化给药方案。

