基于UPLC-QTOF-MS/MS 法的茅苍术与北苍术化学成分分析*
周 洁,汤维维,陈 君
中国药科大学中药学院生药学系,南京210009
苍术为菊科苍术属植物茅苍术Atractylodes lancea(Thunb.) DC.或北苍术Atractylodes chinensis(DC.) Koidz.的干燥根茎,为2020 版《中国药典》所收录,可燥湿健脾、祛风散寒、明目,用于脘腹胀满、泄泻、水肿、风湿痹痛、风寒感冒、眼目昏涩等症[1]。现代药理实验研究表明,苍术具有多种生物学活性,如调整胃肠道运动、降血糖、抗溃疡及抗菌消炎等[2-4]。苍术中含有多种结构类型的化学成分,包括萜类、聚乙烯炔类、三萜及甾体类、芳香族及糖苷类等[5,6]。目前,国内外对苍术中倍半萜及烯炔类等挥发性成分的研究较为深入,而对苍术中非挥发性成分的研究相对较少报道[7,8]。为明晰苍术药材的固有化学成分,有必要对其含有的非挥发性成分进行深入研究,以建立较为完善的苍术质量评价体系。
本实验采用UPLC-QTOF-MS/MS 方法对茅苍术与北苍术75%甲醇提取物中的化学成分进行快速分析,通过高分辨质谱获得各成分的液相色谱保留时间、精确分子质量和特征碎片离子信息,并结合对照品及相关文献数据比对进行成分鉴定[9-13],可为苍术的物质基础研究和质量控制提供实验依据。
1 仪器与药品、试剂
Agilent 1290 UPLC-6530 QTOF-MS/MS(美国Agilent 公司);BT-25S 型电子分析天平(0.01 mg,德国Satarious 公司);Milli-Q 超纯水系统(美国Millipore 公司)。
对照品:绿原酸(批号:MUST-17030620)、新绿原酸 (批号:MUST-17011001)、隐绿原酸 (批号:MUST-17022403)、白术内酯Ⅰ (批号:MUST-17030201)、白术内酯Ⅱ(批号:MUST-17030202)、白术内酯Ⅲ(批号:MUST-17030203)均购自成都曼思特生物科技有限公司(纯度均>98%)。本实验所用茅苍术药材(Atractylodes lancea (Thunb.) DC.)产地湖北,北苍术药材(Atractylodes chinensis (DC.)Koidz.)产地内蒙古,均购自安徽亳州药材市场,经中国药科大学生药学系刘惠娟实验师鉴定确认。
甲醇、乙腈(色谱纯,德国Merck 公司);甲酸(色谱纯,美国ROE 公司);去离子水 (18 MΩ)由Milli-Q 超纯水系统(美国Millipore 公司)制备。
2 实验方法
2.1 对照品溶液的制备
分别称取适量的绿原酸、新绿原酸、隐绿原酸、白术内酯Ⅰ、白术内酯Ⅱ、白术内酯Ⅲ对照品,置于2 mL 量瓶中,加入适量甲醇溶解、定容至刻度,混匀,即得对照品储备液。
2.2 供试品溶液的制备
精密称取苍术干燥粉末(过3 号筛)2.0 g,置于100 mL 具塞锥形瓶中,加入75%甲醇40 mL,加塞密封后称重,超声提取40min(功率250W、频率40kHz),冷却至室温,摇匀静置后再称重,用75%甲醇补足失重,离心10 min(4 ℃,13 000 r·min-1)后,取上清液,0.22 μm 微孔滤膜过滤,即得供试品溶液。
2.3 色谱条件
采用Agilent Infinity Lab Poroshell 120EC-C18(2.1 mm×100 mm,2.7 μm) 色谱柱分离;流动相为0.1%甲酸溶液(A)-乙腈(B),采用梯度洗脱,洗脱程序为0~2 min,10%B;2~6 min,10%~14%B;6~9 min,14%~25%B;9~12 min,25%~60%B;12~20 min,60%~72%B;20~22 min,72%~90% B;22~24 min,90%~100%B;24~26 min,100%B。流速:0.3 mL·min-1;柱温:25 ℃;进样体积:1 μL。
2.4 质谱条件
采用电喷雾离子源(ESI),在正、负离子模式下分别采集数据,质量扫描范围:50~1500 m/z。ESI 离子源参数: 干燥气温度:350 ℃;干燥气流速:10 L·min-1;鞘气温度:350 ℃;鞘气流速:10 L·min-1;雾化气压力:241.3 kPa;毛细管电压:正离子模式4000 V、负离子模式3500 V;裂解电压:120 V;碰撞能量:5、10、20、40 eV。
在进样分析前,利用调谐液对QTOF-MS/MS 的质量轴进行校正,数据采集过程中采用参比离子进行实时校准。在正离子模式下选择m/z 121.050 8 与m/z 922.009 8 离子作为实时校正质量数;负离子模式下选择m/z 112.988 5 与m/z 1 033.988 1 离子作为实时校正质量数。质谱检测时与理论相对分子质量数误差应小于±5 ppm。
3 结果
3.1 UPLC-QTOF-MS/MS 分析
运用建立的UPLC-QTOF-MS/MS 方法对茅苍术与北苍术75%甲醇提取物进行分析。图1~2 分别为茅苍术与北苍术提取物在正、负离子模式下的总离子流图(TIC)。
采用对照品比对化合物极性大小、质谱裂解规律及特征碎片离子分析,以及比对相关化合物结构鉴定文献及数据库查阅等方法,对质谱数据进行解析。此外,质谱检测时分别设定5、10、20、40 V 四个二级电压,通过比较不同电压时的离子丰度,快速寻找化合物的特征碎片离子。所鉴定化合物的保留时间(tR)、相对分子质量、分子式、质量偏差(ppm)以及特征碎片等信息见表1、表2。
从茅苍术与北苍术中均鉴定出78 个化学成分,包括16 个萜类化合物、10 个聚乙烯炔类化合物、25 个有机酸类化合物、17 个糖苷类化合物和10个其它类化合物。
3.2 化合物鉴定
3.2.1 单萜及倍半萜类 在ESI+模式下,单萜类化合物如峰12 得到m/z 179[M+H]+,其二级质谱得到m/z 161[M+H-H2O]+,m/z 151[M+H-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为(4R,S)-4-isopropyl-trans-bicyclo[4.3.0]-2-nonen-8-one。桉叶烷型结构的倍半萜类化合物较多,一般以母核脱H2O,CO 为主,产生m/z 175 的特征碎片离子,通过对各峰的分子离子峰及二级质谱分析,可见峰7、8、10、13、20、22、23、24、25、28、32 均有脱去H2O 及CO等基团后的特征碎片离子,以峰25 为例,在ESI+模式下得到m/z 231[M+H]+,其二级质谱得到m/z 213[M+H-H2O]+,m/z 203[M+H-CO]+,结合精确相对分子质量及与对照品对比,鉴定其为白术内酯Ⅰ。采用类似的方法,通过比较得到的母离子和二级质谱信息,推测峰7 为eudesm-4(15),7-diene-9α,11-diol,峰8 为eudesm-4(15),7-diene-11-ol-9-one,峰10 为白术内酯Ⅲ,峰13 为白术内酰胺,峰20 为3β-羟基苍术酮,峰22 为白术内酯Ⅱ,峰23 为8βethoxyasterolid,峰24 为8β-甲氧基白术内酯Ⅰ,峰28 为芹子二烯酮,峰32 为苍术酮。此外,峰27 得到m/z 259[M+H]+,其二级质谱得到m/z 231[M+H-CO]+,结合精确相对分子质量及与文献[11]对比,鉴定其为7-methoxy-2-methyl-2-(4-methylpent-3-enyl)-2Hchromene。峰29 得到m/z 215[M+H]+,其二级质谱得到m/z 197[M+H-H2O]+,m/z 187[M+H-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为呋喃二烯酮。峰34 得到m/z 259[M+H]+,其二级质谱得到m/z 241[M+H-H2O]+,结合精确相对分子质量及与文献[11]对比,鉴定其为2-(3,7-dimethylocta-2,6-dien-1-yl)-6-methylcyclohexa-2,5-diene-1,4-dione。在ESI-模式下,峰33 得到m/z 231[M-H]-,其二级质谱得到m/z 187[M-H-CO2]-,结合精确相对分子质量及与文献[10,12]对比,鉴定其为木香烃内酯。
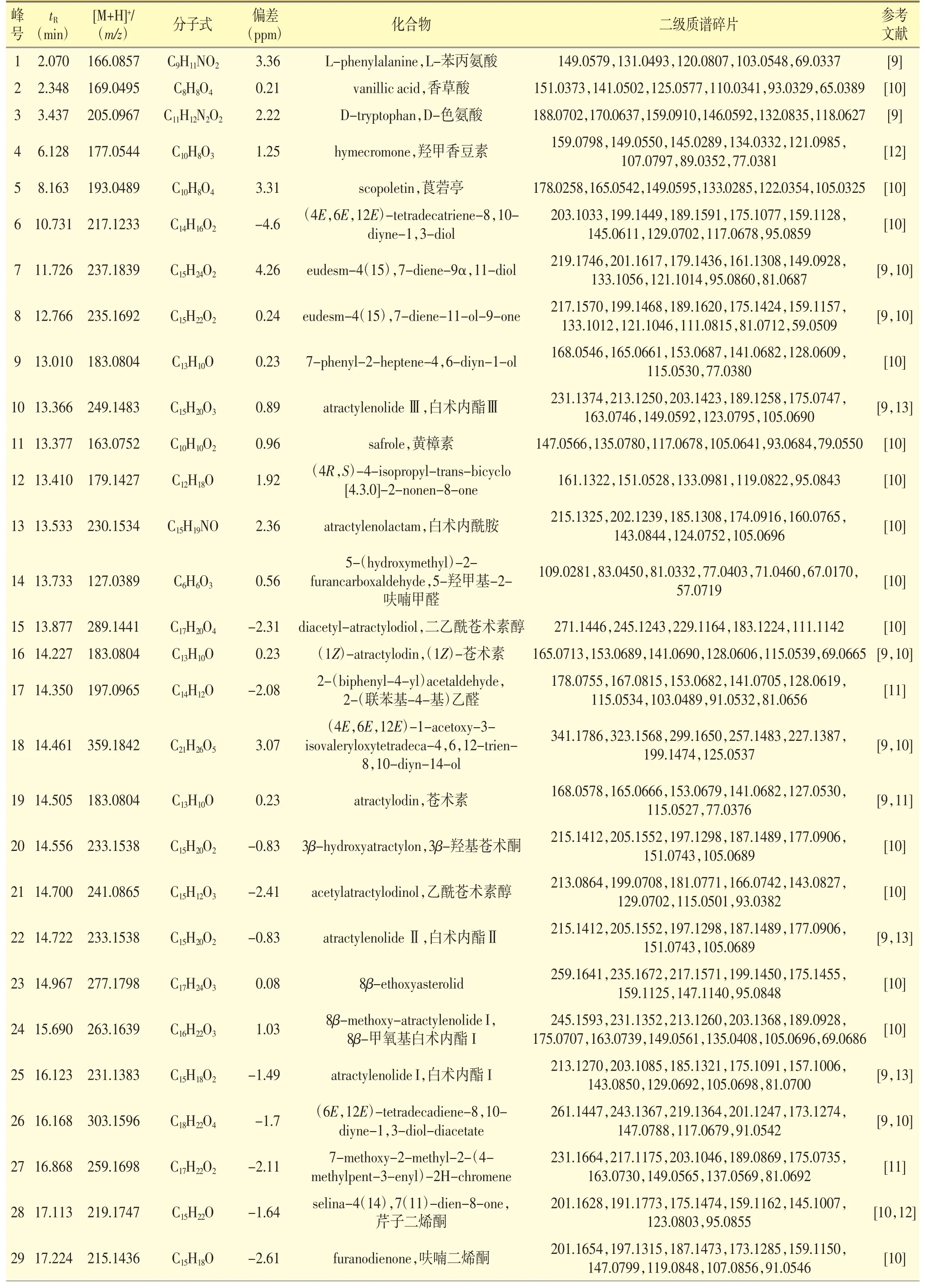
表1 苍术提取物的UPLC-QTOF-MS/MS 定性分析结果(正离子模式)
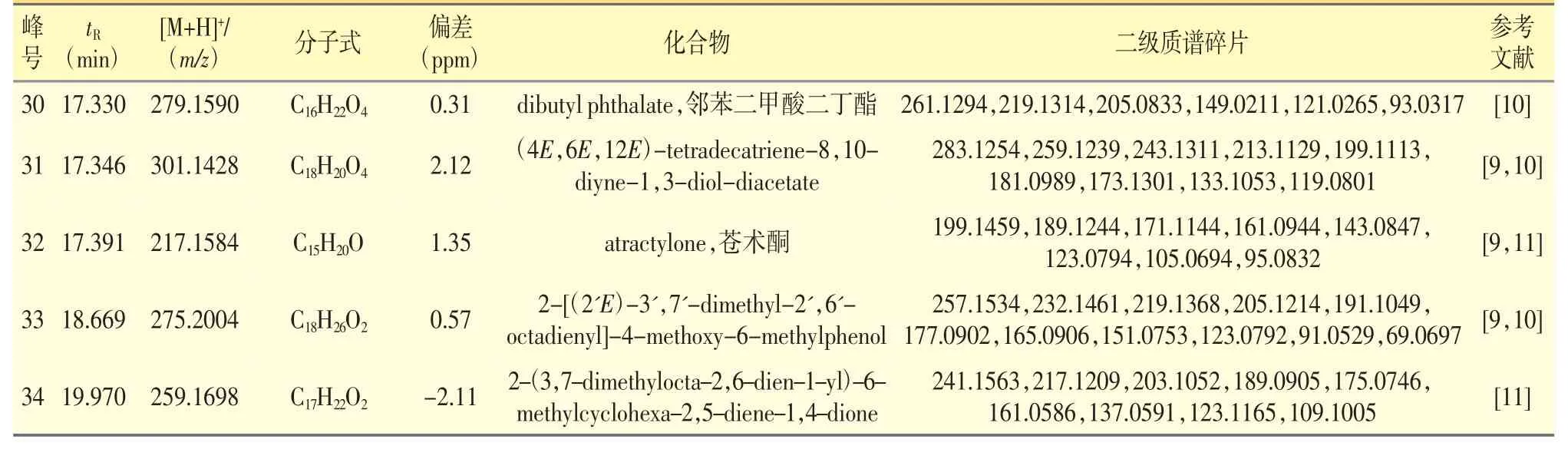
续表1 苍术提取物的UPLC-QTOF-MS/MS 定性分析结果(正离子模式)
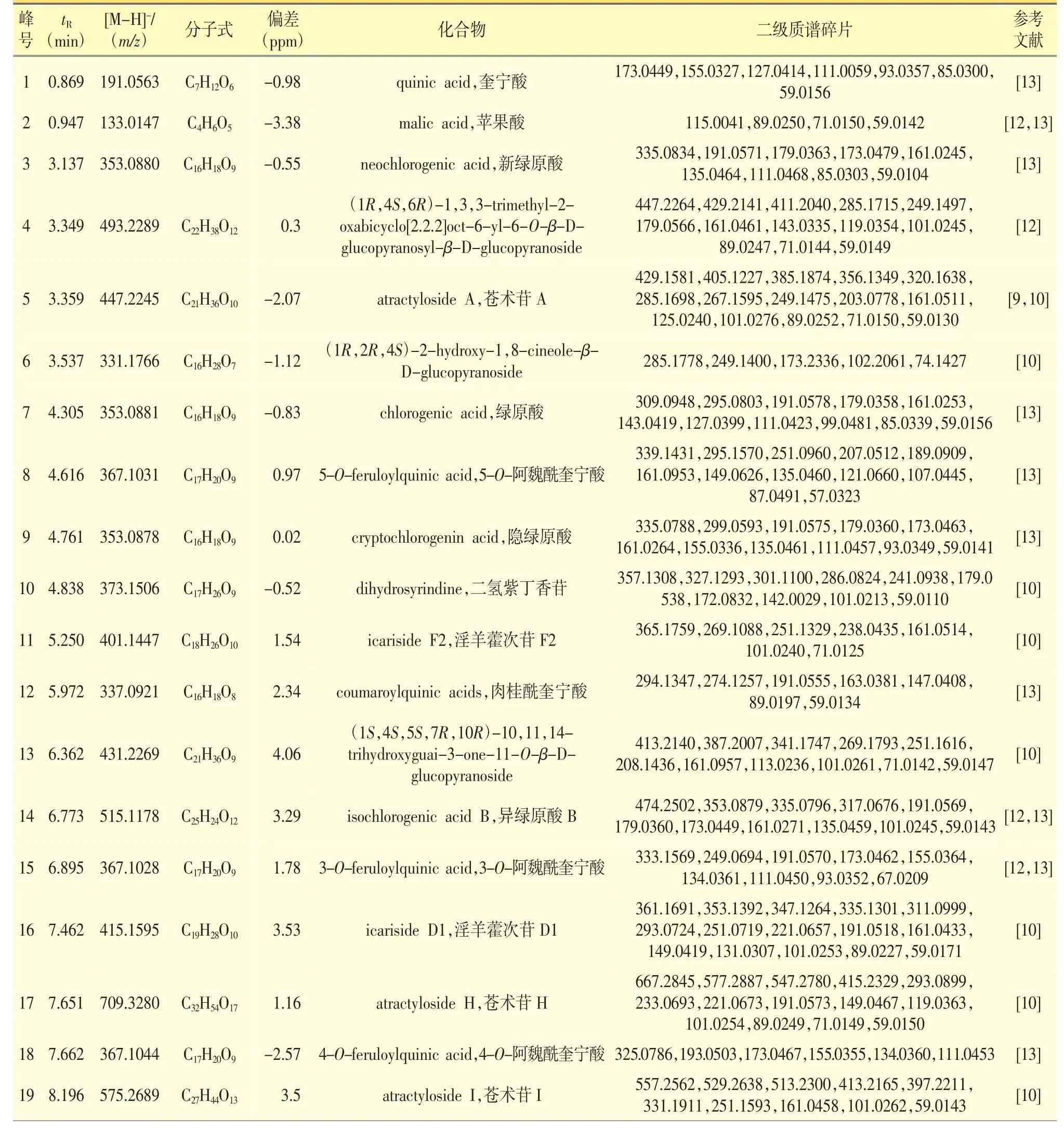
表2 苍术提取物的UPLC-QTOF-MS/MS 定性分析结果(负离子模式)

续表2 苍术提取物的UPLC-QTOF-MS/MS 定性分析结果(负离子模式)
3.2.2 聚乙烯炔类 在ESI+模式下,峰6 得到m/z 217[M+H]+,其二级质谱得到m/z 203[M+H-CH2]+,m/z 199[M+H-H2O]+,结合精确相对分子质量及与文献[10]对比,鉴定其为(4E,6E,12E)-tetradecatriene-8,10-diyne-1,3-dio。峰9、16、19 得到m/z 183[M+H]+,三者为同分异构体,其二级质谱得到m/z 165[M+H-H2O]+,结合精确相对分子质量及与文献[9,10]对比,推测分别为7-phenyl-2-heptene-4,6-diyn-1-ol、(1Z)-苍术素和苍术素。峰15 得到m/z 289[M+H]+,其二级质谱得到m/z 271[M+H-H2O]+,结合精确相对分子质量及与文献[10]对比,鉴定其为二乙酰苍术素醇。峰18 得到m/z 359[M+H]+,其二级质谱得到m/z 341[M+H-H2O]+,m/z 323[M+H-2H2O]+,结合精确相对分子质量及与文献[9,10]对比,鉴定其为(4E,6E,12E) -1 -acetoxy -3 -isovaleryloxytetradeca -4,6,12-trien-8,10-diyn-14-ol。峰21 得到m/z 241[M+H]+,其二级质谱得到m/z 213[M+H-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为乙酰苍术素醇。峰26 得到m/z 303[M+H]+,其二级质谱得到m/z 261[M+H-C3H6]+,结合精确相对分子质量及与文献[9,10]对比,鉴定其为(6E,12E)-tetradecadiene-8,10-diyne-1,3-diol-diacetate。峰31 得到m/z 301[M+H]+,其二级质谱得到m/z 283[M+H-H2O]+,m/z 259[M+H-C3H6]+,结合精确相对分子质量及与文献[9,10]对比,鉴定其为(4E,6E,12E)-tetradecatriene-8,10-diyne-1,3-diol-diacetate。峰33 得到m/z 275 [M+H]+,其二级质谱得到m/z 257 [M+HH2O]+,结合精确相对分子质量及与文献[9,10]对比,鉴定其为2-[(2'E)-3',7'-dimethyl-2',6'-octadienyl]-4-methoxy-6-methylphenol。
3.2.3 有机酸类 在ESI+模式下,峰6 得到m/z 169[M+H]+,其二级质谱得到m/z 151[M+H-H2O]+,m/z 141[M+H-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为香草酸。在ESI-模式下,峰1 得到m/z 191[M-H]-,其二级质谱得到m/z 173[M-HH2O]-,m/z 155[M-H-2H2O]-,结合精确相对分子质量及与文献[13]对比,鉴定其为奎宁酸。峰2 得到m/z 133[M-H]-,其二级质谱得到m/z 115[M-H-H2O]-,结合精确相对分子质量及与文献[12,13]对比,鉴定其为苹果酸。峰12 得到m/z 337[M-H]-,其二级质谱得到m/z 191 奎宁酸特征性碎片离子,结合精确相对分子质量及与文献[13]对比,鉴定其为肉桂酰奎宁酸。峰22得到m/z 193[M-H]-,其二级质谱得到m/z 149[MH-CO2]-,结合精确相对分子质量及与文献[12,13]对比,鉴定其为阿魏酸。峰27 得到m/z 187[M-H]-,其二级质谱得到m/z 169[M-H-H2O]-,结合精确相对分子质量及与文献[12,13]对比,鉴定其为壬二酸。峰31得到m/z 329[M-H]-,其二级质谱得到m/z 311[MH-H2O]-,m/z 293[M-H-2H2O]-,结合精确相对分子质量及与文献[12,13]对比,鉴定其为三棱酸。峰32 得到m/z 263[M-H]-,其二级质谱得到m/z 235[M-HCO]-,结合精确相对分子质量及与文献[10]对比,鉴定其为naphthol。峰38 得到m/z 455[M-H]-,结合精确相对分子质量及与文献[10]对比,推测为齐墩果酸。峰39 得到m/z 227[M-H]-,结合精确相对分子质量及与文献[10]对比,推测为肉豆蔻酸。峰3、7、9 在ESI-模式下得到m/z 353[M-H]-,三者为同分异构体,均为单咖啡酰奎宁酸类化合物,并且具有m/z 191、179和135 的特征性碎片离子,通过参考相关文献及与对照品比对,新绿原酸、绿原酸、隐绿原酸的极性依次降低,鉴定化合物3、7、9 分别为新绿原酸、绿原酸、隐绿原酸。峰8、15、18 在ESI-模式下分子离子峰均为367,具有m/z 191、179、135 的特征性碎片离子,该化合物可能为阿魏酰奎宁酸类,参考其在反相色谱柱的洗脱规律,进而判断上述化合物分别为5-O-阿魏酰奎宁酸、3-O-阿魏酰奎宁酸、4-O-阿魏酰奎宁酸。峰14、26、28 在ESI-模式下分子离子峰均为515,均会失去两分子咖啡酰基、生成m/z 353 的碎片离子峰,继续裂解产生m/z 191、179 的特征碎片离子,推断化合物14、26 和28 分别为异绿原酸B、异绿原酸A 和异绿原酸C。峰36 得到m/z 295[M-H]-,其二级质谱得到m/z 277[M-H-H2O]-,m/z 259[M-H-2H2O]-,结合精确相对分子质量及与文献[11]对比,鉴定其为9,10-环氧-12(Z)-十八碳烯酸。峰37 得到m/z 293[M-H]-,其二级质谱得到m/z 275[M-H-H2O]-,结合精确相对分子质量及与文献[11]对比,鉴定其为(9Z,11E,15Z)-13-羟基-9,11,15-十八碳三烯酸。峰41、42、43、44 的二级质谱中产生一系列m/z 相差14 的碎片离子峰,推测其可能为链状结构,结合精确相对分子质量及与文献[10,11]对比,推测其分别为十八碳-9,12-二烯酸、十六碳烯酸、棕榈酸和十八碳-9-烯酸。
3.2.4 糖苷类 在ESI-模式下,峰6 得到m/z 331[M-H]-,其二级质谱得到m/z 285[M-H-CH2O2]-,结合精确相对分子质量及与文献[10]对比,鉴定其为(1R,2R,4S)-2-hydroxy-1,8-cineole-β-D-glucopyranoside。峰20 得到m/z 371[M-H]-,其二级质谱得到m/z 335[M-H-2H2O]-,结合精确相对分子质量及与文献[9,10]对比,鉴定其为紫丁香苷。峰40 得到m/z 397[M-H]-,其二级质谱得到m/z 379[M-H-H2O]-,结合精确相对分子质量及与文献[10]对比,鉴定其为(5R,7R,10S) -isopterocarpolone -β -D -glucopyranoside。峰4、5、13、19、23、24、25、29、30 均有脱去葡糖基 (Glc)m/z 162 后的特征碎片离子,以峰5 为例,在ESI-模式下得到m/z 447[M-H]-,其二级质谱得到m/z 285[M-H-C6H10O5]-,结合精确相对分子质量及与文献[10]对比,鉴定其为苍术苷A。采用类似的方法,通过比较得到的母离子和二级质谱信息,推测峰4 为(1R,4S,6R)-1,3,3-trimethyl-2-oxabicyclo [2.2.2]oct-6-yl-6-O-β-D-glucopyranosyl-β-Dglucopyranoside,峰13 为 (1S,4S,5S,7R,10R)-10,11,14-trihydroxyguai-3-one-11-O-β-D-glucopyranoside,峰19 为苍术苷I,峰23 为苍术苷F,峰24 为苍术苷E,峰25 为 (1S,5R,7R,10R)-secoatractylolactone-11-O-β-D-glucopyranoside,峰29 为苍术苷G 2-O-β-D-glucopyranoside,峰30 为苍术苷G。峰10、11、16、17、21 均有脱去芹糖基(Api)m/z 132 或芹糖基-(1→6)葡糖基(Api1—6Glc)后的特征碎片离子,以峰17 为例,在ESI-模式下得到m/z 709[M-H]-,其二级质谱得到m/z 577[M-H-C5H8O4]-,m/z 415[M-H-C5H8O4-C6H10O5]-,结合精确相对分子质量及与文献[10]对比,鉴定其为苍术苷H。采用类似的方法,通过比较得到的母离子和二级质谱信息,推测峰10 为二氢紫丁香苷,推测峰11 为淫羊藿次苷F2,推测峰16 为淫羊藿次苷D1,推测峰21 为(2E)-decene-4,6-diyne-1,8-diol-8-O-β-D-apiofuranosyl-(1→6)-β-D-glucopyranoside。
3.2.5 其它类 在ESI+模式下,峰1 得到m/z 166[M+H]+,峰3 得到m/z 205[M+H]+,结合精确相对分子质量及与文献[9]对比,鉴定其分别为L-苯丙氨酸、D-色氨酸。峰4 得到m/z 177[M+H]+,其二级质谱得到m/z 159[M+H-H2O]+,m/z 149[M+H-CO]+,结合精确相对分子质量及与文献[12]对比,鉴定其为羟甲香豆素。峰5 得到m/z 193[M+H]+,其二级质谱得到m/z 165[M+H-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为莨菪亭。峰11 得到m/z 163[M+H]+,其二级质谱得到m/z 135[M+H-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为黄樟素。峰14得到m/z 127[M+H]+,其二级质谱得到m/z 109[M+H-H2O]+,m/z 81[M+H-H2O-CO]+,结合精确相对分子质量及与文献[10]对比,鉴定其为5-羟甲基-2-呋喃甲醛。峰17 得到m/z 197[M+H]+,其二级质谱得到m/z 167[M+H-CH2O]+,结合精确相对分子质量及与文献[11]对比,鉴定其为2-(联苯基-4-基)乙醛。峰30 得到m/z 279 [M+H]+,其二级质谱得到m/z 261[M+H-H2O]+,结合精确相对分子质量及与文献[10]对比,鉴定其为邻苯二甲酸二丁酯。
在ESI-模式下,峰34 得到m/z 723[M-H]-,其二级质谱得到m/z 677[M-H-CH2O2]-,结合精确相对分子质量及与文献[12]对比,鉴定其为(8Z,8'Z)-1,1',6,6' -tetrahydroxy -5,5' -diisopropyl -3,3' -dimethyl-8,8'-bis{[(1-phenylethyl)amino]methylene}-2,2'-binaphthalene-7,7'(8H,8'H)-dione。峰35 得到m/z 677[M-H]-,其二级质谱得到m/z 593[M-HC5H8O]-,结合精确相对分子质量及与文献[12]对比,鉴定其为galnon。
4 讨论
本实验对苍术药材的提取条件进行了优化,最终采用75%甲醇作为提取溶剂、超声提取40 min 的方法,该方法具有提取时间短、提取效率高的特点。为了获取更丰富的离子信息,更加全面地推测化合物的结构,本实验同时选用了正、负离子两种质谱扫描模式。另外,通过考察不同流动相体系,最终选用了能有效改善峰形和离子化效果的0.1%甲酸溶液作为水相。
苍术中化学成分较为复杂,各类成分的极性相差较大,通过优化洗脱条件,使尽可能多的成分在色谱柱上实现较好分离。
本研究采用UPLC-QTOF-MS/MS 联用技术对两种苍术基原药材的化学成分进行了快速定性分析,结合各成分在正、负离子模式下的精确分子质量、碎片离子以及保留时间等信息,并通过对照品以及现有文献和相关数据库比对分析,从茅苍术与北苍术75%甲醇提取物中共鉴定出78 个化学成分,其中包括16 个萜类化合物、10 个聚乙烯炔类化合物、25 个有机酸类化合物、17 个糖苷类化合物、10 个其它类化合物。
茅苍术与北苍术中均鉴定得到78 个共有化学成分,各成分相对含量上存在差异,但未鉴定得到非共有成分,可能系两者基原存在种属差异,但在化学成分上并没有本质的差异[10],后续可结合植物代谢组学方法进行差异成分的探讨。

