肝内胆管癌微血管侵犯术前影像学诊断
周萌,周洋,张纯慧,郑桐森
肝内胆管癌(intrahepatic cholangiocarcinoma,ICC)是继原发性肝癌后第二大肝脏恶性肿瘤[1,2]。发病隐匿,恶性程度高,患者就诊时多已达中晚期无法行根治性手术治疗,加之临床上缺乏有效肿瘤筛查及诊断性肿瘤标志物,故导致ICC患者诊疗较困难,预后极差,5年生存率低于10%[3]。
据肿瘤形态学特征,ICC又分为团块型(IMCC)、管周浸润型、管内生长型。IMCC占比大约是60%,是最常见肝内胆管癌[4]。本研究主要研究团块型肝内胆管癌(IMCC)。早期研究发现血管侵犯与肿瘤患者不良预后和总生存期有关[5]。血管侵犯根据侵犯血管大小和分布可分为大血管侵犯和微血管侵犯(microvascular invasion,MVI)。术前可通过影像学检测大血管侵犯,但是MVI只能通过术后病理检测。文献报道原发性肝癌术前增强磁共振某些影像特征可预测微血管侵犯[6]。本研究旨在分析术前肝内胆管癌MVI核磁征象从而进一步指导临床医生对外科手术治疗方案或术后治疗方案选择。

图1 研究选择标准和排除标准
材料与方法
1.临床资料
搜集2014年12月-2019年6月行外科手术92例肝内胆管癌患者。纳入标准(图1):①病理证实肝内胆管癌且病理报告信息全面;②术前未行任何抗肿瘤治疗如化疗、放疗、化疗栓塞术等;③术前患者病例资料完整;④术前1个月内行Gd-EOB-DTPA-MR检查且影像图片可进一步分析;⑤术前无其他部位转移;⑥团块型肝内胆管癌且仅有1个病灶;⑦手术切缘阴性,肿瘤为外科手术完全切除;⑧肿瘤大小≥10 mm。最终搜集7例符合标准ICC患者,8例病理证实存在微血管侵犯。其中,47例患者男31例,女16例,年龄43~77(58.7±8.1)岁。MVI阳性组男4例、女4例,年龄54~77(62.0±9.8)岁;甲胎蛋白(AFP)>25 μg/L 2例,Ca19-9>40 μg/L 4例,CEA>5 μg/L 2例; 5例患者有吸烟史;3例患者有饮酒史;4例患者有乙肝病史,2例患者有肝硬化病史。 MVI阴性男27例、女12例,年龄44~74(58.0±7.7)岁;甲胎蛋白(AFP)>25 μg/L 7例,Ca19-9>40 μg/L 17例,CEA>5 μg/L 7例;23例患者有吸烟史,11例患者有饮酒史;16例患者有乙肝病史,13例患者有肝硬化病史;并分别分析搜集两组患者生化指标,分析患者肝脏功能和病理特征,MVI阳性组3例存在大血管侵犯;4例病灶周围有卫星结节。MVI阴性组5例存在大血管侵犯;5例病灶周围有卫星结节。两组患者临床和病理特征如表1。
2.方法
统计学方法:采用SPSS软件(v.22.0;SPSS,Chicago,IL)处理数据,用Fisher检验来分析分类变量,如性别、肝脏背景、吸烟饮酒史、大血管侵犯、微卫星结节及影像特征等。用U检验来分析连续性变量如年龄、脏生化指标、瘤标志物大小等,P<0.05有统计学意义;Logistic方法用来分析这些指标与MVI发生关系,单因素与多变量Logistic分析,计算比值比(Odds ratios ORs)和95%的置信区间(confidence intervals CIs),P<0.05具有统计学意义。
影像学方法:患者影像图均由3.0T-全身-MR 影像系统(Philips Full Digital Magnetic Resonance Ingenia 3.0T MRI)扫描获得,系统配备正交数字化体线圈和增强三维(3D)涡轮场回波序列扫描系统。从肝脏顶部到下边缘扫描,厚度设定为4 mm。所有增强MRI影像图像由PACS系统(Pathspeed,GE Medical Systems Integrated Imaging Solutions,Mt.Prospect,IL,USA)行图像处理及分析,该系统可在每种情况下适当调整最佳窗口设置,具有高诊断准确性以及发现病变能力从而提高诊断准确性。最后,由2位影像科专家(具有10年以上肝脏核磁阅片经验且对这些患者临床和病理信息不知情)分别对47例患者影像图进行分析。
病理学方法:病理切片由2名病理科医师(均有10年工作经验)独立分析,诊断依据《中国原发性肝癌诊疗规范(2017版)》对微血管侵犯病理诊断标准。
结 果
1.单因素分析MVI阳性和MVI阴性患者临床病理特征
本研究最终确诊MVI阳性8例,阴性39例,MVI阳性率17.0%。MVI阳性组肿瘤周围卫星结节发生与MVI阴性组比较存在差异(P<0.05),连续性变量年龄(F=1.195,P=0.337)无统计学意义。其余特征比较无显著差异(P>0.05,表2)。
2.单因素分析MVI阳性和MVI阴性患者影像特征

表1 该项研究临床和病理特征
单因素Logistic分析结果显示肿瘤周围淋巴结肿大与肝内胆管癌患者MVI发生有关系(P<0.05),连续性变量肿瘤大小(F=0.593,P=0.881)无统计学意义。其余特征均显示无关(P>0.05,表3,图2、3)。
讨 论
肝内胆管癌(intrahepatic cholangiocarcinoma,ICC)是肝内胆道系统最常见恶性肿瘤,是肝脏第二大恶性肿瘤[7]。大部分ICC患者早期临床表现不明显,ICC缺乏特异性肿瘤标记物,临床上消化道肿瘤标志物如CA19-9、CEA虽然有助于增加ICC诊断效益,但其在胰腺癌、结直肠癌等其他消化道肿瘤往往也升高,使得早期筛查ICC变得困难。

表2 患者临床和病理特征比较
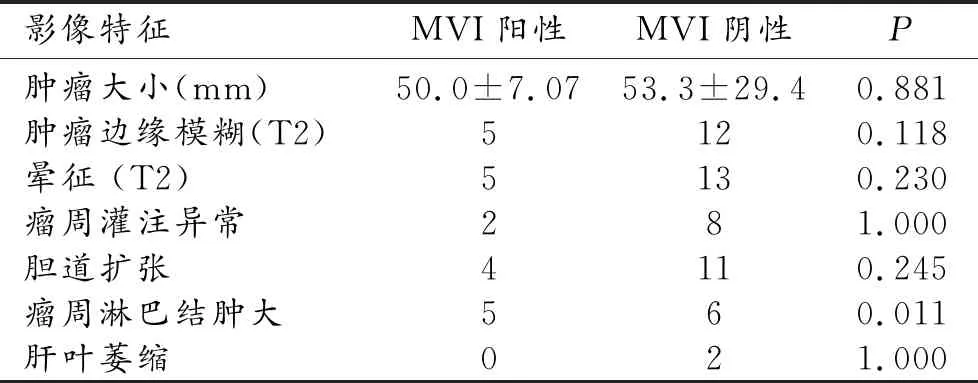
表3 患者影像特征比较
目前,外科手术病灶根治性切除是ICC是最重要治疗手段,R0根治性切除术后5年RFS可达45.7%。但是,出现明显黄疸或腹痛等临床症状时往往伴随其他部位转移,疾病已进入晚期状态,只有大约20%~40%患者可行外科手术治疗[8]。肝内复发和转移,术后远期生存也不理想,5年生存率23.6%~35%[9],R0切除术后生存率58%[10]。最年大量研究表明微血管侵犯是影响术后肝内胆管癌预后一个重要因素,术后病理证实存在MVI患者,往往需要在R0切除后行术后辅助化疗[11]。因此,本课题组大胆推测若是术前通过影像检查预测ICC患者MVI,进一步选择最佳外科手术方式,尽量将微转移灶完整切除或许可延长MVI阳性患者术后总生存期(OS)和无疾病生存期(PFS),减少复发率。争取在术前就能通过影像检测来判断ICC患者是否存在MVI显得尤为重要。
本研究显示肿瘤周围卫星结节、肿瘤周围淋巴结肿大与MVI阴性组比较存在差异(P<0.05),其余特征比较无显著差异(P>0.05)。
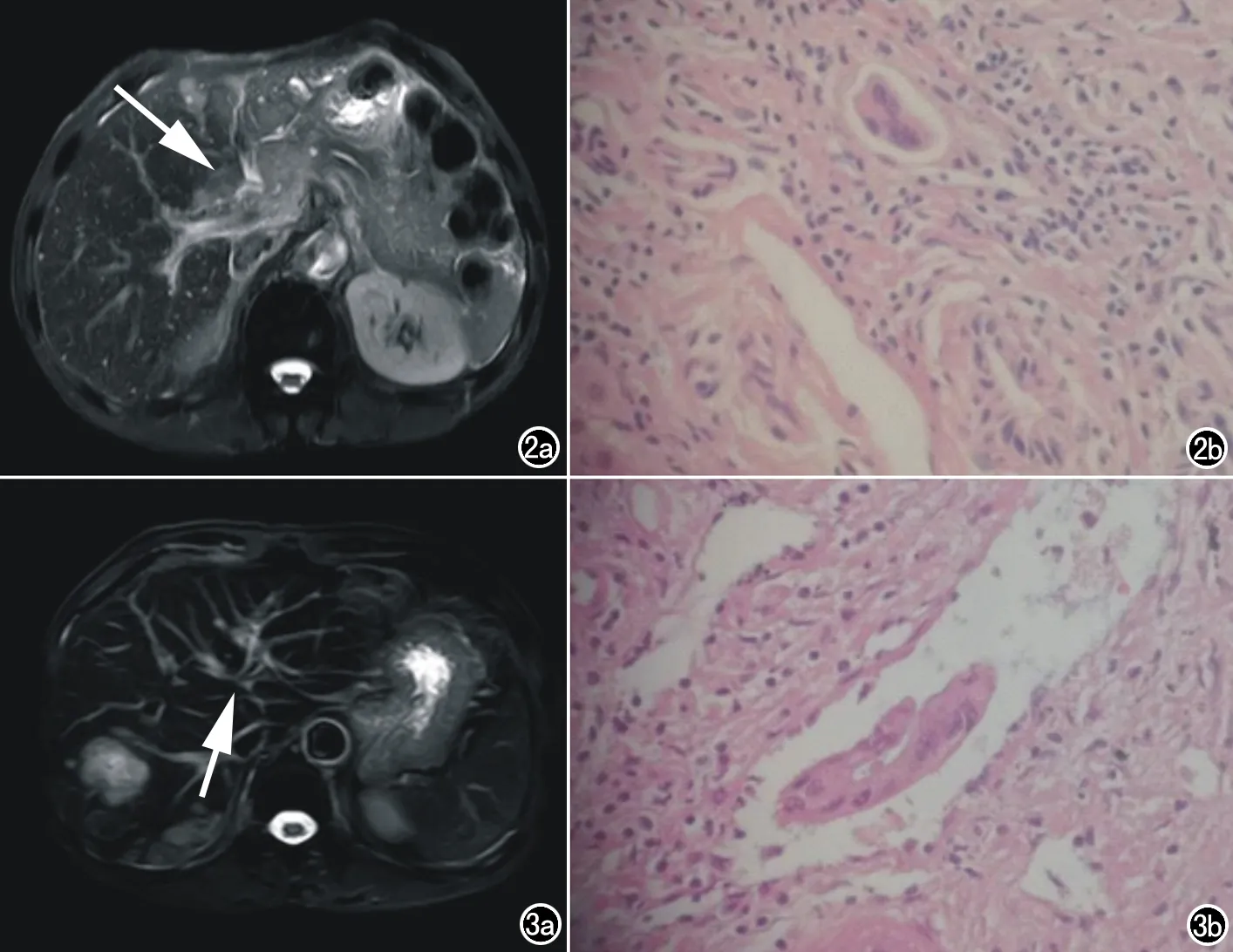
图2 女,53岁,肝内胆管癌患者,病理确诊该患者存在微血管侵犯。a) 增强MRI示病灶周围有增大淋巴结(箭); b) 显微镜(苏木精-伊红染色,×40)示微血管侵犯征象。 图3 男,47岁,肝内胆管癌患者,病理确诊该患者存在微血管侵犯。a) 增强MRI示病灶周围微卫星结节(箭); b) 显微镜(苏木精-伊红染色,×40)示该微血管侵犯征象。
本研究发现肿瘤周围卫星结节发生、肿瘤周围淋巴结肿大与肝内胆管癌患者MVI发生有关系,其中肿瘤周围淋巴结肿大可作为ICC患者发生MVI独立预测因子。美国麻省总医院(MGH)和哈佛医学院研究发现小鼠模型癌细胞在体内扩散通常到达第一个部位就是淋巴结,而且转移性淋巴结癌细胞能够通过入侵淋巴结血管而逃逸到血液中发生血管侵犯,从而导致在身体其他部位产生转移瘤[12]。Spolverato[12]已经确认区域淋巴结转移与微血管侵犯风险增加独立相关。Javier[13]认为淋巴管在Glisson鞘内伴有门静脉,肝动脉或胆管,并在肝门处聚集在12~15个独立淋巴管中。这样,当发生转移性淋巴结转移时,它通常伴随着血管侵犯。但是,由于血管侵犯不易检测,因此常表现为淋巴结肿大。因此,这些继往研究和证据也恰好和本研究结果相符。
被大多数影像专家认可诊断淋巴结转移标准中MRI确定转移性LN在短轴直径>8~10 mm时准确性更高[13]。本课题组据recist 1.1标准,继往认为淋巴结短径>10 mm且淋巴结内部密度改变,边缘清晰淋巴结视为肿大淋巴结。因此,本课题组将磁共振图像中淋巴结短径>10 mm视为淋巴结肿大。

