色素络合荧光法检测饲料中的盐酸氯丙嗪和奋乃静
■李军德 梅浩男 宋吉英*
(1.青岛农业大学,山东青岛266109;2.青岛农业大学化学与药学院,山东青岛266109)
自1883年德国化学家Bemthsen成功发现并合成吩噻嗪以来,吩噻嗪类化合物得到了广泛的应用。盐酸氯丙嗪(Chlorpromazine hydrochloride,CPZ)和奋乃静(Perphenazine,PPZ)是吩噻嗪类的代表性药物,因具有镇定、止吐、降低动物代谢等作用,二者在畜禽生产中有一定的应用,通常会在饲料中进行添加,而其蓄积性残留会对人体健康造成危害[1]。因此,对饲料中添加性药物筛查和分析检测方法的探索越来越重要。荧光分析法因灵敏度高、操作简便,在盐酸氯丙嗪和奋乃静的分析检测中得到了广泛应用[2-14]。盐酸氯丙嗪和奋乃静因其母核中有吩噻嗪结构,本身有内源荧光,但内源荧光强度较弱,特别是样品中含量低的话,直接进行分析检测很难被检测到,因此可通过一些反应增强其荧光强度。本研究在传统的荧光分析方法基础上加以改进,在盐酸氯丙嗪和奋乃静加入色素,形成的络合物荧光强度明显增强,可成功用于饲料样品中吩噻嗪类药物的痕量分析检测,为饲料添加剂的安全合理使用提供依据。
1 材料与方法
1.1 主要仪器与试剂
仪器:F-2500型荧光分光光度计(日本Hitachi公司);GL-12B 离心机(上海安亭科学仪器厂);BP-10酸度计(北京赛多利斯科学仪器有限公司);AR124CN电子天平(常州奥豪斯仪器有限公司);RE-52AA 型旋转蒸发器(上海亚荣生化仪器厂)。
试剂:盐酸氯丙嗪标准品(批号:100460-200501,中国药品生物制品检定所);奋乃静标准品(批号:100133-201403,中国食品药品检定所);醌茜素(上海绿鸟科技发展有限公司);大黄素(瑞迪生物科技有限公司);色谱乙醇(天津市科密欧化学试剂有限公司);试验用水均为超纯水;市售饲料样品。
分别取盐酸氯丙嗪、奋乃静、醌茜素、大黄素标准品0.020 0、0.020 0、0.002 5、0.002 5 g,准确称量,用乙醇溶解并定容至50 ml 棕色容量瓶中,得到浓度分别为0.40、0.40、0.05、0.05 mg/ml 各标准溶液,作为储备液备用。
1.2 光谱分析参数和分析测定
λEX=258 nm,λEM=452 nm,扫描范围EX-220~380 nm,EM-400~550 nm,狭缝宽度EX-5 nm,EM-5 nm,扫描速度300 nm/min,延迟时间0 s,电压400 V。
在盐酸氯丙嗪和奋乃静标准溶液加入一定量的醌茜素溶液,使醌茜素和吩噻嗪药物的质量比为20∶100,调整溶液的pH 值为5~6 的弱酸性环境,20 ℃条件下反应0.5 h进行荧光扫描。
1.3 饲料样品的预处理
市售饲料样品粉碎,称取样品5.0 g左右,置于碘量瓶中,加入25 ml乙醇,磁力搅拌30 min,离心,上清液旋蒸至干,用5 ml 乙醇溶解烧瓶底部的残留物,溶液用一次性0.45 μm 有机滤膜过滤,加入醌茜素,调整溶液的pH 值为5~6 的弱酸性环境,20 ℃下络合反应0.5 h,待测。
1.4 盐酸氯丙嗪和奋乃静的激发波长与发射波长的确定
取一定浓度的盐酸氯丙嗪和奋乃静标准溶液,在不同的激发波长下对其荧光光谱扫描,以确定其荧光发射波长λEM;根据得到的λEM,对盐酸氯丙嗪和奋乃静进行激发光谱扫描,以确定其荧光发射波长λEX。
1.5 盐酸氯丙嗪-醌茜素络合反应影响因素的试验
1.5.1 确定络合反应质量比的试验
取6 支棕色容量瓶,加入一定量的盐酸氯丙嗪,再加入不同量的醌茜素溶液,使醌茜素和盐酸氯丙嗪的质量比分别为1∶100、5∶100、10∶100、20∶100、40∶100、80∶100,调整溶液pH 值为5~6,20 ℃下反应0.5 h后进行荧光光谱扫描并比较其荧光强度。
1.5.2 确定络合反应pH值的试验
取5支棕色容量瓶,加入醌茜素和盐酸氯丙嗪溶液,使其质量比为20∶100,调整溶液的pH 值分别为2、3、4、5、6、7、8、9、10,20 ℃下反应0.5 h 后进行荧光光谱扫描并比较其荧光强度。
1.5.3 确定络合反应时间
取5支棕色容量瓶,加入醌茜素和盐酸氯丙嗪溶液,使其质量比为20∶100,调整溶液的pH值为5~6,20 ℃下反应0.5、1.0、1.5、2.0、4.0 h后进行荧光光谱扫描并比较其荧光强度。
1.5.4 确定络合反应温度
取5支棕色容量瓶,加入醌茜素和盐酸氯丙嗪溶液,使其质量比为20∶100,调整溶液的pH值为5~6,分别在20、30、40、50、60 ℃条件下反应0.5 h进行荧光光谱扫描,
1.5.5 正交试验
单因素之间对试验结果是相互影响的,在单因素试验的基础上,设计四因素三水平正交试验,正交试验的因素和水平见表1。按照表1的因素和水平安排正交试验内容,根据荧光强度确定因素主次关系。
1.6 奋乃静-醌茜素络合反应影响因素
在奋乃静中加入醌茜素,奋乃静-醌茜素络合物荧光强度的影响因素,采用与1.5 类同的试验方法进行考察。
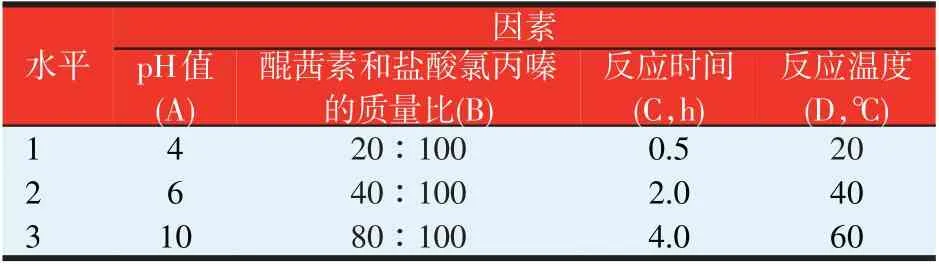
表1 正交试验的因素和水平
1.7 大黄素和醌茜素对吩噻嗪类药物荧光增敏效果对比
试验各取3 份相同浓度的盐酸氯丙嗪和奋乃静标准溶液,一份做参比,另外两份分别加入大黄素和醌茜素并在最佳试验条件反应后进行荧光光谱扫描。
1.8 标准工作曲线的制备
取不同体积的盐酸氯丙嗪和奋乃静储备液,依次配制成系列浓度分别为0.5、2.0、5.0、10.0、20.0 μg/ml的标准溶液,加入醌茜素,调整溶液的pH值为5~6,20 ℃下络合反应0.5 h,测其荧光强度,以溶液的浓度(c)为横坐标,荧光强度(F)为纵坐标,做标准工作曲线。
1.9 加标回收试验
在市售饲料样品中分别加入不同量的盐酸氯丙嗪和奋乃静,用乙醇提取,按照1.3的方法进行处理和测定,根据测定结果计算加标回收率。所有试验平行3次,结果取平均值。
1.10 数据处理与分析
试验中数据处理采用Origin 8.0统计分析软件进行处理和计算,结果以“平均值”表示。
2 结果与分析
2.1 盐酸氯丙嗪和奋乃静的激发波长与发射波长
按照1.4 的步骤进行光谱扫描,不同激发波长下盐酸氯丙嗪和奋乃静的荧光谱图见图1。盐酸氯丙嗪和奋乃静的发射波长λEM分别为453 nm和454 nm,二者基本相同;在不同激发光波长照射下,目标物的荧光强度也各不相同;在得到的发射波长下对盐酸氯丙嗪和奋乃静进行激发光谱扫描,激发光谱见图2,其激发波长λEX均为258 nm。

图1 不同激发波长下盐酸氯丙嗪和奋乃静的发射光谱
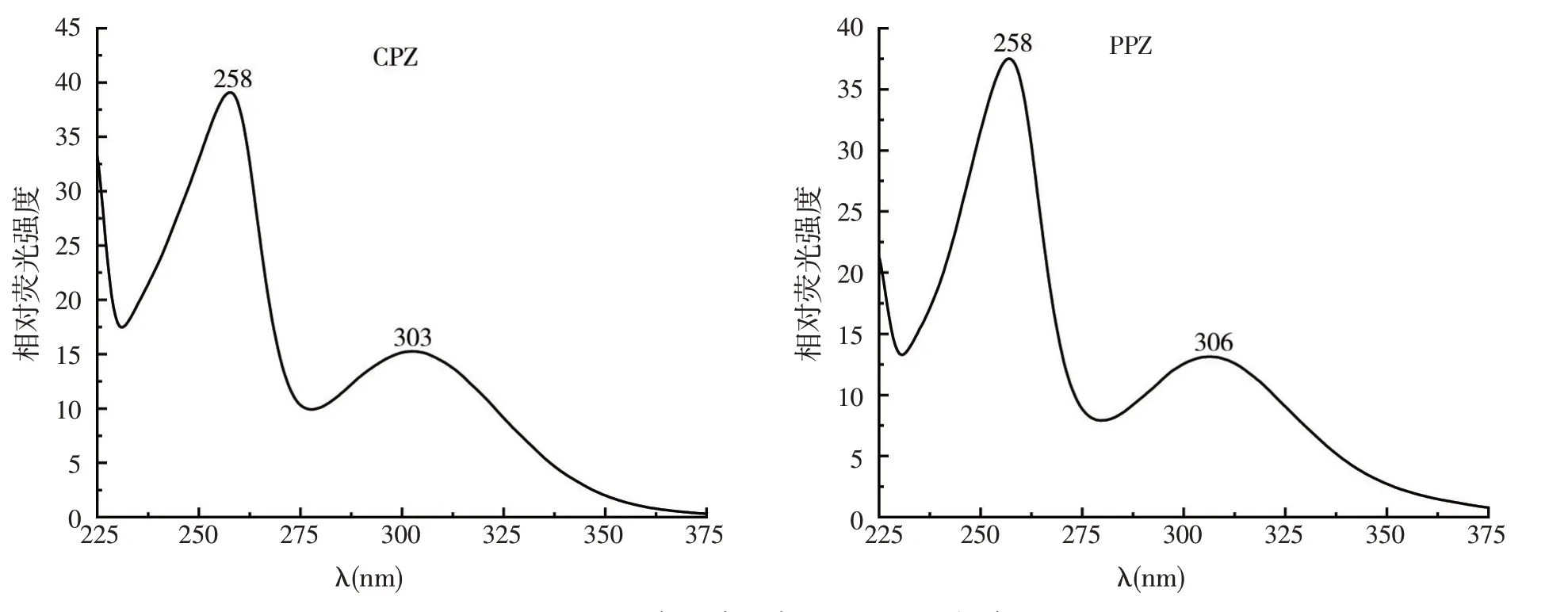
图2 盐酸氯丙嗪和奋乃静的激发光谱
2.2 影响盐酸氯丙嗪-醌茜素络合反应的因素
2.2.1 醌茜素和盐酸氯丙嗪的质量比
按照1.5.1 的试验方法进行光谱扫描,不同质量比条件下盐酸氯丙嗪-醌茜素络合物的对比荧光谱见图3。由图3 可知,醌茜素和盐酸氯丙嗪的质量比不同,络合物的荧光强度也各不相同,但其荧光发射峰波长基本相同。随着醌茜素和盐酸氯丙嗪质量比的增大,络合物荧光强度逐渐增强,当质量比为20∶100时,络合物荧光强度最大;质量比超过20∶100时,荧光强度开始下降。
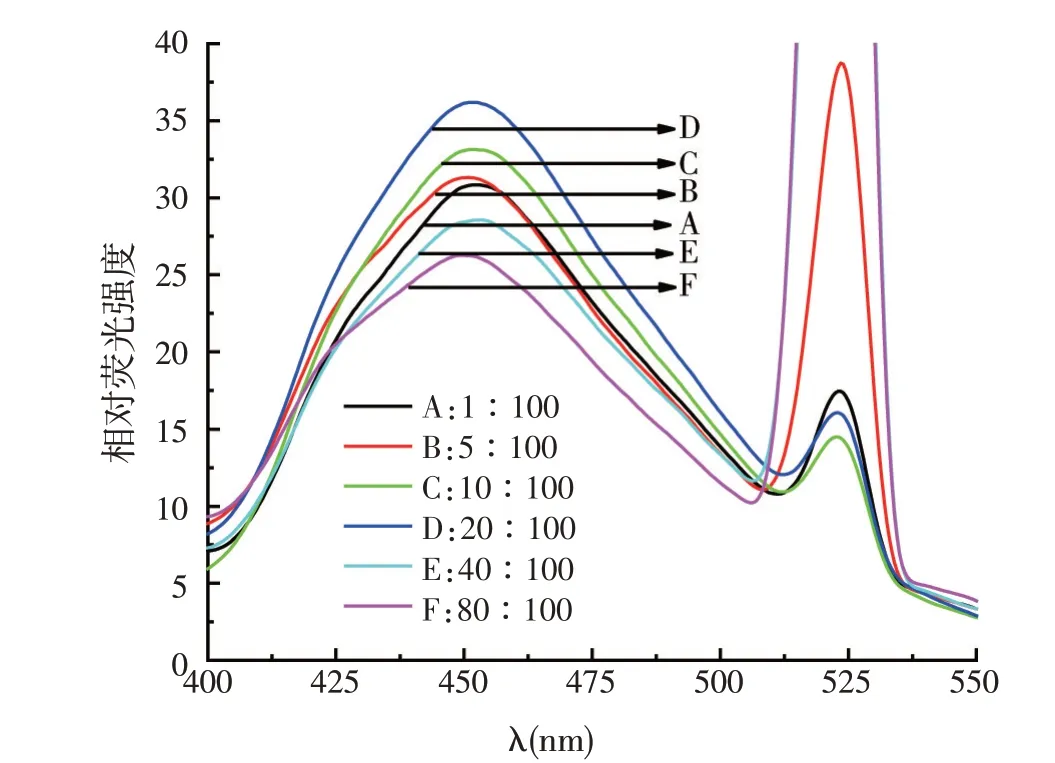
图3 醌茜素和盐酸氯丙嗪的质量比对络合物荧光强度的影响
2.2.2 络合反应的pH值
按照1.5.2的试验方法进行光谱扫描,不同pH值条件下盐酸氯丙嗪-醌茜素络合物的对比荧光谱见图4。由图4 可知,酸性条件下,溶液酸性越弱,络合物的荧光强度越大,pH值为5~6时,荧光强度较大;当pH值大于6即是碱性环境下,荧光强度逐渐减弱。

图4 pH值对盐酸氯丙嗪-醌茜素络合物荧光强度的影响
2.2.3 络合反应时间
按照1.5.3 的试验方法进行光谱扫描,不同反应时间下盐酸氯丙嗪-醌茜素络合物的对比荧光谱见图5。由图5 可知,随着反应时间的增加,络合物的荧光强度减弱,因为时间越长,络合物的稳定性会降低,荧光强度也会随之减弱,反应时间控制在0.5 h 内。
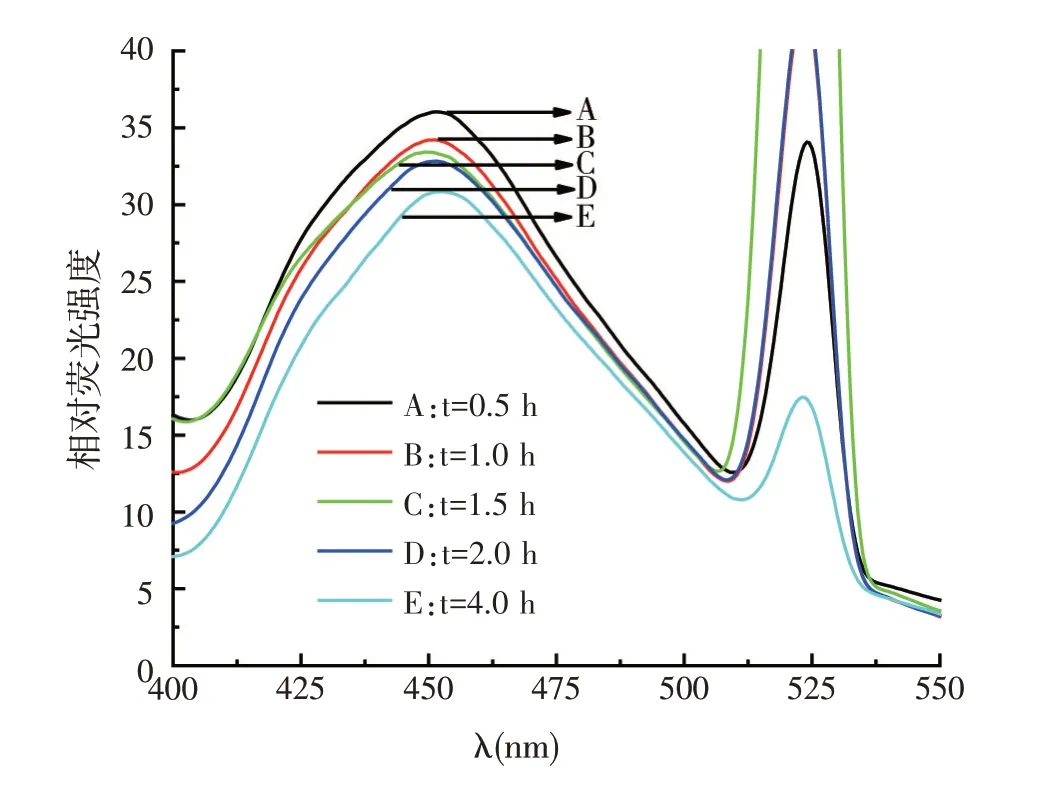
图5 反应时间对盐酸氯丙嗪-醌茜素络合物荧光强度的影响
2.2.4 络合反应温度
按照1.5.4 的试验方法进行光谱扫描,不同反应温度条件下盐酸氯丙嗪-醌茜素络合物的对比荧光谱见图6。由图6可知,温度升高,络合物的荧光强度减弱,因为络合物对热稳定性差,温度升高会使其分解从而使荧光强度减弱,反应温度控制在20 ℃。
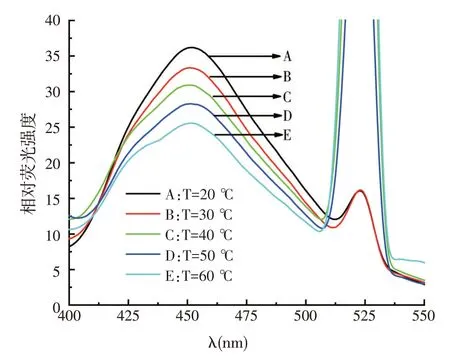
图6 温度对盐酸氯丙嗪-醌茜素络合物荧光强度的影响
2.2.5 正交试验数据
按照1.5.5的正交试验方法对每个试验组进行光谱扫描,正交试验结果的考察指标为络合物的荧光强度,正交试验可确定因素影响的主次关系和最优试验方案。由表2可知,不同因素和水平组合所得的试验结果各不相同,根据得到的因素主次关系和最优试验方案,正交试验结果和单因素试验结论一致。
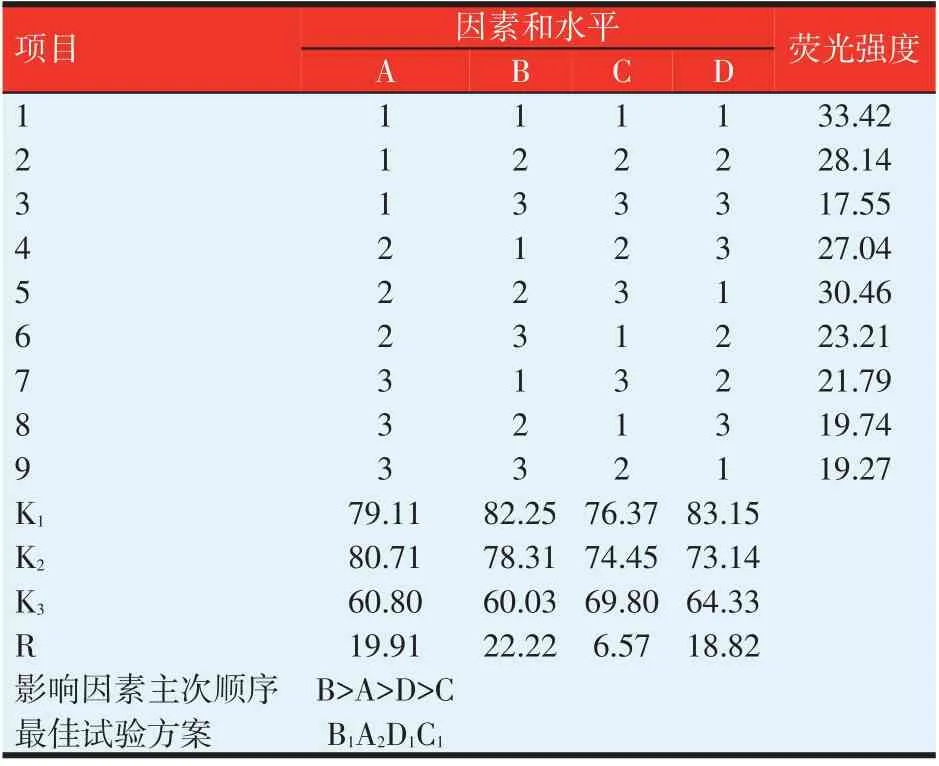
表2 正交试验和结果分析
2.3 盐酸氯丙嗪和奋乃静与醌茜素形成络合物的最佳试验条件(见表3)

表3 吩噻嗪药物与醌茜素形成络合物的最佳试验条件
表3 列出了盐酸氯丙嗪和奋乃静与醌茜素形成络合物的最佳试验条件,包括溶液的pH、醌茜素和吩噻嗪药物的质量比、反应时间和反应温度。
2.4 大黄素和醌茜素对吩噻嗪类药物荧光增敏效果分析
按照1.8 的试验方法进行光谱扫描,荧光增敏效果的对比图谱见图7。大黄素和醌茜素对盐酸氯丙嗪和奋乃静均有荧光增敏作用,但醌茜素的荧光增敏效果要高于大黄素,故试验选择醌茜素作为增强盐酸氯丙嗪和奋乃静荧光强度的络合剂,加入醌茜素后,盐酸氯丙嗪和奋乃静形成的络合物,其荧光发射波长都发生了轻微的蓝移,发射波长λEM均为452 nm。
2.5 方法的性能数据(见图8)
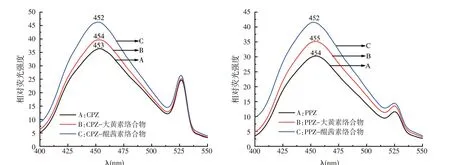
图7 盐酸氯丙嗪和奋乃静与不同色素络合的荧光光谱
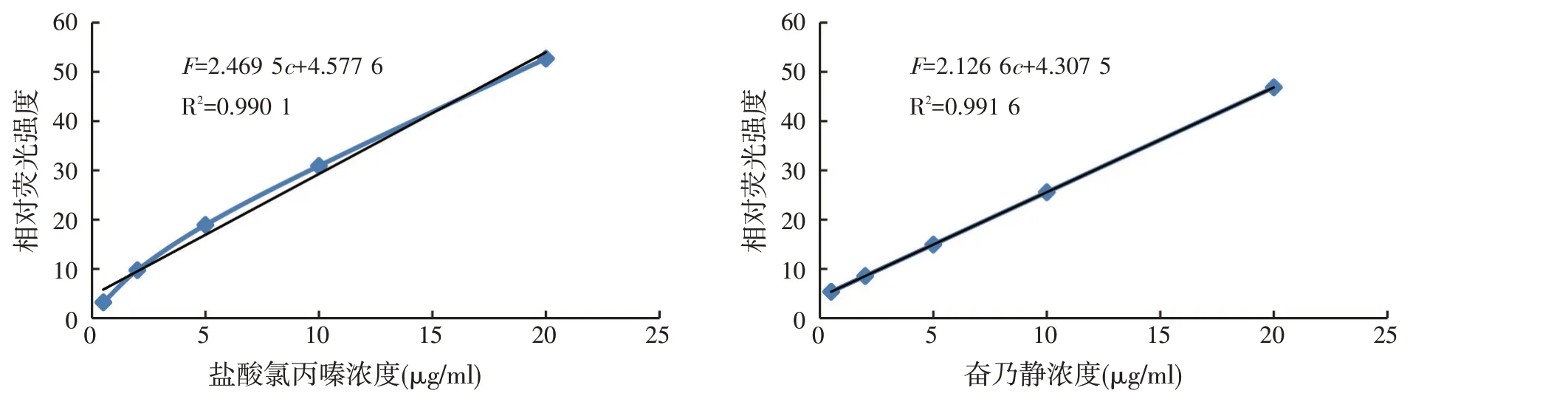
图8 盐酸氯丙嗪和奋乃静的标准工作曲线
按照1.7 的方法以溶液的浓度(c)为横坐标,荧光强度F为纵坐标,做标准工作曲线,得盐酸氯丙嗪的线性回归方程为F=2.469 5c+4.577 6,R2=0.990 1,线性范围0.5~20.0 μg/ml;奋乃静的线性回归方程为F=2.126 6c+4.307 5,R2=0.991 6,线性范围0.5~20.0 μg/ml。加标回收试验中盐酸氯丙嗪和奋乃静的平均加标回收率分别为101.3%和97.8%,相对标准偏差RSD 分别为4.3%和5.4%。
3 讨论
3.1 盐酸氯丙嗪和奋乃静的激发波长
盐酸氯丙嗪和奋乃静的激发光谱图中均有258 nm和303(306)nm 两个激发峰,在303(306)nm 的激发波长下,盐酸氯丙嗪和奋乃静的荧光强度都很弱,故试验选择258 nm作为盐酸氯丙嗪和奋乃静的最大激发波长。盐酸氯丙嗪和奋乃静的激发波长和发射波长相同,是因为二者具有相同的吩噻嗪母核结构,只是吩噻嗪环上的N原子所连的基团存在差异,但这两种不同基团对吩噻嗪环的荧光强度没有显著的影响。
3.2 pH值对络合物荧光强度的影响
溶液的酸碱性会对吩噻嗪类药物的荧光强度造成较大影响,这是由吩噻嗪类药物的分子结构决定的,溶液pH值会直接影响其电子云分布,使吩噻嗪类药物的荧光光谱发生变化。当pH 值<5 时,与醌茜素络合的盐酸氯丙嗪是强阳离子,荧光强度较弱;当pH值为5~6 时,盐酸氯丙嗪是两性离子,络合物的荧光强度也随之增大;当体系pH值继续升高,盐酸氯丙嗪变为阴离子,导致络合物的荧光强度逐渐减弱。
3.3 反应机理
吩噻嗪类药物本身有内源荧光,但其内源荧光强度相对较弱。部分色素对物质的荧光强度有着较大的影响,大黄素和醌茜素均具有高共轭双键结构,是良好的π电子受体[14];作为吩噻嗪类的代表性药物,盐酸氯丙嗪和奋乃静分子结构中的吩噻嗪母核决定了两种分子都具有良好的给电子性,因此吩噻嗪类药物可与大黄素和醌茜素形成络合物使其荧光强度增强,吩噻嗪母核中氮原子的质子化作用可使形成的络合物平面刚性结构更稳定。从分子结构来看,醌茜素分子的平面结构刚性比大黄素更稳定,因而与吩噻嗪类药物分子形成的络合物也更加稳定,对络合物的荧光增敏效果也更明显。
4 结论
醌茜素对盐酸氯丙嗪和奋乃静等吩噻嗪类药物有明显的荧光增敏作用,可与其形成络合物,络合物的荧光强度增强。
络合反应的最佳条件为醌茜素和吩噻嗪药物的质量比20∶100,pH 值为5~6 的弱酸性环境,20 ℃下反应0.5 h。
本试验建立了一种在吩噻嗪类药物中加入醌茜素增强其荧光强度以对吩噻嗪类药物进行检测的荧光分析法,该方法简单、快速,可用于饲料样品中吩噻嗪类药物的含量测定。

