民族药龙骨风化学成分研究
卢汝梅,黎云清,王 肖,张进燕,李 兵,韦建华
(广西中医药大学 药学院,广西 南宁 530200)
广西常用民族药龙骨风(Caulis Alsophilae)为桫椤科植物桫椤(Alsophilaspinulosa(Wall.ex Hook.) Tryon)的茎干,具有祛风除湿、活血散瘀、清热解毒、止咳平喘、强筋骨、杀虫等功效。桫椤又名树蕨,主产于福建、广东、广西、海南、贵州、云南、四川等地,在广西主要分布在百色、靖西、德保、武鸣、苍梧、容县、罗城、龙胜、浦北、金秀、凤山等地[1-2]。龙骨风在不同民族药中都有应用[3]:苗药中称为冷落庶,用以治疗小儿疳积;壮药中称为谷地、龙骨风,具有通调龙路、火路,祛风毒,除湿毒,强筋骨之功效,用于核尹(腰痛)、痿约(阳痿)、林得叮相(跌打损伤)、发旺(风湿骨痛)等病[4];瑶药中称为龙骨风,是瑶药最具特色的老班药中“十八风”之一,具有抑菌和镇痛等作用,用于治疗风湿骨痛、咳嗽哮喘、慢性支气管炎、肾虚腰痛、肾炎水肿等[5]。研究表明:龙骨风主要含萜类、黄酮、酚酸、甾体等成分[6]。本课题组前期对龙骨风的化学成分进行初步研究,分离鉴定新化合物龙骨风新苷A、桫椤脑苷酯A、桫椤脑苷酯B、桫椤内酯酸A和桫椤内酯酸B,以及已知化合物海松酸、6β-羟基-24-乙基-胆甾-4-烯-3-酮、decumbic acid、对香豆酸-4-O-β-D-吡喃葡萄糖苷、反式咖啡酸-4-O-β-D-吡喃葡萄糖苷、2-甲基延胡索酸、桫椤诺生A、原儿茶醛、原儿茶酸、豆甾烷-3,6-二酮、β-谷甾醇、胡萝卜苷等22个化合物[7-8]。
为了更好阐明龙骨风的化学物质基础,发现其中活性成分和先导化合物,在前期工作基础上,本课题组采用硅胶、大孔吸附树脂、MCI GEL CHP-20P、Flash C18和Sephadex LH-20柱色谱等方法对其化学成分进行分离,得到20个化合物,分别鉴定为豆甾醇(1)、棕榈酸(2)、正十三烷(3)、羽扇豆醇(4)、对香豆酸(5)、棕榈酸甘油酯(6)、24(R)-24-乙基-6β-羟基-4-胆甾烯醇-3-酮(7)、24(R)-24-ethyl-5α-cholestane-3β,5α,6β-triol(8)、阿魏酸(9)、大黄素(10)、牡荆素(11)、芹菜素(12)、二氢芹菜素(13)、3,4二羟基苯丙烯酸(14)、heptadec-(9Z)-enoic acid(15)、芦丁(16)、inoseavin A(17)、salviniside Ⅱ(18)、对香豆酸-4-O-β-D-吡喃葡萄糖苷(19)、异槲皮苷(20)。其中化合物1~5、7~10、13、15~18、20为首次从龙骨风中分离得到。
1 仪器与材料
Bruker Avance III 500 MHz、Avance III 800 MHz核磁共振仪(瑞士Bruker公司);Waters Autospec Premier p776质谱仪(美国Waters公司);CPA225D型分析天平(赛多利斯科学仪器有限公司);XT4-100A控温型显微熔点测定仪(北京科仪电光仪器厂);AB-8大孔吸附树脂(南开大学树脂厂);Flash C18色谱柱(日本岛津公司);MCI GEL CHP-20P树脂(日本三菱化学公司);Sephadex LH-20(美国pharmacia公司);硅胶(粒径75~150 μm、48~75 μm)及其余化学试剂(分析纯,国药集团化学试剂有限公司)。
龙骨风药材购于广西靖西端午药市,经广西中医药大学韦松基教授鉴定为桫椤科植物桫椤(Alsophilaspinulosa(Wall.ex Hook.) Tryon)的茎干。
2 提取与分离
龙骨风粗粉28 kg,用体积分数80%乙醇冷浸提取3次,每次4 d。提取液减压浓缩得到乙醇提取物,加水悬浮后依次用石油醚(60~90 ℃)、乙酸乙酯、正丁醇萃取,回收溶剂,得到石油醚部位85 g,乙酸乙酯部位230 g,正丁醇部位80 g。
取石油醚部位80 g,硅胶柱色谱分离,以石油醚-乙酸乙酯(80∶1 → 50∶1 → 30∶1 → 15∶1 → 10∶1 → 5∶1 → 2∶1 → 1∶1 → 0∶1,体积比)梯度洗脱,得到9个流份Fr.A1~Fr.A9。Fr.A4用硅胶、Sephadex LH-20柱色谱分离和重结晶,得到化合物1(210 mg)、2(4.6 mg)和3(5.1 mg);Fr.A5用硅胶柱色谱纯化,丙酮重结晶,得到化合物4(6.0 mg);Fr.A6经MCI GEL CHP-20P和Sephadex LH-20柱色谱分离,得到化合物5(6.0 mg)和6(20 mg);Fr.A7经MCI GEL CHP-20P和Sephadex LH-20柱色谱纯化,得到化合物7(20 mg);Fr.A8用Sephadex LH-20柱色谱纯化,得到化合物8(4.6 mg)。
取乙酸乙酯部位100 g,热水溶解,不溶物用硅胶柱色谱分离,以氯仿-甲醇(20∶1 → 10∶1 → 5∶1 → 3∶1→1∶1 → 0∶1,体积比)梯度洗脱,得到6个流份Fr.B1~Fr.B6。Fr.B2经MCI GEL CHP-20P和Sephadex LH-20柱色谱分离,得到化合物9(2.8 mg)和10(3.2 mg);Fr.B3经MCI GEL CHP-20P柱色谱分段后,Fr.B3-3用丙酮重结晶得化合物11(4.0 mg);Fr.B3-5和Fr.B3-6分别用Sephadex LH-20柱色谱纯化,得到化合物12(3.2 mg)和13(6.0 mg)。乙酸乙酯部位水溶部分经聚酰胺柱色谱分离,以水-乙醇梯度洗脱,得到5个流份Fr.C1~Fr.C5。Fr.C2经MCI GEL CHP-20P和Sephadex LH-20柱色谱分离,得到化合物14(5.0 mg)和15(2.6 mg);Fr.C3经MCI GEL CHP-20P和Sephadex LH-20柱色谱分离,得到化合物16(8.2 mg)、17(5.0 mg)和18(7.0 mg)。
取正丁醇部位180 g,用AB-8大孔树脂柱色谱分离,用水-甲醇梯度洗脱,得到5个流份Fr.D1~Fr.D5。Fr.D3和Fr.D4分别用MCI GEL CHP-20P、Flash C18和Sephadex LH-20柱色谱反复纯化,得到化合物19(2.8 mg)和20(2.6 mg)。
3 结构鉴定
化合物1:白色粉末,m.p.165~167 ℃,三氯化锑反应显阳性。与豆甾醇对照品共薄层色谱,在3种溶剂系统中展开检识,二者的Rf值均相同,且混合熔点不下降。故化合物1鉴定为豆甾醇。
化合物2:白色片状结晶。EI-MS(m/z):256[M]+。1H-NMR(500 MHz,Pyr-d5):2.50(2H,t,J=7.4 Hz,H-2),1.76(2H,m,H-3),1.24~1.31(24H,m,H-4~15),0.86(—CH3)。13C-NMR(125 MHz,Pyr-d5):35.0(C-2),32.2(C-3),30.0(C-4~C-7),30.0(C-8,C-9),29.9(C-10,C-11),29.8(C-12),29.7(C-13),25.7(C-14),23.0(C-15),14.3(—CH3),176.1(—COOH)。以上波谱数据与文献[9]报道基本一致,故化合物2鉴定为棕榈酸。
化合物3:白色粉末,m.p.-6~-4 ℃。与正十三烷对照品共薄层色谱,在3种溶剂系统中展开检识,二者的Rf值均相同,且混合熔点不下降。故化合物3鉴定为正十三烷。
化合物4:白色针晶,m.p.212~215 ℃。与羽扇豆醇对照品共薄层色谱,用3种不同溶剂系统展开检识,二者的Rf值均相同,且混合熔点不下降。故化合物4鉴定为羽扇豆醇。
化合物5:白色针晶。EI-MS(m/z):164[M]+,147[M - OH]+,119[M - COOH]+。1H-NMR(800 MHz,CD3OD):7.43(2H,d,J=8.0 Hz,H-2,6),6.79(2H,d,J=8.0 Hz,H-3,5),7.56(1H,d,J=16.0 Hz,H-7),6.27(1H,d,J=16.0 Hz,H-8)。13C-NMR(201 MHz,CD3OD):127.4(C-1),131.0(C-2,6),116.8(C-3,5),161.0(C-4),145.9(C-7),115.8(C-8),171.7(C-9)。以上波谱数据与文献[10]报道基本一致,鉴定化合物5为对香豆酸。
化合物6:白色粉末。EI-MS(m/z):331[M+H]+,299,256,239,213,134,112,98,91,74。1H-NMR (500 MHz,CD3OD):4.16(1H,dd,J=4.4 Hz,H-1a),4.12(1H,dd,J=4.4 Hz,H-1b),3.82(1H,m,H-2),3.56(1H,m,H-3a),3.53(1H,m,H-3b),2.34(2H,t,J=7.5 Hz,H-2′),1.63(2H,m,J=7.2 Hz,H-3′),1.28~1.32(24H,m,H-4′~15′),0.88(3H,t,J=7.1 Hz,—CH3)。13C-NMR(125 MHz,CD3OD):66.5(C-1),71.1(C-2),64.0(C-3),175.5(C-1′),34.9(C-2′),26.0(C-3′),28.1(C-4′),30.2~30.8(C-5′~13′),33.1(C-14′),23.7(C-15′),14.4(—CH3)。以上波谱数据与文献[11]报道基本一致,鉴定化合物6为棕榈酸甘油酯。
化合物7:白色片状结晶。EI-MS(m/z):429[M+H]+,414,411,400,269,245,227,152。1H-NMR(500 MHz,CDCl3):5.81(1H,s,H-4),4.35(1H,s,H-6),0.74(3H,s,H-18),1.37(3H,s,H-19),0.92(3H,d,J=6.6 Hz,H-21),0.82(3H,d,J=6.9 Hz,H-26),0.81(3H,d,J=6.9 Hz,H-27),1.27(2H,m,H-28),0.85(3H,dd,J=7.5 Hz,H-29)。13C-NMR(125 MHz,CDCl3):37.1(C-1),34.3(C-2),200.5(C-3),126.3(C-4),168.6(C-5),73.3(C-6),38.5(C-7),29.7(C-8),53.6(C-9),38.0(C-10),21.0(C-11),39.6(C-12),42.5(C-13),56.0(C-14),24.2(C-15),28.2(C-16),55.9(C-17),19.5(C-19),36.1(C-20),18.7(C-21),33.9(C-22),26.0(C-23),45.8(C-24),29.1(C-25),19.8(C-26),19.0(C-27),23.1(C-28)。以上波谱数据与文献[12]报道基本一致,鉴定化合物7为24(R)-乙基-6β-羟基-4-胆甾烯醇-3-酮。
化合物8:白色粉末。EI-MS(m/z):449[M+1]+。1H-NMR(500 MHz,Pyr-d5):4.82(1H,m,H-3),2.95(1H,dd,J=12.7,11.4 Hz,H-4a),2.26(1H,dd,J=12.7,3.5 Hz,H-4b),0.73(3H,s,H-18),1.66(3H,s,H-19),0.98(3H,d,J=6.6 Hz,H-21),0.86(3H,d,J=6.8 Hz,H-26),0.83(3H,d,J=7.2 Hz,H-27),0.86(3H,t,J=6.8 Hz,H-29)。13C-NMR(125 MHz,Pyr-d5):32.6(C-1),33.4(C-2),67.4(C-3),42.9(C-4),75.9(C-5),76.3(C-6),35.8(C-7),31.3(C-8),46.0(C-9),39.2(C-10),22.8(C-11),40.7(C-12),43.1(C-13),56.6(C-14),24.7(C-15),28.7(C-16),56.6(C-17),12.4(C-18),17.3(C-19),36.6(C-20),19.0(C-21),34.3(C-22),26.5(C-23),46.1(C-24),29.5(C-25),19.3(C-26),20.0(C-27),23.4(C-28),12.2(C-29)。以上波谱数据与文献[13-14]报道基本一致,鉴定化合物8为24(R)-24-ethyl-5α-cholestane-3β,5α,6β-triol。
化合物9:白色针晶。EI-MS(m/z):194[M]+,179[M-CH3]+。1H-NMR(500 MHz,CD3OD):7.17(1H,d,J=2.0 Hz,H-2),6.81(1H,d,J=8.2 Hz,H-5),7.06(1H,dd,J=2.0 Hz,H-6),7.60(1H,d,J=15.9 Hz,H-7),6.31(1H,d,J=15.8 Hz,H-8),3.88(3H,s,—OCH3)。13C-NMR(125 MHz,CD3OD):127.8(C-1),111.7(C-2),150.5(C-3),149.4(C-4),115.9(C-5),124.0(C-6),146.9(C-7),116.5(C-8),171.0(C-9),56.4(—OCH3)。以上波谱数据与文献[15]报道基本一致,鉴定化合物9为阿魏酸。
化合物10:黄色粉末。EI-MS(m/z):270[M]+。1H-NMR(500 MHz,CD3OD):7.09(1H,brs,H-2),7.56(1H,brs,H-4),7.16(1H,d,J=2.5 Hz,H-5),6.53(1H,d,J=2.4 Hz,H-7),2.42(3H,s,—CH3)。13C-NMR(125 MHz,CD3OD):163.5(C-1),125.2(C-2),149.5(C-3),121.7(C-4),134.7(C-4a),110.2(C-5),166.7(C-6),109.1(C-7),168.1(C-8),110.5(C-8a),191.7(C-9),114.9(C-9a),183.3(C-10),136.8(C-10a),22.0(3-CH3)。以上波谱数据与文献[16]报道基本一致,鉴定化合物10为大黄素。
化合物11:黄色粉末。EI-MS(m/z):432[M]+。1H-NMR(500 MHz,DMSO-d6):13.15(1H,s,5-OH),10.91(1H,brs,7-OH),10.33(1H,brs,4′-OH),6.76(1H,s,H-3),6.25(1H,s,H-6),8.02(2H,d,J=8.8 Hz,H-2′,6′),6.88(2H,d,J=8.9 Hz,H-3′,5′),4.68(1H,d,J=9.9 Hz,Glc-1″)。13C-NMR(125 MHz,DMSO-d6):164.4(C-2),102.9(C-3),182.6(C-4),156.5(C-5),98.6(C-6),163.0(C-7),104.5(C-8),160.9(C-9),105.1(C-10),122.1(C-1′),129.4(C-2′,6′),116.3(C-3′,5′),161.6(C-4′),73.8(Glc-1″),71.3(Glc-2″),79.1(Glc-3″),71.0(Glc-4″),82.3(Glc-5″),61.7(Glc-6″)。以上波谱数据与文献[17-18]报道基本一致,鉴定化合物11为牡荆素。
化合物12:淡黄色粉末。EI-MS(m/z):270[M]+。1H-NMR(800 MHz,CD3OD):6.57(1H,s,H-3),6.18(1H,d,J=1.6 Hz,H-6),6.43(1H,d,J=0.81 Hz,H-8),7.84(2H,d,J=8.0 Hz,H-2′,6′),6.92(2H,d,J=8.8 Hz,H-3′,5′)。13C-NMR(201 MHz,CD3OD):166.3(C-2),103.7(C-3),183.8(C-4),163.2(C-5),100.4(C-6),166.2(C-7),95.3(C-8),159.5(C-9),105.0(C-10),123.3(C-1′),129.4(C-2′,6′),117.1(C-3′,5′),162.9(C-4′)。以上波谱数据与文献[19]报道基本一致,鉴定化合物12为芹菜素。
化合物13:白色粉末。EI-MS(m/z):272[M]+,153,152,120。1H-NMR(500 MHz,CD3OD):5.33(1H,dd,J=13.0,3.0 Hz,H-2),3.11(1H,dd,J=17.1,13.0 Hz,H-3a),2.68(1H,dd,J=17.1,3.0 Hz,H-3b),5.87(1H,d,J=2.2 Hz,H-6),5.89(1H,d,J=2.2 Hz,H-8),7.31(2H,d,J=6.7 Hz,H-2′,6′),6.81(2H,d,J=6.7 Hz,H-3′,5′)。13C-NMR(125 Hz,CD3OD):80.5(C-2),44.0(C-3),197.8(C-4),165.5(C-5),97.0(C-6),168.4(C-7),96.1(C-8),164.9(C-9),103.3(C-10),131.1(C-1′),129.0(C-2′,6′),116.3(C-3′,5′),159.0(C-4′)。以上波谱数据与文献[20-21]报道基本一致,鉴定化合物13为二氢芹菜素。
化合物14:橙黄色颗粒状结晶。EI-MS(m/z):180[M]+,163[M-OH]+。1H-NMR(500 MHz,CD3OD)∶7.02(1H,d,J=2.1 Hz,H-2),6.76(1H,d,J=8.2 Hz,H-5),6.92(1H,dd,J=8.2,2.1 Hz,H-6),7.51(1H,d,J=15.9 Hz,H-7),6.21(1H,d,J=15.9 Hz,H-8)。13C-NMR(125 MHz,CD3OD):127.8(C-1),115.0(C-2),149.4(C-3),146.8(C-4),116.5(C-5),122.8(C-6),146.8(C-7),115.8(C-8),171.2(C-9)。以上波谱数据与文献[22]报道基本一致,鉴定化合物14为3,4-二羟基苯丙烯酸。
化合物15:白色粉末。EI-MS(m/z):268[M]+。1H-NMR(800 MHz,CD3OD):2.19(2H,d,J=7.2 Hz,H-2),1.59(2H,m,J=6.9 Hz,H-3),5.33(2H,m,H-9,10),2.02(4H,m,J=5.6 Hz,H-8,11),0.89(3H,t,H-18),1.23~1.35(18H,brm,9-CH2)。13C-NMR(201 MHz,CD3OD):179.4(C-1),36.5(C-2),26.9(C-3),130.9(C-9),130.9(C-10),33.1(C-15),23.7(C-16),14.5(C-17)。以上波谱数据与文献[23]报道基本一致,鉴定化合物15为heptadec-(9Z)-enoic acid。
化合物16:淡黄色粉末,m.p.195~197 ℃,盐酸-镁粉反应呈紫红色,Molish反应阳性,与芦丁对照品共薄层色谱,在3种不同溶剂系统中展开检识,二者的Rf值均相同,且混合熔点不下降。故化合物16鉴定为芦丁。
化合物17:黄色粉末。EI-MS(m/z):462[M]+,分子式为C25H18O9。1H-NMR(500 MHz,CD3OD):6.50(1H,s,H-4),6.70(1H,d,J=15.9 Hz,H-6),7.42(1H,d,J=15.9 Hz,H-7),7.07(1H,d,J=2.0 Hz,H-9),6.79(1H,d,J=8.2 Hz,H-12),6.99(1H,dd,J=8.3,2.0 Hz,H-13),1.97(3H,s,Me-1′),5.57(1H,s,H-2′),5.65(1H,s,H-5′),6.70(1H,d,J=1.4 Hz,H-7′),6.75(1H,d,J=8.3 Hz,H-10′),6.58(1H,dd,J=8.3,2.0 Hz,H-11′)。13C-NMR(125 MHz,CD3OD):160.6(C-1),99.5(C-2),176.8(C-3),95.6(C-4),167.0(C-5),116.6(C-6),139.9(C-7),128.5(C-8),115.1(C-9),146.9(C-10),149.4(C-11),116.6(C-12),122.7(C-13),192.9(C-1′),105.1(C-2′),203.1(C-3′),94.5(C-4′),95.9(C-5′),123.1(C-6′),115.4(C-7′),146.3(C-8′),147.8(C-9′),115.8(C-10′),120.2(C-11′),16.6(Me-1′)。以上波谱数据与文献[24]报道基本一致,鉴定化合物17为inoscavin A。
化合物18:白色簇状结晶。EI-MS(m/z):474[M]+,366,298。分子式C22H18O12,其1H-NMR(500 MHz,CD3OD)和13C-NMR(125 MHz,CD3OD)数据及归属分别见表1和表2。以上波谱数据与文献[25]报道基本一致,鉴定化合物18为salviniside Ⅱ。

表1 化合物18的氢谱数据Tab.1 1H NMR spectroscopic data for compound 18
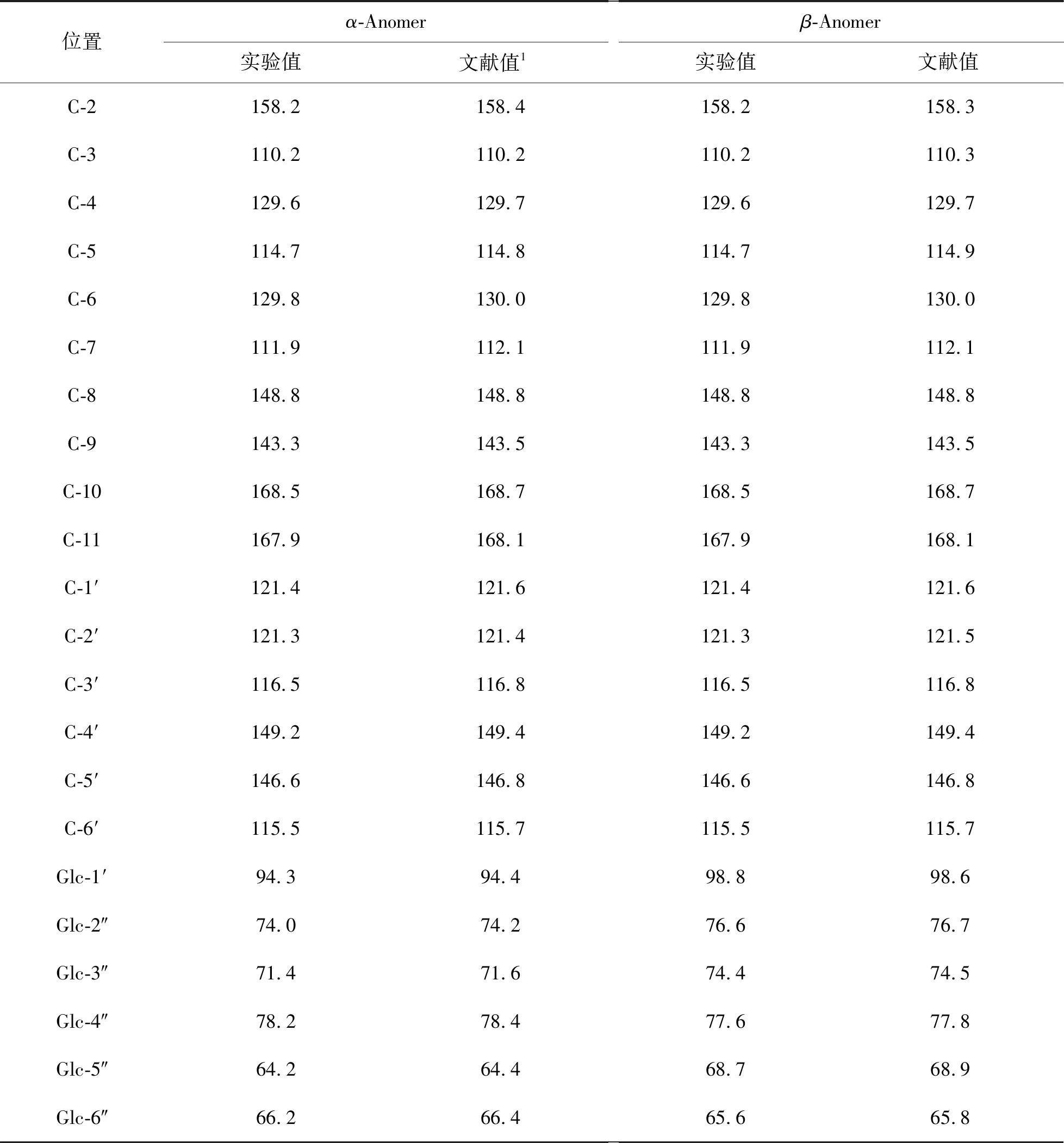
表2 化合物18的碳谱数据Tab.2 13C-NMR spectroscopic data for compound 18
化合物19:白色片状结晶。EI-MS(m/z):326[M]+,164[M-Glu]+,147,分子式C15H18O8。1H-NMR(500 MHz,CD3OD)∶7.55(2H,d,J=8.3 Hz,H-2,6),7.12(2H,d,J=8.3 Hz,H-3,5),7.60(1H,d,J=16.0 Hz,H-7),6.37(1H,d,J=16.0 Hz,H-8),4.96(1H,d,J=7.6 Hz,H-1′),3.73(1H,dd,J=5.2,3.9 Hz,H-2′),3.40(1H,dd,J=8.6,2.0 Hz,H-4′),3.46(1H,ddd,J=3.2,2.3,1.6 Hz,H-5′),3.90(1H,dd,J=6.6,2.1 Hz,H-6′)。13C-NMR(125 MHz,CD3OD):130.7(C-1),131.2(C-2,6),118.1(C-3,5),160.8(C-4),146.0(C-7),117.6(C-8),170.7(C-9),101.8(C-1′),77.9(C-2′),74.8(C-3′),71.3(C-4′),78.4(C-5′),62.5(C-6′)。以上波谱数据与文献[26]报道基本一致,鉴定化合物19为对香豆酸-4-O-β-D-吡喃葡萄糖苷。
化合物20:黄色针晶。EI-MS(m/z):464[M]+,分子式为C21H20O12。1H-NMR(500 MHz,CD3OD):6.20(1H,d,J=2.1 Hz,H-6),6.39(1H,d,J=2.1 Hz,H-8),7.70(1H,d,J=2.2 Hz,H-2′),6.87(1H,d,J=8.5 Hz,H-5′),7.59(1H,dd,J=2.2,2.2 Hz,H-6′),5.25(1H,d,J=7.7 Hz,H-1″),3.68(1H,dd,J=2.4,2.4 Hz,H-6″a),3.58(1H,dd,J=5.4,5.4 Hz,H-6″b)。13C-NMR(125 MHz,CD3OD):159.0(C-2),135.6(C-3),179.5(C-4),166.2(C-5),99.9(C-6),163.1(C-7),94.7(C-8),158.5(C-9),105.6(C-10),123.2(C-1′),116.0(C-2′),145.9(C-3′),149.9(C-4′),117.5(C-5′),123.1(C-6′),104.3(C-1″),75.7(C-2″),78.1(C-3″),71.2(C-4″),78.4(C-5″),62.5(C-6″)。以上波谱数据与文献[21]报道基本一致,鉴定化合物20为异槲皮苷。
4 讨论
本研究从龙骨风中分离获得的成分主要为黄酮类、酚酸类、内酯类和甾体类化合物。其中牡荆素具有抗菌作用,对大肠杆菌、金黄色葡萄球菌、枯草芽孢杆菌均有明显的抑制作用[27];芹菜素具有抗肿瘤、抗炎、抗菌、抗病毒、心脑血管保护等多种活性[28],可见这些黄酮类化合物的活性与龙骨风的功效具有相关性,但是否为其中主要活性成分,还有待于深入研究加以证明。内酯类成分inoseavin A、salviniside Ⅱ均是首次从桫椤科植物中分离得到,文献报道inoseavin A都是从菌类中分得的,具有较好的抗氧化和清除自由基的活性[24,29];salviniside Ⅱ为大环内酯类成分,仅报道以α-Anomer和β-Anomer混合形式从水生蕨类植物人厌槐叶苹中分离得到[25],但其药理活性研究还是空白,值得进一步关注。对香豆酸、阿魏酸、3,4-二羟基苯丙烯酸、对香豆酸-4-O-β-D-吡喃葡萄糖苷和前期分得的原儿茶醛和原儿茶酸,都属于酚酸类成分,酚酸类化合物具有抗炎、抗菌、抗肿瘤、抗氧化清除自由基等作用[30]。根据化学成分的研究结果我们对11个不同产地的龙骨风药材进行HPLC指纹图谱测定,确定了15个共有峰,并对其中5个峰进行指认,分别为原儿茶酸、原儿茶醛、3,4-二羟基苯丙烯酸、对香豆酸和阿魏酸。因此,本研究丰富了对龙骨风化学成分多样性的认识,可为龙骨风药材化学品质评价和阐明其药效物质基础提供参考。

