聚乙烯醇/聚乙烯吡咯烷酮/碘复合水凝胶的制备与性能
宫宇宁,王 奇,王红蕾,关 爽
(长春工业大学化学与生命科学学院,长春130021)
碘是世界公认的安全可靠的杀菌剂,同时也是生物必需的微量元素. 由于具有抗菌谱广及对组织毒性小的优点,碘被广泛应用于临床、卫生、日常生活、农牧养殖业和饮用水等领域. 用碘制成的各类杀菌消毒药品,如碘酊和碘伏等,广泛应用于人体皮肤、黏膜表面、伤口创面及外科器械等的杀菌消毒. 碘伏是碘与表面活性剂的不定型络合物,其中聚乙烯吡咯烷酮碘络合物(PVP-I)作为一种被广泛使用的碘伏,其杀菌效力及杀菌谱与碘相当,同时克服了碘溶解度低、不稳定、易产生过敏反应、对皮肤和黏膜有刺激性及高浓度有毒性等缺点. 与碘酊相比,PVP-I克服了碘酊使用浓度高、刺激性强、对皮肤有灼伤作用、不稳定易挥发、易染黄色及适用范围窄等不足,同时又保留了广谱杀菌性能,在一定浓度下可抑制细菌的繁殖,且对细菌、芽孢、真菌及病毒都能灭杀. 因此近30年来,PVP-I已基本上取代了碘酒和其它含氯含汞杀菌消毒剂[1~7].
PVP-I通过将碘络合在两个吡咯烷酮环的两个羰基氧原子间,可以在水中不断释放出游离碘,游离碘直接卤化菌体蛋白质,与蛋白质的氨基结合,破坏菌体的蛋白质和酶,使微生物因发生代谢障碍而死亡,因此PVP-I能够在较长的时间内保持对细菌繁殖的抑制和灭杀[7]. 但由于碘在阳光和高温下容易分解和升华,因此PVP-I需要在室温避光条件下保存,导致其使用受到很大限制.
水凝胶是一类具有三维网络结构的亲水高分子聚合物,其网络结构可以存储大量的水,具有良好的生物相容性和局部缓释能力,广泛应用于药物缓释及伤口敷料等领域[8~10]. 聚乙烯醇(PVA)水凝胶是一种经典的应用范围广泛的水凝胶,具有吸水能力强、毒性低、生物相容性好及强度相对较高等优点,是修复和再生各种组织的热门材料[11,12],可应用于心脏瓣膜[13]、眼角膜置入[14]、软骨组织[15]及伤口敷料[16]等领域. PVA类水凝胶的交联方式通常有低温冷冻等物理交联方式[17~20]及使用引发剂和交联剂等化学交联方式两类[21~24]. 由于化学交联时有可能残留小分子引发剂或交联剂,这些小分子通常具有较强的反应性,从而使水凝胶具有细胞毒性,并且可能影响水凝胶在作为药物载体时对药物的封包性能,因此化学交联的水凝胶的生物相容性比物理交联的水凝胶要差.
本文将聚乙烯吡咯烷酮碘络合物(PVP-I)与PVA 水凝胶相结合,通过调控PVA 与PVP-I 的比例及改变冷冻时间和冷冻-解冻循环次数等条件,不使用引发剂和交联剂,制备出可调控力学性能的物理交联水凝胶,其保持了水凝胶的生物相容性. 研究了PVA/PVP-I复合水凝胶的微观形貌、水凝胶中碘的释放及水凝胶的抑菌性. 与碘伏消毒液相比,PVA/PVP-I复合水凝胶实现了碘的缓释,延长了消毒持续时间,拓宽了碘类消毒剂的应用范围.
1 实验部分
1.1 试剂与仪器
聚乙烯醇1788(PVA,分析纯),天津市光复精细化工研究所;聚乙烯吡咯烷酮碘络合物(PVP-I,分析纯)、牛肉膏(生物纯)、琼脂(生物纯),上海阿拉丁生化科技股份有限公司;氯化钠(分析纯),北京化工厂;胰蛋白胨(生物纯),国药集团化学试剂有限公司;碘伏消毒液,山东利尔康医疗科技股份有限公司. 实验用水均为去离子水.
AGS-X型电子万能材料试验机,日本岛津公司;Cary 5000型紫外-可见近红外分光光度计,美国安捷伦科技有限公司;Smartlab 型X 射线衍射(XRD)仪,日本理学株式会社,工作电压40 kV,工作电流40 mA,2θ扫描范围为10°~50°,扫描速率5°/min;JSM-7610F 型高分辨热场发射扫描电子显微镜(SEM),日本电子株式会社;IS50 型傅里叶变换红外光谱(FTIR)仪,美国Nicolet 公司,扫描范围400~4000 cm−1;ZF-20D型暗箱式紫外分析仪,巩义市予华仪器有限责任公司.
1.2 PVA/PVP-I复合水凝胶的制备
将一定量的聚乙烯醇粉末溶于90 ℃去离子水中,配制一定质量分数的PVA溶液;冷却至室温后,将一定量的PVP-I溶于上述溶液中,混合搅拌均匀;将混合溶液在40 ℃水浴超声30 min除去气泡,待气泡除净后灌注在厚度为2 mm的模具中,并将模具于-15 ℃下冷冻12~72 h;取出模具,在室温条件下自然解冻,即制得PVA/PVP-I复合水凝胶.
1.3 PVA/PVP-I复合水凝胶的拉伸力学性能测试
使用电子万能材料试验机测试PVA/PVP-I复合水凝胶的拉伸力学性能,固定十字头速率,拉伸速度为50 mm/min. 将样品预切成40 mm长、4 mm宽、2 mm厚的片状哑铃形.
通过下式计算应力值(σ,kPa):

式中,F(N)是负载力,A0(m2)是样品的初始横截面积. 通过下式计算拉伸应变(ε,%):

式中,l(cm)是拉伸变形后样品的长度,l0(cm)是拉伸之前样品的长度.
1.4 PVA/PVP-I复合水凝胶的形态研究
使用高分辨热场发射扫描电镜观察水凝胶的形态结构. 将冷冻干燥后的PVA/PVP-I复合水凝胶样品在液氮中淬冷30 s后脆断,将脆断截面喷金1 min,观察PVA/PVP-I复合水凝胶的微观结构.
1.5 PVA/PVP-I复合水凝胶的体外碘释放
将5 g PVP-I质量分数为1.25%的PVA/PVP-I复合水凝胶浸泡在50 mL去离子水中,并置于37 ℃的恒温水浴摇床中进行培养,振荡速度为50 r/min;经一定时间后,移取1 mL溶液,通过紫外-可见近红外分光光度计测量释放介质中的碘浓度,绘制碘释放曲线.
1.6 PVA/PVP-I复合水凝胶与碘伏消毒液的稳定性对比
将相同碘含量的PVA/PVP-I复合水凝胶和碘伏消毒液分别灌注在石英片制成的模具中,置于暗箱式紫外分析仪中,用波长365 nm的紫外光照射48 h,观察其褪色情况.
1.7 体外抑菌性能
根据GB/T20944.1-2007 标准[25],采用抑菌圈法评价材料的抑菌性. 将枯草芽孢杆菌、大肠杆菌接种到固体平板培养基(胰蛋白胨1%,氯化钠1%,酵母粉0.5%,琼脂粉2%)上,涂布均匀. 将PVA/PVP-I复合水凝胶样品(直径为1 cm、厚度为2 mm的圆柱)置于平板培养基上适宜位置,于37 ℃恒温培养24 h(以纯PVA水凝胶为空白组). 培养结束后检查样品周围是否有抑菌圈并测量拍照.
2 结果与讨论
2.1 红外光谱分析
图1给出PVA,PVP-I 及复合水凝胶的FTIR 谱图,其中谱线a为固体粉末状PVP-I 的红外光谱图,1656 cm−1处为羰基的特征峰;谱线b为PVA水凝胶的红外光谱图,3264 cm−1处为—OH的伸缩振动峰;谱线c为PVP-I 与PVA 质量比为1.25∶10 的复合水凝胶的谱线,其中1656 cm−1处PVP-I羰基特征峰的强度明显下降,3264 cm−1处PVA中羟基伸缩振动峰的强度和宽度都有所增加. 这些结果表明,在复合水凝胶中,PVA 的羟基和PVP-I 中PVP 的羰基形成了分子间氢键.
2.2 PVA/PVP-I复合水凝胶的力学性能
当敷料覆盖在伤口表面时,复杂多变的外界环境和不同部位的运动强度对伤口和敷料都会造成一定的冲击,因此伤口敷料水凝胶需要具有一定力学性能对伤口部位进行保护,防止对伤口产生二次伤害. 为了制备出符合力学强度需求的水凝胶,对水凝胶的单体比例和制备方式进行了深入研究.
由图2 可见,当PVP-I 含量(质量分数)为1.25%时,随着PVA 的含量(质量分数)由5%增加到20%,凝胶的力学强度从58 kPa 提升至1.03 MPa,拉伸形变量从312%提升至482%,弹性模量从2.632 kPa提升至24.117 kPa. 研究结果表明,随着PVA含量的增加,PVA链段自身缠绕,增大了邻近分子链之间的接触,分子间氢键密度增大,使得凝胶内的交联密度逐渐增大,凝胶的力学强度得到了很大的提升.

Fig.1 FTIR spectra of PVP⁃I(a),PVA(b)and PVA/PVP⁃I hydrogel(c)

Fig.2 Mechanical properties of PVA/PVP⁃I hydrogel[w(PVP⁃I)=1.25%,freeze at-15 ℃for 24 h]with different contents of PVA
由图3 可见,PVA 含量为10%的纯PVA 水凝胶在−15 ℃冷冻24 h 后力学强度和形变量分别为63 kPa和302%. 而在相同PVA含量和冷冻时间下,随着PVP-I含量的增加,由于PVA中的羟基和PVP-I中的羰基间逐渐形成大量的氢键,凝胶的力学强度和形变量都显著提升. 但随着PVP-I的继续加入,凝胶力学强度提升的幅度逐渐降低. 这是因为较低含量的PVP-I可以促进与PVA网络形成氢键,而过量的PVP-I使得PVA网络交联密度过大,凝胶网络变硬变脆,导致网络力学强度提升的幅度逐渐降低.
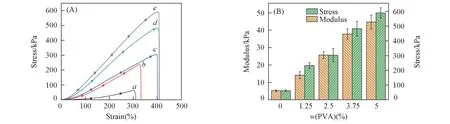
Fig.3 Mechanical properties of PVA/PVP⁃I hydrogel[w(PVA)=10%,freeze at-15 ℃for 24 h]with different contents of PVP⁃I
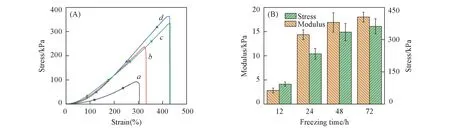
Fig.4 Mechanical properties of PVA/PVP⁃I hydrogels[w(PVA)=10% , w(PVP⁃I)=1.25%, freeze at-15 ℃]with different freezeing time

Fig.5 Mechanical properties of PVA hydrogel[V(PVA)=10%,freeze at-15 ℃]and PVA/PVP⁃I hydrogel[w(PVA)=10%,w(PVP⁃I)=1.25%,freeze at-15 ℃]with different freeze⁃thaw cycles
由于PVA低温结晶的特性,冷冻时间与冷冻-解冻循环次数对PVA水凝胶的力学强度有着显著的影响[26],图4给出在不同冷冻时间的条件下,PVA/PVP-I复合水凝胶力学强度的变化情况. 图5给出不同冷冻循环次数[单次冷冻24 h,冷冻-解冻1次(24 h×1)、单次冷冻12 h,冷冻-解冻2次(12 h×2)、单次冷冻8 h,冷冻-解冻3次(8 h×3)和单次冷冻6 h冷冻-解冻4次(6 h×4)]对纯PVA水凝胶和PVA/PVP-I复合水凝胶力学性能的影响. 随着冷冻时间的延长,交缠的PVA分子链自身及与PVP-I分子链之间形成了分子内/分子间氢键,升温解冻后物理交联的结构得到保存,使得凝胶的强度逐渐增大. 而冷冻-解冻循环过程中会反复增强这种物理交联结构的密度,形成PVA结晶. 在冷冻-解冻循环次数较少时,与纯PVA水凝胶相比,PVA/PVP-I复合水凝胶内PVA分子链自身及与PVP-I分子链间产生的分子内/分子间氢键大幅度提升了水凝胶的力学强度. 但在反复冷冻-解冻循环次数逐渐增多后,PVA/PVP-I复合水凝胶内PVA 分子链自身及其与PVP-I分子链间产生的分子内/分子间氢键不再是提升凝胶力学强度的主要因素,随着PVA半结晶的粒径直径逐渐增大,相当于增加了交联点的强度,使得凝胶的力学强度逐渐增大,导致纯PVA水凝胶和PVA/PVP-I复合水凝胶的力学性能逐渐接近.
2.3 X射线衍射分析
PVA 为结晶聚合物,而且PVA 的结晶会显著提高凝胶的力学强度. 图6 中,纯PVA 水凝胶在2θ=19.28°处的尖锐峰为PVA 的特征峰;PVP-I 为非晶聚合物,随着PVP-I的加入,复合凝胶在2θ=19.80°处出现了明显的衍射峰,而且随着复合凝胶的冷冻-解冻循环次数增加,该衍射峰强度逐渐增加.PVP-I 的加入抑制了PVA 的结晶,从而使结晶程度降低,而随着冷冻-解冻循环次数增加,PVA的结晶度逐渐增加. 说明PVP-I的加入使PVA的结晶结构发生变化,在较低的冷冻-解冻循环次数下,影响复合凝胶强度的主要因素为PVA 分子链自身及与PVP-I分子链间产生的分子内/分子间氢键,随着冷冻-解冻循环次数的增加,PVA 的结晶程度逐渐成为影响复合凝胶强度的主要因素.
2.4 PVA/PVP-I复合水凝胶的形态
图7(A)为PVA 固含量为10%,冷冻时间为24 h 的纯PVA 水凝胶的SEM 照片;图7(B)为PVA 固含量为10%,PVP-I 固含量为1.25%,冷冻时间为24 h 的复合水凝胶的SEM 照片. 可见,冻干后的纯PVA水凝胶的平均孔径约为1~10 μm,而复合水凝胶的平均孔径约为0.5~2 μm,表明随着PVP-I的加入,PVP-I的羰基与PVA的羟基之间形成了大量的氢键,导致水凝胶内部交联密度增大,这种致密的网络结构能有效提升水凝胶的力学性能.

Fig.6 XRD patterns of PVA hydrogel[w(PVA)=10%,freeze at -15 ℃for 24 h], PVA/PVP⁃I hydro⁃gels[w(PVA) =10%, w(PVA/PVP ⁃ I) =1.25%,freeze at -15 ℃] with different freeze⁃thaw cycles(b—e)and PVP-I powder(f)

Fig.7 SEM images of PVA hydroge(A)and PVA/PVP⁃I hydrogel(B)
2.5 PVA/PVP-I复合水凝中碘的释放及稳定性
图8 示出了PVA/PVP-I 复合水凝胶浸泡在水中时碘的释放情况. 随着浸泡时间的延长,溶液在286 nm处的吸收峰(碘的特征吸收峰)逐渐增强,浸泡6 h后,碘的释放量达到78%,说明复合水凝胶的网络结构能够有效控制碘的释放,延长消毒时间.
由于碘的光照稳定性差,使得碘类消毒剂的使用范围受到了诸多限制,如需要在室温下避光保存等. 图9给出PVA/PVP-I复合水凝胶(A)与碘伏消毒液褪色程度(B)的对比照片. 可见,在356 nm波长的紫外灯下照射48 h后,复合水凝胶的褪色程度明显弱于碘伏消毒液的褪色程度. 表明复合水凝胶网络可以有效阻止紫外线对碘的分解,拓宽了碘类消毒剂的应用范围.

Fig.8 Controlled release of iodine from PVA/PVP⁃I hydrogels after 30 min(a), 1 h(b), 2 h(c) and 6 h(d),PVP(e)and I2(f)
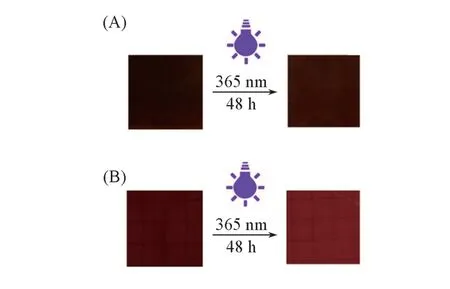
Fig.9 Discoloration under UV 365 nm of PVA/PVP⁃I hydrogel(A)and povidone⁃iodine disin⁃fectant(B)
2.6 抑菌性能
图10示出了PVA/PVP-I复合水凝胶对大肠杆菌和枯草芽孢杆菌生长的抑制结果. 由图10可以看出,空白组在培养皿中无抑菌圈,样品表面和周围的细菌生长繁殖如常情况与其它区域无差别;而实验组周围都有明显的抑菌圈,说明复合水凝胶具有同碘伏消毒液一样的抑菌性,而且可以在较长时间内保持对细菌生长的抑制,这对拓宽碘类消毒剂的应用有非常大的意义.

Fig.10 Photographs of bacterial colony against E. Coli(A,B)and B. subtili.(C,D)
3 结 论
通过改变PVA和PVP-I的含量、冷冻时间及冷冻-解冻循环次数,制备出了可满足多种力学强度的伤口敷料复合水凝胶,研究了复合水凝胶中各组分之间的相互作用. 结果表明,随着PVA和PVP-I含量的增大,复合水凝胶内部的交联密度增大,水凝胶的力学强度增大. 随着冷冻时间和冷冻-解冻循环次数的增加,水凝胶内PVA的结晶程度增加,水凝胶的力学强度也增大. PVA/PVP-I复合水凝胶内部的网络结构可以有效地控制水凝胶内碘的释放. 与常用的碘伏消毒液相比,PVA/PVP-I复合水凝胶内部的碘更加稳定,在紫外线照射下分解的速度更慢. 抗菌测试结果表明,PVA/PVP-I复合水凝胶在一段时间内对大肠杆菌和枯草芽孢杆菌的生长和繁殖有明显的抑制. 这种具有可控的力学强度和抗菌性且可以降低碘分解速度的PVA/PVP-I复合水凝胶可拓宽碘类消毒剂的应用领域,并且为抗菌水凝胶的制备提供了新思路.

