微动力负压护创敷料治疗糖尿病手部感染一例
陈存仁 林璐 魏伟平 张燕 陈开宁
患者,男,69岁,因“发现血糖升高半年余,右手破溃1周”于2017年10月1日入院。半年余前患者因夜尿增多至当地医院查空腹血糖15.45 mmol/L,完善相关检查后诊断为“2型糖尿病”,予“格列齐特、二甲双胍”治疗1月余后至我院就诊,测糖化血红蛋白8.1%,改为“二甲双胍、西格列汀”治疗,患者自述血糖控制良好后便停用上述药物,已近3个月未服药。1周前发现右手中指与无名指间手背处有脓点逐渐增大直至出现破溃流脓,右手肿胀疼痛,至当地医院就诊,给予“抗感染”治疗无好转,为求进一步诊治收入我科。既往史无特殊。体格检查:体温36.5 ℃,呼吸 18次/分,脉搏76次/分,血压132/78 mmHg, 心、肺、腹体格检查无异常。右手中指及无名指间手背侧有一约1.5 cm×1.5 cm的溃疡面,有黄色脓性分泌物,伴恶臭,右手肿胀明显,皮肤颜色发红,皮温增高,伴有疼痛(图1A)。辅助检查:入院后查空腹血糖6.4 mmol/L(3.9~6.1 mmol/L,括号内为正常参考值范围,以下相同)、糖化血清蛋白1.96 mmol/L(1.65~2.15 mmol/L);血常规:白细胞计数14.5×109/L(3.5~9.5×109/L)、中性粒细胞百分比71.7%(40.0%~75.0%);白蛋白32.6 g/L(40.0 g/L~55.0 g/L),血肌酐63 μmol/L(57~97 μmol/L)。脓性分泌物培养结果提示金黄色葡萄球菌感染,对头孢他啶、克林霉素、万古霉素、利奈唑胺、左氧氟沙星敏感。入院后给予患者胰岛素控制血糖、头孢他啶抗感染治疗,同时给予清创引流,生理盐水冲洗,安尔碘消毒后用钝性清创,沿着破溃口将坏死组织清除,取深部脓性分泌物做培养,然后用纱布将分泌物擦拭干净,清创后可见溃疡面约2.0 cm×1.5 cm,未累及肌腱,形状不规则,渗液较多(图1B),给予微动力负压护创敷料覆盖(图1C)。采用指压法判断敷料的饱和度,敷料饱和后给予更换,4天后第一次换敷料,伤口肉芽新鲜,颗粒感明显(图1D)。继续按上述方法共更换敷料3次,23天后患者的伤口完全愈合,同时手指活动无任何影响(图1E)。
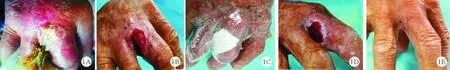
图1 患者手部伤口治疗前后情况(A:入院时;B:清创后;C:微动力负压敷料治疗;D:第一次治疗后;E:伤口愈合)
讨 论
糖尿病足溃疡可导致截肢甚至危及生命[1],而糖尿病手部感染的危害同样不能忽视,因上肢的血供较下肢丰富,感染扩散速度更快,病情进展更迅猛,治疗不及时会增加截肢风险[2]。糖尿病手部感染因其血供丰富,往往渗液量较多,若不能及时控制渗液,不仅会导致细菌滋生、感染加重,而且易形成生物膜,阻碍正常细胞生长[3-4]。伤口在清创后,除了有效抗生素治疗外,严格控制渗液才能及时控制感染。封闭负压引流术能够广泛引流创面的渗液,其疗效已得到公认[5],但是由于不易于手部固定,且可能损伤皮肤[6],限制了其临床应用,而目前使用较多的泡沫型敷料吸水功能有限。微动力负压护创敷料是创面治疗的新型敷料,临床上使用新型材料将创面覆盖后再用医用透明贴膜密封,使之完全贴合,在创面局部形成一个相对封闭的环境,当新型材料因吸收创面渗液而缓慢膨胀后,贴膜也逐渐被抬高,产生的密闭空间逐渐增大,局部形成相对的真空环境,产生“虹吸效应”。海绵体局部吸附腔对创面及其深部软组织产生微负压吸引作用,类似像注射针筒的“唧筒效应”,相较于藻酸盐[8]、泡沫敷料等,其在吸收渗液、减少细菌负荷、控制感染、破坏生物膜的形成、减轻水肿、创造湿性环境及改善微循环等方面更具优势,而且可作为封闭式负压的一个很好的补充。
本例患者在有效清创后应用该敷料,感染得到及时控制,伤口开始出现新鲜肉芽。随着感染持续控制,后续进入肉芽生长及上皮爬行期,这两个时期均需按“湿性愈合”的理念选择敷料。微动力负压护创敷料采用特种聚乙烯醇医用生物材料的三层复合结构,中间是锁液层,具有“水库样蓄液”性能,两面是皮膜层,可以保持湿润,但含液量很低,可保持创面湿润和密封的微环境,为再上皮化提供一个适宜的愈合环境[7]。本例患者在控制感染后进入爬皮期后继续应用该敷料,促进上皮生长,最终实现伤口的愈合。
微动力负压护创敷料在烧伤科已广泛应用于烧伤皮肤的创面治疗,但在治疗糖尿病手部损伤中的应用较少。 微动力负压技术作为一种伤口、创面护创技术的革新,在治疗本例患者的糖尿病手部感染中效果显著,且其临床操作相较于其他传统技术和产品更加方便,不仅缩短了患者的住院时间,也大大减少了医务人员的负担,可作为治疗糖尿病手部感染的新方法。

