荷电下的4,4′-二氨基二苯醚印迹吸附
马明明,杜 茹,楚 楚
西安工程大学环境与化工学院,陕西西安710048
考察吸附过程中的等温吸附模型不仅可以深入了解吸附剂对吸附质的捕获能力,还可以预测具有经济价值的吸附平衡,使吸附更有效、更实惠,并能提高材料的相关性能.因此,对复合吸波材料制备过程中所涉及的吸附现象进行研究,有助于进一步改善材料的电磁波吸收性.常见的吸附模型有Langmuir、Brunauer-Emmett-Teller(BET)、Freundlich、Dubinin-Radushkevich(D-R)、Temkin和Henry等.这6种吸附模型都有各自的适用条件.Langmuir模型假定吸附剂的表面被单分子覆盖,所有的吸附位点相同并且能量守恒,且该吸附剂结构是均匀的[1];Freundlich等温吸附方程是建立在表面能量分布不均一基础上的经验模型,多用于溶液吸附[2].尽管BET等温吸附模型认为固体表面均匀,但却是多层吸附.D-R等温模型以吸附势理论为基础,吸附质以填充的方式贮存在微孔内,真实反映吸附质在微孔中的吸附机理[3].Temkin模型主要考虑吸附剂与溶液中吸附质之间的相互作用力对整个吸附行为和过程的影响[4].Henry等温吸附方程阐述的是吸附质在吸附剂上的线性分配过程.
荷电量是物质在电化学合成过程中的基本参数,可通过循环曲线积分面积获知其大小.按照法拉第定律,电化学反应中物质荷电量Q应与发生反应的物质的量呈正比,因而参与电化学反应的反应物质浓度可用荷电量表示.然而却未见用荷电量研究吸附模型的相关报道.由于采用2次电聚合方法合成的新型吸波材料4,4′-二氨基二苯醚分子印迹聚合物(4,4′-diaminodiphenyl ether molecularly imprinted polymer,4,4′-ODL-MIP)-聚4,4′-二氨基二苯醚(poly 4,4′-diaminodiphenyl ether,P-4,4′-ODL)(4,4′-ODL-MIP-P-4,4′-ODL)[5]的荷电量对其电磁波吸收效率影响较大,而该复合材料的荷电量大小与第2次电聚合过程中4,4′-ODL-MIP印迹吸附4,4′-ODL密切相关,因此,研究4,4′-ODL-MIP对4,4′-ODL的印迹吸附模型及印迹吸附机制十分必要.鉴于此,本研究基于温度为298 K时复合材料的荷电量,拟合Langmuir、BET、Freundlich、D-R、Temkin和Henry 6种吸附等温模型方程,从而确定4,4′-ODL-MIP吸附4,4′-ODL的类型与特点.根据273.15~313.15 K内不同吸附温度下复合材料的荷电量,计算复合材料相应印迹吸附结合常数,以及印迹吸附过程中的焓变ΔH、吉布斯自由能ΔG、熵变ΔS等热力学参数.通过荷电量与吸附时间的拟合方程,明确 4,4′-ODL-MIP印迹吸附4,4′-ODL的动力学方程,由此获得的印迹吸附模型、热力学和动力学参数,可揭示4,4′-ODL-MIP印迹吸附4,4′-ODL的内在规律.
1 实 验
1.1 试剂与仪器
4,4′-二氨基二苯醚(4,4′-diaminodiphenyl ether, 4,4′-ODL)为分析纯,购自山东西亚试剂有限公司;丙烯酰胺为分析纯,购自天津市红岩化学试剂厂;石墨烯粒径为0.5~2.0 μm,厚度为0.8~1.2 nm,购自杭州格蓝丰纳米科技有限公司;无水乙醇为分析纯,购自天津市科密欧化学试剂有限公司;胶水为AB胶,购自广东爱必达胶粘剂有限公司;2B铅笔购自中国第一铅笔有限公司;CHI610D型电化学工作站购自上海辰华仪器厂;KQ5200DE超声波清洗器购自昆山市超声仪器有限公司;数显恒温水浴锅购自上海一恒科学仪器有限公司.
1.2 4,4′-ODL-MIP的制备
1.2.1 石墨烯-铅笔芯的制备
根据文献[6]的方法处理铅笔芯.具体操作步骤为:① 将处理过的铅笔芯电极(pencil electrode, PEC)浸入质量浓度为7.5 mg/mL的石墨烯水分散液10 min,取出干燥;② 再浸入7.5 mg/mL石墨烯石蜡分散液10 min,取出晾干,用称量纸抛光;③ 将铜丝缠绕在已处理的铅笔芯一端并用胶水固定(导电体长度固定为1.0 cm),构成石墨烯-铅笔芯电极(graphene-modified pencil electrode,G-PEC);④ 为了除去电极表面的杂质,将制备好的G-PEC 用无水乙醇超声清洗5 min,晾干后即可使用.
1.2.2 4,4′-ODL-MIP的制备
将制备好的G-PEC、饱和甘汞电极、铂电极分别与工作电极、参比电极、对电极端口相连,然后共同置于含有4,4′-ODL(5.0×10-3mol/L)、丙烯酰胺(2.0×10-2mol/L)的磷酸盐缓冲溶液(pH=6.81)中,以0.1 V/s的扫描速率在-0.3~1.0 V电位范围内循环扫描12圈后,取出 G-PEC,并用二次蒸馏水清洗数次;然后,再将其置于无水乙醇中超声振荡清洗5 min,在 G-PEC表面可获得4,4′-ODL-MIP.
1.3 4,4′-ODL-MIP-P-4,4′-ODL复合材料的制备
以合成的4,4′-ODL-MIP修饰G-PEC作为工作电极,电解液为含5.0×10-3mol/L 4,4′-ODL的磷酸盐缓冲溶液(pH=6.81),按1.2.2节的电化学条件进行第2次电化学聚合,合成4,4′-ODL-MIP-P-4,4′-ODL.
1.4 吸附等温模型实验
将工作电极为4,4′-ODL-MIP修饰的G-PEC,置于含有一定浓度4,4′-ODL(1.0×10-3~5.0×10-3mol/L)的磷酸盐缓冲溶液(pH=6.81)中,在温度为298 K下,测定不同印迹吸附时间下,4,4′-ODL-MIP印迹吸附4,4′-ODL对应的复合材料荷电量Q,直至达到吸附饱和平衡,每组实验均平行做5次,拟合以荷电量表示的吸附等温方程.
1.5 吸附动力学实验
在298 K下,测定并计算第2次电聚合过程中,在50~300 s内,4,4′-ODL-MIP-P-4,4′-ODL荷电量Q的变化,由此模拟动力学方程.
1.6 吸附热力学实验
测定并计算第2次电聚合过程中,在反应温度分别为273.15、283.15、293.15、303.15和313.15 K,吸附平衡时间为160 s时,合成的复合吸波材料4,4′-ODL-MIP-P-4,4′-ODL荷电量Q的变化.
2 结果与讨论
2.1 六种等温吸附模型拟合
2.1.1 Langmuir吸附模型
电化学聚合条件下,Langmuir模型的方程式为
(1)
其中,Qe为平衡荷电量(单位:C);Qt为t时刻的荷电量(单位:C);KL为Laugmuir模型下的结合常数(单位:s).以t/Qt为纵坐标对时间t作图,结果如图1.根据拟合方程t/Qt=0.19t+(18.41±0.14),R2=0.992,可计算出KL=97.79 C2/s,Qe=5.31×10-3C.实验测得的最佳荷电量为3.32×10-3C,比拟合数据小的原因是4,4′-ODL-MIP中的结合位点并非绝对等价,且4,4′-ODL-MIP中存在少数非特异性印迹结合位点,因此,降低了其对4,4′-ODL分子亲和力[7].

图1 Laugmuir模型的拟合曲线
2.1.2 Freundilich吸附模型
Freundlich模型的方程式为
(2)
其中,Qt为t时刻的荷电量(单位:C);KF为Freundlich模型下的结合常数;n为吸附强度,是常数.图2是以lgQt为纵坐标对lgt作图的线性曲线,线性方程lgQt=0.45lgt-(3.39±0.03),R2=0.963.由此计算出KF=3.00×10-4,n=2.22,n>1.1/n值界于0.1~0.5,说明4,4′-ODL-MIP对4,4′-ODL的吸附容易且结合较强,因而在研究范围内属于优惠吸附[8].

图2 Freundlich模型的拟合曲线
2.1.3 Dubinin-Radushkevich吸附模型
D-R等温模型不仅是建立在微孔填充理论的吸附等温模型上,且其可对吸附过程的类型和吸附自由能进行估算[9],方程式为
lnQe=lnQm-βε2
(3)
ε=RTln(1+1/Ce)
(4)
(5)
其中,Qm为理论最大荷电量;β为D-R常数(单位:mol2/kJ2),与吸附平均自由能有关;ε为波拉尼电位(单位:J/mol);T为反应温度(单位:K);ce为溶液平衡浓度(单位:mol/L);R为摩尔气体常数,本研究取R=8.314 J/(mol·K);Ea为活化能(单位:kJ/mol).
图3是实验数据对D-R模型的拟合曲线,其线性方程为lnQe=-0.01ε2+(5.11±0.01),R2=0.991.由于平均吸附自由能E可确定吸附机制,当|E|为1~8 kJ/mol 时,属于物理吸附;当|E|为8~16 kJ/mol 时,属于离子交换或表面络合;当|E|为20~40 kJ/mol时,属于化学吸附[9].计算出这一吸附自由能E=6.31 kJ/mol,因此,4,4′-ODL被4,4′-ODL-MIP吸附是物理吸附的D-R模型.

图3 D-R模型的拟合曲线
2.1.4 Temkin吸附模型
Temkin模型主要是描述吸附质的吸附热随覆盖度增加而线性下降,Temkin模型方程[10]为
Qe=A(lnKT)+A(lnce)
(6)
其中,KT为最大结合能的平衡常数;A为温度和吸附体系性质有关的无因次常数,与吸附热有关.其余参数同2.1.3节.
图4是Qe与lnce的关系曲线,对应的线性方程为Qe=0.30 lnce+(2.23±0.02),R2=0.944.计算出A=0.30.根据文献[11],A值较小说明吸附剂表面与吸附质的作用较弱,因此可以推断4,4′-ODL-MIP对4,4′-ODL的吸附不可能是化学吸附,这与2.1.3节的结果一致.
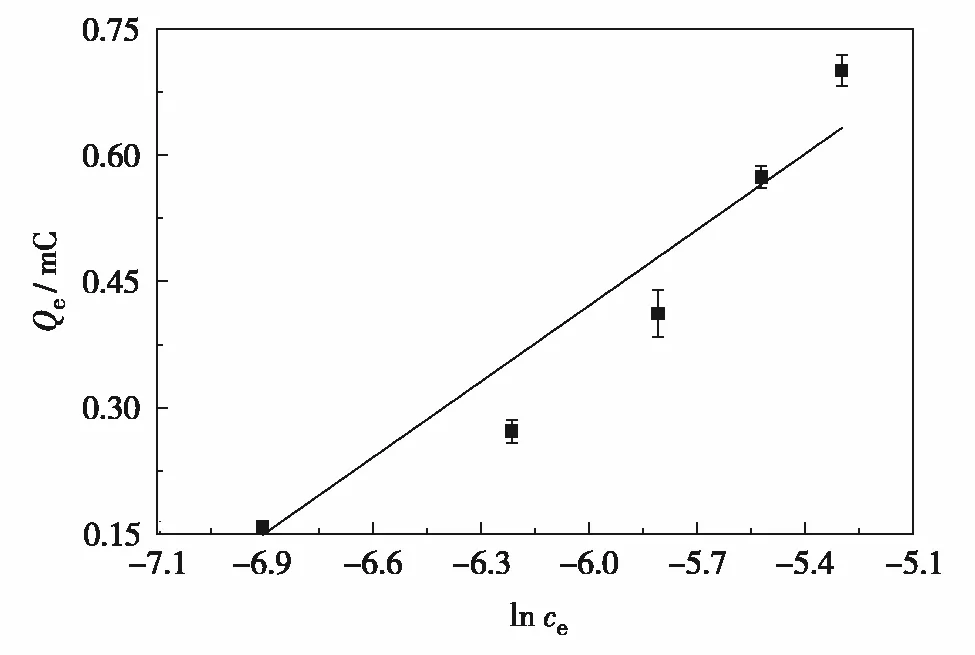
图4 Temkin模型的拟合曲线
2.1.5 Henry吸附模型
Henry模型方程[12]为
Qe=KHce+c
(7)
其中,KH为相间线性吸附分配系数.
图5是Qe与ce的拟合曲线,其线性方程为Qe=0.14ce-3×10-5,R2=0.994,因此,4,4′-ODL-MIP对4,4′-ODL实施的是线性Henry吸附.
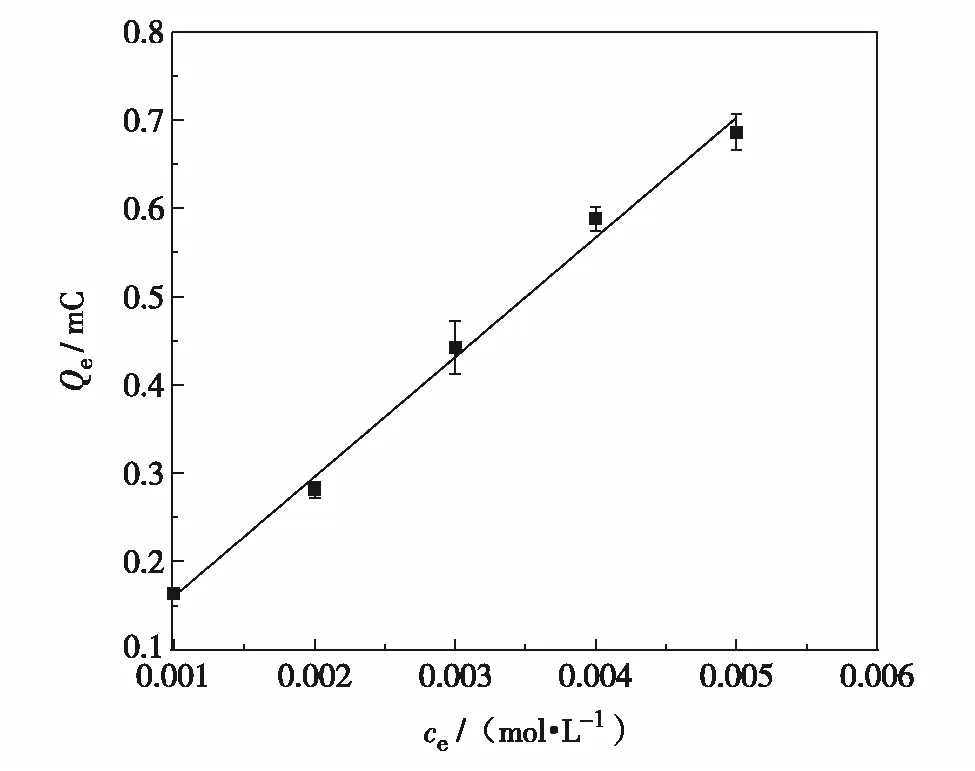
图5 Henry模型的拟合曲线
2.1.6 BET吸附模型
BET模型方程[12]为
(8)
可简化为
(9)
其中,K为平衡常数.
图6是实验数据对BET模型的拟合曲线,其线性方程为ce/Qe(1-ce)=(231.46±2.36)ce+(6.17±0.02),R2=0.668,线性误差大.由此可以看出,4,4′-ODL-MIP对4,4′-ODL的吸附不可能是多层吸附.

图6 BET模型的拟合曲线
2.2 吸附动力学机理
考察了在反应时间为50~300 s内4,4′-ODL-MIP吸附4,4′-ODL的荷电量变化.吸附反应的动力学模型方程有准1级、准2级、Elovich和颗粒内扩散方程[13-14],对应的数学方程分别为
准1级动力学方程为
ln(Qe-Qt)=lnQe-k1t
(10)
准2级动力学方程为
(11)
Elovich方程为
(12)
颗粒内扩散方程为
Qt=k3t0.5+C
(13)
其中,Qe和Qt分别为平衡荷电量和t时刻的荷电量(单位:C);k1为准1级模型的动力学吸附速率常数(单位:s-1);k2为准2级模型的动力学吸附速率常数(单位:C-1·s-1);k3为颗粒内扩散速率常数(单位:C/s0.5);a和b为吸附常数;C为边界常数,其值与边界层对吸附的影响有关.将实验数据分别代入上述4种模型方程进行拟合,拟合参数见表1.由表1可知,Elovich模型的R2=0.93,线性较差,说明4,4′-ODL-MIP对4,4′-ODL的吸附不能用这种动力学模型进行描述,即其吸附过程不存在化学吸附.因此,4,4′-ODL-MIP对4,4′-ODL的吸附反应中存在受液膜和颗粒内扩散同时控制的因素.

表1 四种模型下动力学参数
2.3 吸附热力学机理
在吸附温度范围为273.15~313.15 K内,考察了不同温度下4,4′-ODL-MIP吸附4,4′-ODL的荷电量变化.吸附过程中的ΔS、ΔH和ΔG等参数的计算如式(14)至式(16)[15]:
ΔG=ΔH-TΔS
(14)
(15)
(16)
其中,本研究设R=8.314 J/(mol·K);Kd为热力学平衡常数;c(4,4′-ODL)=5.00×10-3mol/L,为4,4′-ODL的最佳浓度;T为体系温度(单位:K).
根据式(16)计算不同吸附温度下的Kd,并将lnKd与1 000/T进行线性拟合,结果如图7.由图7可知线性拟合方程为lnKd=(-2.77±0.04)×(1 000/T)+(7.20±0.01),R2=0.996,其斜率和截距分别为-2.77和7.20,按照式(15)计算可得ΔH=23.01 kJ/mol,ΔS=59.88 J/(mol·K);根据式(14)可计算出不同吸附温度下的ΔG.

图7 ln Kd对1 000/T的拟合曲线
表2为273.15~313.15 K内不同吸附温度对应的热力学参数.由表2可知,在273.15~313.15 K内,Kd随吸附温度的升高而增大,说明升温有助于吸附反应;而ΔG<0,说明此吸附反应是自发过程;ΔH>0,表明吸附反应是吸热过程.实验中4,4′-ODL-MIP对4,4′-ODL的吸附焓变<40 kJ/mol,说明此吸附过程主要是物理吸附;ΔS>0,表明此吸附过程无序度增大.

表2 印迹吸附热力学参数
结 语
本研究以复合材料4,4′-ODL-MIP-P-4,4′-ODL的荷电量为分析指标,研究在第2次电聚合过程中4,4′-ODL-MIP印迹吸附4,4′-ODL的等温吸附模型、热力学和动力学机制.通过对Langmuir、BET、Freundlich、D-R、Temkin和Henry等6种等温吸附模型曲线的拟合分析,结果表明,只有Langmuir、Henry和D-R三种吸附等温模型符合4,4′-ODL-MIP印迹吸附4,4′-ODL特点,说明4,4′-ODL-MIP是通过单层线性物理吸附实现印迹吸附4,4′-ODL的目标.4种动力学反应方程的拟合曲线显示,受颗粒内扩散和液膜扩散同时控制的4,4′-ODL-MIP印迹吸附4,4′-ODL过程更适合由准1级动力学方程描述.在吸附温度范围为273.15~313.15 K,通过计算此印迹吸附反应的ΔG、ΔH和ΔS和Kd变化趋势,发现增加温度更有利于这个自发熵增的印迹吸附过程.因此,4,4′-ODL-MIP-P-4,4′-ODL复合吸波材料的第2次电化学聚合过程中,荷电的4,4′-ODL-MIP印迹吸附4,4′-ODL无需外力推动,即可使溶液中的大量4,4′-ODL分子自发进入4,4′-ODL-MIP印迹空穴,使4,4′-ODL很容易在电极表面完成电化学聚合反应,从而获取具有最大荷电量(即优良电磁波吸收率)的复合材料.

