一种新型酸化缓蚀剂的制备及性能研究
孟文斐, 王立新, 谭晓琼, 郭玉华, 李世文, 董 勇
(玉门油田分公司钻采工程研究院,甘肃 酒泉 735000)
在石油及天然气的开发过程中,尤其当油气田进入开发后期,开发难度越来越大、经济效益越来越低.油井酸化作业是各油田增产增注的重要措施之一,作业时将一定量的酸液以机械加压的方式注入地层中,溶解掉井底附近的堵塞物质和地层岩石中的某些组分,以扩大油流通道,降低油流阻力,从而达到增产增注的目的[1].该方法虽然提高了采油收率,但在酸化施工中,酸的注入可能造成油气井管材和井下金属设备的表面坑蚀、氢脆和失重腐蚀,有时还可能导致井下管材突发性破裂事故,造成严重经济损失,同时被酸溶蚀的金属铁离子又可能对地层造成伤害.因此,为了防止酸液对油管、套管等设备的腐蚀,在酸液中添加缓蚀剂是必不可少的防腐措施.
目前国内外广泛使用的缓蚀剂包括有机胺类、咪唑啉类、复合吡啶类、硫脲、季铵盐、曼尼希碱类缓蚀剂等[2-5].酸化缓蚀剂的缓蚀性能与其分子中的极性基团在碳钢表面的吸附有关,可分为物理吸附和化学吸附两种类型.物理吸附一般是由范德华力或静电引力引起的吸附,使H+难以接近碳钢,从而达到防腐的目的;化学吸附是指缓蚀剂分子直接以配位键的方式吸附在金属表面,缓蚀剂极性基团上的中心原子(如S、N、O和N)含有孤对电子,能与金属原子表面空的d轨道形成配位键,使得缓蚀剂分子吸附在碳钢表面.曼尼希碱分子是一个螯合配位体,它配位原子上的孤对电子进入铁原子(离子)杂化的d-s-p空轨道,形成配位键,生成稳定的具有环状结构的螯合物吸附在金属表面,形成比较完整的疏水保护膜,达到金属缓蚀的目的.曼尼希碱和西佛碱都具有良好的缓蚀性能,因此在分子结构中引入大π键、杂原子和C=N基团,都能够有效地提高缓蚀剂的缓蚀性能.传统的曼尼希碱缓蚀剂以浓盐酸作为催化剂,使醛酮羰基形成质子化的羰基,从而有利于亲核反应的进行,并复配丙炔醇以提高其缓释性能.在该反应中,利用原料乙二胺自身的碱性来催化相关反应;同时,反应原料二甲氨基苯甲醛和苯乙酮之间存在竞争关系,使得反应中同时存在曼尼希反应和西佛碱反应,使产物具有更好的缓蚀效果.
1 实验部分
1.1 主要仪器及试剂
试剂:浓盐酸、氢氟酸、苯乙酮、甲醛溶液、乙二胺、对二甲氨基苯甲醛、乙醇(分析纯,国药集团化学试剂有限公司);十二烷基苯磺酸钠、聚乙二醇200、聚乙二醇400、四正丁基溴化铵、十二烷基磺酸钠(分析纯,中国天津大茂化学试剂厂);
仪器:电子天平(梅特勒-托利多公司XS205DU)、电磁搅拌器(山东菏泽华康标准仪器厂HJ-4)、电热鼓风干燥箱(扬州鸿都电子有限公司DHG-9)、旋转蒸发仪(上海亚荣生化仪器 RE-52A)等.
1.2 反应原理
利用醛胺酮的缩合反应和羰基氨基之间的西佛碱反应,控制反应物的物质的量的比和优化反应条件,生成如下的目标产物.
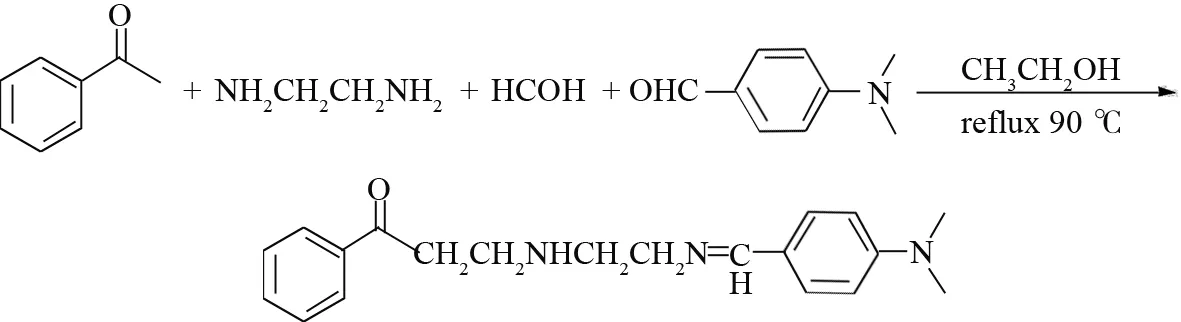
1.3 酸化缓蚀剂的合成
用250 mL三口圆底烧瓶、电磁搅拌器、球形冷凝管、干燥管等组装反应装置,向圆底烧瓶中加入13.7 g苯乙酮、8.5 g对二甲氨基苯甲醛、3.4 g乙二胺、10 g乙醇,然后加入0.5 g十二烷基苯磺酸钠作为两相催化剂,开启搅拌和冷凝水.在搅拌下用恒压滴液漏斗加入37%~40%甲醛水溶液50.1 g,加料完毕后缓慢升温,当温度达到90 ℃时开始回流,反应8 h,切断电源,自然冷却降温.向烧瓶内加入15 g乙醇稀释反应物,搅拌均匀后得到高温酸化缓蚀剂成品.
1.4 缓蚀性能评价方法
按 SY/T 5405-1996《酸化缓蚀剂性能试验方法及评价指标》,采用静态挂片失重法,选用 N80钢片做腐蚀试片,在土酸溶液(12%HCl+3%HF)中加入质量分数为1%的上述合成的酸化缓蚀剂,腐蚀温度为90 ℃,挂片时间4 h,测定试片在酸液中的腐蚀速率,以此来评价合成产物的缓蚀性能.
2 结果与讨论
2.1 合成反应条件的选择
参阅相关文献,初步设定相转移催化剂为十二烷基苯磺酸钠[6-7],加入量为四种原料总质量的0.5%,反应温度为90 ℃,反应时间8 h.分别选取n(苯乙酮)A、n(甲醛)B、n(乙二胺)C、n(对二甲氨基苯甲醛) D 4个影响因素,各选3个水平,在模拟油井酸化的腐蚀环境中进行静态挂片实验,以缓蚀率作为考察指标,确定最佳合成原料物质的量之比.腐蚀条件为:在250 g土酸(12%HCl+3%HF)溶液中,加入2.5 g缓蚀剂,腐蚀温度为90 ℃,腐蚀时间为4 h.选择L9(34)正交表安排实验[8-10],因素水平表见表1.
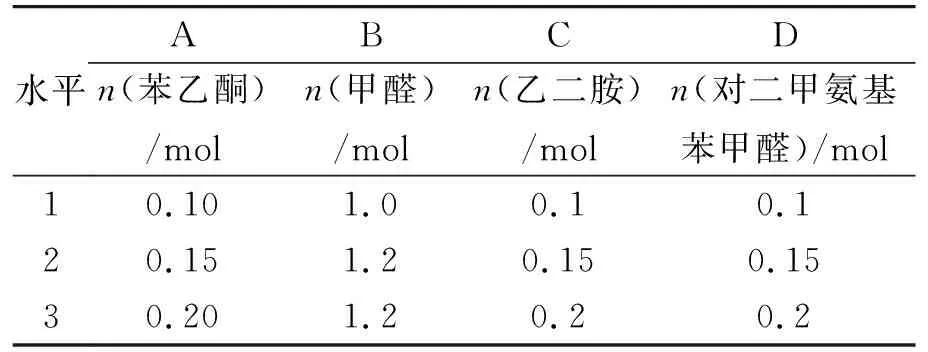
表1 L9(34)因素水平表
具体正交试验条件及结果见表2.
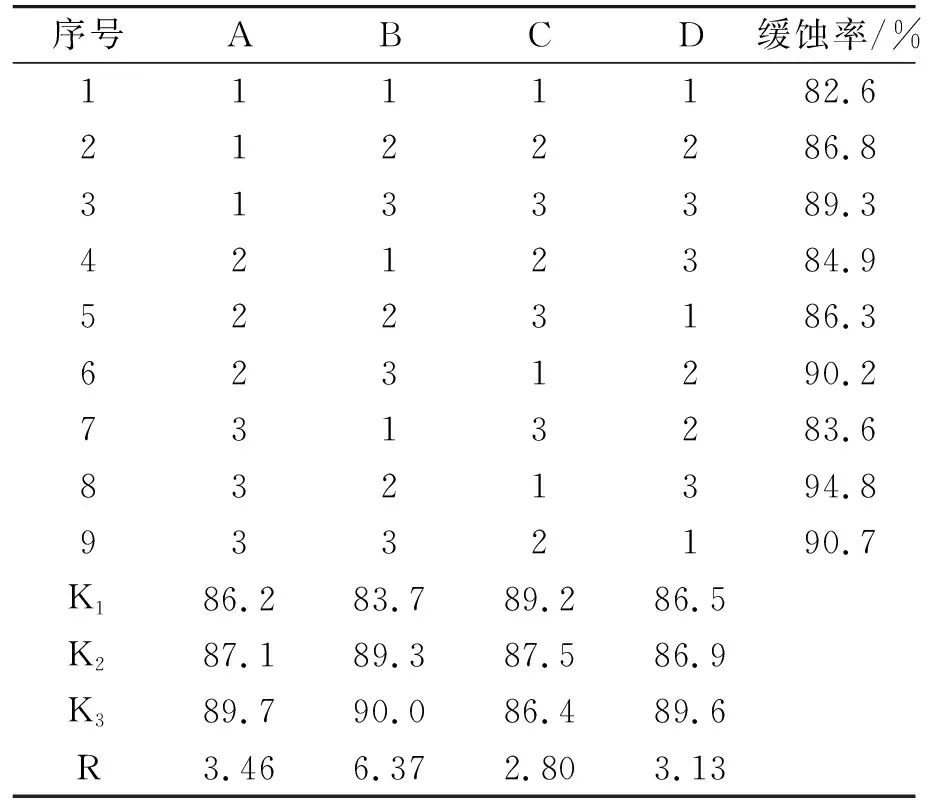
表2 L9(34)具体正交试验
由表2可知,不同的原料配比合成的曼尼希碱缓蚀率有一定的差别,说明原料的摩尔比对合成产物的缓蚀性能有较大影响.对缓蚀性能影响最大的是甲醛,苯乙酮次之,最弱的影响因素为乙二胺,根据以上的分析,确定最佳的合成原料物质的量之比为n(苯乙酮)∶n(甲醛) ∶n(乙二胺) ∶n(对二甲氨基苯甲醛)=1 ∶ 6 ∶ 0.5 ∶ 1.
2.2 反应温度对合成产物缓蚀性能的影响
根据上述正交试验确定的各反应物之间的摩尔比例,通过改变反应温度,在反应8 h后合成了5种不同的酸化缓蚀剂,在模拟油井酸化的腐蚀环境中进行静态挂片实验,φ(缓蚀剂)= 1.0%,腐蚀温度90 ℃,腐蚀时间4 h.在不同温度下合成酸化缓蚀剂,以土酸(12%HCl+3%HF)为腐蚀介质,实验结果见表3.
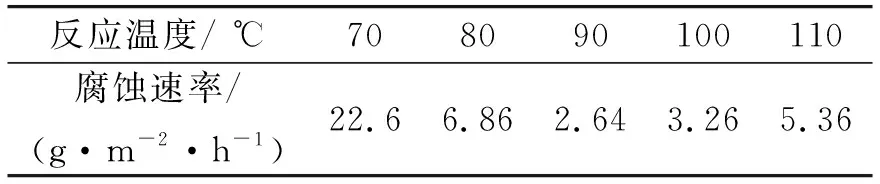
表3 反应温度对合成产物缓蚀性能的影响
由表3可知,在其他条件相同的情况下,选取不同的反应温度,合成的酸化缓蚀性能相差较大.随着反应温度的升高,产物的缓蚀性能先提高后下降.这是由于升高温度有利于亲核加成反应的进行,并使得分子有足够的能量克服反应所需的活化能.当温度超过100 ℃时缓蚀率反而下降,这是由于反应温度过高,副反应增多,缓蚀率降低.因此,确定反应温度为90 ℃.
2.3 反应时间的选择
n(苯乙酮)∶n(甲醛) ∶n(二乙胺) ∶n(对二甲氨基苯甲醛)=1 ∶ 6 ∶ 0.5 ∶ 1,反应温度为90 ℃,通过改变反应时间合成了5种不同的酸化缓蚀剂,在模拟油井酸化的腐蚀环境中进行静态挂片实验,φ(缓蚀剂)=1.0%,以土酸(12%HCl+3%HF)为腐蚀介质、腐蚀温度90 ℃,腐蚀时间4 h,实验结果见表4.
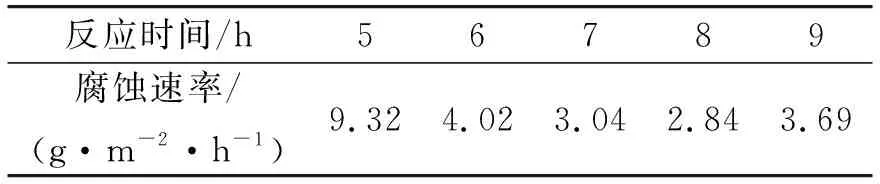
表4 反应时间对合成产物缓蚀性能的影响
从表4可知,随着反应时间的延长,腐蚀速率先降低后增大.当反应时间为7 h时,腐蚀速率基本趋于稳定了,反应时间进一步延长,缓蚀效果没有明显的变化.当反应时间超过8 h,其缓蚀性能逐渐减弱.这是由于随着反应时间累积,甲醛分子之间的加聚反应以及酮羰基之间的加成反应使副产物成为主要产物,降低了缓蚀性能.综合各方面考虑,反应的最佳时间为8 h.
2.4 选择最优的催化剂
n(苯乙酮) ∶n(甲醛) ∶n(二乙胺) ∶n(对二甲氨基苯甲醛)=1 ∶ 6 ∶ 0.5 ∶ 1,反应温度为90 ℃、反应时间8 h.加入质量分数为0.5%的相转移催化剂,在模拟油井酸化的腐蚀环境中,考察加入相转移催化剂对合成的产物缓蚀性能影响.腐蚀条件为:φ(缓蚀剂)=1.0 %,以土酸(12%HCl+3%HF)为腐蚀介质,腐蚀温度90 ℃,腐蚀时间4 h,实验结果见表5.

表5 相转移催化剂对合成产物缓蚀性能的影响
由表5可知,季铵盐类作为相转移催化剂,合成的缓蚀剂的缓蚀效果比聚醚类效果更好.加入两相催化剂后,使原本在两相中不能接触的物质转移到一相而发生化学反应,而且一般相转移催化剂在两相中都会有一定的溶解性,降低了反应所需的活化能和腐蚀速率.因此,以十二烷基苯磺酸钠作为反应的相转移催化剂.
2.5 缓蚀剂加量对缓蚀性能的影响
以土酸(12%HCl+3.0%HF)为腐蚀介质,添加上述缓蚀剂,腐蚀温度90 ℃,腐蚀时间4 h,测定合成的酸化缓蚀剂在上述酸液体系中的缓蚀性能,结果见表6.
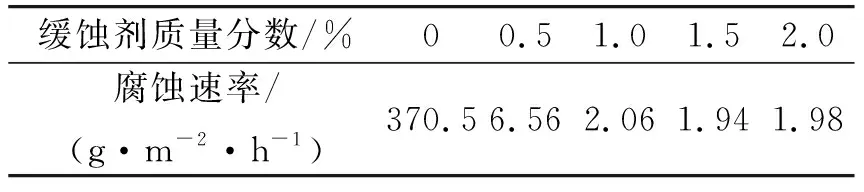
表6 合成产物在土酸中的缓蚀性能
根据酸化缓蚀剂评价标准SY/T 5405-1996,该条件下土酸常压静态腐蚀速率一级标准为2~3 g·m-2·h-1.由表6 可知,质量分数为1%的缓蚀剂在土酸(12%HCl+3.0%HF)中的腐蚀速率为2.06 g·m-2·h-1,达到了行业一级指标要求.
3 合成产物的缓蚀机理分析
观察添加缓蚀剂腐蚀4 h后的N80钢片,缓蚀剂在金属表面形成一层连续或不连续的吸附膜,阻止腐蚀过程中的阳极反应或阴极反应或同时阻止两个电极反应的进行,降低腐蚀速率,提高缓蚀率.通过苯环大π键、C=N键和N原子上的孤对电子,缓蚀剂分子在金属表面的吸附,改变金属表面电荷的状态,尤其是发生吸附活化表面的电荷状态,降低了介质与金属表面接触的可能性,从而到达缓蚀的效果.
4 结论
1) 最佳合成工艺条件:n(苯乙酮) ∶n(甲醛) ∶n(二乙胺) ∶n(对二甲氨基苯甲醛)=1 ∶ 6 ∶ 0.5 ∶ 1,反应温度90 ℃、反应时间8 h,选择十二烷基苯磺酸钠为相转移催化剂,加量为反应物总质量的0.5%.
2) 反应合成的酸化缓蚀剂在土酸(12%HCl+3.0%HF)中的缓蚀性能,优于SY/T 5405-1996标准中的一级指标.

