超高效液相色谱测定饮料中的阿斯巴甜和阿力甜
金博艳
(上海市崇明食品药品检验所 崇明食品安全检测中心, 上海 202150 )
阿斯巴甜和阿力甜作为甜味剂,允许根据限量使用添加至多类食品中,两者均为人工合成的非碳水化合物类的人造甜味剂,因为甜度高,热量低,多被广泛应用于饮料、果冻等食品中作为糖的替代品[1]。虽然人工合成甜味剂在很大程度上有着降低热量的摄入,改善糖尿病人的口感等优点,但是人工合成甜味剂也需限量使用,若超范围使用或者滥用,可能引起不同程度的毒性表现[2,3]。所以对于日常食品中的甜味剂的检测工作还是很有必要的。
目前,各类期刊文献的研究中关于食品中阿斯巴甜和阿力甜的检测方法主要有液相色谱法[4-6]、液相色谱-质谱法[7],但是液相色谱法因紫外-可见光检测器存在末端吸收,会出现吸收光谱向上飘移的现象,导致干扰多,不利于检测,而液相色谱-质谱联用则存在着检测成本高的缺点。考虑日常检测工作需低成本、快速、高效且结果准确,在液相色谱的基础上,选择超高效液相色谱,这样能快速的进行目标物分析,达到高效检测的目的。
1 实验部分
1.1 主要仪器和设备
超高效液相色谱仪(1290 Infinity Ⅱ,安捷伦科技),带有二极管阵列检测器;电子天平(ME104E,梅特勒);水浴锅(SW22,Julabo);匀浆机(T18,IKA);涡旋仪(LP Vortex Mixer,赛默飞);超声震荡仪(SK8200HP,科导);低温高速离心机(ST8R,赛默飞)。
1.2 试剂和耗材
甲醇(4L/瓶,色谱纯,德国CNW);离心管(50mL,上海安谱);水相滤头(0.45μm,安谱);一次性针筒注射器(5mL,上海安谱);一次性滴管(3mL,上海安谱)等。
1.3 实验方法
1.3.1样品前处理
以碳酸饮料作为基质,准确称取样品5g(精确到0.001g)于50mL离心管中,在50℃水浴上除去二氧化碳,经超声震荡提取20min,然后用一级水定容至25ml,混匀,经0.45μm水相滤头过滤后用于超高效液相色谱分析[8]。
以果粒橙等饮料为基质,准确称取样品5g(精确到0.001g)于50mL离心管中,加入5mL水,用高速匀浆机将样品制备均匀,经超声震荡提取20min,然后用一级水定容至25mL,混匀,4000r/min离心5min,将上清液经0.45μm 有机系滤膜过滤后用于超高效液相色谱分析。
1.3.2标准品及标准溶液配制
阿斯巴甜,纯度:99.3% 来源:Sigma-Aldrich, 批号:LRAB6662,称取0.00504g标准品,用水溶解并转移定容至10mL容量瓶中,配制成0.5mg/mL阿斯巴甜标准储备液。
阿力甜,纯度:98% 来源:Toronto Research Chemicals, 批号:1-MJS-5-1-PFZ,称取0.00510g标准品,用水溶解并转移定容至10mL容量瓶中,配制成0.5mg/mL阿力甜标准储备液。
分别吸取阿斯巴甜、阿力甜标准储备液各1mL,定容至5mL,配制成100μg/mL的混合标准使用液。分别吸取混合标准使用液10μL、20μL、30μL、40μL、50μL定容至1mL,配制成1μg/mL、2μg/mL、3μg/mL、4μg/mL、5μg/mL标准系列,待测。
1.3.3超高效液相色谱测定条件
色谱柱:C18柱,粒径1.8μm,规格0.3×10cm;检测器:DAD;流动相程序:甲醇+水恒比例50∶50;流速:0.3mL/min;检测波长:200nm; 带宽:4.0nm;柱温:30℃;进样体积:20μL。
1.3.4数据处理
采用安捷伦Chemstation 工作软件,版本:C.01.07.[27]进行数据处理。
2 结果与讨论
2.1 波长的选择
分别取阿斯巴甜和阿力甜的标准溶液,流动相恒定的情况下,在波长190nm~400nm进行最大波长扫描,结果显示,阿斯巴甜和阿力甜在195~215nm之间均有吸收,且呈递减状态,见图1。取两者的混合标准溶液,选择一个可定量的稳定的浓度,测定不同波长下的产生的相关信息,结果见表1。
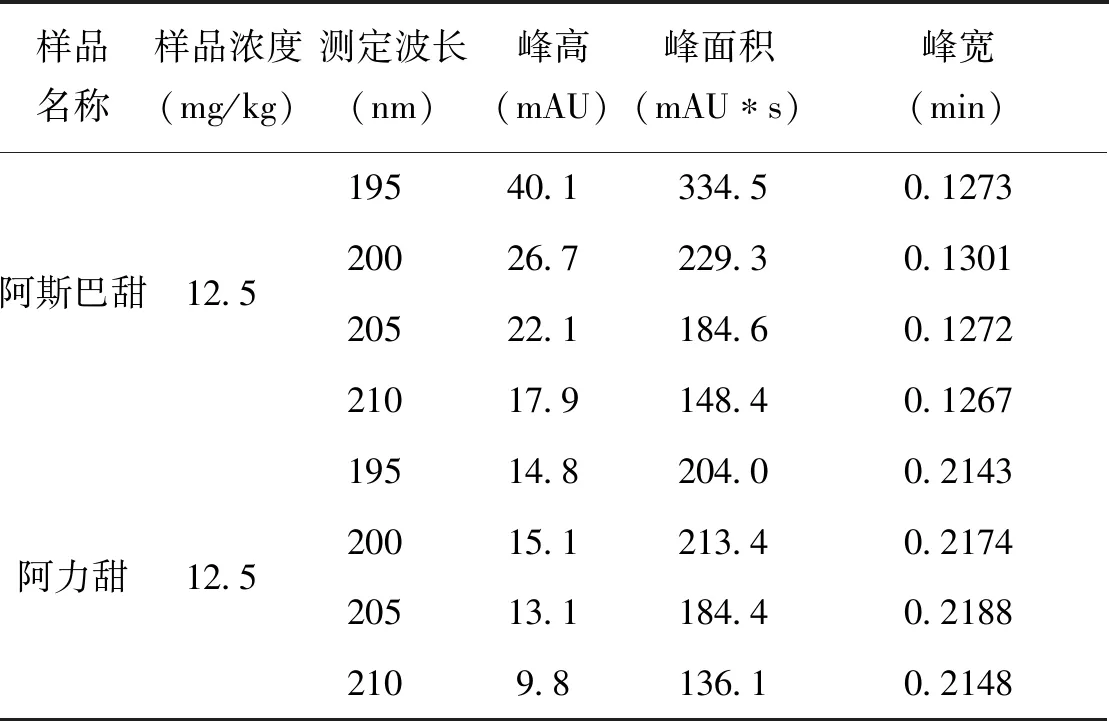
表1 不同波长下阿斯巴甜、阿力甜的吸收值
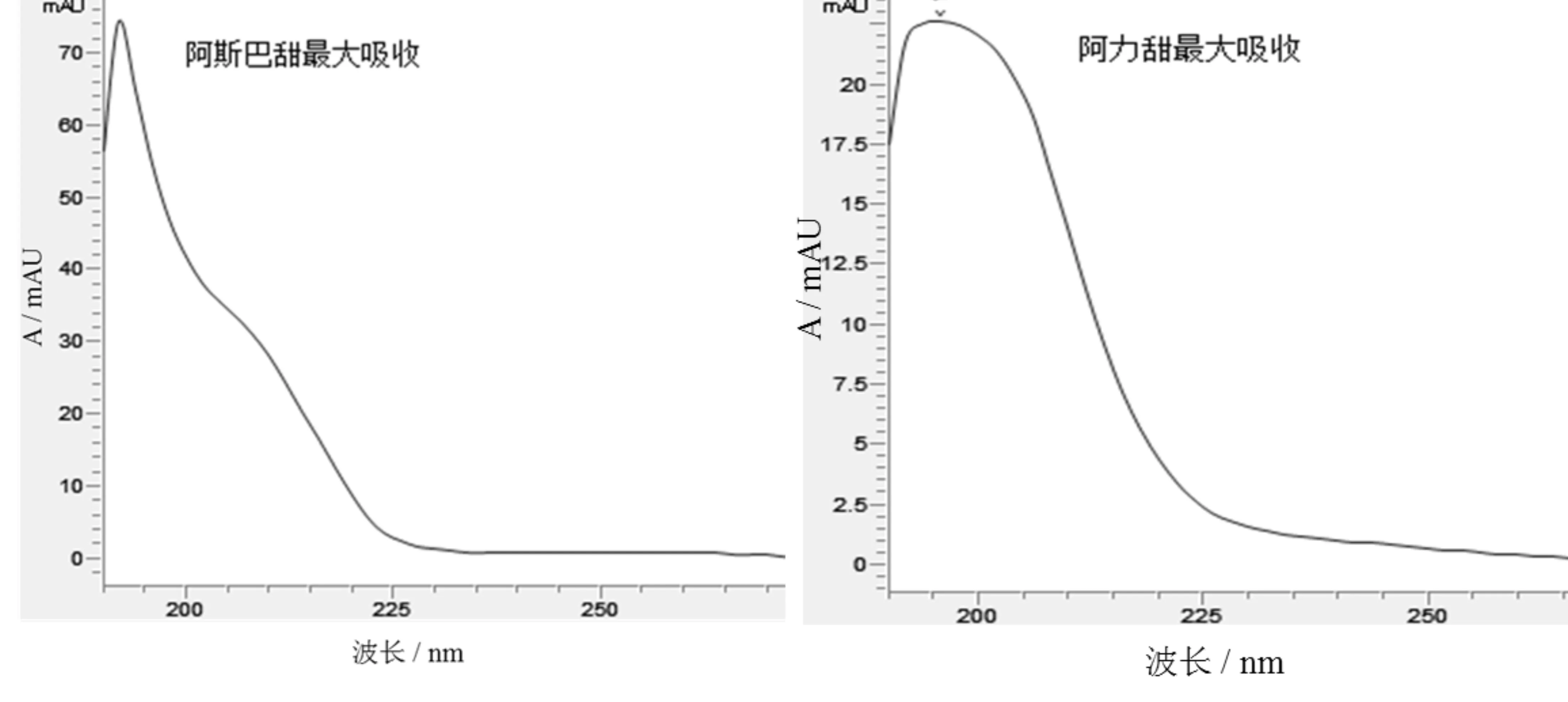
图1 阿斯巴甜和阿力甜的的波长扫描图
根据试验结果显示,阿斯巴甜和阿力甜在195~200nm之间的能同时达到最大吸收,阿斯巴甜在195nm处吸收大于200nm处的吸收,阿力甜在200nm处的吸收大于195nm处的吸收,鉴于这种情况,配制检出限及低于检出限的的标准溶液分别于195、200nm进行测试,结果如表2所示。

表2 检出限及检出限以下的浓度的检测结果
结果显示,在同时进行检测的情况下,阿斯巴甜和阿力甜在200nm条件下的信噪比均优于195nm,所以本方法选取200nm作为阿斯巴甜和阿力甜的检测波长。
2.2 色谱流动相的选择
在波长 200 nm的检测条件下,流动相甲醇与水比例从30∶70到70∶30不同比例进行测试,两组分的出峰时间和分离度如表3。
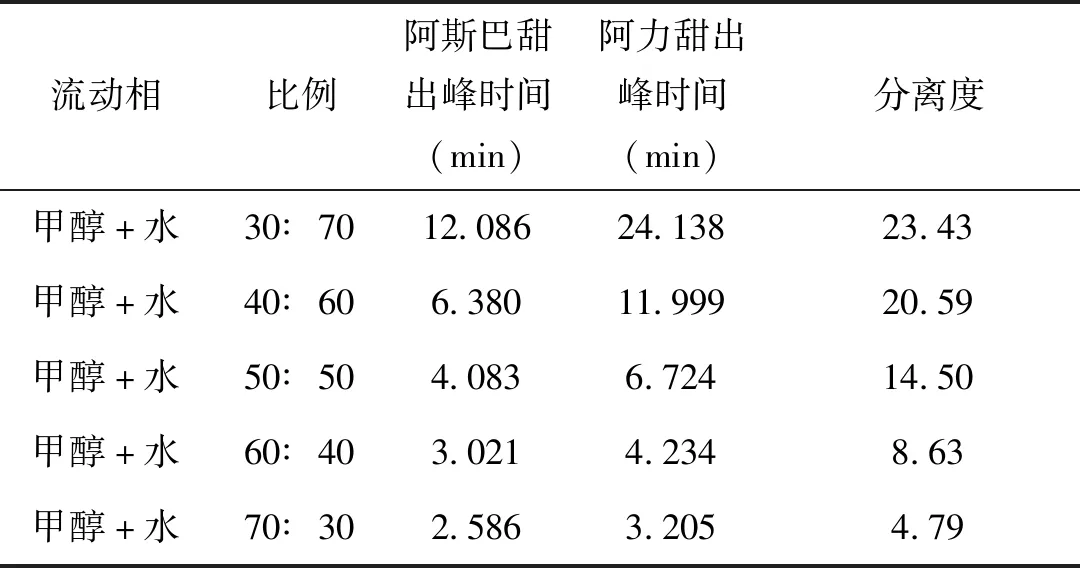
表3 不同比例流动相条件下的2种组分的出峰时间
根据不同比例流动相的试验结果显示,在有机相甲醇比例逐渐增加的情况下,两组分的出峰时间逐渐缩短,当有机相比例超过60%以后,阿斯巴甜的出峰时间跟溶剂峰的出峰时间接近,对目标组分的分离度上有一定的影响,同时考虑饮料中含有其他甜味剂或添加剂的影响,不选择时间跨度小于2分钟的,防止多组分的出峰时间重叠。为了达到高效快速的目的,选择50∶50的甲醇和水作为本方法的流动相,在这个比例下的检测时间能在40+60的基础上缩短一半的检测时间。分离结果如图2所示。
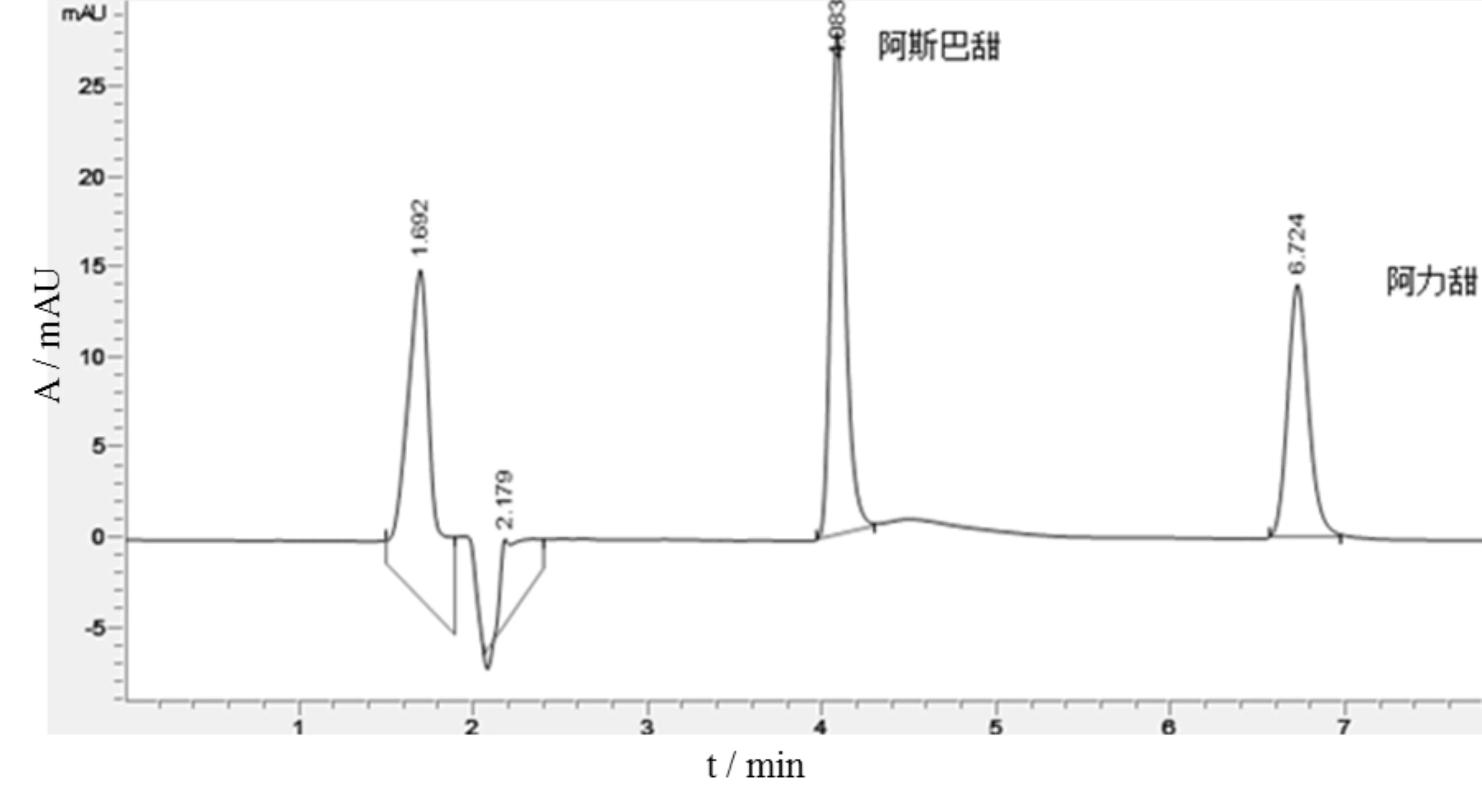
图2 50+50甲醇和水条件下的阿斯巴甜和阿力甜
2.3 标准曲线得回归方程及线性
通过2.1、2.2的不同条件测试,最终以200nm为检测波长,甲醇与水的比例为50∶50作为流动相,测试系列浓度标准工作溶液线性方程及线性系数,结果如表4。

表4 线性范围的回归方程及线性系数
试验得到的两组分的线性系数均在0.998以上,完全符合实验要求。
2.4 精密度及回收率实验
以饮料为基质,进行标准方法GB 5009.263-2016的检出限(1.0mg/kg、5μg)、定量限(3.0mg/kg、15μg)和10倍检出限(10.0mg/kg、50μg)6水平加标实验[9],分别得到精密度及回收率,结果见表5。
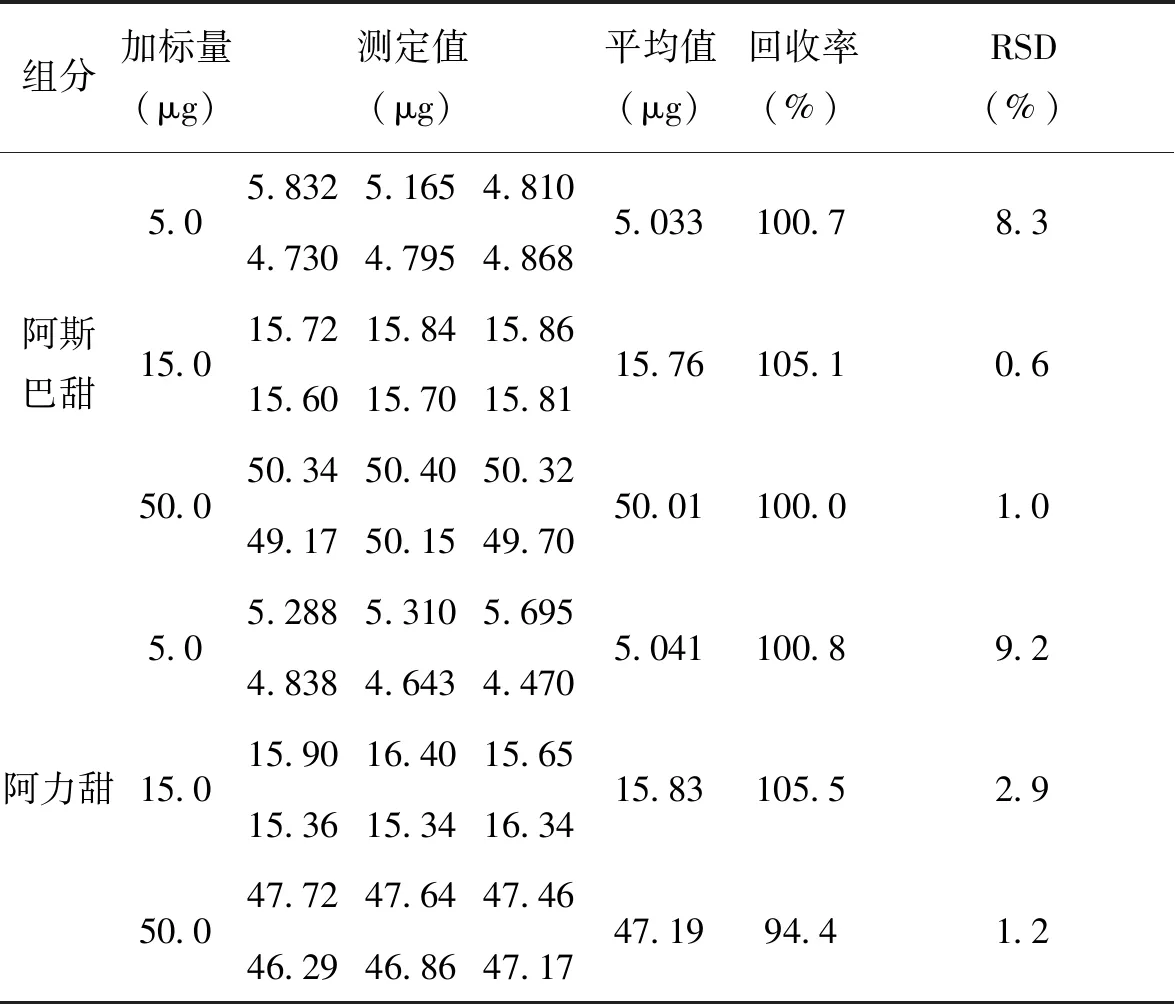
表5 饮料中阿斯巴甜和阿力甜的三水平回收率
实验结果表明,本方法两组分三水平的的回收率在94.4~105.5之间,三水平的精密度测试的相对偏差在0.6~9.2之间,重复性稳定。
3 结论
利用超高效液相色谱,在检测波长200nm,以50∶50的甲醇和水作为流动相,流速0.3mL/min的条件下,能使饮料中的阿斯巴甜和阿力甜的检出限达到0.75mg/kg ,低于国家标准GB 5009.263-2016方法检出限1mg/kg,且信噪比均大于3,符合检测要求。同时,随着流动相中有机相甲醇比例增加,使目标物的出峰时间大大缩短,有效的缩短了检测的时间,提高了检测效率。本法前处理简单,检测快速高效,分离度好,适用于日常饮料中两种甜味剂的检测。
——致癌

