壳聚糖微球对四环素-铜离子复合污染水体的吸附性能
马军冠, 张 旭, 陈培宇, 刘勇成, 武 轶, 赵 莹, 赵传起, 杨悦锁
(沈阳大学 环境学院, 辽宁 沈阳 110044)
近年来,中国逐渐成为抗生素生产和使用的大国,城市污水中各类抗生素残留远高于欧美国家[1].抗生素对抑制人类、植物和动物体内的微生物生长具有十分显著的效果.但如果大量的抗生素进入生态系统,可能会造成环境中抗生素耐药基因污染,增强细菌耐药性,甚至导致超级细菌的出现[2],从而给生态平衡和人体健康带来潜在的风险.同时,由于人类活动的影响,抗生素污染往往伴有严重的重金属污染.例如,含有Cu、Zn元素的抗生素是畜牧养殖业饲料中常见的添加剂,在我国某猪场粪便中检测到Zn、Cu元素的质量分数超过8 000和400 mg·kg-1,金霉素、土霉素的平均质量分数为 3.57和9.09 mg·kg-1[3].这些元素经过动物的粪尿排出,与抗生素形成复合污染,最终进入水环境.随着越来越多的污染物进入环境,抗生素-重金属复合污染已经成为水体环境污染中普遍存在的现象[3],广泛存在于城市污水、农业废水和养殖业废水中,其中饲料工业及畜禽养殖业是抗生素-重金属复合污染的重灾区.即使在浓度水平较低的情况下,这种复合污染的毒理学效应仍较为突出.长期暴露于抗生素与重金属的复合污染物中,可能会导致抗药性基因的产生和传播,甚至多重抗药性基因的进化.抗生素和重金属复合污染不仅会影响到污染物在环境中的化学过程,还会影响污染物的生物效应[4],从而破坏生态环境,危害人体健康.
壳聚糖(chitosan)是一种由几丁质(chitin)经过脱乙酰作用得到的天然有机物.在环境领域,壳聚糖作为絮凝剂和螯合剂,主要用于工业废水、微污染源水处理和重金属提取及回收等方面[5-6].壳聚糖分子上的羟基、氨基和N-乙酞基,使壳聚糖表现出高的溶解性能和反应活性.例如,Jia等[7]利用氨基酸改性壳聚糖,实现了对诺氟沙星(NOR)、磺胺嘧啶(SDZ)以及泰乐菌素(TYL)等抗生素的高效吸附;Bratskaya等[8]探讨了羧乙基壳聚糖在絮凝/沉淀法中去除水中重金属离子(Cu2+、Zn2+和Ni2+)的潜力.目前对壳聚糖吸附重金属或有机物等单一污染物的研究较多,对复合污染物的吸附作用和机制研究则较少涉及,而且所用的壳聚糖都是在水中分散的,不利于处理和回收,因此如何利用壳聚糖较强的亲水性和吸附性用于复合污染物处理,是目前亟待解决的关键问题.本文制备了壳聚糖微球,表征了其形貌和表面性质,并考察了壳聚糖微球对重金属(Cu2+)、四环素(tetracyclines,TC)和其复合污染物的吸附性能与机理.
1 材料与方法
1.1 壳聚糖微球的制备与表征
准确称取2.50 g壳聚糖(百灵威科技有限公司),超声并搅拌溶解于浓度为0.17 mol·L-1的100 mL醋酸(天津化学试剂厂)溶液中,利用蠕动泵(保定雷弗流体科技有限公司)以60滴每分钟的速率将壳聚糖溶液滴于3 g·L-1的NaOH(天津化学试剂厂)溶液中,形成微球,静置24 h,使反应完全.用超纯水将壳聚糖微球洗至中性,将该微球置于150 mL甲醇(赛默飞世尔(中国)有限公司)溶液中,加入15 mL戊二醛溶液(体积分数为30%)进行交联反应,持续5 h后,再用乙醇、超纯水清洗数次,置于-20 ℃环境下真空冷冻干燥,得到壳聚糖微球.本文中,实验所用试剂均为分析纯.
将壳聚糖微球样品喷金后置于日立冷场发射扫描电镜(SU8020)下表征其表面形貌.然后用Nicolet iS 10型傅立叶变换红外吸收光谱(FT-IR)表征样品表面的化学基团.
1.2 静态吸附实验
静态吸附实验用来测试壳聚糖微球的吸附特性.过程如下:溶剂采用0.02 mol·L-1的NaCl溶液[6](为模拟真实水体环境,文中所有溶液配制时都采用此浓度NaCl溶液作为溶剂),溶质为四环素(百灵威科技有限公司)和CuSO4·5H2O(国药集团有限公司),分别制备初始质量浓度为1 000 mg·L-1的3种溶液,分别为TC溶液,Cu2+溶液,Cu2+和TC的混合溶液(质量比为1∶1).为了区别壳聚糖微球对混合溶液中Cu2+和TC吸附协同效应的影响,Cu2+和TC的混合溶液分为2瓶溶液,分别标为TC-Cu溶液和Cu-TC溶液,TC-Cu为测试聚糖微球对混合溶液中TC的吸附所设,Cu-TC为测试聚糖微球对混合溶液中Cu2+的吸附所设,将溶液分别稀释不同的倍数(10、12.5、20、25和50倍),储存备用.
1.2.1 pH的影响
用FA2204B型电子天平(天津市光明化学仪器有限公司)分别称取25 mg壳聚糖微球置于4个棕色瓶中,在每个瓶中分别加入质量浓度为50 mg·L-1的TC、Cu2+、TC-Cu溶液和Cu-TC溶液10 mL,用HCl(1 mmol·L-1)和 NaOH(1 mmol·L-1)溶液将4个溶液调至不同pH值(3.0~7.0),置于25 ℃恒温摇床中进行吸附实验,24 h后分别过0.45 μm滤膜,取上清液,测定4个溶液吸附平衡的质量浓度.TC溶液、TC-Cu溶液、Cu-TC溶液的平衡质量浓度通过紫外分光光度计(U-3900,日立)测定,TC溶液吸收波长为357 nm,TC-Cu溶液、Cu-TC溶液的吸收波长为371 nm;Cu2+质量浓度采用原子吸收光谱仪(AA-220)测量.每个样品设定2个平行样,取其平均值.
壳聚糖微球的吸附容量Qe,mg·g-1,通过式(1)计算,
(1)
式中:ρ0和ρe分别为初始时刻和平衡时刻溶液中的污染物质量浓度,mg·L-1;V为溶液体积,L;m为吸附剂的质量,g.
1.2.2 吸附时间与吸附动力学
在该部分实验中,设置TC、Cu2+、TC-Cu溶液和Cu-TC溶液的初始质量浓度为50 mg·L-1,溶液的pH值为5.0.为了探讨吸附时间的影响,设置不同的取样时间(5~480 min)进行取样分析,其他步骤同1.2.1.
本文中,通过准一级动力学模型(式(2))和准二级动力学模型(式(3))来模拟抗生素、铜离子在吸附剂上的吸附过程.
式中:t为时间,min;Qe和Qt分别是平衡时和时间t时,污染物在单位质量壳聚糖上的吸附量,mg·g-1;k1是准一级动力学速率系数,min-1;k2是准二级速率系数,g·mg-1·min-1.
利用最小乘二法可以计算出污染物在吸附剂表面的初始吸附速率v0,mg·g-1·min-1,
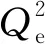
(4)
1.2.3 污染物初始质量浓度与吸附等温线
为了探讨不同污染物质量浓度对于吸附过程的影响,分别将不同初始质量浓度的TC(20~80 mg·L-1)、Cu2+(30~80 mg·L-1)、TC-Cu和Cu-TC(40~120 mg·L-1)溶液倒入样品瓶中,溶液的pH值设置为5.0,其他过程如1.2.1.
在恒定温度下,吸附容量与溶液平衡浓度的关系曲线称为吸附等温线.常用的吸附等温方程为Langmuir方程(式(5))和Freundlich方程(式(6)).
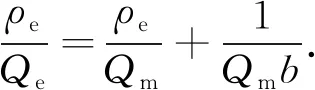
(5)
式中:Qm是污染物在吸附剂表面的理论最大吸附量,mg·g-1;b是与吸附能有关的系数,L·mg-1.
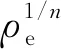
(6)
式中:K为Freundlich吸附系数,mg1-nLn·g-1;n为常数,通常大于1.
在Langmuir 等温吸附模型中,利用系数b,可以计算出平衡参数或分离常数RL:
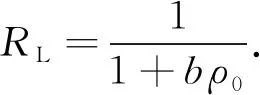
(7)
2 结果与讨论
2.1 壳聚糖微球的表征
壳聚糖微球的表面形貌如图1所示.从图中可以看出,经过聚合与交联作用,壳聚糖分子形成了固态的三维吸附材料,壳聚糖内部呈现出高度发达的海绵状结构.这种高孔隙通道的结构除了增加接触面积以外,同时具有较好的传质性能,可以保证吸附材料与水中污染物充分接触.

(a) 放大10000倍(b) 放大100000倍
将壳聚糖制成三维颗粒结构,还可以有效防止粉末状吸附剂的流失,使其易于回收.

C—N基团的特征吸收峰;1 370 cm-1处为C—O的特征吸收峰,1 050 cm-1处特征峰对应于C—O—C的反对称伸缩振动峰[11-12].
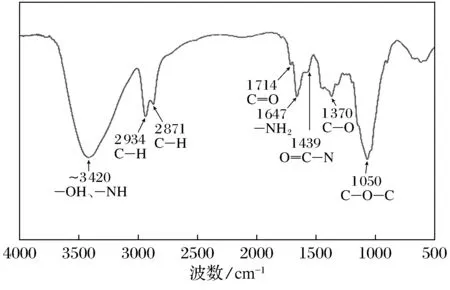
图2 壳聚糖微球的FTIR图Fig.2 FTIR picture of chitosan microspheres
2.2 壳聚糖微球的吸附性能
2.2.1 pH值的影响
pH值对吸附过程的影响如图3所示.实验结果表明,pH值对壳聚糖微球吸附TC的影响较弱,但对吸附Cu2+及二者复合污染物的影响显著.随着pH值的增加,TC的吸附容量略有下降,总体变化不大;与TC不同,在加入Cu2+之后,可以发现,壳聚糖对TC-Cu复合污染物的吸附能力大幅度提高.同时,壳聚糖对TC-Cu复合污染物的吸附随pH值的升高而增加,与单独吸附Cu2+的变化一致.从吸附去除率来看(图3(b)),壳聚糖单独吸附TC,其吸附去除率为50%~60%,加入铜离子后,吸附去除率接近100%(pH=5),说明铜离子的加入对TC的吸附有较好的促进作用;相比之下,加入TC也可以在一定程度上提高Cu2+在壳聚糖表面的吸附,说明二者具有协同吸附的效果.
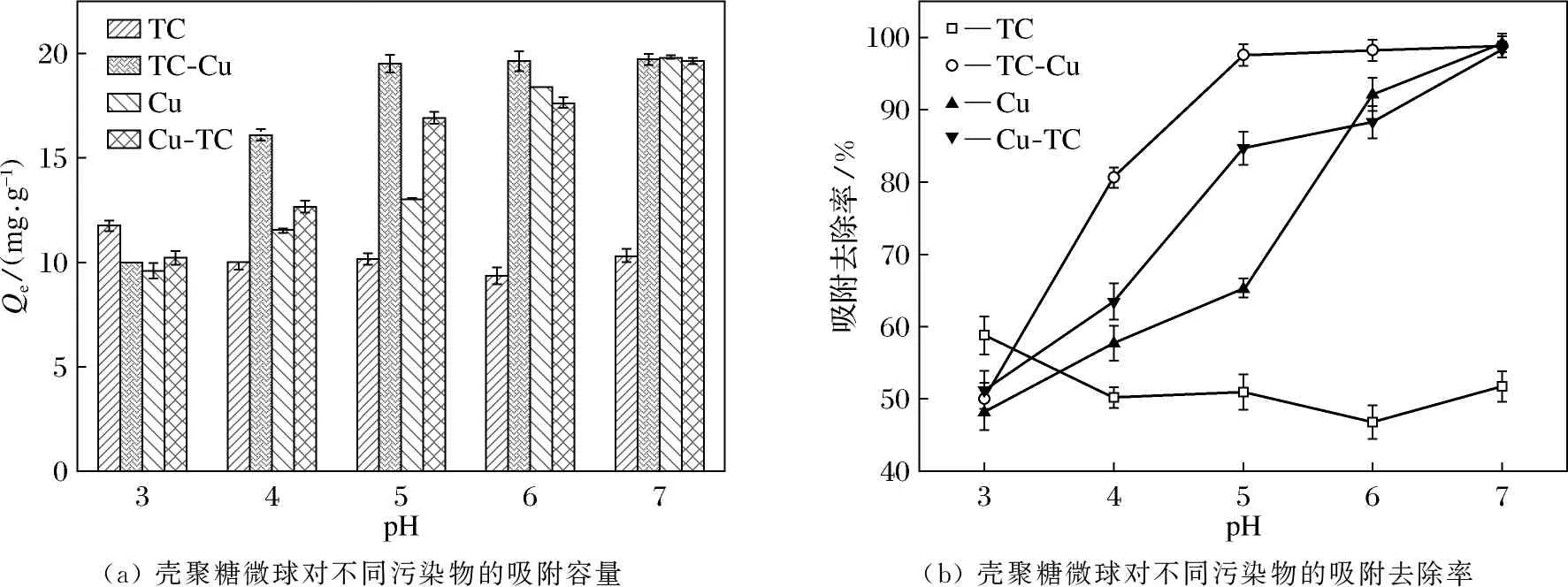
(a) 壳聚糖微球对不同污染物的吸附容量(b) 壳聚糖微球对不同污染物的吸附去除率
分析原因,与壳聚糖的电荷性及TC的带电情况有关.吸附剂壳聚糖分子中带有大量氨基,在酸性溶液中易成盐,呈阳离子性质[7].TC在水溶液中存在3个电离平衡常数,分别为pKa1=3.30,pKa2=7.68,pKa3=9.68,因此在不同 pH 的情况下可离解为4种不同形态[13]:阳离子形态(TC+)、两性离子形态(TC±)、阴离子形态(TC-)和双阴离子形态(TC2-).在本实验设定的pH范围内,TC主要以两性TC±的形式存在,此时TC的环状结构与壳聚糖的环状结构形成了稳定π-π键,因此受到pH值的影响较小.在加入Cu2+以后,Cu2+与酸性环境中的H+竞争吸附位点,同时,与带正电荷的壳聚糖表面产生排斥作用,因此pH值较低时,吸附容量较小;随着pH值的提高,排斥作用减弱,吸附容量有所提高.当pH值高于6.5时,Cu2+有生成沉淀的趋势,吸附去除率均接近100%,因此本文中不在讨论碱性pH值对吸附的影响.
2.2.2 吸附动力学曲线
壳聚糖微球吸附TC、Cu2+及其复合污染的动力学曲线如图4所示.实验结果表明,壳聚糖对于污染物的吸附均快速达到了平衡;壳聚糖单独吸附TC或者Cu2+的趋势类似,在100 min时可以完成90%的吸附过程,此后逐渐达到动态平衡;而对于复合污染,吸附过程在20 min内即可达到90%以上,缩短了吸附时间.且对于复合污染物的吸附容量要高于单一污染物吸附,说明二者具有协同吸附的效果.壳聚糖对于Cu2+的吸附能力要强于TC,分析原因是壳聚糖表面存在大量的活性基团,对于Cu2+的络合吸附能力要高于吸附TC的π-π作用力.
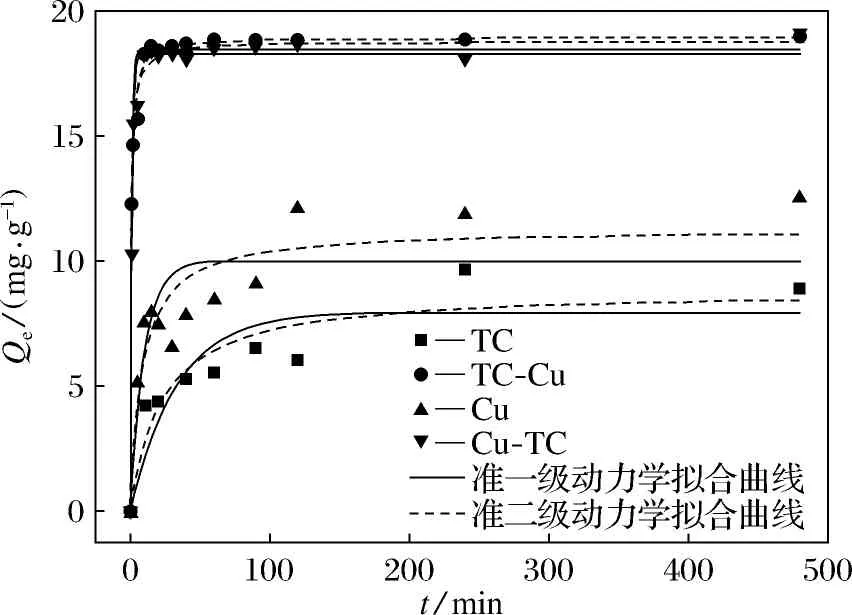
图4 壳聚糖微球的吸附动力学曲线
为评价吸附过程的控速步骤和吸附机理,分别采用准一级和准二级动力学模型对吸附数据进行拟合,由模型的拟合程度可推断TC和Cu2+的吸附控速步骤,拟合结果如表1所示.由表1可知,壳聚糖吸附TC与Cu2+以及二者的复合污染物更符合准二级动力学模型,且污染物的平衡吸附容量计算值也与实验值更为接近.这些结果表明壳聚糖对2种污染物的吸附过程是由化学反应控制,而不是单纯的物理扩散控制[14].对比二级吸附速率常数k2可以发现,壳聚糖吸附剂对于Cu2+的吸附要快于TC,说明壳聚糖对于Cu2+的静电作用力要强于与TC分子间的π-π作用力;而对于复合污染物的吸附要快于单一污染物,说明TC与Cu2+在壳聚糖表面具有明显的协同吸附作用.此外利用式(4)计算可知,壳聚糖对污染物的初始吸附速率v0与k2的变化情况基本一致.
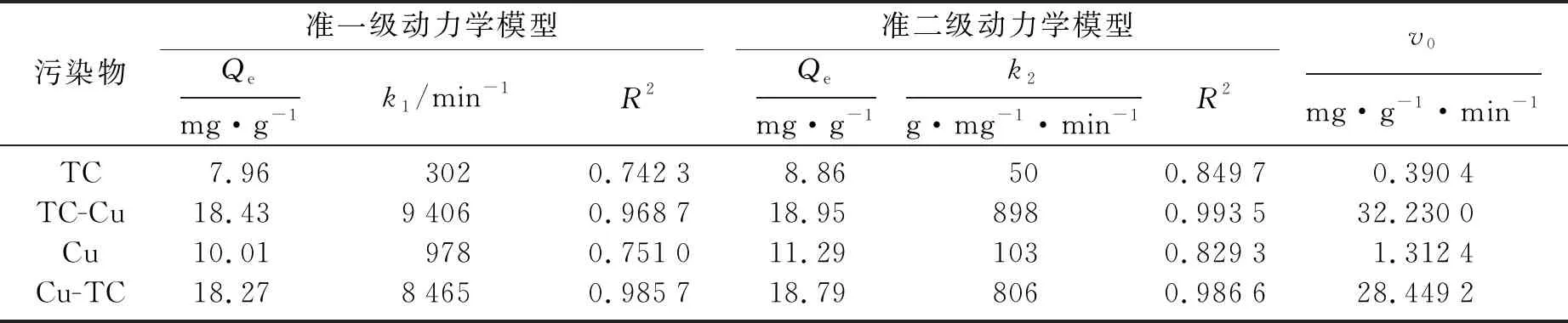
表1 壳聚糖微球吸附污染物的准一级动力学与准二级动力学拟合参数
2.2.3 吸附等温线
图5为壳聚糖微球在等温下对TC、Cu2+、TC-Cu和Cu-TC污染物的吸附容量与平衡质量浓度作图所得的吸附等温线.分别用Langmuir和Freundlich模型对吸附过程进行拟合,相关的数据如表2所示.通过结果可知,2种模型对壳聚糖吸附TC与Cu2+以及TC-Cu均具有较好的拟合效果,通过比较相关系数R2可知,Freundlich模型更适合模拟壳聚糖的吸附过程.对比最大理论吸附量Qm(通过Langmuir模型获得)可以发现,相比于单一污染物吸附,壳聚糖微球对于复合污染物吸附均有所提高,说明TC和Cu2+具有协同吸附的效应.通过比较RL值,可以评价吸附过程难易程度:不易吸附(RL>1);线性吸附(RL=1);容易吸附(0 图5 壳聚糖微球的吸附等温曲线 表2 壳聚糖微球吸附污染物的Langmuir与Freundlich等温吸附模型Table 2 Langmuir and Freundlich isotherm adsorption model for the adsorption of pollutants by chitosan microspheres 2.2.4 壳聚糖吸附TC-Cu复合污染物的机理 对壳聚糖微球吸附TC-Cu复合污染物的机理进行分析(图6),主要有以下3种:首先壳聚糖的环状结构易与苯环结构化合物形成π-π共轭作用,因此对芳香族化合物、抗生素、染料等有机污染物都有较好的去除效果;其次,—OH、—NH2等官能团也会与TC等污染物分子上的活性基团形成氢键作用,加强吸附效果;第三,Cu2+在壳聚糖与TC之间存在稳定的架桥作用,Cu2+先吸附于壳聚糖表面,同时,又与TC形成络合物[16],加强了壳聚糖对TC的吸附.壳聚糖表面丰富的—NH2基团,易与Cu2+发生络合反应,因此可高效吸附水中的Cu2+. 图6 壳聚糖微球吸附TC-Cu复合污染物的机理Fig.6 Adsorption mechanism of chitosan microspheres for adsorption of TC-Cu multi-pollutants 本实验利用壳聚糖微球作为吸附剂,研究其吸附TC、Cu2+及其复合污染物的性能,得到以下结论. 1) 壳聚糖微球内部呈现出高度发达的孔隙结构,表面含有大量的—OH与—NH2等基团. 2) pH值对壳聚糖微球吸附TC的影响较弱,对吸附Cu2+及二者复合污染物的影响显著.与单一污染物相比,复合污染物的吸附容量大幅度提高,说明TC与Cu2+具有协同吸附的效果.吸附过程更符合准二级动力学模型和Freundlich模型,说明壳聚糖微球吸附TC等污染物由多分子层的化学扩散控制. 3) 吸附机理主要包括π-π共轭作用、氢键作用以及Cu2+在壳聚糖与TC之间的架桥作用等,共同构成壳聚糖微球对TC与Cu2+及其复合污染物的吸附机制.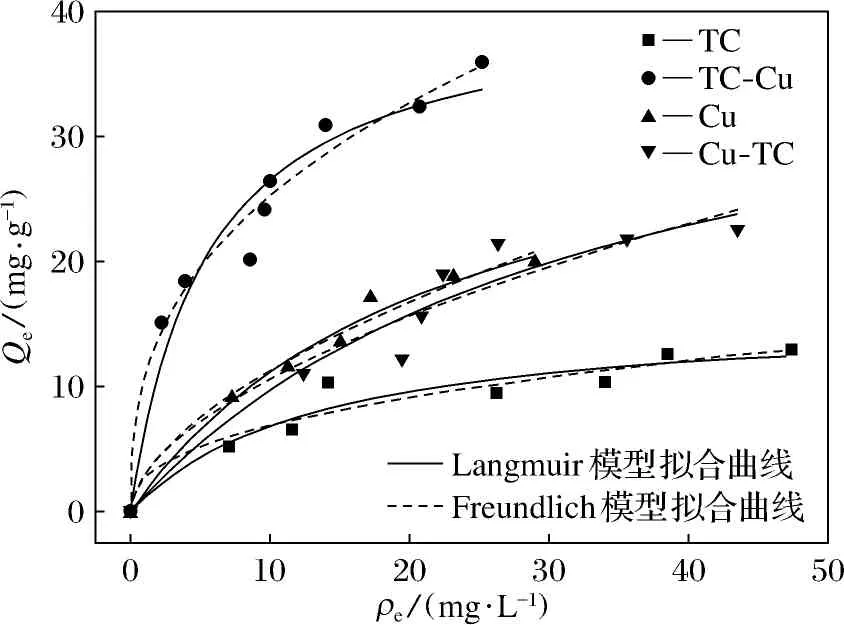
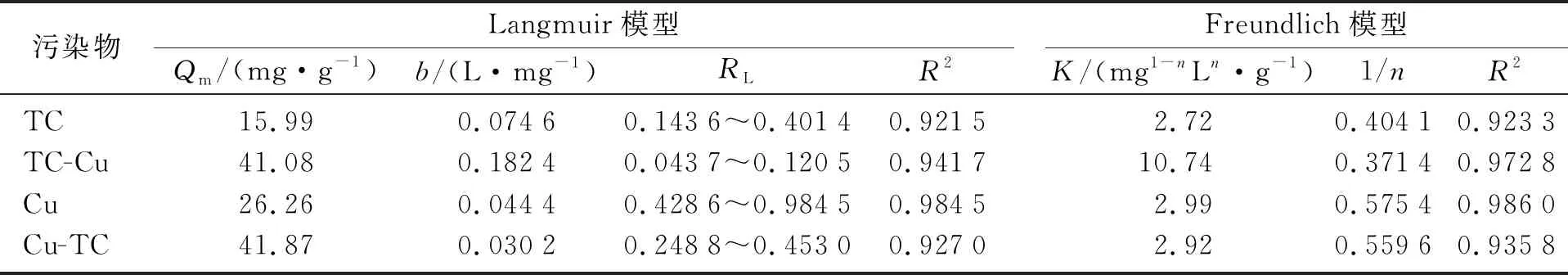
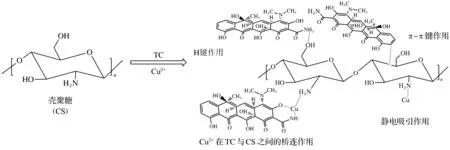
3 结 论

