真实世界中延迟与急诊经皮冠状动脉介入治疗并置入药物洗脱支架对ST段抬高型心肌梗死患者远期预后的影响
姚晶 宋莉 刘臣 周鹏 赵汉军 颜红兵
100037 中国医学科学院 北京协和医学院 国家心血管病中心 阜外医院冠心病中心[姚晶(进修生)、宋莉、刘臣、周鹏、赵汉军、颜红兵];154100 鹤岗市人民医院心内科(姚晶)
国内外研究均显示,能够在发病后12 h内接受直接经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)的 ST段抬高型心肌梗死(ST-elevation myocardial infarction,STEMI)患者仅占1/3[1-2]。对于错过最佳时间窗的患者,延迟PCI的时机和疗效一直是个广受争议的话题。本研究通过对发病后72 h内行PCI成功并置入药物洗脱支架(drug-eluting stent,DES)的STEMI患者进行回顾性分析,比较急诊和延迟PCI对远期预后的影响。
1 对象和方法
1.1 研究对象
本研究为单中心回顾性观察随访研究。连续入选2013年于中国医学科学院阜外医院就诊并于发病后72 h内行PCI成功并置入DES的STEMI患者303例,其中男性246例,女性57例,年龄23~86岁,平均(57.6±11.9)岁。入选标准:(1)年龄≥18岁;(2)符合STEMI的诊断标准[3];(3)于发病后72 h内行PCI成功并置入DES;(4)随访资料完整。排除标准:(1)由外院转入前已行急诊PCI;(2)已行溶栓治疗;(3)拟行择期冠状动脉旁路移植术。入选患者根据PCI时机不同分为两组:延迟PCI(12~72 h)组77例和急诊PCI(<12 h)组226例。本研究获阜外医院伦理委员会批准(审批号:2017-866),因本研究为回顾性研究,伦理委员会同意免签知情同意书。
1.2 PCI方法及药物治疗
所有患者术前给予氯吡格雷负荷量300~600 mg和阿司匹林负荷量300 mg。术后氯吡格雷75 mg/d,至少12个月;阿司匹林75~100 mg/d,长期维持。术中抗凝药物主要应用普通肝素(100 IU/kg),极少数出血高危患者选择比伐卢定。术中Ⅱb/Ⅲa受体拮抗剂、抽吸导管和主动脉内球囊反搏的选择性使用以及预扩张和后扩张与否均由术者决定。PCI成功标准:术后残余狭窄≤20%、TIMI血流3级且无急性再闭塞、急诊冠状动脉旁路移植术、术中死亡等严重并发症。其他药物治疗包括他汀类、血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂、β受体阻滞剂、螺内酯、利尿剂和硝酸酯类药物等均参照指南建议。
1.3 资料收集和随访
由经过统一培训的调查医生查阅电子病历收集资料。包括患者的基本信息、病史、诊断、介入治疗、药物使用、住院期间不良事件和门诊随诊等资料。病历信息经2次核对后录入数据库。
要求患者出院后1、3和6个月返院门诊复诊,同时每6个月由随访小组进行电话随访,持续时间至少2年。主要终点为主要不良心血管事件(major adverse cardiovascular events,MACE),包括心原性死亡、心肌梗死、明确或可能的支架血栓[按美国学术研究联合会(Academic Research Consortium,ARC)定义[4]]及缺血性卒中,次要终点为缺血驱动的靶血管血运重建。对所有不良事件的判断均需获得书面证据,并经两名研究人员核对,达成一致后录入数据库。
1.4 统计学方法

2 结果
2.1 两组基线特征比较
急诊PCI组患者的吸烟比例显著高于延迟PCI组(72.1%比59.7%,P=0.04),而有卒中病史的患者比例(9.7%比20.8%,P=0.01)和术前左房直径[35(32,37)mm比35(33,39)mm,P=0.04]均显著低于延迟PCI组,两组左室舒张末径和左室射血分数比较差异均无统计学意义,见表1。
延迟PCI组行PCI前症状持续不缓解或仍反复发作者67例(87.0%),其中血流动力学不稳定者11例(14.3%);症状已完全缓解者10例(13.0%)。
2.2 两组冠状动脉造影和介入治疗特征比较
除发病-进门时间显著延长外,延迟PCI组的进门-球囊扩张时间也显著长于急诊PCI组,且延迟PCI组的中位发病-球囊扩张时间超出急诊PCI组728.5 min。急诊PCI组患者的TIMI 0级血流比例显著高于延迟PCI组(78.8%比53.2%,P<0.01),而TIMI 3级血流比例显著低于延迟PCI组(10.7%比37.7%,P<0.01),置入DES的个数少于延迟PCI组(1.6±0.9比1.9±1.0,P=0.01),见表2。

表2 两组患者的冠状动脉造影和介入治疗特征比较
2.3 梗死相关动脉完全闭塞的亚组分析
对于梗死相关动脉完全闭塞的亚组患者,除延迟PCI组女性比例高于(31.7%比17.4%,P=0.04)发病-进门、进门-球囊扩张和发病-球囊扩张的中位时间长于(均为P<0.01)和置入DES个数超过(1.9±1.0比1.6±0.8,P=0.03)急诊PCI组以外,其他基线、冠状动脉造影和介入治疗特征比较差异均无统计学意义,见表1和2。
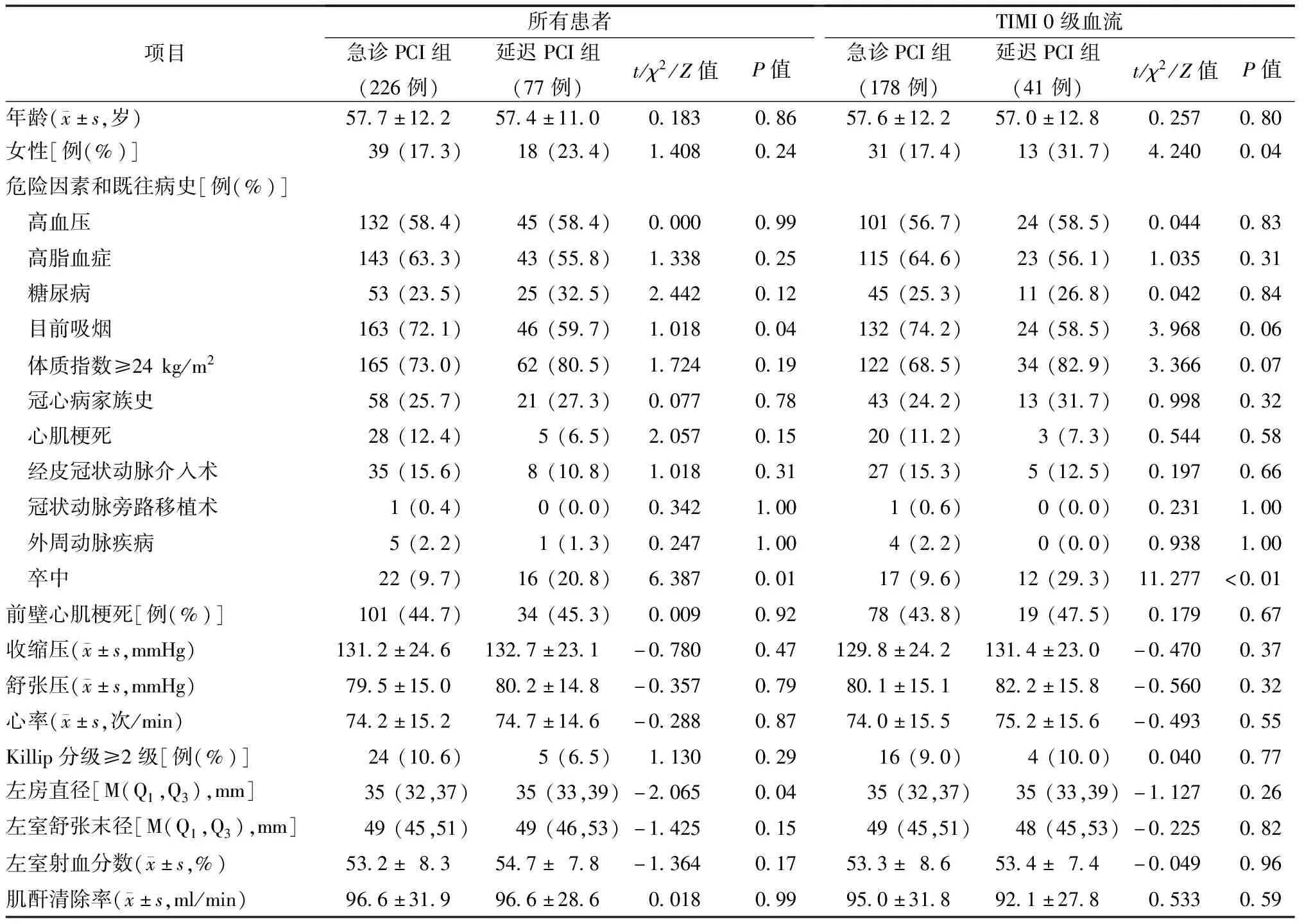
表1 两组患者的基线特征比较
2.4 两组患者住院期间的2年临床终点事件比较
两组患者住院期间MACE、心原性死亡、明确/可能的支架血栓、缺血性卒中以及缺血驱动的靶血管血运重建的发生率均有增加的趋势,但差异无统计学意义,梗死相关动脉完全闭塞的亚组患者分析结果基本一致。两组间2年MACE(8.4%比9.1%,P=0.85)和缺血驱动的靶血管血运重建(4.4%比5.2%,P=0.76)发生率无显著性差异;对于梗死相关动脉完全闭塞的亚组患者,两组间2年MACE(8.4%比12.2%,P=0.45)和缺血驱动的靶血管血运重建(5.6%比7.3%,P=0.71)发生率亦无显著性差异(表3)。

表3 两组患者临床预后比较[例(%)]
2.5 倾向性评分匹配分析
校正两组主要基线特征(年龄、性别、高血压、糖尿病、吸烟、卒中史、梗死部位和Killip分级)进行1∶1倾向性评分匹配。分析显示,除住院期间临床终点事件发生率比较无显著性差异外,两组间2年MACE(8.1%比9.5%,P=0.77)和缺血驱动的靶血管血运重建(5.4%比5.4%,P=1.00)发生率亦无显著性差异(表4)。

表4 倾向性评分匹配后两组特征和临床终点事件比较
3 讨论
国内外指南建议STEMI患者再灌注治疗的最佳时间窗为发病后12 h之内,主要是基于早期的溶栓试验结果和缺血再灌注的动物模型研究,而在该时间窗内实施PCI的疗效与安全性方面还缺乏足够证据。由于比较不同时间窗内实施PCI的临床试验结果并不一致,对于错过指南建议时间窗的STEMI患者,延迟PCI的时机和潜在获益一直存在争议。
STEMI发生后,梗死相关血管的血栓性闭塞往往不同于动物实验中的钳夹或球囊扩张所致的持续性完全闭塞,而是呈现间断性和动态性的闭塞。另外,有些患者描述的心肌缺血症状存在模糊性,所以报告的症状持续时间可能并不确切。近期研究显示,即使血管闭塞超过12 h,再灌注治疗仍可获益[5-7]。影像学证据[8]和临床观察性研究[9-10]也提示,直接PCI对于发病12~72 h的STEMI患者仍可获益,尽管与12 h内行直接PCI的患者相比最终梗死面积显著增加,但仍可挽救大量濒死心肌。各国指南根据近期临床试验结果建议,对于发病>12 h同时存在血流动力学或心电不稳定或持续存在心肌缺血症状或客观证据的STEMI患者,应行直接PCI治疗。BRAVE-2随机对照试验[11-12]纳入发病12~48 h且病情稳定的STEMI患者,结果显示直接PCI与药物保守治疗相比显著减少了最终梗死面积,临床预后亦有所改善。主要基于这项研究结果更新的欧洲心脏病学会指南建议,对于发病后12~48 h就诊的STEMI患者应考虑实施常规直接PCI策略(Ⅱa-B)[3]。
尽管缺乏相关研究数据,对延迟就诊的STEMI患者实施直接PCI并置入DES已成为目前国内很多PCI术者的日常临床实践。总体上讲,延迟PCI的获益主要包括缓解持续的心肌缺血、挽救濒死心肌、改善心室重构、稳定电活动、缩短住院时间并减少医疗费用。然而,就诊时间延迟的患者往往血栓已部分机化,梗死面积较大且已呈透壁性坏死,直接PCI术中发生无复流、心功能恶化和心脏破裂的风险增加,所以手术安全性一直受到质疑。本研究以12 h为界限比较急诊PCI与延迟PCI并置入DES对STEMI患者远期临床预后的影响,包括了冠状动脉完全和不完全性闭塞以及病情稳定和不稳定等真实世界的多种临床情况。结果发现,在发病12~72 h内行延迟PCI并置入DES与指南推荐的标准直接PCI(<12 h)相比,对住院期间和2年MACE和缺血驱动的靶血管血运重建发生率的影响无显著性差异,即使梗死相关动脉持续完全闭塞。由于两组间部分基线特征存在差异,我们进行了1∶1倾向性评分匹配以校正主要的基线特征,分析结果与总体结果基本一致。
目前指南建议急诊PCI时置入支架优于单纯的球囊扩张血管成形术。近期研究显示,新一代DES与金属裸支架或与第一代DES相比安全性更好,疗效相似甚至更佳,尤其是支架内血栓、再次心肌梗死和靶病变再次血运重建的发生率更低[13-15]。本研究中90%以上的STEMI患者均置入新一代DES,延迟PCI组与急诊PCI组比较再发心肌梗死、支架血栓和缺血驱动的靶血管血运重建率相似。
本研究存在一定局限性:(1)非随机性的观察性研究,但两组的主要基线和介入治疗特征基本平衡,保证了两组间的可比性,并且倾向性评分匹配分析的结果与总体结果基本一致;(2)单中心研究,阜外医院是大型的心血管专科医院,延迟PCI组患者近1/3是由外院转入,由于整体的临床实践模式存在差异,所以研究结果可能难以推及其他综合性医院;(3)样本量偏小,可能需要扩大样本量和更长期的临床随访;(4)缺少心功能随访指标。
总之,对于未能在最佳时间窗内行急诊PCI的STEMI患者,及时进行延迟PCI并置入DES不失为一种积极的治疗选择,其2年的临床预后可能不劣于急诊PCI患者。
利益冲突:无

