吉非替尼联合化疗治疗晚期非小细胞肺癌的疗效分析△
李华兴 刘爱武 康渭岚 丘伟贤 苏国兰 黄伟豪(广东同江医院神经内科 广州 518054)
近年来,在我国生活方式、环境、饮食结构不断变化,肺癌的发生率显著升高。据不完全统计[1],将近80%的肺癌患者为NSCLC。NSCLC是一种特殊肺癌,具有较强的侵袭性,极易发生局部浸润、远处转移,预后普遍较差[2]。吉非替尼是临床新型的抗肿瘤药物,对机体免疫功能影响较小,且毒副作用相对较轻。本文为进一步探究吉非替尼联合化疗在晚期NSCLC临床治疗中的疗效及对免疫功能影响,纳入2016年6月—2018年12月收治的60例晚期NSCLC患者研究,报道如下。
1 资料与方法
1.1 一般资料:2016年6月—2018年12月为研究时段,医院伦理委员会批准本项研究,选取本院收治的60例晚期NSCLC患者,随机平均分为两组。实验组(30例):女性12例,男性18例;年龄49~75岁,平均年龄(62.52±5.44)岁;TNM 分期:21 例 III期、9例IV期。参照组(30例):女性13例,男性17例;年龄50~74岁,平均年龄(62.49±5.42)岁;TNM 分期:23例 III期、7例 IV 期。两组相比 P>0.05,可比较。
纳入标准:①均符合《晚期非小细胞肺癌抗血管生成药物治疗中国呼吸领域专家共识(2016年版)解读》[3]中对“NSCLC”诊断标准;②TNM分期在III-IV期;③预计生存期在6月以上;④均已对知情同意书签字。
排除标准:①哺乳期、妊娠期;②中途退出;③合并其他恶性肿瘤;④合并心力衰竭、呼吸衰竭;⑤合并免疫、内分泌、血液系统疾病;⑥存在酒精、药物滥用史;⑦合并神经病变;⑧研究前进行抗肿瘤治疗。
1.2 治疗方法:参照组第1天、第8天,予以1 000 mg/m2吉西他滨,于30 min内静脉滴注;第1~4天,予以75 mg/m2顺铂,静脉滴注,4 w为1周期,共计治疗3周期。实验组在参照组给药基础上,予以吉非替尼,口服,250 mg/次,1次/d,4 w为1周期,共计治疗3周期。
1.3 观察指标与判定标准:①临床疗效具体判定标准[4]:CR(完全缓解):病灶完全消失,1月内无新病灶出现;PR(部分缓解):病灶消失50%以上,1月内无新病灶出现;SD(稳定):病灶消失25%~49%,1月内无新病灶出现;PD(进展):出现新病灶。总有效率=(CR+PR)/总例数×100%。②免疫功能指标、CA50、CYFRA21-1:治疗前、治疗3周期后,抽取空腹静脉血5 mL,以3 000 r/min速率离心处理10 min,10 mm离心半径,以全自动免疫分析仪(型号:MD-IA-1000,武汉明德生物科技股份有限公司)检测CD3+、CD4+、CD4+/CD8+、CD8+;以 ELISA(酶联免疫吸附法)检测 CA50(糖类抗原 50)、CYFRA21-1(血清细胞角蛋白19片段),试剂均由上海卡努生物科技有限公司提供,一切操作谨遵相关标准。③不良反应发生情况:统计用药期间恶心呕吐、腹泻、血小板减少、白细胞减少发生率。
1.4 统计学方法:数据以SPSS26.0软件检验,独立样本t检验计量资料(免疫功能指标、CA50、CYFRA21-1),以(±s)形式表示;χ2检验计数资料(临床疗效、不良反应发生情况),以[n(%)]表示。P<0.05表示差异存在统计学意义。
2 结果
2.1 对比两组临床疗效:实验组临床总有效率(96.67%)明显比参照组(70.00%)高,P<0.05,见表 1。
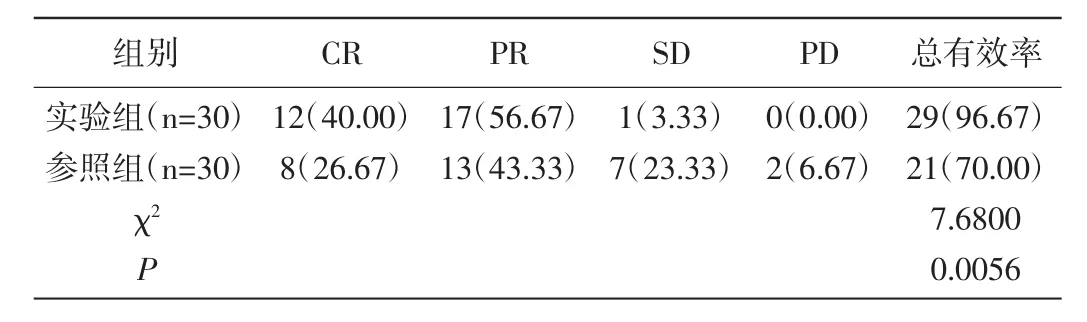
表1 对比两组临床疗效[n(%)]
2.2 对比两组免疫功能指标、CA50、CYFRA21-1:两组治疗前免疫功能指标、CA50、CYFRA21-1 比较,P>0.05;实验组治疗 3 个疗程后CD3+、CD4+、CD4+/CD8+指标均明显比参照组高,实验组治疗3个疗程后CD8+、CA50、CYFRA21-1指标明显比参照组低,差异均有统计学意义(P<0.05)。见表 2。
表2 对比两组免疫功能指标、CA50、CYFRA21-1(±s)

表2 对比两组免疫功能指标、CA50、CYFRA21-1(±s)
注:治疗前、治疗3个疗程后组内对比,aP<0.05;治疗前、治疗3个疗程后组内对比cP>0.05;治疗3个疗程后组间对比,bP<0.05。
组别 时间 CD4+(%)CD8+(%)CD3+(%)CD4+/CD8+(%)CA50(U/mL)CYFRA 21-1(ng/mL)治疗前实验组(n=30) 治疗3个疗程后治疗前参照组(n=30) 治疗3个疗程后38.26±1.52 38.14±1.24bc 38.29±1.52 30.25±1.11a 31.26±2.62 28.16±1.41bc 31.29±2.52 31.16±2.52a 58.26±5.62 57.92±5.59bc 58.33±5.59 51.16±2.44a 1.28±0.62 1.22±0.42bc 1.29±0.59 1.04±0.62a 29.06±3.62 17.12±1.05bc 29.08±3.59 23.62±2.22a 5.62±0.31 2.01±0.12bc 5.66±0.29 3.52±0.66a
2.3 对比两组不良反应发生情况:实验组不良反应发生率(23.33%)与参照组(26.67%)比较,P>0.05。见表3。
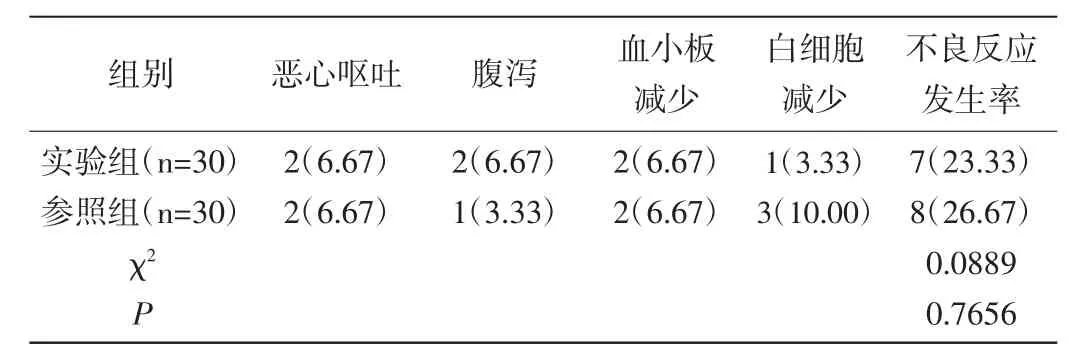
表3 对比两组不良反应发生情况[n(%)]
3 讨论
既往有研究表明[5],EGFR(表皮生长因子受体)在肺癌患者机体中呈高表达状态,与预后、临床分期有着极为密切的联系。EGFR异常活跃,则会加快NSCLC患者肿瘤细胞的增殖、转移,抑制EGFR,则会阻断肿瘤血管生长,防止癌细胞转移、生长,加快肿瘤组织凋亡[6,7]。CYFRA21-1属于酸性蛋白,CYFRA21-1表达与肿瘤生长趋势呈正相关;CA50属于肿瘤糖类抗原,是一种广谱肿瘤标志物,CA50高表达会加快恶性肿瘤患者病情进展。本研究显示,实验组临床总有效率(96.67%)明显比参照组(70.00%)高,实验组免疫功能指标显著优于参照组,CA50、CYFRA21-1指标明显比参照组低,P<0.05,提示吉非替尼在NSCLC治疗中,临床疗效显著、确切。吉非替尼属于EGFR-TKI,可有效降低酪氨酸酶活性,阻断肿瘤细胞信号通路,削弱癌细胞对周围组织的黏附效应,进而达到抑制肿瘤细胞侵袭、增殖的目的,促进肿瘤细胞凋亡,发挥抗肿瘤效果[8,9]。实验组不良反应发生率(23.33%)与参照组(26.67%)比较,P>0.05,提示吉非替尼的毒副作用相对较轻,分析原因与吉非替尼对于正常组织无杀伤作用,保护正常组织机能有关,是一种安全性较高的抗肿瘤药物。
综上所述,晚期NSCLC吉非替尼联合化疗治疗,可有效抑制肿瘤生长,对免疫功能影响较小,不良反应发生率较低,值得推广。

