黄连煎煮液抗念珠菌增效作用的体外实验研究
吴盘红,谢婷,王海燕,范瑞强
(1.河南省中医院,河南郑州450002;2.广东省中医院,广东广州510120;3.河南中医药大学第一附属医院,河南郑州450000)
外阴阴道念珠菌病(Vulvovaginal candidiasis,VVC)是困扰育龄期女性的临床常见病多发病,主要表现为外阴严重瘙痒和灼痛,严重降低患者的生活质量。据估计约3/4的女性在育龄期至少患过1次VVC,其中一半患者经历过复发,有5%~8%的成年女性1年发作4次以上,即复发性VVC(Recurrent vulvovaginal candidiasis,RVVC)[1]。国内外研究数据均表明,目前导致VVC的病原菌仍以白念珠菌为主,占比达70%~90%,而在非白念珠菌中感染中则以光滑念珠菌最为常见,其中光滑念珠菌对三唑类抗真菌药物耐药率也最高[2-3]。因此,对于RVVC患者人群,除白念珠菌感染外,光滑念珠菌感染扮演了重要角色。硝酸咪康唑被欧洲国际性病控制联盟列为治疗VVC首选药物[4],但由于该药物多年来的临床上的广泛应用,其耐药现象也在不断的增加,特别对于RVVC,让临床选择可用的有效的药物治疗面临严重困难,故寻找探索研究新型的抗真菌药物成分或者已有及新型的抗真菌药物增效剂已经成为研究的热点、重点和难点。
香莲外洗液是广东省中医院的院内名方,作为院内制剂广泛应用于手足癣、体癣、VVC及其他外阴瘙痒性疾病的治疗,临床疗效显著。同时,实验室研究证实该药物有显著的抗真菌效应,并可诱导对唑类耐药的白念珠菌菌株恢复对唑类药物的敏感性[5-6]。中药黄连味苦,性寒,有清热燥湿、泻火解毒的功效,是香莲外洗液组方的君药成分之一。为更深入的探讨香莲外洗液的具体作用机制,本研究以其君药黄连为切入点,应用微量肉汤稀释法[7]测定并比较黄连煎煮液、2%硝酸咪康唑溶液单独以及联合应用于白念珠菌和光滑念珠菌的最低抑菌浓度(MIC),同时采用联合抑菌指数(FICI)来判断二者是否有联合效应,以期为临床VVC治疗方案的选择提供确切的实验室依据。
1 材料与方法
1.1 培养基及试剂 科玛嘉显色培养基、RPMI-1 640液体培养基、萨布罗培养基(SDA)、无菌96孔培养板、可换滤膜针头式过滤器(均购自广州市迪景微生物科技有限公司),离心管、振荡器、微量移液器、ESCO超净工作台、无菌聚乙烯小管、电子分析天平仪等。
1.2 药物 黄连煎煮液:黄连(生产企业:康美药业股份有限公司;产地:四川;批号:120300891;生产日期:2012年3月27日)10 g,放入药煲后加纯化水300 mL,浸泡30 min后,先用大火烧开,后用小火煎40 min,尼龙网过滤,药渣再加300 mL纯化水,大火烧开后小火煎煮40 min,尼龙网过滤出药液,将2次煎煮的滤液合并,得到药液269 mL,用纯化水将药液定容为200 g/L,用0.22 μm的可换滤膜针头式过滤器重复过滤灭菌后,置于无菌离心管容器中,并封口置于-20℃冰箱中恒温保存。
2%硝酸咪康唑溶液(上海世康特制药有限公司;国药准字号:H31022700),规格:20 mL(含硝酸咪康唑0.4 g,浓度为2%)。
1.3 实验菌种 所有菌种均来自于广东省中医院妇科门诊VVC患者的白带标本(2010年9月1日—2011年2月30),所收集的临床标本用科玛嘉显色培养基确证是白念珠菌菌株、光滑念珠菌菌株者各15株;质量控制菌株:近平滑假丝酵母菌标准菌株ATCC 22019、克柔假丝酵母菌标准菌株ATCC 6258,第二军医大学长海医院赠送。置于-80℃超低温冰箱保存。
1.4 白念珠菌和光滑念珠菌的培养及鉴定 白念珠菌的培养和鉴定:取临床确诊为VVC的外阴阴道分泌物标本,将棉签蘸取适量的标本成井字形涂于沙保氏培养基上,37℃恒温箱中培养24~48 h,肉眼可见菌落后,将呈白色、奶油色菌落分离并转种于科嘉玛显色板上,37℃恒温箱中再培养24~48 h后,肉眼可见各色菌落,挑出呈绿色或者翠绿色的菌落,同时用YBC酵母菌鉴定卡进行鉴定,选用鉴定为白念珠菌者,共选用15株。
光滑念珠菌的培养和鉴定:培养方法和操作步骤同白念珠菌,挑出紫红色的菌落,并同时用逆转录聚合酶链反应(RT-PCR)试剂盒进行检测鉴定,确定为光滑念珠菌菌株者,共15株。
为了进一步保证实验中选用菌株的纯度及活力,再次将白念珠菌、光滑念珠菌二次接种在沙保氏培养基上,37℃恒温箱中培养24~48 h,后放置10℃恒温箱中保存备用。
1.5 选用微量液基稀释法进行体外药敏实验 依据是美国临床实验室标准协会(CLSI)提出的标准(M27-A3方案)[7]。
1.5.1 药物的配制 在CLSI提出的标准中,因无2%硝酸咪康唑溶液的相关研究内容,所以本研究实验操作及步骤均参照CLSI中提供的氟康唑的实验方法。药物剂量公式:所需药物量=稀释剂用量(mL)×贮存液浓度(μg/mL)/药物有效力(μg/mg)。2%硝酸咪康唑溶液用培养液来稀释,使贮存液浓度为1280μg/mL,实际应用浓度范围为0.125~128μg/mL;黄连煎煮液原液浓度为200 mg/mL,实际应用浓度范围为0.244~20 mg/mL。(药物贮存液置于无菌聚乙烯小瓶,并放置于-70℃冰箱保存)。
1.5.2 菌悬液的制备 首先用消毒接种环在实验菌株沙保氏培养基上刮取直径>1 mm的菌落,将菌落加至试管内,试管内装适量0.85%的无菌生理盐水,接着用消毒接种环研磨菌块至均匀,为了更好的将菌块混匀,最后将试管置于漩涡振荡器上震荡约10 s,至此菌悬液制成。用比浊仪测量菌悬液浊度,用0.85%的无菌生理盐水菌使悬液浊度达调到0.5 麦氏浊度,相当于(1×106~5×106)CFU/mL,用血细胞计数板镜来确定其是否在此范围。用上述制备好的RPMI1640培养基1∶20倍稀释后再1∶50倍稀释至最终浓度为(1×103~5×103)CFU/mL。
1.5.3 接种 排列方式:96孔板上每4排为1组实验药物,即每1个菌株每1组药物设计平行4排实验。
单用2%硝酸咪康唑溶液组:在96孔板的平行4排每1排第1孔加入160 μL的RPMI培养基,其余各孔加入100 μL后,在第1孔加入40 μL的配制好的2%硝酸咪康唑溶液,搅拌混匀后,接着用微量移液器从第1孔中吸取100 μL到第2孔,搅拌混匀后,接着用微量移液器从第2孔中吸取100 μL到第3孔,搅拌混匀,同样的方法和步骤,连续倍比稀释至第11孔,搅拌混匀,从第11孔吸取100 μL弃去,每1排最后1孔为第12孔,为不含药物的生长对照孔(只含培养液和菌液)。最后在每孔中加入100 μL菌悬液,搅拌混匀。此时单用2%硝酸咪康唑溶液组96孔板的平行4排从第1孔至第11孔经过2倍的等比稀释之后,每孔的药物浓度分别为128、64、32、16、8、4、2、1、0.5、0.25、0.125 μg/mL。
单用黄连煎煮液组:分别在96孔板的平行4排的每1空加入100 μL的RPMI培养基,然后在每排第1孔加入100 μL的黄连煎煮液,搅拌混匀后,用微量移液器从第1孔中吸取100 μL移到第2孔,搅拌混匀,用同样的方法和步骤,从第2孔中吸取100 μL移到第3孔,搅拌混匀,连续倍比稀释至第11孔,搅拌混匀,从第11孔吸取100 μL弃去,每1排最后1孔为第12孔,为不含药物的生长对照孔(只含培养液和菌液)。最后在每孔中加入100 μL菌悬液,搅拌混匀。此时单用黄连煎煮液组96孔板的平行4排从第1孔至第11孔经过2倍的等比稀释之后,每孔的药物浓度分别为50、25、12.5、6.25、3.125、1.563、0.781、0.391、0.195、0.098、0.048 mg/mL。
2%硝酸咪康唑溶液+黄连煎煮液组:首先在96孔板平行4排第1孔到第12孔分别加入100 μL的RPMI培养基,接着在每排第1孔分别加入40μL的2%硝酸咪康唑溶液,和60 μL的黄连煎煮液,搅拌混匀,然后用微量移液器从第1孔中吸取100 μL到第2孔,搅拌混匀,按照同样的方法和步骤,接着用微量移液器从第2孔中吸取100 μL到第3孔,连续倍比稀释至第11孔,搅拌均匀,从第11孔吸取100 μL弃去;每排最后1孔为第12孔,为不含药物的生长对照孔(只含培养液和菌液)。最后在12孔中分别加入菌悬液各100 μL,搅拌混匀。此时2%硝酸咪康唑溶液+黄连煎煮液组96孔板的平行4排从第1孔至第11孔经过2倍的等比稀释之后,每孔含有2%硝酸咪康唑溶液药物浓度分别为128、64、32、16、8、4、2、1、0.5、0.25、0.125μg/mL,每孔含有黄连煎煮液的浓度为 30、15、7.5、3.75、1.875、0.9375、0.468、0.234、0.117、0.059、0.025 g/L。
质控菌株的接种方法同以上步骤。每组实验平行对照做4次。最后将制好的96孔板置37℃恒温箱孵育48 h,观察并记录结果。同时弃掉结果差异大的孔板。
1.5.4 质量控制 同时近平滑假丝酵母菌标准菌株ATCC22019、克柔假丝酵母菌标准菌株6258按照上述方法和步骤进行MIC测定,进行质量控制。
1.5.5 MIC的判定 48 h的孵育结束之后,肉眼比较各孔的生长情况,并与对照孔进行比较评分。4分:浊度不减低,表示生长无抑制;3分:浊度轻度降低,表示生长轻微减少或者相当于生长对照孔的75%;2分:浊度明显减低,表示生长明显减少或者相当于生长对照孔的50%;1分:轻微模糊,表示轻微生长或者相当于生长对照孔的25%;0分:肉眼观察澄清或者未见生长。记录每1组的每孔评分。实验过程中,如果发现药物浓度高的孔反而较药物浓度低的孔生长多,或者呈现出对照孔异常生长,或者结果表现为标准菌株不在质控范围时,均进行重复实验。本实验中以生长明显减少,以及约相当于生长对照孔的50%(约50%受试菌被抑制生长),作为MIC值判断终点。
1.5.6 联合用药效果评价[7]实验结果以FICI来判断二者的联合效应。FICI:MICA联合/MICA单独+MICB联合/MICB单独。当FICI≤0.5时为协同作用;0.5< FICI≤1 时为相加作用;L<FICI≤4 时为无关作用;当FICI>4时为拮抗作用。
1.6 统计学方法 实验研究所有数据均用SPSS 19.0统计软件进行处理;计量资料采用均数±标准差表示,2组计量资料间的比较采用独立样本t检验,若非正态分布或方差不齐采用秩和检验。组间率的差异比较采用卡方检验。建议水平为α=0.05,双侧检验。
2 结果
2.1 质控结果 质控菌株ATCC22019、ATCC6258MIC值分别在 0.5~0.25 μg/mL 和 4~8 μg/mL 之间,结果符合CLSI所推荐的M27-A3的48 h标准,表示结果均在控,实验条件及操作均符合要求。
2.2 单用2%硝酸咪康唑溶液、黄连煎煮液及二者联用作用于临床15株白念珠菌、光滑念珠菌的MIC值。
单用2%硝酸咪康唑溶液作用于15株白念珠菌MIC 值见表 1,平均 MIC 值为(14.0±14.99)μg/mL;单用2%硝酸咪康唑溶液作用于15株光滑念珠菌的MIC 值见表 1,其 MIC 均值为(14.88±25.15)μg/mL。单用2%硝酸咪康唑溶液作用于白念珠菌、光滑念珠菌的MIC值比较,P>0.05表明2%硝酸咪康唑溶液对白念珠菌、光滑念珠菌的敏感性差异无统计学意义,见表2。
单用黄连煎煮液作用于15株白念珠菌MIC值见表 1,其 MIC 均值为(8.18±7.38)mg/mL。单用黄连煎煮液作用于15株光滑念珠菌的MIC值见表1,其 MIC 均值为(9.38±4.09)mg/mL。单用黄连煎煮液作用于白念珠菌、光滑念珠菌的MIC值比较,P>0.05为差异无统计学意义;表明黄连煎煮液对白念珠菌、光滑念珠菌的敏感性差异无统计学意义,见表2。
表1 单用和联用2%硝酸咪康唑溶液、黄连煎煮液作用于白念珠菌、光滑念珠菌的MIC值 (±s)
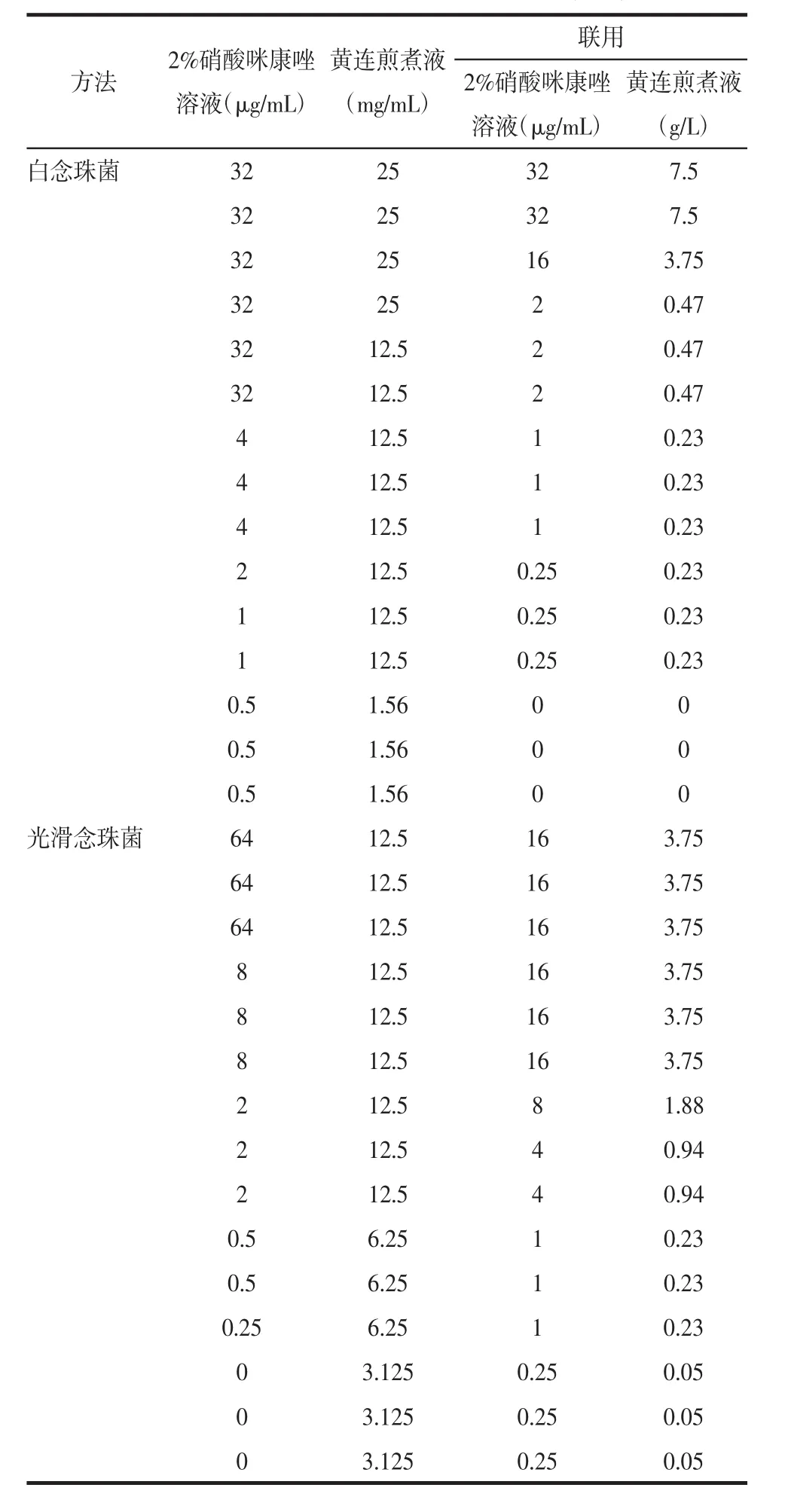
表1 单用和联用2%硝酸咪康唑溶液、黄连煎煮液作用于白念珠菌、光滑念珠菌的MIC值 (±s)
黄连煎煮液(g/L)白念珠菌 32 25 32 7.5 32 25 32 7.5 32 25 16 3.75 32 25 2 0.47 32 12.5 2 0.47 32 12.5 2 0.47 4 12.5 1 0.23 4 12.5 1 0.23 4 12.5 1 0.23 2 12.5 0.25 0.23 1 12.5 0.25 0.23 1 12.5 0.25 0.23 0.5 1.56 0 0 0.5 1.56 0 0 0.5 1.56 0 0光滑念珠菌 64 12.5 16 3.75 64 12.5 16 3.75 64 12.5 16 3.75 8 12.5 16 3.75 8 12.5 16 3.75 8 12.5 16 3.75 2 12.5 8 1.88 2 12.5 4 0.94 2 12.5 4 0.94 0.5 6.25 1 0.23 0.5 6.25 1 0.23 0.25 6.25 1 0.23 0 3.125 0.25 0.05 0 3.125 0.25 0.05 0 3.125 0.25 0.05方法 2%硝酸咪康唑溶液(μg/mL)黄连煎煮液(mg/mL)联用2%硝酸咪康唑溶液(μg/mL)
2%硝酸咪康唑溶液+黄连煎液共同作用于15株白念珠菌的MIC值,其中2%硝酸咪康唑的MIC值见表 1,其均值为(5.98±11.28)μg/mL。黄连煎煮液的MIC值见表1,其MIC均值为(1.43±2.63)mg/mL。二者的FICI=0.53,表明黄连煎煮液+2%硝酸咪康唑溶液共同作用于白念珠菌后,表现为相加作用,见表2。黄连煎煮液对2%硝酸咪康唑溶液抗白念珠菌有较好的抗菌增效作用。
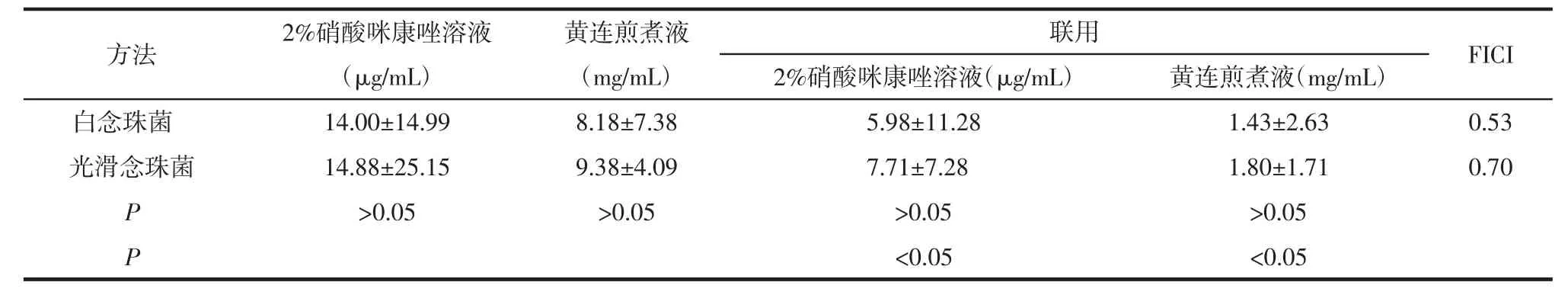
表2 单用和联用2%硝酸咪康唑溶液、黄连煎煮液作用于临床菌株的MIC均值及FICI值
2%硝酸咪康唑溶液+黄连煎煮液共同作用于15株光滑念珠菌的MIC值,其中2%硝酸咪康唑溶液的MIC值见表1,其MIC均值为(7.71±7.28)μg/mL。其中黄连煎煮液的MIC值见表1,其MIC均值为(1.80±1.71)mg/mL。二者的 FICI=0.70,表明 2%硝酸咪康唑溶液+黄连煎煮液共同作用于白念珠菌后,表现为相加作用,见表2。黄连煎煮液对2%硝酸咪康唑溶液抗光滑念珠菌有较好的抗菌增效作用。
2%硝酸咪康唑溶液、黄连煎煮液二者单用作用于白念珠菌、光滑念珠菌的MIC值和2%硝酸咪康唑溶液+黄连煎煮液共同作用后的MIC值比较,行单样本t检验,P<0.05为差异有统计学意义;说明联用后二者对白念珠菌、光滑念珠菌的敏感性均明显增加。
3 讨论
黄连为毛茛科的黄连、三角叶黄连或云连的干燥根茎。始载于《神农本草经》,一直被列为上品[8]。《本草纲目》载曰:“其根连珠而色黄,故名”[9]。该药性寒味苦,气味俱厚,归心、胃、肝、大肠经,可去除中焦湿热,泻心火,为清热燥湿、泻火解毒之要药。
黄连在临床上的应用非常广泛,其抗菌作用是在历年文献报道中最多的,有“中药抗生素”的美称。黄连的抗菌谱较广,无论是对于真菌如各类念珠菌感染[10-11]等,还是革兰氏阳性菌如金黄色葡萄球菌[12]、耐甲氧西林金黄色葡萄球菌[13-14]、超广谱-β内酰胺酶肺炎球菌感染等,革兰氏阴性菌如铜绿假单胞菌[15-16]、大肠埃希菌[17-18]、耐药鲍曼不动杆菌[19-20]、淋病奈瑟氏菌感染[21]等,均有很好的抗菌作用。广泛用于皮肤系统、呼吸系统、消化系统、血液系统、泌尿系统以及浅表真菌感染类疾病。
现代药理研究证明:黄连的主要有效成分为:黄连素、香草酸、落叶松树脂醇、小檗碱,丹参素甲酯、氧化小檗碱等[22]。黄连尤其是黄连的活性成分如小檗碱在体外细胞研究中发现有广泛的药理活性,广泛应用于抗菌抗炎、神经调节、抗肿瘤、抗糖尿病等几大方面。大量的研究表明黄连的功效可能和中药黄连多靶点的作用机制有关[23]。对于深部真菌感染(白念珠菌),黄连提取液同样有非常理想的抗真菌作用,研究表明黄连的醇提取物较黄连水提取物能更好地抑制白色念珠菌的活性[24]。基于以上研究基础及黄连作用机制的复杂性,笔者未采用黄连的某一成分如黄连素等进行研究,而是选用黄连煎煮液,这样能更全面的了解中药黄连的抑制皮肤念珠菌的效果。而黄连在抗真菌的作用体外研究表明[25]:黄连能抑制白念珠菌生长,同时能下调阴道组织中转化生长因子(TGF)-β1的表达,通过下调 TGF-β1的表达,来改善阴道局部的免疫状态,这可能是黄连抑制白念珠菌病发生及复发的重要作用机制,因此推测黄连有望成为一种新的治疗复发性白念珠菌阴道炎的靶向药物,而其具体详细的作用机制值得进一步研究。
本体外实验表明,2%硝酸咪康唑溶液、黄连煎煮液在抗阴道白念珠菌、光滑念珠菌方面均有稳定可靠的抑菌效果。2%硝酸咪康唑溶液联用黄连煎煮液后,二者MIC值均较单用明显降低,而且这种降低差异有统计学意义(P<0.05);一定程度上说明,联用黄连煎煮液后增强了2%硝酸咪康唑乳液对白念珠菌及光滑念珠菌对药物的敏感性,增强了二者的抑菌作用,从而表现出较单用药物更理想的抑菌作用。本课题组前期研究表明:香莲外洗液在临床研究和实验室的研究中对2%硝酸咪康唑溶液均有明显的抑菌作用和增效作用[26-27]。而黄连是香莲外洗液的君药之一,黄连在本体外实验中发挥的作用和香莲外洗液的作用效果保持一致,单用即对白念珠菌、光滑念珠菌均有明确的抑菌作用,同2%硝酸咪康唑溶液联用之后,对白念珠菌、光滑念珠菌的抑菌作用增强,表现出对2%硝酸咪康唑溶液明显的协同作用和增效作用。这一发现为单药外用及复方中药治疗VVC有效抑菌性及联用抗真菌药后的增效性进一步提供了实验室依据,为治疗顽固性复发性念珠菌阴道炎的治疗提供一种新的有效的方法,同时也为临床其他皮肤真菌治疗的药物选择提供了参考方案。
值得说明的是,虽然二者联用后对白念珠菌、光滑念珠菌的敏感性均明显增加,但通过比较2%硝酸咪康唑溶液+黄连煎煮液共同作用于白念珠菌、光滑念珠菌的MIC值,笔者发现2%硝酸咪康唑溶液对白念珠菌、光滑念珠菌的MIC值比较差异无统计学意义,表明白念珠菌和光滑念珠菌均对2%硝酸咪康唑溶液普遍敏感;另外,联用后黄连煎煮液对白念珠菌、光滑念珠菌的MIC值比较差异无统计学意义,表明白念珠菌、光滑念珠菌对黄连煎煮液普遍敏感;以上数据在一定程度上说明,二者联用后对白念珠菌、光滑念珠菌的增效作用是相当的,没有表现为对白念珠菌或者光滑念珠菌抑菌更明显的现象。一定程度上表明二者对白念珠菌和光滑念珠菌抑制的普遍性、稳定性和有效性。
由于实验条件的限制,本研究结果存在一定的局限性。其中可能的影响因素在于以下2个方面:一是药物的选择及实验方法本身的不足可能产生的对结果的影响,CLSL推荐的M27-A3方案中所用药物为氟康唑药粉剂,而本研究中所用药物为2%硝酸咪康唑溶液,这主要是考虑到临床的实际需求。因为医者们在临床中治疗外阴念珠菌性阴道炎最常用的药物成分是硝酸咪康唑成分,硝酸咪康唑也是欧洲国际性病控制联盟列为治疗VVC首选药物[4],为了进一步验证硝酸咪康唑成分在体外对念珠菌的抑菌能力,以及体外联用黄连煎煮液的抑菌效果,所以实验中选用了硝酸咪康唑溶液(硝酸咪康唑没有粉剂)。这样实验数据对临床VVC的治疗方案的选择更有指导意义说服力。此外,本实验严格按照CLSI推荐的M27-A3方案,参照氟康唑药敏操作规范进行的。而其他文献报道中较少采用此标准,一般采用纸片法,通过观察抑菌圈的大小等进行判定,因此所采用的方法和判定标准有所不同,可能会导致最终结果的差异。二是菌株来源及保存,既往文献报道中多采用标准菌株,而本实验所采用的菌株均为临床VVC患者阴道分泌物中培养出的菌株,不同的菌株也有可能会导致结果有所不同。此外,由于广东省中医院实验室的条件所有限,标本很难长时间保存。工作用的菌株置于10℃冰箱中贮藏,为了保证其活性,需要每隔2周进行1次接种培养,虽然实验在最短的时间内完成,但仍无法避免菌株的多次反复接种,菌株的反复接种是否会发生菌种变异,是否会导致对药物的敏感性不同,也是值得思考的问题。综上,在以上实验结果中,部分结果标准差偏大,可能和以上因素导致的一定误差有关。部分结果差异明显的,均抛弃。本实验过程均设有质控菌株,所有实验均在控,表明以上数据是可靠的。
综上,在体外实验中,黄连煎煮液、2%硝酸咪康唑溶液有明显的抑制白念珠菌、光滑念珠菌的作用;二者对白念珠菌和光滑念珠菌的抑菌作用是普遍的,有稳定性和有效性特点。2%硝酸咪康唑溶液联用黄连煎煮液后,明显增强了对2%硝酸咪康唑溶液对白念珠菌及光滑念珠菌对药物的敏感性,同时增强了2%硝酸咪康唑溶液的抑菌作用。本实验结果对于临床治疗VVC的指导意义重大,尤其是对于RVVC,不仅为中药单药外用治疗VVR有效抑菌性及联用抗真菌药后的增效性进一步提供了实验室依据,同时也为治疗顽固性复发性念珠菌阴道炎的治疗提供一种新的有效的靶向治疗方法。随着相关研究的深入,可望为VVC的致病机制探究提供新的切入点,为VVC的临床治疗提供更加有效安全的方法。
备注:该研究是作者在广东省中医院攻读博士研究生期间完成。

