钠离子电池磷酸盐正极材料研究进展
曹鑫鑫,周江,潘安强,梁叔全
中南大学材料科学与工程学院,长沙 410083
1 引言
随着高新科技的快速发展和城镇化进程的不断深入,能源和环境问题成为人类面临的重大挑战。目前人类消耗的能源主要是由煤炭、石油和天然气等化石燃料提供的。但是,地球上的化石燃料是历经上亿年才演化而成的,其储量有限且不可再生。同时,伴随着传统能源的大量消耗,衍生了一系列严峻的环境问题,如温室气体排放、酸雨、雾霾、热污染等。因此,优化能源供给结构、探索和应用可再生清洁能源、提高能源储存和转化效率、控制三废污染排放、改善气候环境成为世界能源格局可持续发展的重要战略目标。在新能源开发中,水能、太阳能、风能、潮汐能、生物能等绿色可再生清洁能源技术都具有重大的应用价值1。但这些能源供给的不稳定性和间歇性极大的限制了其并网使用。因此,开发与可再生新能源适配的高效储能系统尤为重要。另一方面,新能源汽车的推广是解决石油短缺和城市污染问题的有效途径。动力电池技术是新能源汽车发展的核心,开发高比能、高安全、低成本、长寿命的动力电池已成为新能源汽车持续发展和市场推广的瓶颈和关键所在。此外,随着移动互联网和通讯技术的高速发展,便携式电子设备、人工智能装备等正在迅速走进千家万户并改变着人们的生活方式,也推动着高能量密度、高安全二次电池技术的迅速发展。因此,开发二次电池储能新技术关系到人类的可持续发展与生产生活方式的改变2。
现有的二次电池体系包括铅酸电池、镍镉电池、钒液流电池、高温钠硫电池、锂离子电池和钠离子电池等3。其中铅酸电池和镍镉电池能量密度低、污染环境且存在记忆效应。钒液流电池运行和维护的成本较高,且钒氧化物易析出破坏电池结构。高温钠硫电池需要较高的工作温度,其安全问题不容小觑。锂离子电池由于其自放电慢、循环寿命长、无记忆效应、能量/功率密度高等优势在电化学储能领域占据主导地位。自从索尼公司在上世纪九十年代将锂离子电池成功商业化以来,锂离子电池的应用已经从最初的消费类电子产品迅速扩张到新兴电动/混合动力汽车、电网储能、航空航天等领域。锂离子二次电池如火如荼的迅速发展也使锂资源短缺的问题日益突出。锂在地壳中的含量约为0.0065%,其分布不均衡且提取难度大。这极大限制了锂离子电池在大规模储能领域的广泛应用4。
钠离子电池具有与锂离子电池类似的电化学脱嵌机理,且钠在地壳中的储量丰富(约占地壳储量的2.75%)、价格低廉(工业级碳酸钠约250美元/吨),近些年受到广泛关注5。但由于钠的离子半径比锂大,使得钠离子的扩散动力学迟缓,且易引起宿主材料体积应变,开发可稳定脱嵌钠离子的材料成为钠离子电池发展的关键6。另外,钠与锂相比原子质量更大且标准电极电势更高,可见钠离子电池的能量密度低于锂离子电池。但是钠离子电池以其成本和环保优势有望替代铅酸电池应用于低速交通和储能领域。
目前针对钠离子电池的研究主要集中在开发新型高能量密度电极材料、开发高安全性能的固态电解质、负极金属保护技术及电池管理系统等。其中,正极材料是直接影响电池整体性能的核心因素,它既是钠离子电池比能量提高的瓶颈,也是决定钠离子电池成本的最重要因素(约占整个电池成本的35%–40%)7,8。因此,钠离子电池技术能否取得新突破,其关键在于电极材料的创新研究。探索新型正极材料、调控材料结构、弄清电极结构与电化学性能之间的构效关系对发展高性能钠离子电池具有重要的科学意义与实际应用价值。
2 钠离子电池概述
2.1 钠离子电池的组成和特征
钠离子电池的结构与锂离子电池类似,一般由正极、负极、电解液、隔膜、集流体和电池壳等组成,如图1所示9。正极材料一般是电位较高的嵌钠化合物,如过渡金属层状氧化物NaxMO2(M为过渡金属)、聚阴离子型化合物和普鲁士蓝类似物等。负极材料一般是电极电位较低的碳材料、合金类材料及金属氧化物、硫化物等。电解液一般用有机溶剂和钠盐配制而成,常用的有机溶剂有碳酸乙烯酯(EC)、碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、乙二醇二甲醚(DME)、碳酸丙烯酯(PC)、碳酸甲乙酯(EMC)和氟代碳酸乙烯酯(FEC)等,常用的钠盐有高氯酸钠(NaClO4)、六氟磷酸钠(NaPF6)、双(三氟甲基磺酰)亚胺钠(NaTFSI)和三氟甲基磺酸钠(NaCF3SO3)等。隔膜一般是玻璃纤维、聚丙烯(PP)或聚乙烯(PE)微孔膜,主要用于隔离正负极材料防止内部短路,同时确保钠离子能够自由穿梭。
图1 钠离子电池的组成示意图9Fig. 1 Schematic of the composition for sodium-ion battery system 9.
与商业化锂离子电池相比,钠离子电池具有许多潜在的优势。首先是资源优势,钠是地壳中丰度排名第六的元素,大量存在于长石、方钠石和岩盐等矿物中。此外,海洋是一个巨大的钠资源库,其中氯化钠的含量约为2.7%。因此,作为钠离子电池原材料的钠金属和钠盐是非常廉价的。其次,钠离子电池的集流体更便宜、轻便。铝金属与锂容易发生反应生成二元合金,但对于钠是稳定的。因此,在钠离子电池中,铝可以取代昂贵的铜作为负极的集流体,且铝的密度低于铜,更有利于电池质量能量密度的提升。第三,金属钠比锂更柔软,可以通过机械压力或者改进隔膜的机械性能来抑制钠枝晶的形成10。但是钠离子电池也存在致命的缺陷,金属钠的熔点较低,易产生热失控现象。另一方面,钠离子半径比锂离子大34%,使得钠离子更难嵌入电极材料晶体结构中,发生化学反应。由于钠离子的体积较大,储钠材料的比容量一般低于储锂化合物,且其晶体结构中需要足够大的间隙来容纳钠离子。
2.2 钠离子电池的工作原理
图2为钠离子电池的工作原理示意图11。采用不同的正负极材料,其脱嵌钠离子的机理有所不同。这里以层状NaMnO2为正极材料、硬碳为负极材料的钠离子电池为例阐述其工作原理,其正负极反应式如下:
正极反应:
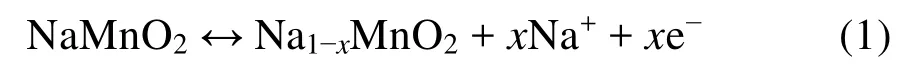
负极反应:
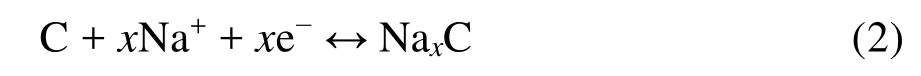
电池反应:
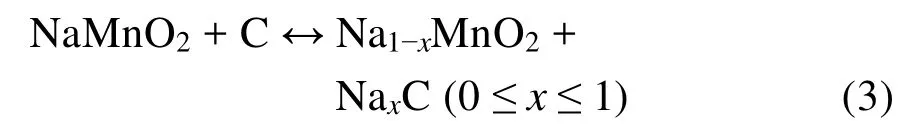
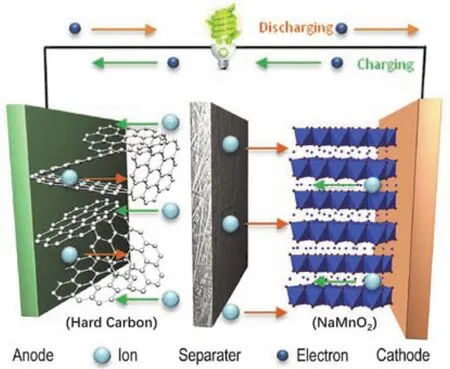
图2 钠离子电池的工作原理示意图11Fig. 2 Schematic of mechanism illustration for sodium-ion battery 11.
充电时,在外电压的作用下正极材料发生氧化反应同时伴随着钠离子从其晶格中脱出,钠离子穿过电解液和隔膜到达负极并嵌入硬碳负极中。此时正极处于贫钠状态,而负极处于富钠状态,同时外电源提供的补偿电荷流向负极使其发生还原反应。正负极之间形成电势差,同时将电能转化为化学能储存于钠离子电池中。放电过程恰好相反,钠离子从负极材料中脱出,经过电解液的传输到达正极并嵌入正极材料晶格中。同时电子经外电路从负极流向正极,即形成驱动电流。可见,钠离子电池的工作原理与锂离子电池非常相似。所以钠离子电池材料体系的创新探索可以借鉴锂离子电池较为成熟的研究经验。
2.3 钠离子电池正负极材料概述
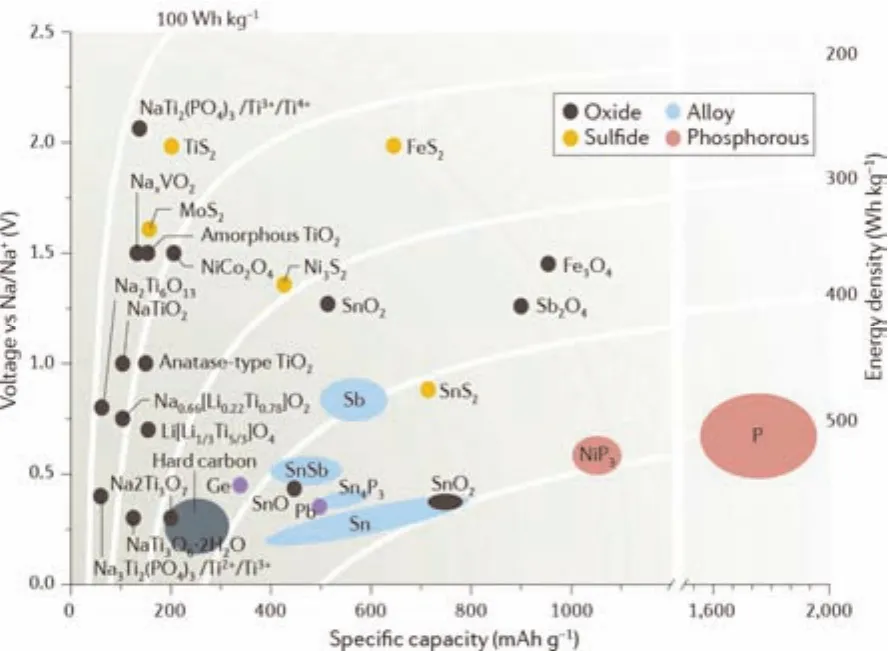
图3 钠离子电池负极材料的工作电压和比容量对比12Fig. 3 Operation voltages versus specific capacities of sodium-ion battery anode materials 12.
对于钠离子电池负极材料,一般要求较低的输出电位,通常在0.0–1.0 V (vsNa+/Na)之间。理想的钠离子电池负极材料应具有以下特征:高可逆的质量和体积比容量、相对正极更低的电位平台、高倍率性能、长循环寿命、低成本、优异的稳定性和环境兼容性。图3总结了钠离子电池负极材料的工作电位和比容量特性12。主要包括三类:(1)碳基材料,包括硬碳、软碳、石墨烯和碳纳米纤维等;(2)合金类,许多金属或非金属元素,如锡、锑、锗和磷等都可以和钠金属合金化,来充当钠离子电池的负极材料;(3)过渡金属氧化物和硫化物等。硬碳是钠离子电池最受关注的负极材料,可以释放出高达350 mAh·g-1的比容量,已非常接近石墨中的储锂容量。异质原子掺杂和结构优化可以有效提升碳材料的储钠性能,但是需要精准控制掺杂类型及掺杂量。对于大规模储能应用,应该首选生物质碳材料。降低制备成本、提高储钠容量、提升首次库伦效率和倍率性能是目前碳基负极材料亟需解决的关键问题。同时,需要对硬碳材料中的钠离子存储机制进行深入解析,研究表面含氧官能团如羧基、羰基与醛基等对电极过程的影响,揭示比表面、褶皱、杂原子、缺陷结构等对电化学行为的作用规律,为开发高性能、实用型的硬碳负极材料奠定理论基础13。转化反应类材料具有较高的可逆容量,但是循环稳定性和倍率性能有待进一步提升。电子导电性差和体积变化大严重影响了其性能的发挥。通过材料结构纳米化和导电碳修饰可以克服部分缺陷。但转化反应中结构重排引起的电压滞后现象需更深入的研究和解决14。合金化反应类材料是一种极具潜力的高容量钠离子电池负极材料,特别是锡、锑和磷。与钠合金化过程中伴随着巨大的体积膨胀会导致容量迅速衰减。通过碳包覆、纳米化、金属间复合可以有效提升材料的结构稳定性。探索合适的纳米结构及复合金属表界面储钠机制的解析仍存在巨大的挑战15。此外,钛基材料也受到一定的关注,但其储钠性能有待进一步提升,且需要深入理解钛基材料与电解液之间的催化反应并寻求有效抑制方法16。
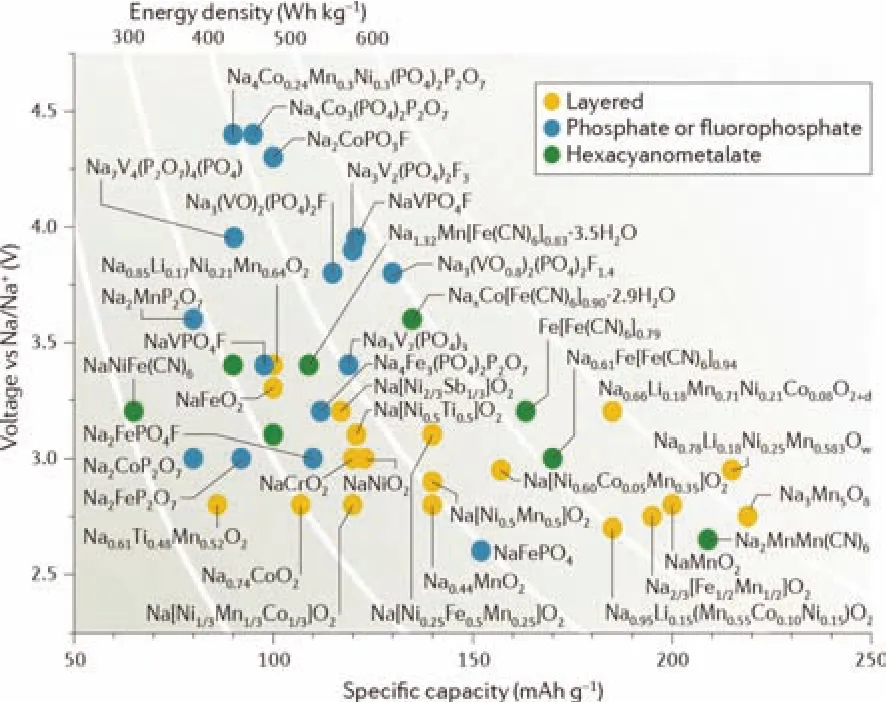
图4 钠离子电池正极材料的工作电压和比容量对比12Fig. 4 Operation voltages versus specific capacities of sodium-ion battery cathode materials 12.
图4总结了钠离子电池正极材料的工作电位和比容量特性12。根据材料的晶体结构与化学成分可以将钠离子电池正极材料分为三大类,它们都有合适的空间和通道供钠离子存储和输运。其中包括:(1)过渡金属氧化物类NaxMO2(M = Co、Mn、Fe或Ni),层状过渡金属氧化物具有α-NaFeO2型结构,氧原子为立方密堆积排列,结构中形成了供钠离子扩散的一维、二维或三维通道。(2)普鲁士蓝类似物,这类材料具有一个立方体框架(KM2(CN)6),由于其开放的立方框架结构和充足的空间间隙位置,允许碱金属离子可逆的脱出和嵌入。(3)聚阴离子化合物是另一类极具发展前景的正极材料,由于其结构稳定性好、安全性高、随充放电体积变化小等优势而受到广泛关注。聚阴离子强烈的诱导效应可以调节过渡金属氧化还原对的能量,从而产生较高的工作电压。NASICON (Na Super Ionic Conductor)型化合物具有菱方晶胞结构,离子迁移速率快。这些化合物的分子通式为A3M2(XO4)3(A为碱金属阳离子,M为过渡金属,X为P、Si、As等),NASICON框架由XO4四面体与MO6八面体共享角原子组成。M2(XO4)3开放的框架结构可供钠离子快速传输,其晶胞间隙至少可以容纳4个碱金属阳离子。因此,NASICON型化合物是一种很有前景的钠离子电池正极材料。氟磷酸盐类化合物,包括Na2MnPO4F、NaVPO4F、Na3V2(PO4)2F3、Na1.5VOPO4F0.5和Na2FePO4F等,碱金属离子存在于MO4F2(M为过渡金属)的隧道结构中。高电负性的F离子与磷酸根结合,由于氟离子的强诱导作用,使活性氧化还原对的电压升高,形成了一类很有潜力的高能量密度正极材料。
3 影响钠离子电池工作电压的因素
钠离子电池的工作电压是由整个电池体系的多个组分共同决定的,包括正极、负极和电解液。通常正极和负极的化学势差称为工作电压,即电池的开路电压(Voc)17:

而在实际放电过程中的电压又存在少量降低,这与离子在电解液和电极/电解液界面的输运有关17:

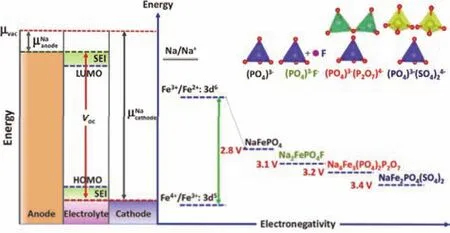
图5 钠离子电池铁基聚阴离子正极材料的能量图18Fig. 5 Schematic derivation of the energy diagram of iron-based mixed polyanion cathode materials for sodium-ion batteries 18.
其中电压损失η称为极化或过电势。如图5所示18,钠离子电池的工作电压受电解液的电化学窗口的限制,由最高占据分子轨道(Highest Occupied Molecular Orbital,HOMO)和最低未占分子轨道(Lowest Unoccupied Molecular Orbital,LUMO)的能量差决定。在选择正负极材料时,正极材料的电化学势μC需位于电解液HOMO上方,负极材料的电化学势μA需位于电解液LUMO的下面。当正极材料的电化学势μC低于电解液HOMO时,电解液中的电子会被正极材料俘获,从而电解液被氧化和钝化,导致正极材料表面形成固液界面层,加剧极化。当负极材料的电化学势高于电解液LUMO时,负极材料的电子会被电解液夺取,因而电解液被氧化,反应产物在负极材料颗粒表面形成固液界面层(Solid Electrolyte Interface Film,SEI膜)。SEI膜的形成消耗的电解液中的钠离子且增加了电池的内阻,导致电池的功率和容量降低19。研究表明,钠离子电池中碳酸酯类电解液的最高稳定电压上限约为4.2 V,而当正极材料如层状氧化物的氧化还原电位超过电解液的HOMO极限时,将限制了其能量密度的发挥20。
影响钠离子电池输出电压的另一个重要因素是正极材料的工作电压。由于电池的能量密度取决于材料的比容量和工作电压,因此,通过提升高比容量正极材料(如过渡金属氧化物和磷酸盐类)的工作电压是一种提高电池的能量密度的有效途径。正极材料的工作电压和其过渡金属氧化还原对的电势直接相关,过渡金属离子的电子结构(3d4s)中3d轨道电子的失去或获得对应于充放电过程中的氧化或还原。通常对于相变反应机制的同系列材料MX (M为过渡金属,X为F、O、S、N、P),其工作电压的排序为:Cu > Ni > Co > Fe > Mn >Cr > V > Ti,而阴离子P轨道能级的位置会对电极材料的电压产生影响,对于不同阴离子的化合物,其工作电压的排序一般为:氟化物 > 氧化物 >硫化物 > 氮化物 > 磷化物21。此外,同样的正极材料在不同的电池体系中的工作电压也有所不同,一般遵循的规律为:Li电池> K电池 > Na电池 > Mg电池 > Al电池21。
在聚阴离子类化合物中,由于强电负性的聚阴离子基团诱导效应的不同,使得过渡金属氧化还原对的电势也有所区别。图5中以铁基聚阴离子化合物为例,分析了(PO4)3-、(PO4)3-F-、(PO4)3-(P2O7)4-、(PO4)3-(SO4)24-四种聚阴离子对Fe2+/Fe3+氧化还原对的费米能级的影响18。不同聚阴离子的组合可以通过结构的多样性和不同程度的诱导效应来调节氧化还原电压高度。这种通过聚阴离子组合调控氧化还原对能级进而调控电极材料工作电压的方法也适用于其它的电化学氧化还原对,如Mn2+/Mn3+、V3+/V4+、Ni2+/Ni3+、Co2+/Co3+等19。
由此可见,钠离子电池的工作电压主要取决于正负极之间的电势差,而普遍认为正极材料是提升钠离子电池比能量的瓶颈,因此需要大力开发先进的正极材料。目前,对钠离子电池正极材料的研究主要集中在三类化合物。第一类是钠过渡金属氧化物,这些材料具有高可逆容量和高工作电位,但它们中的大多数仍存在不可逆相转变、空气中不稳定和性能退化严重等问题。另一类是普鲁士蓝类似物,这些材料具有良好的工作电压、循环稳定性和倍率能力,其实际应用的主要障碍是晶格缺陷、热不稳定性和低振实密度。聚阴离子化合物是另一类极具发展前景的正极材料,由于其结构稳定性好、安全性高、随充放电体积变化小等优势而受到广泛关注。迄今为止,许多铁、钒和锰基聚阴离子化合物已经被广泛和深入的研究。
4 钠离子电池磷酸盐正极材料
聚阴离子化合物是由强共价键构成的三维框架结构,因此具有较高的结构稳定性。其稳定的框架结构具有快速的钠离子扩散速率且离子脱嵌过程中体积变化小、相变少,从而保障了在钠离子电池中良好的循环稳定性和优异的安全性。但聚阴离子化合物中庞大的阴离子基团也会导致其比容量低且电子导电性差。聚阴离子化合物结构多变、种类繁多,包括磷酸盐、氟磷酸盐、焦磷酸盐、混合磷酸盐等。
4.1 正磷酸盐类
4.1.1 NaFePO4
NaFePO4是最早被研究的钠离子电池聚阴离子型正极材料,如图6所示,它具有两种不同的结构类型:磷铁钠矿相(Maricite phase,m-NaFePO4)和磷铁锂矿相(Triphylite phase,t-NaFePO4)。t-NaFePO4是由共顶点的FeO6八面体和PO4四面体共边构成空间骨架,沿着b轴方向,t-NaFePO4具有一维的钠离子扩散通道(图6b)。而m-NaFePO4的结构是由共角的FeO6八面体和PO4四面体构成,其结构中没有钠离子的输运通道(图6a)。因此,通常认为磷铁钠矿相NaFePO4是一种没有电化学活性的结构。
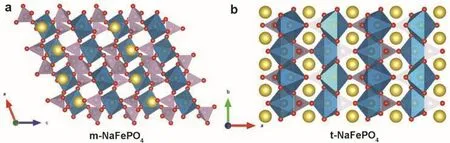
图6 NaFePO4的两种晶体结构:(a)磷铁钠矿相;(b)磷铁锂矿相Fig. 6 Crystal structures of (a) Maricite-type and (b) Triphylite-type NaFePO4.
NaFePO4的热力学稳定相是磷铁钠矿相而非磷铁锂矿相,亚稳态的t-NaFePO4在480 °C以上就会相变为热力学稳定的m-NaFePO422,因此传统的高温固相法难以合成t-NaFePO4。Baudrin等23最先发现LiFePO4结构中的锂离子可以被钠离子取代。之后,研究者们对t-NaFePO4的制备和表征进行了一系列研究。采用在有机溶液或者水溶液中的化学或电化学离子交换反应可以制得纯相t-NaFePO424–26。Cao等26以LiFePO4/C为工作电极、活性炭作为对电极、Ag/AgCl为参比电极,在水溶液中通过的两步电化学转化过程制备了微球结构的磷铁锂矿相NaFePO4。得到的NaFePO4/C正极在0.1C的倍率下释放出111 mAh·g-1的比放电容量和良好的循环稳定性,经过240此循环后容量可以保持90%。同时,他们采用传统的电化学技术发现在放电时Na+嵌入的过程中存在一个中间相Na2/3FePO4,证实了在脱钠和嵌钠的过程中均存在相同的两步相变反应。Pan等25采用类似的离子交换法成功制备了高纯的橄榄石结构NaFePO4,通过从头计算法和实验相结合,证明了在水系电解液和阴极界面处的离子交换动力学与有机电解液相比更快。此外,他们采用原位同步辐射和非原位XRD研究了t-NaFePO4在脱嵌钠时的相变过程。如图7所示,在充电的过程中,NaFePO4首先完全转变为中间相Na2/3FePO4,随后进一步脱钠形成FePO4。在放电时,FePO4首先部分转变为中间相Na2/3FePO4,同时伴随着NaFePO4的形成,随着钠离子的进一步嵌入,最终完全转变为NaFePO4。Saracibar等27通过密度泛函理论(Density Functional Theory,DFT)计算结合高分辨同步辐射X射线衍射(XRD)发现NaxFePO4(0 ≤x≤ 1)存在两个稳定的中间相Na2/3FePO4和Na5/6FePO4,计算得到NaFePO4和Na2/3FePO4的嵌钠电压差为0.16 V,这与实验观察到的电压不连续相一致。Nazar等28报道了新型亚稳态橄榄石结构的金属磷酸钠盐。他们采用在熔融盐中的低温(100 °C)固相反应将NH4[Mn1-xMx]PO4·H2O (M = Fe、Ca、Mg)转化为Na[Mn1-xMx]PO4,将钠离子电池橄榄石结构正极材料拓展到Na[Mn1-xMx]PO4(M = Fe、Ca、Mg)。与橄榄石型LiMPO4(M = Fe、Mn)不同,在Na1-xMn0.5Fe0.5PO4中观察到了连续固溶过程的离子脱嵌机制。
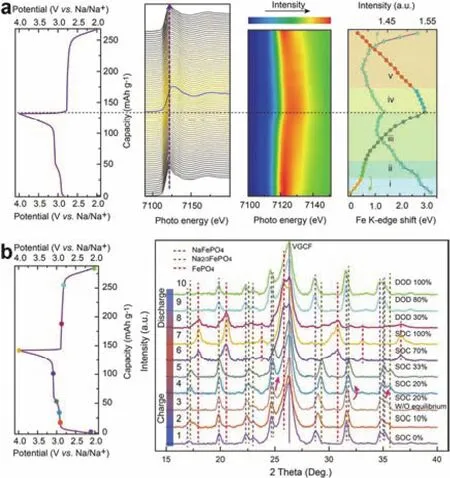
图7 NaFePO4首圈循环过程中的(a)原位同步辐射铁K边X射线吸收近边结构和(b)非原位XRD 25Fig. 7 (a) In situ synchrotron Fe K-edge XANES and (b)ex situ XRD studies of the NaFePO4 during initial cycles 25.
研究者们还对NaFePO4和LiFePO4的结构和电化学动力学行为进行了对比研究29–31。Wang等29通过实验手段对比了NaFePO4和LiFePO4的热力学和动力学行为,通过平衡电位、离子扩散系数和反应电阻的对比研究发现NaFePO4中的钠离子扩散缓慢且接触和荷转移电阻更大,导致了其倍率性能较差。Nakayama等31通过第一性原理DFT计算发现NaFePO4和LiFePO4中的电子迁移能几乎没有区别,而NaFePO4中的钠离子迁移能比LiFePO4的锂离子迁移能更大。因此,研究者们通过导电聚合物包覆32、微钠结构控制26,29及电解液优化33等手段对t-NaFePO4进行性能改性。
在很长一段时间里,人们认为磷铁钠矿相NaFePO4是不具有电化学活性的,这一定论被Kang等打破34。他们采用量子力学计算与实验手段相结合首次证明m-NaFePO4结构中的钠离子可以可逆脱出和嵌入。通过对m-NaFePO4中离子脱嵌机理的研究发现其结构中所有的Na+都可以脱出。非原位XRD和同步辐射分析结果表明钠离子首次脱出后,m-NaFePO4转化为非晶α-FePO4,使得钠离子的传输势垒大大减小。m-NaFePO4首次放电比容量为142 mAh·g-1,为理论值的92%,且具有优异的稳定性,经过200次循环后容量保持率为95%。最近,Fan等35采用静电纺丝法成功制备了氮掺杂碳纤维封装m-NaFePO4量子点复合材料(图8a,b),这种独特的微纳结构可以有效增加活性材料的利用率、提升电子和离子的传输速率且稳定电极的结构。这种m-NaFePO4/C复合材料在0.2C的倍率下释放出145 mAh·g-1高可逆容量,即使在高达50C的大倍率下仍可释放61 mAh·g-1的比放电容量,且在5C的倍率下经过6300次循环后容量可保持89%(图8c)。此外,研究者们通过增加m-NaFePO4的无序化程度36、构建快速电子传输网络37,38和构筑协同优势的复相材料39等手段来提升磷铁钠矿相NaFePO4的电化学性能。Huang等40通过水热法合成了一种分级结构的Na0.67FePO4/CNT复合材料,其放电比容量为143 mAh·g-1,循环性能较稳定。但其首次充电容量非常低,这限制了其实际应用。
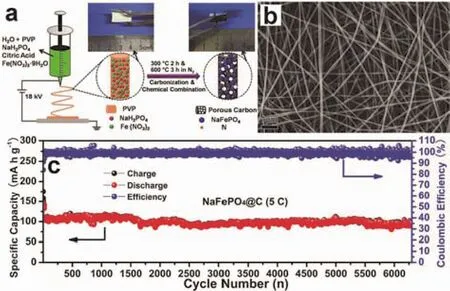
图8 NaFePO4@C的(a)制备过程示意图,(b) SEM图像和(c)长循环性能35Fig. 8 (a) Schematic illustration of the preparation process, (b) SEM image, and (c) long-term cycling performance of the NaFePO4@C 35.
与NaFePO4类似,NaMnPO4也有两种晶体结构:磷铁钠矿型结构和橄榄石型结构。据报道,采用高压环境中的离子交换法可以制备出橄榄石型NaMnPO4,采用低温(400 °C)固相法可以合成磷铁钠矿NaMnPO441。Johnson等42测试了NaCoPO4用于钠离子电池正极材料时的性能表现。然而,目前报道的这两种材料都没有表现出很好的电化学性能,但通过结构优化和电解液改性等手段有望获得更好的性能。
4.1.2 NASICON结构Na3V2(PO4)3
NASICON结构材料具有快速的钠离子传输通道和稳定的三维框架结构,在电极材料、固态电解质等领域被广泛研究。通常这种化合物以热力学稳定的菱方晶胞结构(空间群:)存在。但是部分A3M2(PO4)3(A = Li、Na,M = Cr、Fe、Zr)类材料也以单斜结构存在,且在高温条件下表现出可逆的结构相变43。Na3V2(PO4)3是一种代表性的NASICON结构材料,作为钠离子电池正极材料受到广泛的关注。如图9a所示,NASICON结构中Na3V2(PO4)3是由VO6八面体和PO4四面体组成共价骨架[V2P3O12],骨架之间形成了三维互联的隧道结构和两种钠离子分布间隙位置(M1和M2)。在钠离子电池中,Na3V2(PO4)3基于V3+/V4+和V2+/V3+氧化还原对的工作电压分别为3.4和1.6 V,因此Na3V2(PO4)3既可以用作正极材料又可以用于负极材料,对应的理论容量分别为118和50 mAh·g-144。
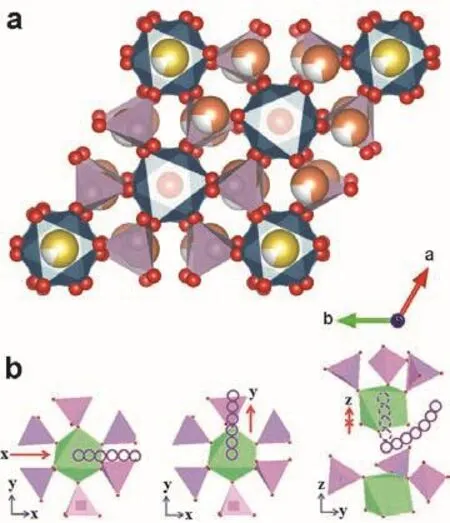
图9 Na3V2(PO4)3的(a)晶体结构和(b)离子迁移路径45Fig. 9 (a) Crystal structure and (b) ion migration paths of Na3V2(PO4)3 45.
研究者们采用多种谱学技术、电化学、理论计算等手段来探究Na3V2(PO4)3中钠离子的储存机理。为了解析Na3V2(PO4)3结构中的离子扩散通道,Ji等45通过第一性原理计算研究了其离子迁移活化能。结果表明,Na3V2(PO4)3结构中沿着x、y方向的两条通道和另一条弯曲的迁移通道构成了其三维的离子输运路径(图9b)。Hu等46采用电化学原位XRD技术研究了Na3V2(PO4)3中钠离子的脱嵌机制(图10a),随着钠离子的脱出,Na3V2(PO4)3的衍射峰逐渐变弱而NaV2(PO4)3的衍射峰逐渐增强,在嵌钠后Na3V2(PO4)3的结构又能完全恢复,表明在3.4 V处的钠离子脱出/嵌入是典型的两相反应机制,而Na3V2(PO4)3和脱钠相之间的体积变化仅为8.26%。他们还通过球差矫正环形明场相扫描电子显微技术(ABF STEM)直接观察到了钠离子的脱出位置47。图10b,c中显示了Na3V2(PO4)3和NaV2(PO4)3的钠原子的位置,其中Na3V2(PO4)3中钠原子同时占据M1和M2位置,而NaV2(PO4)3中的钠原子只占据M1位置,说明只有M2位置的钠离子参与电化学脱嵌反应,与ABF图像相对应的线型分布情况也验证了这一结果(图10c,d)。
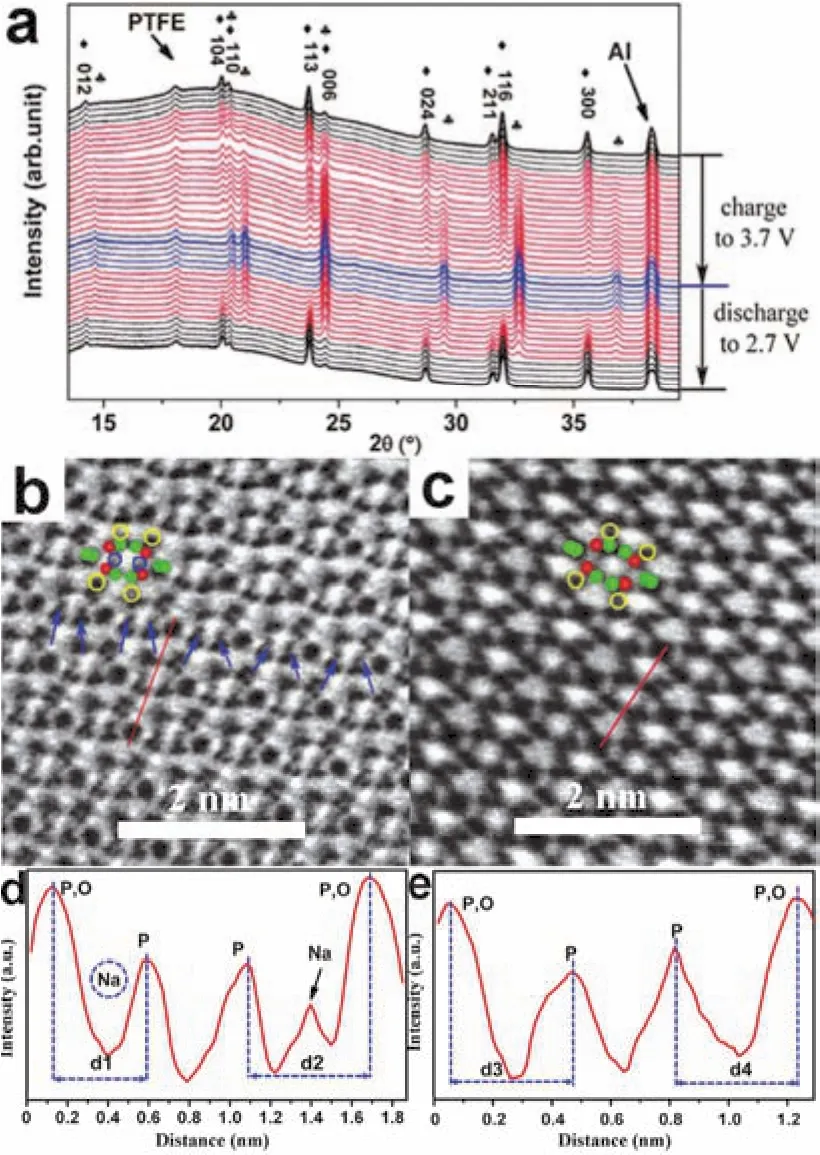
图10 (a) Na3V2(PO4)3/Na电池的原位XRD谱,♦ Na3V2(PO4)3, ♣ NaV2(PO4)3 46;(b) Na3V2(PO4)3和(c) NaV2(PO4)3沿着[]晶带轴的STEM ABF图像47;(d) Na3V2(PO4)3和(e) NaV2(PO4)3沿着ABF图像的线型分布47Fig. 10 (a) In-situ XRD patterns of the Na3V2(PO4)3/Na cell, ♦ Na3V2(PO4)3, ♣ NaV2(PO4)3 46; STEM ABF images of(b) Na3V2(PO4)3 and (c) NaV2(PO4)3 along the []projection 47; Line profiles along in the ABF images of(d) Na3V2(PO4)3 and (e) NaV2(PO4)3 47.
尽管Na3V2(PO4)3具有结构稳定、工作电压较高等优点,但低电导率依然是其商业应用的主要阻碍。Chen的团队48最先报道了一步固相法制备碳包覆Na3V2(PO4)3,在有机体系钠离子电池中表现出3.4 V (vsNa+/Na)的电压平台。其首圈充放电比容量分别为98.6和93 mAh·g-1,表明碳包覆可以有效改善Na3V2(PO4)3的储钠性能。在过去的几年中,研究人员采用了许多不同的方法来克服这个缺点,主要涉及微纳结构调控、表面包覆改性、元素掺杂等49–51。为了优化Na3V2(PO4)3的微观形貌,进一步提升其电子导电性和结构稳定性,研究人员尝试了各种合成策略,如传统的固相反应52、溶胶凝胶法53、静电纺丝法54、水热和溶剂热法等55。Mai等56采用一种基于水热反应的自牺牲模板法合成了三维Na3V2(PO4)3纳米纤维,他们首次提出一种基于反应时间的由外向内的形貌演化机制。合成的Na3V2(PO4)3正极材料在钠离子半电池和全电池中均表现出优异的循环稳定性和倍率性能。最近,Cao等55通过水热反应法制备了一系列由纳米片组装的Na3V2(PO4)3/C分级微球,制备的Na3V2(PO4)3/C纳米晶被氮掺杂碳紧密包覆。他们系统研究了水热反应时间和前驱体浓度对Na3V2(PO4)3/C微纳结构的影响并提出了结构生长机制(图11)。作为钠离子电池正极材料,Na3V2(PO4)3/C多孔微球表现出优异的倍率性能和循环稳定性,在100C倍率时可释放99.3 mAh·g-1的放电比容量,在20C倍率下经过10000次长循环后容量保持79.1%。采用Na3V2(PO4)3/C为正极、SnS/C纤维为负极的钠离子全电池能量密度可达223 Wh·kg-1。独特的微纳结构设计和氮掺杂碳包覆有效构筑了双连续的电子和离子扩散通道,增加了电极和电解液的接触面积同时增强了结构稳定性,进而造就了Na3V2(PO4)3/C多孔微球优异的电化学性能。
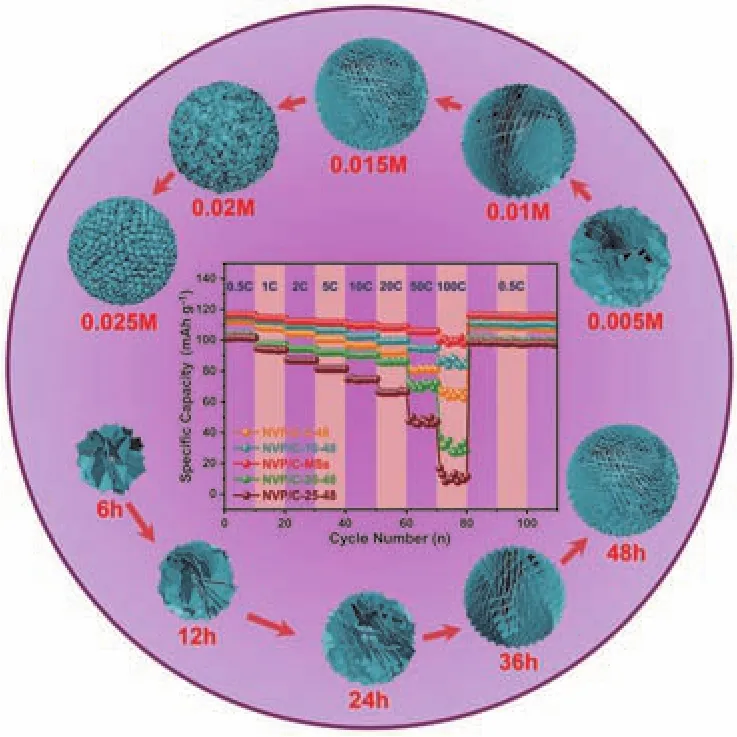
图11 水热反应法制备的Na3V2(PO4)3分级微球的形貌演化过程和倍率性能55Fig. 11 Morphological evolution process and rate performance of Na3V2(PO4)3 hierarchical microspheres prepared by hydrothermal reaction 55.
表面改性也被广泛应用来提升Na3V2(PO4)3的电子导电性。碳包覆由于具有高电子导电性、成本低廉、化学稳定、在合成时或合成后都可以引入等优势,成为最具吸引力并被广泛使用的一种手段。研究者们采用了多种碳源和导电碳骨架来构筑碳包覆层。自从Balaya等57首次报道以阳离子表面活性剂作为碳源合成具有良好循环稳定性和优异倍率性能的Na3V2(PO4)3/C,研究者们开发了众多不同的碳包覆技术。Cao等52设计了一种在熔融烃类化合物中的固态反应制备三维石墨烯笼包覆Na3V2(PO4)3纳米片材料的方法(图12a)。他们在合成过程中使用的油酸不仅作为碳源,而且作为阴离子表面活性剂引导晶体定向生长。Na3V2(PO4)3纳米片被原位生成的3 nm厚的类石墨烯碳紧密覆盖。作为正极材料,石墨烯包覆Na3V2(PO4)3纳米片表现出优异的电化学性能,包括接近理论值的可逆容量(1C倍率下的可逆容量为115.2 mAh·g-1),优异的倍率性能(200C倍率下的比容量为75.9 mAh·g-1),并具有出色的循环稳定性(在50C倍率下30000圈循环后容量保持率为62.5%) (图12b)。此外,刻蚀掉Na3V2(PO4)3后残余的三维石墨烯笼也可作为钠离子电池的负极材料,并在0.1 A·g-1时提供242.5 mAh·g-1的比容量。分别使用这两种正极和负极材料的钠离子全电池可提供高比容量和良好的循环稳定性(图12c)。为了得到兼具高倍率性能和稳定性的Na3V2(PO4)3材料,另一种表面改性的有效策略是将Na3V2(PO4)3纳米晶粒嵌入相互连通的高导电碳骨架中。由于有机碳源高温热解后的导电碳大部分是无定型碳,而化学气相沉积法是一种制备一维石墨烯、二维碳纳米管等高导电碳材料的有效手段。因此,Cao等58采用简单、经济的化学气相沉积法构筑了分级结构碳骨架修饰的Na3V2(PO4)3。由类石墨烯包覆层和碳纳米管交联组成的分级碳骨架有效提升了Na3V2(PO4)3的电子传输效率,该材料在0.2C倍率时释放出接近理论值的容量,在30C倍率下经过20000次循环后容量保持率为54%。此外,氧化物包覆、导电聚合物包覆等也可以有效地提升Na3V2(PO4)3的电化学性能59。

图12 三维石墨烯笼包覆Na3V2(PO4)3纳米片的(a)合成示意图、(b)长循环性能和(c)全电池性能52Fig. 12 (a) Schematic illustration of the fabrication,(b) ultralong-life cycling performance, and (c) sodium-ion full-cell performance of 3D graphene capped Na3V2(PO4)3 nanoflakes 52.
元素掺杂是优化Na3V2(PO4)3电化学性能的另一种有效手段。Yang等60将较轻的Mg掺杂到Na3V2(PO4)3中V的位点,可以有效提升电极材料的性能。与未掺杂的Na3V2(PO4)3相比,采用简单溶胶凝胶法制备的Mg掺杂Na3V2-xMgx(PO4)3/C复合材料在倍率性能和循环性能方面均有明显提高。Goodenough等61设计并合成了一系列NASICON结构NaxMV(PO4)3(M = Mn、Fe、Ni) (图13a),其中Na4MnV(PO4)3正极材料在3.6和3.3 V处显示出两个电压平台,分别对应于Mn3+/Mn2+和V4+/V3+氧化还原对。此外,Na4MnV(PO4)3正极材料表现出97%的首圈库伦效率和长达1000次的循环寿命,是一种很有应用前景的高比能正极材料。最近,他们又开发出了一种具有更高电压平台的Na3MnZr(PO4)3钠离子电池正极材料62(图13b)。为了进一步提高碳包覆效果和其电子导电性,Wang等63在包覆碳层中引入氮掺杂。氮掺杂碳包覆Na3V2(PO4)3正极材料的电化学性能明显提升,尤其是其倍率性能。此外,他们还详细探讨了不同位置的氮原子掺杂对电化学性能的影响,结果表明,氮掺杂可以在包覆碳层中引入一些缺陷,促进Na+的输运和存储。最近,Yu等64通过构筑氮、硫共掺杂的石墨烯多孔导电骨架来改善Na3V2(PO4)3的电子导电性。此外,在V位置的多价离子掺杂(如Ni2+、Cr3+、Al3+)和Na位置的单价离子掺杂(如Li+、K+)都可以调控Na3V2(PO4)3的电子结构和离子扩散通道65–67。
除了研究较多的钒基NASICON结构材料,还有很多其它的NASICON结构化合物也可以用于钠离子电池,例如NaTi2(PO4)3、NaSn2(PO4)3、NaZr2(PO4)3、Na3Fe2(PO4)3、Na3Co2Fe(PO4)3、Na3TiFe(PO4)3、Fe2(MoO4)3、Na2Ni2(PO4)3等68,69。通过调整NASICON结构中过渡金属原子的类型对可以调控其在钠离子电池中的工作电压,为高比能钠离子电池正极材料的开发提供可能。
4.1.3 非晶型磷酸盐
目前常用的二次电池正极材料都是晶体材料,晶体材料中的离子存储受晶体结构、结晶性、择优取向及结构稳定性等因素影响。通常晶体材料中的离子脱嵌受其晶格中的传输通道影响。而非晶材料与晶体材料中原子团簇的排列方式是不同的,非晶材料中的原子团簇是短程有序且它们随机相连70,71。因此,非晶材料的XRD谱中没有衍射峰,传统的谱学技术很难表征。由于非晶材料具有长程无序而短程有序的特征,它们也具有一些独特的优势,例如各向同性、增强动力学、自由体积、利于调整晶格畸变等50。因此,非晶材料在钠离子电池中具有一定的应用潜力。Kim等72研究了不同价态离子(一价、二价、三价)在非晶FePO4中的储存性质(图14),在钠离子电池中,表现出高达179 mAh·g-1的比容量,同时他们发现在钠离子嵌入的过程中非晶FePO4有向结晶NaFePO4转变的趋势。Zhang等73,74进一步研究了FePO4嵌钠过程中的相变规律,他们发现非晶FePO4在嵌钠过程中同时转变为非晶NaFePO4和t-NaFePO4,而结晶FePO4在嵌钠过程中相变为m-NaFePO4。

图 13 (a) Na4MnV(PO4)3 61和(b) Na3MnZr(PO4)3 62的XRD谱和晶体结构Fig. 13 XRD patterns and crystal structures of (a)Na4MnV(PO4)3 61 and (b) Na3MnZr(PO4)3 62.
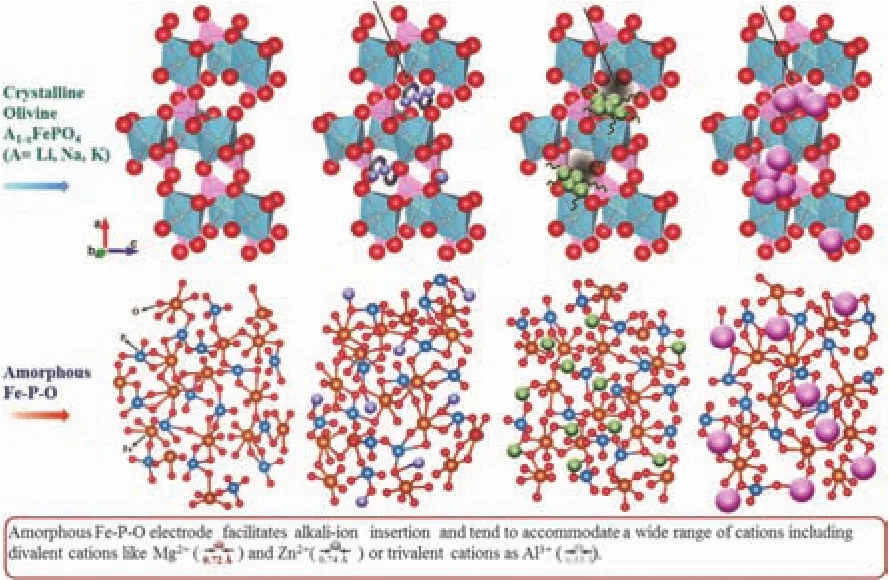
图14 碱金属离子嵌入结晶和非晶FePO4电极72Fig. 14 Schematic representation of alkali-ions(Li/Na/K) insertion in crystalline and amorphous FePO4 electrode hosts 72.
碳包覆/复合是提升非晶FePO4储钠性能的有效手段。Hu等75采用水热法成功制备了一种单壁碳纳米管连接多孔FePO4纳米颗粒,在0.1C的倍率下可以释放120 mAh·g-1的储钠容量。Cao等76采用简单的化学诱导沉淀法制备了一种介孔碳骨架修饰的非晶FePO4,制备的FePO4/C在20 mA·g-1电流密度下的首次放电比容量为151 mAh·g-1,且经过200次循环后其容量仍可保持94%。此外,研究者们还采用石墨烯77、多壁碳纳米管78、碳化聚苯胺79等构筑导电网络来改性非晶FePO4的电化学性能。
形貌调控也可以有效改善非晶FePO4的电化学性能,低维尺寸或者分级多孔结构可以有效缩短离子的固相传输距离、提供更多的电化学活性位点。Pan等80制备了一种二维非晶FePO4纳米片,由于其尺寸效应有效缩短了钠离子的传输距离和较大的比表面积增加了电容的贡献,非晶FePO4纳米片在0.1C倍率下可以表现出168.9 mAh·g-1的首次放电比容量,在1C倍率下经过1000次循环容量保持率为92.3%。此外,研究者们通过多种物理或化学手段合成了不同形貌的非晶FePO4材料,包括纳米球81、纳米线82等。无钠正极材料不利于实际产业应用,Tong等83通过模板法制备了中空结构的非晶NaFePO4,其首次放电比容量为152.1 mAh·g-1且经过300次循环其容量仍可保持94%,在高达10C的倍率下仍可释放出67.4 mAh·g-1的比容量。非晶磷酸盐正极材料的研究虽然取得了一些进展,但由于非晶材料结构的特殊性,关于其体相结构的热力学和动力学特性以及与电化学性能之间的深层关系还有待深入研究。
4.1.4 其它正磷酸盐 (VOPO4,NaVOPO4)
NaxVOPO4(x= 0, 1)也是一类很有潜力的钠离子电池正极材料。VOPO4具有多种不同的晶体结构 (图 15), 包 括 α/αI/αII-VOPO4, β-VOPO4, γ-VOPO4,δ-VOPO4,ε-VOPO4和ω-VOPO484。目前报道的NaVOPO4通常包括三种不同的结构(图15),分别为α-NaVOPO4(三斜晶系,空间群:P21/c),β-NaVOPO4(正交晶系,空间群:Pnma),和αINaVOPO4(四方晶系,空间群:P4/nmm)85。Goodenough等86最先将单斜晶系NaVOPO4用于钠离子电池正极材料,发现其工作电压为3.6 V (vsNa+/Na)并可以释放出90 mAh·g-1的可逆容量。Ong等84采用第一性原理计算对比研究了β、ε和αI三种VOPO4化合物的热力学稳定性、工作电压、能带结构和扩散动力学行为,发现只有αI-VOPO4表现出较低的钠离子扩散迁移势垒。Aparicio等87结合密度泛函理论计算和分子动力学方法研究了α、β和αI三种NaVOPO4化合物的离子扩散、电子结构和离子掺杂特性。结果表明,α、β和αI相分别表现出二维、一维和三维的离子迁移路径,其中αINaVOPO4表现出最优的离子扩散速率、通道和活化能,是一种很有潜力的钠离子电池正极材料。
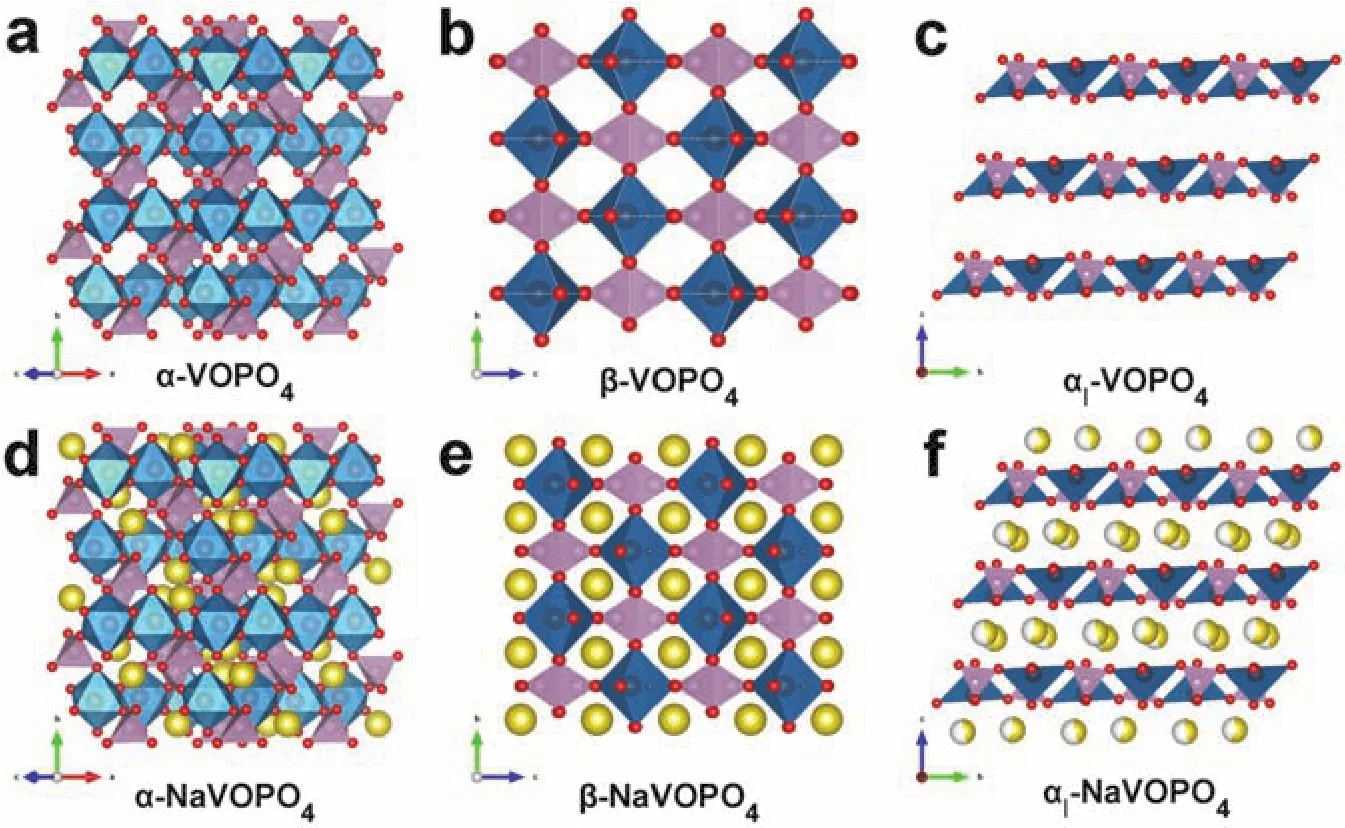
图15 VOPO4和NaVOPO4的晶体结构Fig. 15 Crystal structures of VOPO4 and NaVOPO4.
Manthiram等88采用化学方法将四方晶系αILiVOPO4中的锂离子脱出,制备了层状结构αIVOPO4正极材料,基于V4+/V5+氧化还原对,αIVOPO4的工作电压在3.5 V (vsNa+/Na)左右,且嵌钠后可以转变为层状αI-NaxVOPO4。电化学测试结果显示,纯相αI-VOPO4表现出110 mAh·g-1的可逆容量,通过与rGO复合后,其放电比容量高达150 mAh·g-1。最近Ren等89通过水热反应法直接制备了层状结构NaVOPO4,这种层状材料表现出3.5 V (vsNa+/Na)的工作电压、高达144 mAh·g-1的比放电容量和良好的循环稳定性(经过1000次循环后容量保持67%),其优异的电化学性能归因于层状结构提供了快速的钠离子迁移路径、导电碳修饰利于快速的电子传输。此外,他们通过原位XRD和原位同步辐射技术详细研究该层状NaVOPO4中的储钠机制。最近,Whittingham等90研究了一种新型KVOPO4材料的储钠性能。Yu等91,92通过二维材料的层间工程制备了不同层间距的VOPO4材料,并研究了它们层间距对离子存储的影响规律。此外,它们还将层状VOPO4应用于钠离子全电池中93,94,制备了一系列高比能且极具应用潜质的钠离子全电池器件。
4.2 氟磷酸盐类
4.2.1 NaVPO4F
如图16a,b所示,通常认为NaVPO4F含有两种不同的晶体结构:(1)低温单斜晶系结构,与NaAlPO4F (ICSD#40522)的晶体结构相同,其空间群为C2/c;(2)高温四方晶系结构,与Na2.82Al2(PO4)2F3(ICSD#88805)的晶体结构相同,其空间群为I4/mmm18。早在2003年,Barker等95就已经将四方晶系结构NaVPO4F应用于钠离子电池中,采用NaVPO4F作为正极、硬碳为负极的钠离子全电池显示出两对充放电电压平台且可以释放出82 mAh·g-1的可逆容量。之后针对NaVPO4F的研究大部分集中在其单斜相,Zhang等96采用一种高温熔融混合法合成了单斜结构NaVPO4F/C纳米片,制备的复合材料具有优异的电化学性能(图16c),在0.2C倍率下的首次放电比容量为135 mAh·g-1,在20C倍率下经过1500次循环后其容量仍能保持90.4%,他们还采用原位XRD技术证明了NaVPO4F中钠离子的两相反应存储机制(图16d)。

图16 (a)单斜晶系和(b)四方晶系NaVPO4F的晶体结构;NaVPO4F的(c)充放电曲线和(d)原位XRD谱96Fig. 16 Crystal structures of (a) monoclinic and (b) tetragonal NaVPO4F, (c) charge-discharge curve and(d) in situ XRD pattern of NaVPO4F 96.
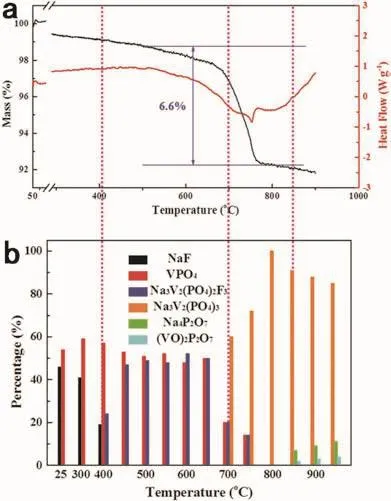
图17 (a)原料在氩气下加热过程中的TGA/DSC曲线和(b)基于原位XRD谱半定量计算的成分变化情况106Fig. 17 (a) The TGA/DSC curves of raw materials upon heating in Ar fl ow; (b) The corresponding specific compositional changes calculated by semiquantitative calculation of in situ XRD patterns 106.
研究者们采用碳包覆、形貌调控和离子掺杂等手段进一步提升NaVPO4F的储钠性能。Ruan等97制备了石墨烯包覆NaVPO4F复合材料,其平均工作电压高达3.95 V (vsNa+/Na)且首次放电比容量为120.9 mAh·g-1。之后研究者们采用多种碳包覆手段来提高NaVPO4F复合材料的电子导电性98–100。Jiao等101采用静电纺丝技术制备了一维结构NaVPO4F/C纳米纤维,NaVPO4F纳米颗粒(约为6 nm)均匀地分散在导电碳纤维骨架中,基于形貌和微观结构特征,复合材料表现出优异的电化学性能,在1C倍率下的放电比容量为126.3 mAh·g-1,在高达50C的倍率下仍可释放61.2 mAh·g-1的容量,在2C的倍率下经过1000次循环后容量仍能保持96.5%。此外,研究者们还通过构筑三维多孔交联网络、三维多孔珊瑚状结构等来改性NaVPO4F/C的储钠性能102,103。离子掺杂也可以调控NaVPO4F的电化学性能,Al和Cr被用于掺杂元素来改性NaVPO4F104,105。
尽管针对NaVPO4F的研究取得了一系列进展,但仍有研究者对NaVPO4F材料是否真实存在保持怀疑。最近,Li等106采用变温原位XRD技术研究了摩尔比为1 : 1的NaF和VPO4在固相反应过程中的成分和结构变化情况(图17),结果表明在不同温区存在三种化学反应:
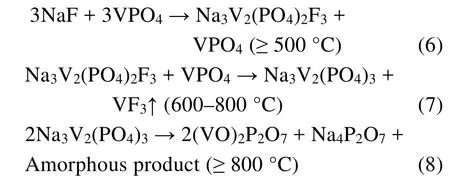
他们认为通过高温固相烧结法是不可能合成单斜晶系和四方晶系结构的NaVPO4F。关于NaVPO4F材料存在性问题的争论仍未终止,采用理论计算结合先进的分析表征技术进行深入研究不可或缺。
4.2.2 Na3(VO1-xPO4)2F1+2x (0 ≤ x ≤ 1)
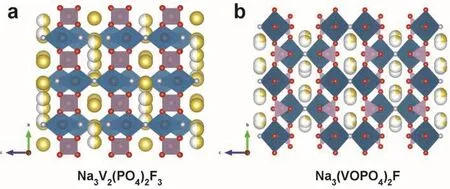
图18 (a) Na3V2(PO4)2F3和(b) Na3(VOPO4)2F的晶体结构Fig. 18 Crystal structures of (a) Na3V2(PO4)2F3 and (b) Na3(VOPO4)2F.
Na3V2(PO4)2F3是一种很有前景的钠离子电池正极材料,其结构中3个钠离子脱嵌时具有高达192 mAh·g-1的理论容量。由于(PO4)3-基团的强诱导效应和F-离子的高电负性,Na3V2(PO4)2F3具有较高的工作电压,其理论能量密度约为507 Wh·Kg-1,这个值与目前商业化LiFePO4的能量密度(530 Wh·Kg-1)非常接近。如图18a所示,Na3V2(PO4)3F3的晶体结构属于四方晶系的P42/mnm空间群,其中[V2O8F3]双八面体和[PO4]四面体相互桥接构成三维框架,在[110]和[001]方向有钠离子的快速迁移通道。Ji等107较早将Na3V2(PO4)3F3应用于钠离子电池中,发现其在3.3、3.5和4.0 V处有三个放电平台。Kang等108采用理论计算与实验相结合进一步研究了Na3V2(PO4)3F3的相反应机理。结果表明,钠离子是通过单相反应在宿主材料中可逆脱嵌且Na3V2(PO4)3F3脱钠相的晶体结构非常稳定。研究人员进一步通过第一性原理计算揭示了Na3V2(PO4)3F3材料中钠离子的迁移机制109,结果表明,Na3V2(PO4)3F3结构中的两个钠离子,即Na(1)和Na(2)通过两步电化学过程可逆脱嵌,同时伴随着V3+/V4+的氧化还原反应。图19a,c进一步说明了氧化还原的相变过程及其晶体结构中钠离子的分布情况110。普遍认为Na3V2(PO4)3F3结构中只有两个钠离子参与反应,而第三个钠离子不具电化学活性。最近,Tarascon团队111通过设计一种无序NaxV2(PO4)2F3材料成功激活了其结构中的第三个钠离子的电化学活性。如图19b所示,此材料在1–4.8 V的电压范围内可以可逆脱嵌3个钠离子,最后一个是在1.6 V (vsNa+/Na)电压处重新嵌入的。以此无序NaxV2(PO4)2F3材料作正极、硬碳作为负极的钠离子全电池能量密度有望提升15%–20%。
如图18b所示,基于体相结构设计研究者们还开发了一系列介于Na3V2(PO4)3F3(x= 0)和Na3(VO)2(PO4)2F (x= 1)之间的混合价态Na3(VO1-xPO4)2F1+2x(0 ≤x≤ 1)化合物,这里1-x代表材料中的氧含量,与Na3(VO1-xPO4)2F1+2x中的晶胞参数和晶胞体积密切相关。Na3(VO)2(PO4)2F的晶体结构属于四方晶系的I4/mnm空间群。研究者们采用理论计算和原位/非原位谱学技术研究了Na3(VO1-xPO4)2F1+2x材料中的钠离子脱嵌机制。Rojo等112,113研究了Na3V2O2x(PO4)2F3-2x和Na3V2O2(PO4)2F中的钠离子存储机制,发现了两相反应和固溶反应并存的反应机制,且随着成分的不同其电化学脱嵌机制也不尽相同。Kang等114采用理论计算结合实验验证的手段研究了Na3(VO1-xPO4)2F1+2x化合物中V3+/V4+和V4+/V5+氧化还原对的组合、钠离子占位、F/O比例对工作电压的影响(图20a)及其钠离子脱嵌机制。此外,他们发现通过体相结构调控,可以开发新型高能量密度的Nay(VO1-xPO4)2F1+2x正极材料,Kang等115设计了一种新型正极材料Na1.5VPO4.8F0.7,此材料的理论能量密度约为600 Wh·Kg-1,对应于V3.8+/V5+氧化还原对其每个晶胞单元中有1.2个离子能够可逆脱嵌。电化学测试结果显示此Na1.5VPO4.8F0.7正极材料具有优异的循环稳定性,经过100次循环容量保持率为95%,500次循环后可以保持84%的放电比容量。虽然Na3(VO1-xPO4)2F1+2x(0 ≤x≤ 1)化合物理论上具有很高的能量密度,但是由于电解液稳定电压窗口的限制,其结构中的第三个钠离子很难脱出,Goodenough等116通过理论计算预测采用Cl替换Na3V2O2(PO4)2F结构中的O形成的Na3V2Cl2(PO4)2F化合物有望实现第三个钠离子的可逆脱嵌(图20b),其理论能量密度高达758 Wh·Kg-1,但这一结论目前还没有被实验验证。

图19 (a) Na3V2(PO4)2F3中Na+脱出过程中的电压-成分曲线110;(b)无序相NaxV2(PO4)2F3中激发第三个Na+的电化学活性111;(c)基于Rietveld精修获得不同Na3V2(PO4)2F3脱钠相的钠分布情况110Fig. 19 (a) Potential-composition electrochemical curves obtained upon Na+ extraction from Na3V2(PO4)2F3 110. (b) Trigger the activity of the third sodium electrochemically via the formation of a disordered NaxV2(PO4)2F3 phase 111. (c) Sodium distribution obtained from Rietveld refinement of the different phases upon sodium extraction from Na3V2(PO4)2F3 110.
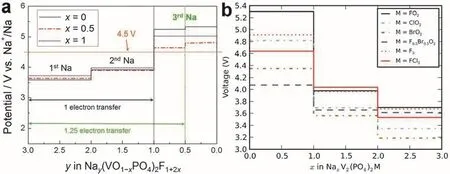
图 20 (a)第一性原理计算的 Nay(VO1-xPO4)2F1+2x (0 ≤ x ≤ 1; 0 ≤ y ≤ 3)的成分–电压曲线 114;(b) NaxV2(PO4)2M中不同阴离子(M)掺杂对其电压的影响116Fig. 20 (a) Voltage–composition curves for the Nay(VO1-xPO4)2F1+2x (0 ≤ x ≤ 1; 0 ≤ y ≤ 3) electrodes from first-principles calculations 114. (b) Comparison of the voltage profiles of NaxV2(PO4)2M with different anion (M) substitutions 116.

图21 Na3V2(PO4)2F3立方体/石墨烯复合材料的制备过程及其在20C倍率下的长循环性能117Fig. 21 Preparation procedure of Na3V2(PO4)2F3 microcubes/graphene composite and its long cycling performance at 20C rate 117.
Na3(VO1-xPO4)2F1+2x(0 ≤x≤ 1) 类材料的本征电子导电性较差,严重影响了其电化学性能的发挥,研究者们采用导电层包覆/复合、掺杂和微纳结构调控等手段进行改性研究。Liang等117制备一种Na3V2(PO4)2F3@rGO复合材料(图21),表现出高达3.8 V (vsNa+/Na)的工作电压平台和优异的循环稳定性,组装成全电池具有291 Wh·Kg-1的能量密度。研究发现三维石墨烯网络可以提供连续的电子和离子传输通道,并缓解钠离子嵌入和脱出过程中产生的应力以及体积变化,有助于提高材料的倍率性能和循环稳定性。此外,研究者们还采用有序介孔碳(CMK-3)118、三维石墨烯119、碳纳米管120、石墨烯量子点121等导电材料包覆/复合手段来提升Na3(VO1-xPO4)2F1+2x化合物的电子导电性。Zhang等122研究了不同化合价的钛离子(Ti2+、Ti3+、Ti4+)掺杂对Na3V2(PO4)2F3电化学性能的影响,发现合适的钛离子掺杂可以有效提升Na3V2-xTix(PO4)2F3材料的电子导电性和离子传输速率,优化后的材料在0.2C的倍率下可以释放出125 mAh·g-1的可逆容量,即使在40C的高倍率下仍可释放104 mAh·g-1的容量。此外,研究者们还研究了Ru123、Mn124等元素掺杂对Na3(VO1-xPO4)2F1+2x类材料物理化学特性的影响。Xia等125通过微乳液调控的水热反应法制备了一种RuO2包覆的Na3V2O2(PO4)2F纳米线,其直径约为50 nm,结合了导电层包覆和纳米结构优势,制备的复合材料在1C的倍率下可释放出120 mAh·g-1的比容量,在20C的倍率下经过1000次循环后其放电比容量仍可保持95 mAh·g-1。此外,研究者们还采用多种物理或化学手段制备了Na3V2O2(PO4)2F/rGO微球126、Na3(VO)2(PO4)2F/C纳米立方体121、Na3(VOPO4)2F多层微球127等结构来提升Na3(VO1-xPO4)2F1+2x正极材料的电化学性能。
4.2.3 Na2MPO4F (M = Fe、Mn、Co、Ni)
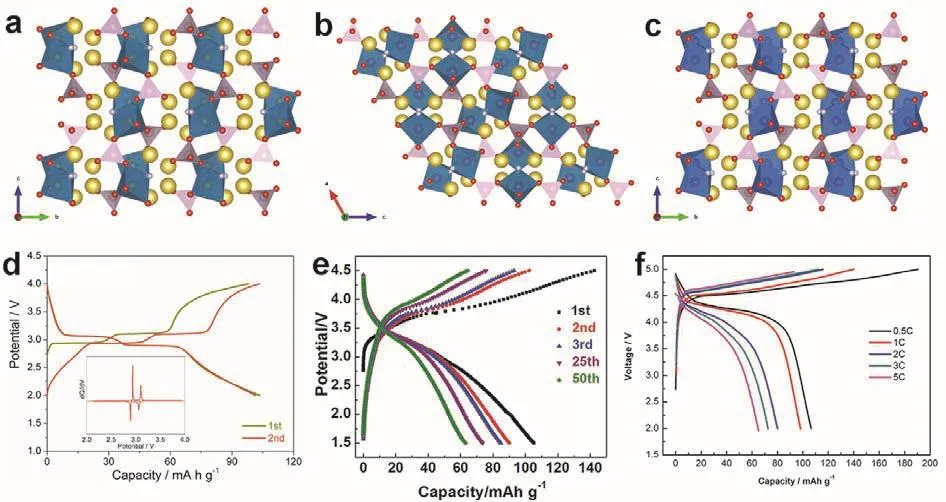
图22 (a,d) Na2FePO4F、(b,e) Na2MnPO4F和(c,f) Na2CoPO4F的晶体结构和相应的充放电曲线131,137,138Fig. 22 Crystal structures and corresponding charge-discharge curves of (a, d) Na2FePO4F,(b, e) Na2MnPO4F, and (c, f) Na2CoPO4F 131,137,138.
研究人员一直都在寻找基于Fe2+/Fe3+氧化还原对的新型、环保的铁基碱金属氟磷酸盐。Nazar团队128首次报道了一种Na2FePO4F新材料。随后,她们又报道了一种类似的新型Na2CoPO4F材料129。如图22a,c所示,这两种材料的晶体结构都属于正交晶系Pbcn空间群,其结构中共面的MO4F2八面体通过F原子桥接形成M2O7F2单元,这些双八面体M2O7F2单元和PO4四面体共角形成二维的框架结构,两个钠离子位于MPO4F层间。为了弄清原子尺度特征如何影响层状Na2FePO4F的电化学性能,她们团队采用原子模拟计算方法探索了钠离子的传导行为和固有缺陷特性130,结果表明,钠离子更倾向于沿着层间能量较低的a面和c面方向迁移。Shao等131采用原位XRD技术研究了Na2FePO4F的储钠机制(图23a),如图22d所示131,在2.0–4.0 V (vsNa+/Na)电压区间内,Na2FePO4F/C正极材料的充放电曲线显示出两对可逆的电压平台,对应于两步可逆相变反应:Na2FeIIPO4F ↔ Na1.5FePO4F ↔NaFeIIIPO4F,且Na2FeIIPO4F与其氧化物NaFeIIIPO4F之间的体积变化仅为3.7%,因此在钠离子脱嵌过程中结构应变较小132。通过碳包覆和粘结剂优化,Na2FePO4F/C复合材料表现出优异的电化学性能,在4C的倍率下经过1000次循环后其容量保持率为84.7% (图23b)。为了改善Na2FePO4F材料的储钠性能,研究者们尝试了多种材料改性手段,包括碳包覆133,134和材料微纳结构调控等135,136。
研究者们也将其它过渡金属氟磷酸盐化合物应用于钠离子电池中,如Na2CoPO4F和Na2MnPO4F137,138,它们都可以通过高温固相法、溶胶凝胶法和水热法制备。Na2CoPO4F是高压钠离子电池良好的候选材料,在4.3 V (vsNa+/Na)附近有一个高电压平台(图22f),基于单电子转移其理论容量为122 mAh·g-1,对应理论能量密度为524 Wh·kg-1137。Na2MnPO4F也是一种潜在的钠离子电池高压正极材料,其晶体结构属于单斜晶系P21/n空间群(图22b)。Yang等138采用喷雾干燥法制备了一种Na2MnPO4F/C微球,其首圈放电比容量接近110 mAh·g-1(图22e)。
此外,一些新型过渡金属氟磷酸钠盐在钠离子电池中也有很大的研究价值和应用潜力,包括:Na4NiP2O7F2139、Na2Mg(PO4)F140、Na3Ti2P2O10F141、Na7Fe7(PO4)6F3142等。目前关于一些新型高压氟磷酸盐正极材料的电化学反应机制解析及结构、性能优化的研究还比较少,在储能机制解析和材料性能优化方面仍需努力。
4.3 焦磷酸盐类
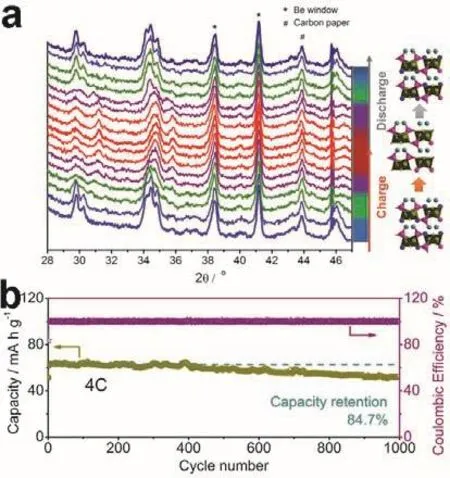
图23 Na2FePO4F的(a)原位XRD谱和(b)循环性能131Fig. 23 (a) In situ XRD patterns and (b) cycling performance of the Na2FePO4F 131.
4.3.1 NaMP2O7 (M = Fe、Ti、V)
另一类很有潜力的钠离子电池正极材料是焦磷酸盐材料,如NaMP2O7(M = Ti、V、Fe),Na2MP2O7(M = Fe、Mn、Cu、Co),Na4-αM2+α/2(P2O7)2(2/3 ≤α≤ 7/8, M = Fe、Mn)等。它们具有不同的晶体结构,包括:三斜晶系(P1空间群)、单斜晶系(P21/C空间群)和四方晶系(P42/mnm空间群)。NaFeP2O7具有两种不同的晶体结构,如图24a,b所示,NaFeP2O7-I和NaFeP2O7-II都属于单斜晶系P21/C空间群。NaFeP2O7-I是由共享角的FeO6八面体和PO4四面体构成,其结构中在[001]方向具有钠离子迁移的通道。这种NaFeP2O7-I在高温条件下(≥ 750 °C)很容易转变为热力学稳定的NaFeP2O7-II相。NaFeP2O7-II的晶体结构是由共享角的FeO6八面体和PO4四面体组成的笼状结构,其中P-O-P的夹角为132.86°143。这种结构中的钠离子位于细长的笼子中,在[101]方向有钠离子的迁移路径144。但是,目前还没有针对NaFeP2O7储钠性能的研究报道。
此外,NaVP2O7和NaTiP2O7也被关注和报道145,146,它们的晶体结构和NaFeP2O7-II类似(图24c)147。Okada等148采用高温固相法制备了NaVP2O7并研究了其作为钠离子电池正极材料的性能表现,其平均工作电压为3.4 V (vsNa+/Na),理论容量为108 mAh·g-1,但在0.05C倍率下的首次放电比容量仅为38.4 mAh·g-1。最近,Kalaiselvi等149研究了AVP2O7/C (A = Li、Li0.5Na0.5、Na)化合物作为钠离子电池负极材料的性能表现。
4.3.2 Na2MP2O7 (M = Fe、Co、Mn、Cu)
Na2MP2O7(M = Fe、Co、Mn、Cu) 是另一类焦磷酸钠盐化合物,它们的晶体结构通常以三斜、四方和正交结构存在。如图25a所示,Na2FeP2O7是由共角的FeO6八面体二聚体[Fe2O11]通过共角或共边的方式与PO4四面体连接而成,钠原子存在于其框架结构中。Yamada组150最早将Na2FeP2O7应用于钠离子电池中,他们测试了Na2FeP2O7材料的电化学性能,获得了82 mAh·g-1的可逆容量,发现Fe2+/Fe3+的氧化还原电位位于2.5和3 V左右(图25c)。他们还发现由于焦磷酸根稳定的结构,Na2FeP2O7材料和脱钠相NaFeP2O7具有良好的热稳定性,在600 °C时都不发生热分解或析氧反应151。Choi等152采用理论模拟与实验验证相结合的方法深入研究了Na2FeP2O7材料的结构特征、电化学性能和热力学行为。他们采用同步辐射X射线衍射谱结合DFT计算对Na2FeP2O7的晶体结构进行了深入研究。结果表明,其晶胞中含有8个钠原子位点,DFT计算结果显示,Na1位点的能量高于Na2–Na8位点,Na1沿[011]方向迁移的能量势垒最低(0.48 eV)。因此,在动力学和热力学方面,Na1都是最容易脱嵌的钠原子位点。准平衡电势结果和第一性原理计算结果一致表明,Na2FeP2O7的电化学过程包括两种反应机制:一种是2.5 V左右的单相反应,另一种是2.5–3.0 V电压范围内的连续的两相反应。
之后的一系列研究都旨在优化Na2FeP2O7材料的电化学性能。例如,通过碳纳米管修饰的Na2FeP2O7材料表现出优异的倍率性能153。由于Mn2+/Mn3+电化学活性氧化还原对具有较高的工作电势,通过锰掺杂可以将Na2FeP2O7材料的平均工作电压提升至3.2 V (vsNa+/Na)154。非原位XRD和CV测试结果表明,由于钠配位环境和钠占位率的不同,Na2Fe0.5Mn0.5P2O7中发生的是单相反应。此外,研究者们也通过导电材料包覆/复合155、原子掺杂156、电解液优化157等手段进一步提升Na2FeP2O7的电化学性能。
Na2MnP2O7具有两种不同的三斜晶系结构:Na2MnP2O7-I和Na2MnP2O7-II,它们具有类似的结构框架,但不同的晶胞大小和Mn-O-Mn、P-O-P键角(图25a,b)。Choi和Yamada等158,159将Na2MnP2O7应用于钠离子电池中,在3.8 V (vsNa+/Na)左右具有良好的电化学活性并释放出90 mAh·g-1的可逆容量(图25d)。他们采用第一性原理计算发现电化学性能提升的主要是由于原子的重排程度低,降低了电子传导和离子相界迁移的障碍。通过石墨烯修饰可以有效提升Na2MnP2O7的电化学性能160。
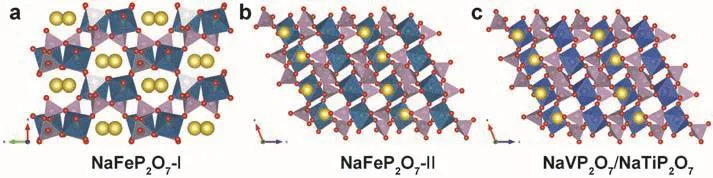
图24 (a) NaFeP2O7-I、(b) NaFeP2O7-II和(c) NaVP2O7/NaTiP2O7的晶体结构Fig. 24 Crystal structures of (a) NaFeP2O7-I, (b) NaFeP2O7-II, and (c) NaVP2O7/NaTiP2O7.
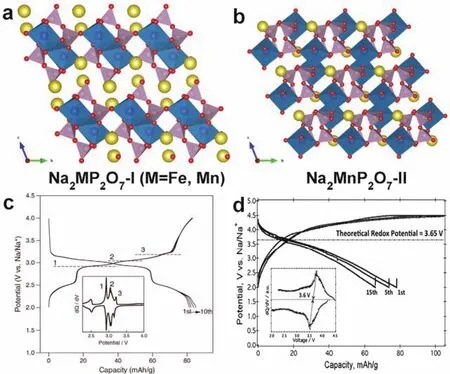
图25 (a) Na2MP2O7-I (M = Fe, Mn)和(b) Na2MnP2O7-II的晶体结构;(c) Na2FeP2O7 150和(d) Na2MnP2O7 159的充放电曲线Fig. 25 Crystal structures of (a) Na2MP2O7-I (M = Fe, Mn) and (b) Na2MnP2O7-II.Charge-discharge curves of (c) Na2FeP2O7 150 and (d) Na2MnP2O7 159.
研究人员也对高压正极材料Na2CoP2O7进行了研究。Na2CoP2O7具有三种不同的晶体结构,分别为正交晶系Pna21空间群、三斜晶系P1空间群和四方晶系P42/mnm空间群144。Yamada等161报道了一种正交结构(空间群Pna21)的Na2CoP2O7,此材料结构中具有二维的离子扩散通道,平均工作电压为3 V。Jung课题组162成功制备了富含钠缺陷的三斜晶系Na2CoP2O7,显著提升其能量密度。通过引入缺陷来驱动电极材料电化学反应活性也为其它新材料的设计开发提供了新思路。
4.3.3 Na4-αM2+α/2(P2O7)2 (2/3 ≤ α ≤ 7/8,M = Fe、Mn)
非化学计量比的焦磷酸盐Na4-αM2+α/2(P2O7)2(2/3 ≤α≤ 7/8,M = Fe、Fe0.5Mn0.5、Mn)也表现出良好的储钠性能163。图26a为Na3.12Fe2.44(P2O7)2的晶体结构示意图,属于三斜晶系P1—空间群,其三维框架是由共角的Fe2P2O22和Fe2P4O20基本单元呈中心对称连接而成,每个基本单元包含两个FeO6八面体和两个P2O7基团。Nazar等163发现Na3.12Fe2.44(P2O7)2正极材料的可逆容量约为90 mAh·g-1,平均工作电位为3.0 V (vsNa+/Na)左右(图26b)。Chou等164采用原位同步辐射XRD技术和密度泛函理论计算揭示了Na3.32Fe2.34(P2O7)2中的离子存储机理,结果表明在钠离子脱嵌过程中,Na3.32Fe2.34(P2O7)2发生的是单相转变且其结构中具有一维的离子迁移路径。
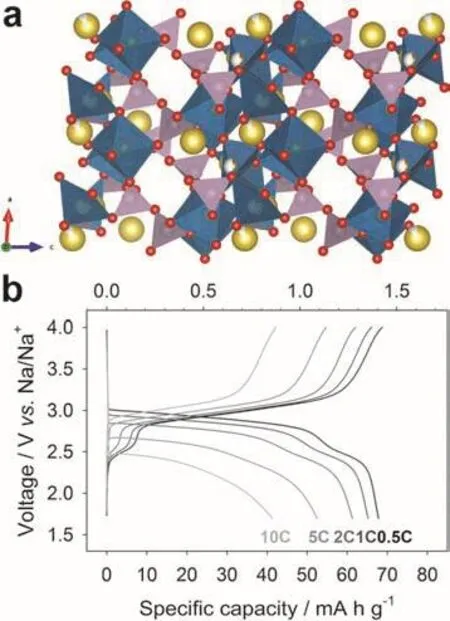
图26 Na3.12Fe2.44(P2O7)2的(a)晶体结构和(b)充放电曲线163Fig. 26 (a) Crystal structure and (b) charge-discharge curves of Na3.12Fe2.44(P2O7)2 163.
研究人员采用多种材料改性策略对Na3.12Fe2.44(P2O7)2化合物的储钠性能进行研究。Li等165–167通过导电碳材料的包覆或复合有效提升了Na3.12Fe2.44(P2O7)2的电子导电性。Deng等168,169通过多种生物化学手段构筑了三维多孔结构的Na3.12Fe2.44(P2O7)2,有效缩短了钠离子的迁移路径且暴露了更多的电化学活性位点。
4.3.4 Na7V3(P2O7)4
具有不同结构的钒基焦磷酸盐也得到了一些研究。如图27a为Na7V3(P2O7)4的晶体结构,属于单斜晶系C2/c空间群,其结构中VO6八面体和P2O7基团共角形成三维的钠离子迁移路径。Kang等170最先将Na7V3(P2O7)4作为正极材料应用于钠离子电池中(图27b),其氧化还原电位约为4.13 V (vsNa+/Na),在钠离子脱嵌过程中,其晶胞变化仅为1%,在1C的倍率下充放电时,经过600次循环后其容量仍可保持75%。Deng等171–173通过生物化学手段构筑了多种不同三维微纳结构的Na7V3(P2O7)4/C复合材料,其电化学性能得到了显著提升。此外,在寻找钠离子电池新型正极材料的进程中,其它过渡金属焦磷酸钠盐也得到了初步研究,如Na1.82Mg1.09P2O7174、Na7Fe4.5(P2O7)4175、t-Na2(VO)P2O7176和δ-(MoO2)2P2O7等。
4.4 混合磷酸盐类
4.4.1 Na4M3(PO4)2P2O7 (M = Mn、Fe、Co、Ni)
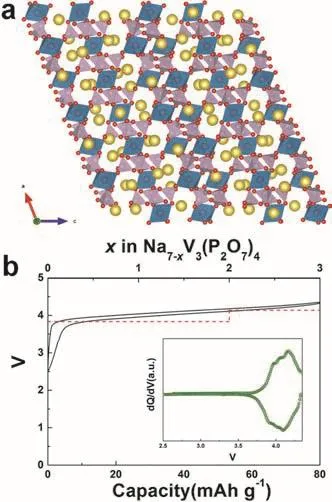
图27 Na7V3(P2O7)4的(a)晶体结构和(b)充放电曲线170Fig. 27 (a) Crystal structure and (b) charge-discharge curves of Na7V3(P2O7)4 170.
将不同的聚阴离子结合在一起,可得到一系列结构新颖、电化学活性高的高压正极材料。早期关于混合多价阴离子类化合物Na4M3(PO4)2(P2O7)(M = Fe、Mn、Co、Ni)的研究主要集中在材料结构解析。近年来,研究人员将它们应用于钠离子电池中。如图28a所示,这些材料中PO4四面体和MO6八面体共角组成双链,层间通过焦磷酸根的P—O—P键桥接,相邻的两层之间形成沿着[010]和[001]方向延伸的离子扩散通道177。Kang等178使用第一性原理计算和实验相结合的方法最先研究了Na4Fe3(PO4)2(P2O7)材料的储Li/Na性能,其作为钠离子电池正极材料释放出129 mAh·g-1的可逆容量且平均工作电压为3.2 V (vsNa+/Na)。Yang等179通过电化学原位XRD和核磁共振(NMR)技术研究了Na4Fe3(PO4)2(P2O7)中的相转变机制(图28b),Na4Fe3(PO4)2(P2O7)材料中钠离子的脱出和嵌入过程是一种不完全的固溶反应,存在明显的局部晶格畸变,固态NMR结果也印证了这一结论。电化学测试结果显示(图28c),制备的Na4Fe3(PO4)2(P2O7)/C复合纳米材料在0.05C的倍率下首次放电比容量为110 mAh·g-1且平均工作电压为3.1 V (vsNa+/Na)。
研究者们采用多种改性策略来优化Na4Fe3(PO4)2(P2O7)的结构,进而提升其储钠性能。最近,Chou等180采用溶胶-凝胶法制备了不同微纳尺度的Na4Fe3(PO4)2(P2O7)/C复合材料,在0.05C和20C的倍率下分别释放出113和80.3 mAh·g-1的放电比容量,在20C的倍率下经过4400次循环后其放电比容量仍能保持69.1%且表现出优异的高低温特性。Cao等181,182采用三维石墨烯修饰、纳米形貌控制的方法得到了性能优异的Na4Fe3(PO4)2(P2O7)正极材料。
Nose等183将Na4Co3(PO4)2P2O7作为正极材料应用于钠离子电池中,其在4.1–4.7 V (vsNa+/Na)的电压范围内显示出多步氧化还原反应(图28d),可逆放电比容量为97 mAh·g-1。他们还报道了另一种多元混合磷酸盐化合物Na4Co2.4Mn0.3Ni0.3(PO4)2P2O7,其在4.2和4.6 V左右出现两对氧化还原电位184。Kang课题组185也将混合磷酸盐材料的研究扩展到了Na4Mn3(PO4)2(P2O7),作为钠离子电池正极材料,Na4Mn3(PO4)2(P2O7)中Mn2+/Mn3+氧化还原电位高达3.84 V (vsNa+/Na)且释放出109 mAh·g-1的比放电容量(图28e)。他们基于第一性原理计算和实验相结合,证明了钠离子在三维扩散通道中具有较低的活化能,因此该材料具有优异的倍率性能(20C),且Jahn-Teller效应引起的晶格畸变有助于打开钠离子的扩散通道从而有效提升了离子迁移速率。此外,Passerini等186最先研究了Na4Ni3(PO4)2(P2O7)的储钠特性(图28f),发现基于Ni2+/Ni3+氧化还原对的平均输出电压高达4.8 V (vsNa+/Na)。

图28 (a) Na4M3(PO4)2(P2O7) (M = Fe、Mn、Co、Ni)的晶体结构;Na4Fe3(PO4)2(P2O7)的(b)原位XRD谱和(c)充放电曲线179;(d) Na4Co3(PO4)2(P2O7) 183、(e) Na4Mn3(PO4)2(P2O7) 185和(f) Na4Ni3(PO4)2(P2O7) 186的充放电曲线Fig. 28 (a) Crystal structures of Na4M3(PO4)2(P2O7) (M = Fe, Mn, Co, Ni). (b) in situ XRD patterns and(c) charge-discharge curves of Na4Fe3(PO4)2(P2O7) 179. Charge-discharge curves of (d) Na4Co3(PO4)2(P2O7) 183,(e) Na4Mn3(PO4)2(P2O7) 185, and (f) Na4Ni3(PO4)2(P2O7) 186.
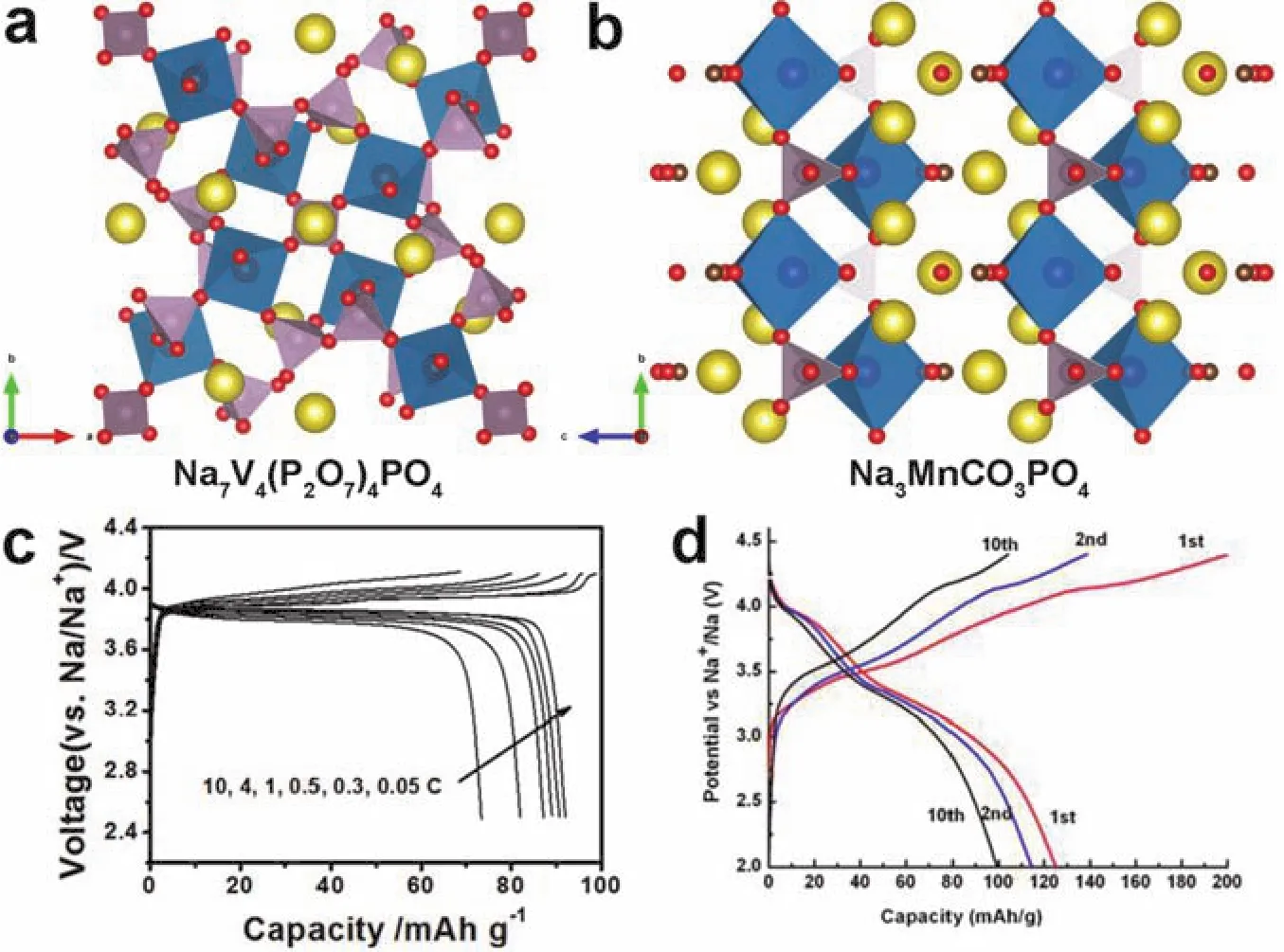
图29 (a,c) Na7V4(P2O7)4PO4 187和(b,d) Na3MnCO3PO4 191的晶体结构和对应的充放电曲线Fig. 29 Crystal structures and corresponding charge-discharge curves of (a, c) Na7V4(P2O7)4PO4 187 and(b, d) Na3MnCO3PO4 191.
4.4.2 Na7V4(P2O7)4PO4
Na7V4(P2O7)4PO4也是一种广受关注的混合磷酸盐化合物,如图29a所示,其晶体结构属于四方晶系P21c。Choi等187研究了Na7V4(P2O7)4PO4的储钠性能,表现出高达3.8 V (vsNa+/Na)的工作电压(图29c),在0.5C倍率下经过1000次循环后其容量保持率为78%。Zhang等188通过恒电流间歇滴定(GITT)技术发现Na7V4(P2O7)4PO4在充放电过程中存在中间相Na5V3.5+4(P2O7)4PO4。此外,研究者们采用导电碳修饰189、构筑分级结构189、形貌调控190等手段进一步改善Na7V4(P2O7)4PO4的电化学性能。
4.4.3 Na3MPO4CO3 (M = Fe、Mn、Co、Ni、V)
5 总结与展望
锂离子电池因为其高能量密度、长寿命等特点在电动汽车和储能领域中得到了广泛的应用。聚阴离子磷酸盐电极材料相比于其它正极材料具有更好的安全性能和循环稳定性,在电动汽车等应用领域具有独特的优势。钠离子电池因其具有原材料资源丰富、价格低廉等突出优点,近年来被视为是继锂离子电池之后可作大规模储能系统应用的理想体系。因此,探寻资源丰富、经济环保具有优良电化学性能的储钠电极材料已成为当前的一个研究热点。聚阴离子型化合物因具有更稳定的结构和更大的离子扩散通道等特性备受各国科学家的青睐。虽然磷酸盐正极材料在理论上具有很好的应用前景,但电子导电性差和容量偏低等缺陷极大的限制了其走向广泛应用。
本文概述了钠离子电池的组成、工作原理、正负极材料和面临的问题,指出了提升钠离子电池能量密度的关键在于正极材料的优化设计并总结了影响钠离子电池正极材料工作电压的内部和外部因素,详细综述了钠离子电池磷酸盐正极材料的最新进展,包括正磷酸盐类、氟磷酸盐类、焦磷酸盐类和混合磷酸盐类化合物,通过对磷酸盐材料的晶体结构、储钠机理和改性策略等方面的综述,揭示材料成分、结构与电化学性能之间的本征关系,为聚阴离子磷酸盐正极材料的持续改性和新型磷酸盐高压正极材料的探索开发提供指导。
今后,在聚阴离子磷酸盐体系正极材料方面还需要努力的方面包括:(1)开发新型高比能磷酸盐正极材料。对新型高电压、高容量聚阴离子正极材料进行设计和材料性能预测,通过理论计算分析离子类型、浓度、离子占位对聚阴离子型正极材料本征结构、储钠容量、储钠电位、离子输运、电子结构等的影响,量化其特殊的体相结构与电化学本征特性关系。(2)磷酸盐正极材料电化学机理研究。借助系列电池原位表征技术,分析电极材料工作过程中的相转变、界面作用机制,探究微纳米电极材料结构、成分和形貌与其电化学性能的内在关联,为电极材料优化、电池系统优化提供更精准科学指导。(3)开发与磷酸盐正极材料适配的耐高压电解液。研究电解液成分、浓度、添加剂种类等对电解液活性、电化学稳定窗口的影响。探索制备耐高压窗口稳定、储能效率高的电解液新途径。揭示电极/电解液异质界面作用机制,弄清界面快速荷质传输规律。(4)开发钠离子全电池。综合研究磷酸盐正极与电解质、负极之间的相互作用,全电池系统在高低温环境中的电化学表现,研究其相容性和匹配性。通过正交实验寻找出最优的电池组合,优化电池组装工艺,制备全电池单体,评估材料在全电池体系中的综合表现。

