不同发酵时间对乌虾酱风味的影响
栾宏伟,朱文慧,*,祝伦伟,步 营,*,李学鹏,励建荣,季广仁
(1.渤海大学食品科学与工程学院,生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心,辽宁锦州 121013;2.锦州笔架山食品有限公司,辽宁锦州 121007)
虾酱(shrimp paste),又名虾膏,是我国沿海地区以及东南亚各国的传统发酵调味品[1]。虾酱是以毛虾、乌虾等小型虾类为原料经腌制、搅拌、发酵而制成的粘稠酱状食品,其味道鲜美,风味独特[2-3],富含蛋白质、多肽、氨基酸、卵磷脂、脑磷脂及矿物质等营养物质[4]。虾酱含盐量一般在20%~30%[5],是韩国、日本、泰国、马来西亚、缅甸、新加坡、老挝、印尼、菲律宾和越南等东南亚国家常用的调味品;我国主要分布在海南、广东、广西、辽宁、天津、山东、江苏、浙江、福建等沿海地区[1,5-6]。
风味是决定虾酱等水产调味品品质的重要因子,明确虾酱中风味物质的组成是其风味调控与保持的基础。虾酱的发酵是一个复杂过程,在虾酱发酵过程中蛋白水解是风味和营养形成的主要决定因素[7]。原料在微生物和酶的共同作用下,通过分解蛋白质和脂肪等基质,产生多肽、氨基酸等营养物质以及醛、酮、醇、吡嗪、含硫类等多种小分子风味化合物,对最终虾酱产品的风味和品质起到决定性的作用[5-6]。据报道,多肽和游离氨基酸是虾酱典型风味形成的主要物质基础[8],虾酱发酵的时间不同,其风味也不同,因此,有必要研究不同发酵过程中虾酱风味物质的变化规律。
本实验选取不同发酵时期的虾酱,通过可反映虾酱品质的氨基酸态氮(Amino acid nitrogen,AAN)、可溶性肽、电子鼻、电子舌味觉值作为评价指标,并结合挥发性风味物质检测,研究不同发酵时间下虾酱的风味品质变化,为制备高品质虾酱提供理论参考。

表1 化学传感器及其对应的敏感物质类型Table 1 Chemical sensors corresponding to different types of volatile substances
1 材料与方法
1.1 材料与仪器
乌虾酱 锦州笔架山食品厂提供;新鲜及体长约0.5 cm的乌虾,打捞于渤海湾;食盐 中国盐业总公司;酪氨酸标准品(HPLC≥98%) 北京索莱宝科技有限公司;硫酸铜、硫酸钾、硫酸、氯化钾、酒石酸、碳酸钠、氢氧化钠、三氯乙酸 分析纯,天津市天力化学试剂有限公司。
RCD-1A高速均质乳化机 常州越新仪器制造有限公司;PEN 3便携式电子鼻(传感器阵列由10个金属氧化物传感器组成) 德国Airsense公司;SA402B电子舌 日本Insent公司;Kjeltec 8400全自动凯氏定氮仪 丹麦Foss公司;UV2550紫外可见分光光度计 日本SHIMADZU公司。
1.2 实验方法
1.2.1 原料制备与选取 将乌虾进行清理除杂并分级挑选,然后与食盐按照1∶0.3 (w/w)混合后置于发酵缸中,即总食盐添加量为虾重量的30%,装缸后用食盐(包含在总食盐添加量中)洒在顶部封存,三层纱布覆盖,从发酵第三个月开始每天早晚各搅拌两次,自然发酵1~3年。分别于2016年4月,2017年4月和2018年4月从同一缸中取样装瓶,4 ℃保存备用。
1.2.2 氨基酸态氮含量测定 根据王文秀等[9]的方法,采用甲醛滴定法对氨基酸态氮(Amino acid nitrogen,AAN)含量进行测定。取样品5.0 g定容至100 mL,再取20 mL与60 mL蒸馏水混合并用0.05 mol/L NaOH滴定至pH8.2,然后向混合物中加入10 mL、40%的甲醛溶液。最后,使用0.05 mol/L NaOH将混合物滴定至pH9.2,记录消耗的NaOH体积以确定ANN含量。计算公式如下:
式中:V1为空白所消耗NaOH的量(mL);V2为样品所消耗NaOH的量(mL);V3为参与反应样品体积(mL);C为NaOH浓度(mol/L)。
1.2.3 多肽含量测定 样品前处理:取3.0 g样品,加入27 mL 5% TCA溶液,均质后于4 ℃放置1 h,5000 g/min离心10 min,取上清液用5% TCA定容至50 mL。
样品溶液的测定:取1 mL处理好的样液,加入5 mL碱性铜试液(取氢氧化钠10 g,碳酸钠50 g,加水400 mL使溶解,作为甲液;取酒石酸钾0.5 g,加水50 mL使其溶解,另取硫酸铜0.25 g,加水30 mL使其溶解,将两液混合作为乙液。临用前,合并甲、乙两液,并加水至500 mL),于20~25 ℃放置10 min,再加0.5 mL福林酚试剂(1 mol/L),立即摇匀,在20~25 ℃保温30 min,于500 nm测定吸光值。每个样品4组平行。
标准曲线制作:取1 mL样品溶液加入酪氨酸标准品(200 μg/mL),配制浓度梯度为0、20、40、60、80、100、120 μg/mL的溶液作为对照品溶液。按照上述步骤,每个梯度4组平行。所得标准曲线为:y=0.004x-0.0067,R2=0.9998。
1.2.4 电子鼻分析 根据样品顶空挥发物通过传感器的电阻值G与基准气体通过传感器的电阻值G0的比值而进行数据处理和模式识别[10]。传感器由10种金属氧化物半导体型(Metal oxide semiconductor,MOS)化学传感元件组成,每型传感元件对应的主要敏感物质见表3[10-11]。
取5 g样品于50 mL烧杯中,用保鲜膜密封,25 ℃平衡10 min,运用电子鼻传感器对样品进行检测。检测时间120 s,清洗时间120 s,数据采集时间为90~95 s,每个样品做三次平行重复。
1.2.5 电子舌分析 将5.0 g虾酱样品溶于100 mL蒸馏水中均质,10000 r/min离心10 min,取上清液备用。将电子舌配套传感器和参比电极内部加入内部液(3.3 mmol/L KCl+饱和氯化银),并分别将传感器置于参比溶液(30 mmol/L KCl+0.3 mmol/L酒石酸)、参比电极置于3.3 mmol/L KCl溶液中活化24 h。自检后,在室温下通过电子舌对每种样品的苦味、苦味余味、涩味、涩味余味、咸味、鲜味和丰富度进行分析。每个样品重复4次,保留3组稳定的数据,取平均值。
1.2.6 HS-SPME/GC-MS测定
1.2.6.1 检测样品制备 取样品约5.0 g,置于萃取瓶中,磁力搅拌器45 ℃加热搅拌平衡10 min,然后插入装有2 cm-50/30 μm DVB/CAR/PDMS StableFlex纤维头的手动进样器,顶空萃取30 min后取出,快速移出萃取头并立即插入GC仪进样口(温度250 ℃)中,热解吸3 min进样。
1.2.6.2 检测条件 色谱柱:HP-5MS毛细管柱(30 m×0.25 mm×0.25 μm);升温程序:柱温40 ℃,保留2 min,以5 ℃/min升温至120 ℃,保持1 min;再以12 ℃/min升温至250 ℃,并保持10 min;载气为He;载气流量1.0 mL/min;不分流进样;溶剂延迟时间1.5 min。电子电离源;离子源温度230 ℃;四极杆温度150 ℃;电子能量70 eV;接口温度280 ℃;质量扫描范围30~550 a.m.u.。定性定量分析:对总离子流图中的各峰经质谱计算机数据系统检索及核对NIST 11和Wiley 7.0标准质谱图。
1.3 数据处理
采用SPSS 19.0进行数据的统计分析,P<0.05表示差异显著;通过Origin 8.5分析数据制图;电子鼻数据运用电子鼻配套的WinMuster软件对测定数据进行主成分分析(Principal component analysis,PCA);电子舌数据采用SA402B配套分析软件进行处理。
2 结果与分析
2.1 氨基酸态氮和多肽含量分析
氨基酸态氮是判定发酵产品发酵程度的特性指标,能够反映产品的老化程度及风味特点,该指标越高,说明虾酱中氨基酸含量越高,鲜味越好[12]。由图1可知,虾酱的氨基酸态氮含量随发酵时间的延长而逐渐增高,从1年的1.281 g/100 g增加到3年的1.614 g/100 g。发酵1年和2年虾酱氨基酸态氮含量差异不显著,而发酵1、2年与3年虾酱氨基酸态氮含量差异显著(P<0.05)。由图2可知,随着发酵时间的延长,多肽即可溶性肽含量也呈增加的趋势,由发酵1年的0.655 g/100 g增加到3年的0.814 g/100 g。发酵1年和2年虾酱多肽含量差异不显著,而发酵1、2年与3年虾酱多肽含量差异显著(P<0.05)。由此可知,发酵3年的虾酱品质最好。在发酵过程中,虾体中内源性蛋白酶和微生物产生的蛋白酶共同作用使蛋白质降解[13],不溶性蛋白转化为可溶性蛋白,同时有较多的可溶性蛋白转化为肽、氨基酸、氨基态氮等小分子物质,形成了风味前体物质[14],可溶性肽对于虾酱的风味和营养都有重要影响。肽是由蛋白质大分子降解得到的,从营养学角度来说,肽比同一氨基酸组成的蛋白质的消化吸收率要高,且风味优于单个氨基酸,且不易导致过敏现象。虾酱发酵3年时达到较好品质。
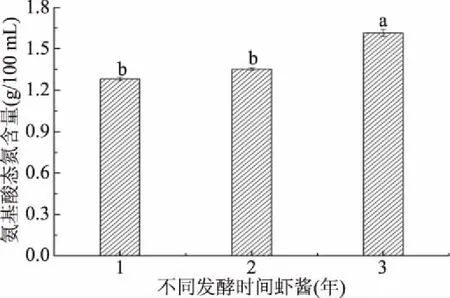
图1 不同发酵时间的乌虾酱氨基酸态氮含量Fig.1 Contents of amino acid nitrogen in shrimp paste
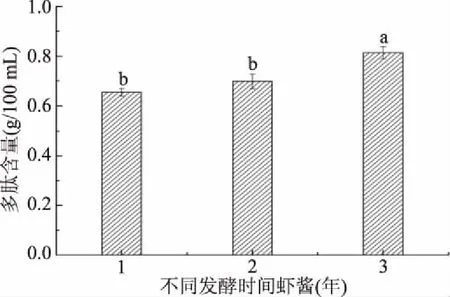
图2 不同发酵时间的乌虾酱多肽含量Fig.2 Contents of polypeptides in shrimp paste
2.2 电子鼻分析
PCA分析是将多变量线性转换选出较少重要变量的一种多元统计分析方法,可对传感器获取的多指标信息进行数据转换和降维,并对特征向量进行线性分类,最终在PCA图上显示主要的两维图,贡献率越大,越能更好地反映样品信息[15-16]。
由图3可知,不同发酵时间下虾酱的第1主成分(PC1)和第2主成分(PC2)的贡献率分别为99.91%和0.089%,累积贡献率为99.99%,表明两个主成分基本代表了样品的主要信息特征。每个样品的3次不重复进样构成一个独立的族群,说明分析的重复性良好;不同发酵时间下虾酱的数据点有重叠,不能完全区分开,且在PC1上无明显差异,在PC2上存在差异但差异较小,说明电子鼻不能很好地区分三种虾酱,即不同发酵时间下虾酱的气味差异不明显[17-18]。
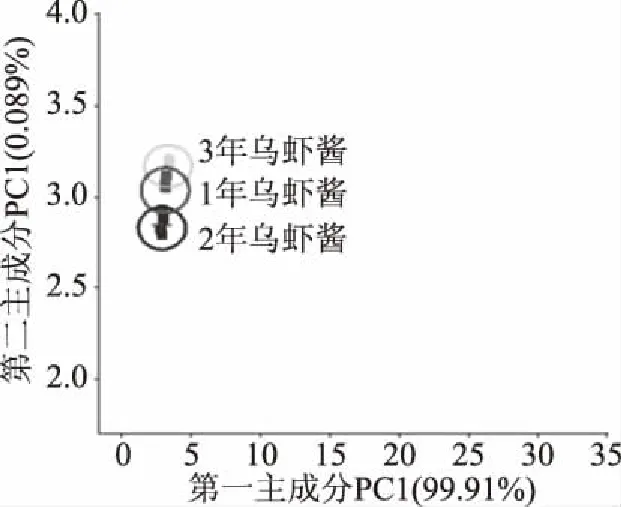
图3 不同发酵时间的乌虾酱电子鼻PCA分析Fig.3 The PCA results of E-nose analysisin different fermentation time
2.3 电子舌分析
图4是不同发酵时间乌虾酱的滋味组成分析。由图4可知,鲜味、鲜味回味(浓厚感)和咸味是虾酱最为重要的味觉指标。不同发酵时间虾酱样品对应的鲜味强度有较为明显的差别,随着发酵时间的延长,虾酱的鲜味强度依次增强。鲜味回味与鲜味的变化规律相同,回味代表了样品滋味的持久性和丰富程度。鲜味回味不仅与鲜味物质的绝对含量有关,还与鲜味物质的种类密切相关[19-20]。由本实验结果可知,3年虾酱的浓厚感最为强烈。三种虾酱的咸味响应值均较高,虾属于海水养殖品种,对环境物质有较强的吸附能力,且虾酱在制作中需要盐分,因此,虾酱会呈现出较高的咸味。咸味主要由Na+、K+等无机阳离子产生,它们的存在可以在一定程度上对咸味以外的其他滋味起到增强作用[20]。鲜味强度与无机离子含量可能也有关系[19-20]。虾酱都具有一定的苦味。发酵前2年虾酱的苦味值接近,且偏高;3年份虾酱的苦味值要明显低于前两种虾酱。三种虾酱样品的涩味值均较小,不在感知范围内[21],表明涩味对虾酱的滋味贡献小。
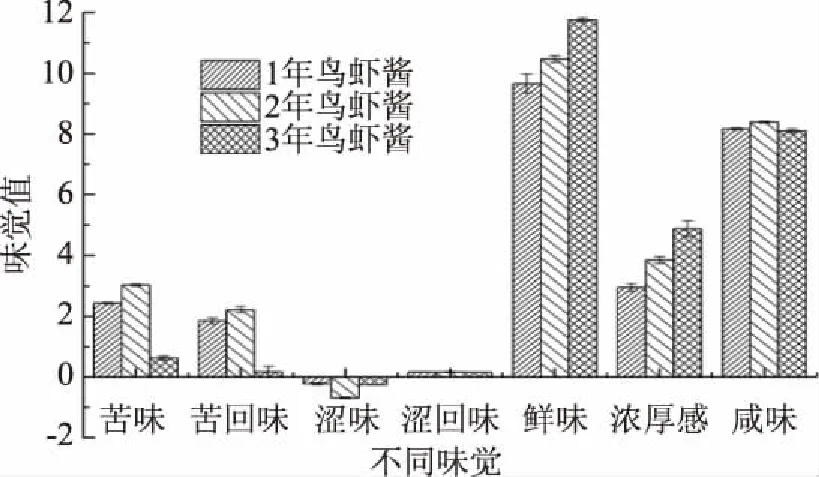
图4 不同发酵时间的乌虾酱电子舌分析Fig.4 E-tongue analysis of shrimp pastein different fermentation time
2.4 挥发性化合物分析
三种不同发酵时间的乌虾酱中鉴定出的挥发性风味物质组成及其相对百分含量如表2所示。由表2可知,三种虾酱样品均含有丰富的挥发性化合物,发酵1~3年乌虾酱中风味成分种类和相对含量均有一定的差异,主要挥发性风味物质分别有42种,46种和44种,包括醛类化合物、酮类化合物、酯类化合物、烃类化合物、呋喃类化合物、含硫含氮化合物以及苯环化合物。
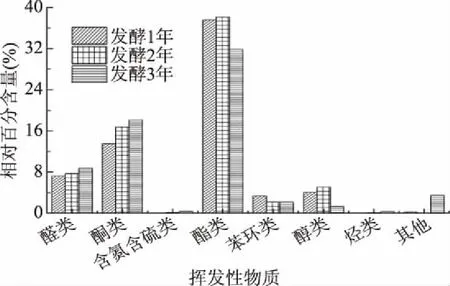
图5 不同发酵时间乌虾酱挥发性物质种类分析Fig.5 Volatile substance types ofshrimp paste in different fermentation time
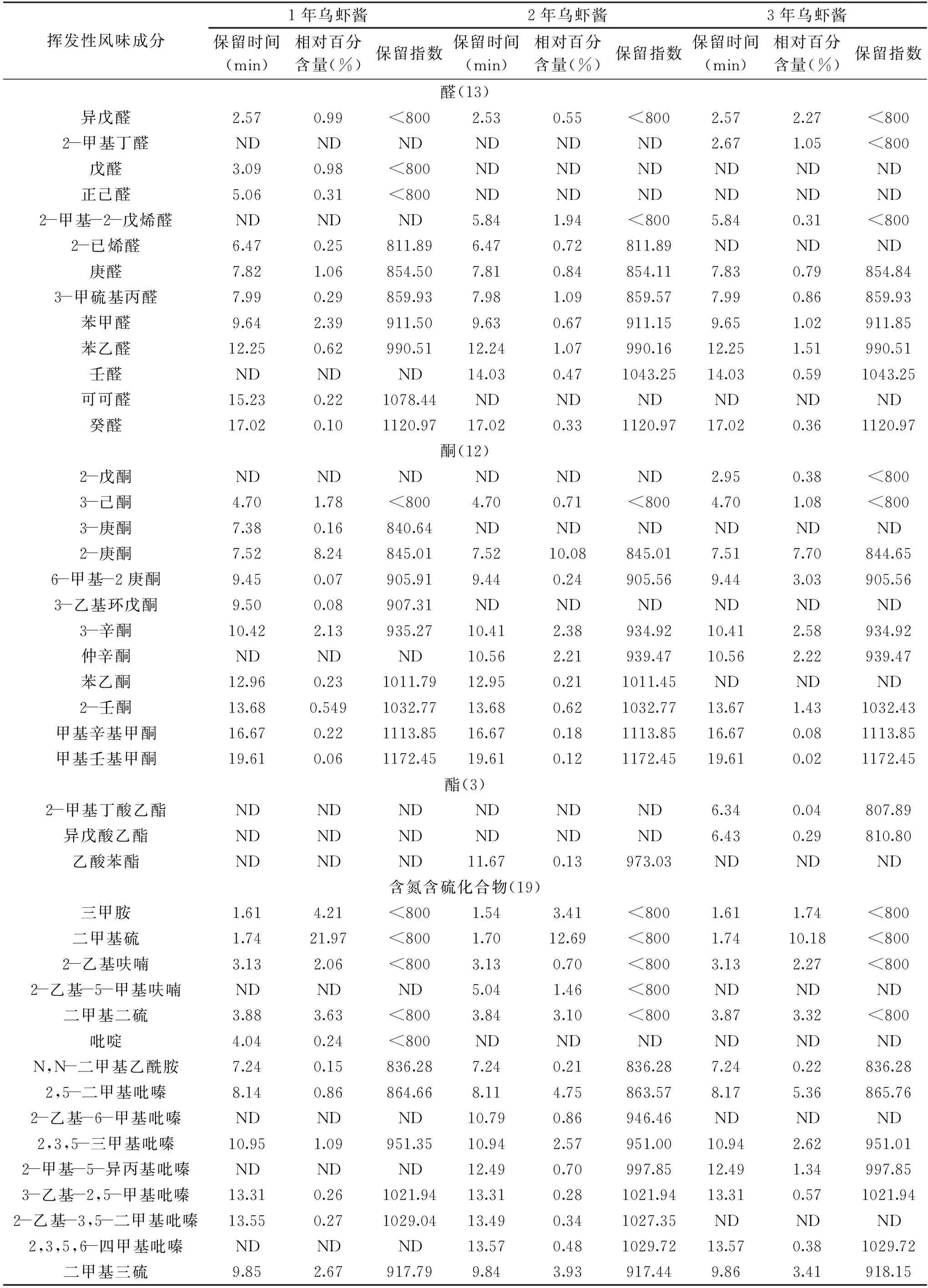
表2 不同发酵时间乌虾酱的挥发性物质分析Table 2 Volatile substances of shrimp paste in different fermentation time
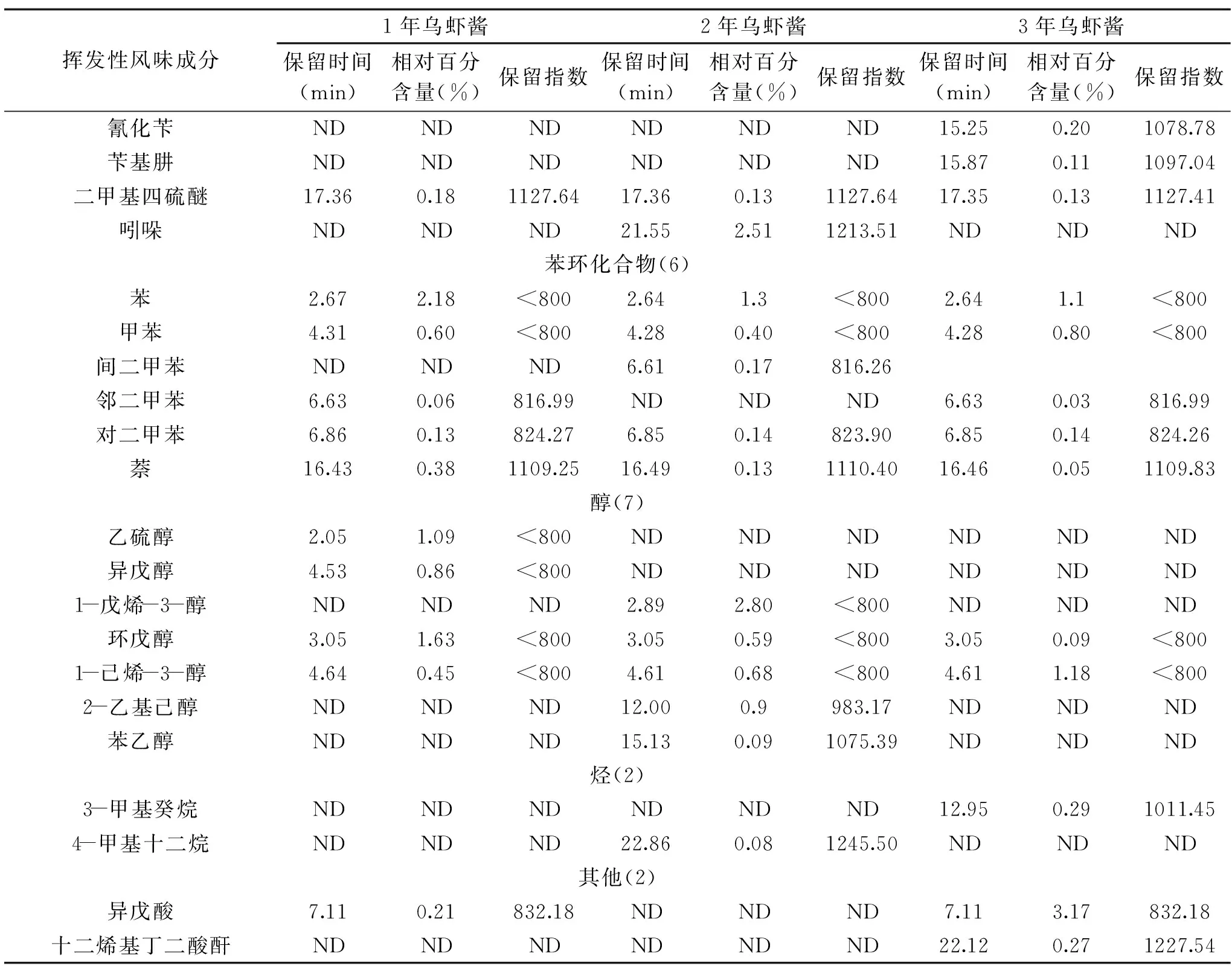
续表
醛类化合物的气味阈值一般较低,是存在于虾肉中的一种重要风味挥发物,其来源可能是由氨基酸的降解反应或不饱和脂肪酸氧化生成的,对发酵水产品的风味特征起重要作用[22-23]。5~9个碳原子的直链饱和/不饱和醛具有青香、油香、脂香气息,10~12个碳原子时具有柠檬味和橘皮味[24]。发酵1~3年乌虾酱中总共检测到13种醛类物质,分别含有10种、9种、9种,其主要的共性成分有异戊醛、庚醛、3-甲硫基丙醛、苯甲醛、苯乙醛、癸醛。随着发酵时间的延长,其总相对百分含量逐渐增加,发酵3年虾酱中醛类的相对百分含量最高为8.76%。庚醛具有强烈的、令人不愉快的、粗糙刺鼻的油脂气味[25],其相对百分含量随着发酵时间的延长而逐渐减少,发酵3年虾酱中的相对百分含量最低。正己醛在发酵1年的虾酱中被检测到,其具有油脂和青草气,高浓度时有酸败、令人作呕的气味,有研究认为这可能是由n-6多不饱和脂肪酸氧化产生[26]。2-甲基丁醛、苯甲醛和苯乙醛具有令人愉快的杏仁味、坚果香和水果香[27],2-甲基丁醛在发酵3年的虾酱中被检测到,而苯甲醛和苯乙醛在三种虾酱中均有检出,且相对百分含量较高,推测可能是虾酱中的特征风味化合物。
酮类化合物由多不饱和脂肪酸的热氧化或降解、氨基酸降解或微生物氧化产生。酮类物质阈值远高于其同分异构体的醛,但由于具有独特的清香和果香味,可能对虾酱风味有一定的增强作用[28]。发酵1~3年乌虾酱中共检出12种酮类物质,分别含有10种、9种、9种,其主要的共性成分有3-己酮、2-庚酮、6-甲基-2庚酮、3-辛酮、2-壬酮、甲基辛基甲酮、甲基壬基甲酮。随着发酵时间的延长,其总相对百分含量逐渐增加,发酵3年的虾酱中酮类的想对百分含量最高为18.14%。3-辛酮具有水果微带薰衣草的气味,2-庚酮具有梨香味,2-壬酮具有焦糖香和脂肪味[27-29],上述物质在三种虾酱中均有检出,且相对百分含量较高,说明其对虾酱香气的贡献较大。
酯类化合物一般具有水果香气[30]。总共在虾酱样品中检测到3种酯类化合物,1~3年的虾酱中分别含有0种、1种和2种。其中3年虾酱的相对百分含量最高,但也仅含有0.33%,而其在其他虾酱中也很少有检测到,故而可以认为酯类化合物对于虾酱的香气贡献较小。
含氮含硫类化合物也是虾酱中主要的挥发性风味物质之一,总共检测到19种,1~3年的样品分别含有12种、16种和14种,且其相对百分含量随发酵时间的延长先增高后降低,发酵2年时的相对百分含量最高,达到38.12%,其次是发酵1年(37.59%)、3年(31.85%)的虾酱。其主要的共性成分有三甲胺、二甲基硫、2-乙基呋喃、二甲基二硫、N,N-二甲基乙酰胺、2,5-二甲基吡嗪、2,3,5-三甲基吡嗪、3-乙基-2,5-甲基吡嗪、二甲基三硫、二甲基四硫醚。二甲基二硫和二甲基三硫主要呈蔬菜香、洋葱香等,三种虾酱中均有检测到,且相对百分含量较高,徐丹萍等[31]在发酵泡菜中检测出这类物质,推测其可能是发酵类食品的特征风味物质。吡嗪类物质是脂肪氧化后又参与美拉德反应的产物,呈现的主要是肉香味和烤香味。吡嗪类既是酱的特征性风味物质,也是虾肉的主要风味物质[32-34]。虾酱中共检测到7种吡嗪类化合物,其相对百分含量岁发酵时间延长而增高,其中3年虾酱中含量最高(10.27%),其次是2年虾酱(9.98%)。3-乙基-2,5-甲基吡嗪和2,3,5-三甲基吡嗪在三种虾酱中均有检出,具有坚果香、可可和烘烤香等,是一类具有低风味阈值的重要挥发性成分[35]。
醇类化合物的阈值通常较高,一般具有芳香、植物香、酸败和土霉味,可能是由于脂肪酸二级氢过氧化物的分解、脂肪的氧化分解或由羰基化合物还原生成[34-36]。三种虾酱中的共性成分有环戊醇、1-己烯-3-醇,一般具有肉味、蘑菇味和温和油脂味[36],对虾的风味有一定贡献。
烃类物质可能源于脂肪酸中烷氧自由基的均裂[37],由于阈值较高,对整体风味贡献较小。在三种虾酱样品中只检出两种烃类物质,含量也很低。烃类化合物可以在某种特定条件下形成醛和酮,是产生虾酱腥味的一种潜在因素[38]。有报道,碳原子数在8~19之间的烷烃存在于甲壳类和鱼类的挥发物中,但由于阈值较高对整体风味贡献不大[39]。
3 结论
利用SPME-GC-MS、电子鼻、电子舌技术以及氨基酸态氮和多肽含量的测定,对乌虾酱发酵期间的挥发性成分相对含量变化进行研究得出,发酵1~3年期间,乌虾酱的氨基酸态氮含量由1.281 g/100 g增长到 1.614 g/100 g,多肽含量由0.655 g/100 g增加到0.814 g/100 g;随发酵时间延长,虾酱中的氨基酸态氮和多肽含量均呈增长趋势;发酵1~3年乌虾酱中的主要挥发性风味物质分别有42种,46种和44种,随发酵时间延长,醛类化合物、酮类化合物、酯类化合物、吡嗪类化合物、烃类化合物、呋喃类化合物的相对含量增加,而除吡嗪类和呋喃类以外的含硫含氮化合物以及苯环化合物的相对含量减少。通过对虾酱在发酵期间挥发性成分进行分析,可以发现对样品整体风味贡献最大的为醛类、酮类和含硫含氮化合物中的吡嗪类;电子鼻PCA分析不能有效区分不同发酵时间样品的品质变化,电子舌结果显示发酵3年时的虾酱口感优良,鲜味突出,明显优于发酵前期的产品。综合研究发现乌虾酱发酵3年时口感更为协调,品质较好。

