低剂量齐拉西酮联合低剂量舍曲林治疗难治性精神分裂症的疗效和安全性研究
郎小娥,薛晓燕,侯 鑫,何 潇,柴 娜,梁 瑛,侯钦强
精神分裂症(schizophrenia,SZ)是一种复发率高、致残率高、死亡率高和疾病负担重的慢性重性精神疾病,其中有20%~30%的病人对抗精神病药物(APs)治疗反应差甚至根本无效,产生阻抗而成为难治性精神分裂症(treatment-resistant schizophrenia,TRS)[1]。即在持续正规治疗后精神症状仍然无法得到有效改善,导致精神分裂症病人发病率和死亡率上升,增加医疗费用,并严重影响病人生活质量[2]。TRS的识别和有效治疗目前仍然是临床上的一大难题。研究显示,氯氮平治疗TRS病人的有效率为30%~60%[3]。2015中国精神分裂症防治指南也指出:尽管氯氮平治疗TRS有效,作为TRS的一线药物,但仍然有30%~50%的TRS病人采用氯氮平治疗无效或不能耐受氯氮平的不良反应,而支持氯氮平联合增效策略对TRS的疗效证据不足,最好的疗效仅获得中等效应值。目前主流观点还是坚持保证氯氮平的足量(300~800mg/d)和足疗程(至少8周)治疗[4]。但是氯氮平存在影响造血系统[5]、代谢综合征高风险以及高剂量时降低癫痫发作阈值和过度镇静等潜在的安全性风险。因此,探究非氯氮平的有效治疗策略,包括其他非典型抗精神病药物的单药或联合治疗具有重要意义。本研究探讨低剂量齐拉西酮联合低剂量舍曲林治疗难治性精神分裂症的疗效和安全性。现报道如下。
1 资料与方法
1.1 研究对象 选取2018年6月—2019年6月就诊于山西医科大学第一医院精神卫生科的TRS病人132例作为研究对象。所有受试者均签署知情同意书,研究方案获得山西医科大学第一医院伦理委员会批准。
1.2 纳入标准 ①符合DSM-Ⅳ中精神分裂症的诊断标准;②符合Conley等制定的TRS诊断标准:过去5年经过至少两种化学结构不同的抗精神病药物足量治疗,每种抗精神病药物至少治疗6周后,未获临床改善[简明精神病评定量表(Brief Psychiatric Rating Scale,BPRS)评分≥45分,临床总体印象-严重度量表(CGI-S)评分≥4分,或4项阳性症状中至少2项≥4分者],5年内病人的社会功能没有处于良好的阶段;③阳性与阴性量表(Positive and Negative Syndrome Scale,PANSS)评分≥60分。
1.3 排除标准 ①有QTc间期延长病史者;②伴有严重心律失常、窦性心动过缓和心肌酶异常者;③有乙醇或药物滥用史者;④伤人毁物、自杀、外跑和肇事的TRS病人需要紧急行改良电痉挛治疗(modified electra convulsive therapy,MECT)或其他方法治疗者;⑤入组前进行血常规、血生化、性功能系列、心电图、脑电图、胸部X线片、心脏和腹部彩超等检查,排除共病器质性疾病病人,同时排除曾用药物毒副反应导致上述各项检查指标异常的病人。
1.4 脱落标准 ①治疗6周症状加重或改善不明显者;②QTc间期延长>485 ms,心率<50次/min,严重心律失常,显著ST-T改变者;③自行要求退出研究者。
1.5 治疗方法 将132例TRS病人随机分为试验组与对照组,每组66例。试验组给予低剂量齐拉西酮胶囊(江苏恩华药业股份有限公司)40~60 mg/d;低剂量舍曲林片(辉瑞制药有限公司)25~75 mg/d。对照组给予中高剂量齐拉西酮胶囊80~160 mg/d。服用其他药物治疗者需事先经过 7 d的药物洗脱期。两组入组时伴有严重失眠或焦虑症状病人口服2~4 mg/d氯硝西泮片(江苏恩华药业股份有限公司),以尽快改善睡眠和控制焦虑激越症状。两组均治疗24周。
1.6 观察指标 ①收集两组TRS病人一般人口学资料;②药物疗效指标:分别于治疗前及治疗后第4周、第8周、第12周和第24周末,由两名高年资主治医师以上职称的精神科医生经过一致性培训后对两组病人进行PANSS量表、汉密尔顿抑郁量表(HAMD-17)、汉密尔顿焦虑量表(HAMA)、CGI-S和个人和社会功能量表(Personal and Social Performance Scale,PSP)等评估;③心脏毒副作用指标:测定两组病人心电图,记录其QTc间期、心率,同时检测血清肌酸激酶(CK)、肌酸激酶同工酶(CK-MB)、α-羟丁酸脱氢酶(α-HBD)和乳酸脱氢酶(LDH)水平,计算齐拉西酮胶囊心脏毒副作用导致的脱落率。

2 结 果
2.1 两组病例脱落情况 在随访治疗的第24周末,试验组脱落8例,其中QTc间期延长>485 ms 2例,失访3例,自动退出2例,治疗8周后疗效不佳者换用其他药物治疗者1例;对照组脱落11例,其中药物的心脏毒副反应导致9例脱落(QTc间期延长>485 ms 5例;QTc间期延长>485 ms同时伴有心率减慢至45次/min,出现晕厥2例;出现频发多源室性期前收缩且ST-T显著改变2例),失访2例。由于齐拉西酮心脏毒副作用导致的脱落率,对照组为13.6%(9/66),试验组为3.0%(2/66),对照组明显高于试验组(P<0.05)。
2.2 两组一般资料比较 两组年龄、首次发病年龄、性别、受教育年限、病程、首发TRS例数和复发TRS例数比较差异均无统计学意义(P>0.05)。详见表1。

表1 两组一般资料比较
注:两组各项比较,P>0.05。
2.3 两组不同时间PANSS评分比较 两组治疗前PANSS各维度评分比较差异无统计学意义(P>0.05)。试验组治疗后第4周、第8周、第12周、第24周末PANSS总分明显低于对照组(P<0.01),第12周、第24周末阳性症状评分明显低于对照组(P<0.05或P<0.01),第8周、第12周、第24周末阴性症状、一般精神病理症状评分明显低于对照组(P<0.05或P<0.01)。详见图1。
2.4 两组不同时间HAMD、HAMA、PSP和CGI-S评分比较 两组治疗前HAMD、HAMA、PSP、CGI-S评分比较差异无统计学意义(P>0.05)。试验组治疗后第4周、第8周、第12周、第24周末HAMD-17、HAMA评分明显低于对照组(P<0.01),第12周、第24周末PSP评分明显高于对照组(P<0.01),第8周、第12周、第24周末CGI-S评分明显低于对照组(P<0.05或P<0.01)。详见图2~图5。

与对照组同时间点比较,*P<0.05,#P<0.01。图1 两组不同时间点PANSS评分比较(A:两组不同时间点PANSS总分变化;B:两组不同时间点阳性症状评分变化;C:两组不同时间点阴性症状变化;D:两组不同时间点一般精神病理评分变化)

与对照组同时间点比较,*P<0.01。图2 两组不同时间点HAMD评分比较

与对照组同时间点比较,*P<0.01。图3 两组不同时间点HAMA评分比较

与对照组同时间点比较,*P<0.01。图4 两组不同时间点PSP评分比较
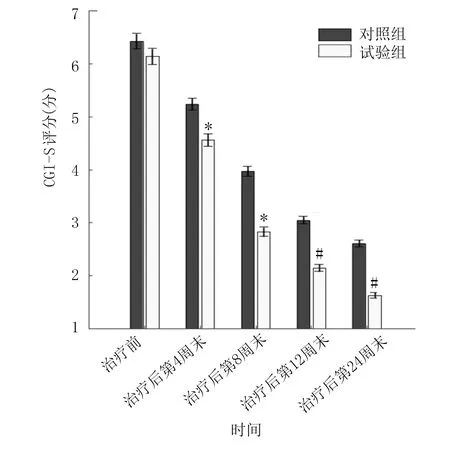
与对照组同时间点比较,*P<0.05,#P<0.01。图5 两组不同时间点CGI-S评分比较
2.5 两组不同时间心脏毒副作用比较 两组治疗前QTc间期、心率及血清CK、CK-MB、α-HBD、LDH水平比较差异无统计学意义(P>0.05)。试验组治疗后第4周、第8周、第12周、第24周QTc间期及血清CK-MB、LDH水平明显低于对照组(P<0.01),第24周CK低于对照组(P<0.01),第8周、第12周、第24周α-HBD明显低于对照组(P<0.05或P<0.01),第4周、第8周、第12周、第24周心率高于对照组(P<0.01)。详见图6~图11。

与对照组同时间点比较,*P<0.01。图6 两组不同时间点血清CK水平比较

与对照组同时间点比较,*P<0.01。图7 两组不同时间点血清CK-MB水平比较

与对照组同时间点比较,*P<0.05,#P<0.01。图8 两组不同时间点α-HBD水平比较

与对照组同时间点比较,*P<0.01。图9 两组不同时间点血清LDH水平比较

与对照组同时间点比较,*P<0.01。图10 两组不同时间点QTc间期比较

与对照组同时间点比较, *P<0.01。图11 两组不同时间点心率比较
3 讨 论
研究表明,TRS与一般精神分裂症可能是相对独立的疾病,TRS或为一组相对独立的疾病亚型,精神分裂症中的难治型或许并非只是更严重的精神分裂症,与治疗应答型比较,还可能存在不同的发病机制和危险因素(如较长时间未治疗的精神病病人与更差的治疗结局相关)[6]。TRS脑影像学研究表明,灰质体积缩小极有可能是TRS独有的特征,区别于非难治性(对非氯氮平抗精神病药物治疗有效)精神分裂症。此外,TRS病人的额颞叶区灌注减少而白质体积和基底核灌注增加[7]。脑萎缩在TRS病人中发生率较高[8]。TRS神经病理机制中主要涉及5-羟色胺(5-HT)与谷氨酸系统异常。TRS病人与非难治性精神分裂症病人相比,其前扣带回谷氨酸水平较高,高前扣带回谷氨酸水平和低血浆5-HT水平能够预测首发精神分裂症病人对抗精神病药物疗效更差的结局。氯氮平是目前国内外公认的唯一对TRS有治疗效果证据的抗精神病药物,它通过拮抗5-羟色胺2A(5-HT2A)受体和减少谷氨酸释放发挥抗TRS作用。精神分裂症病人前额叶皮质的5-羟色胺1A(5-HT1A)受体密度减低,氯氮平对5-HT1A受体有较高的亲和力,显示出较低的锥体外系症状,表明5-HT1A受体与精神分裂症有密切的相关性[9]。目前仍未找到TRS的有效治疗方法。氯氮平成为治疗TRS的金标准[10],并有严格的使用规范以降低其不良反应[11]。由于氯氮平在TRS治疗中的特殊作用,国际学者将氯氮平足量(至少500 mg/d,或至少间隔1周以上的2次血浆谷浓度≥350 ng/mL)、足疗程(至少3个月)治疗无反应的TRS病人特定命名为“氯氮平难治性精神分裂症(clozapine-resistant schizophrenia)”,主要的治疗策略为氯氮平联合其他抗精神病药物或物理治疗,但是疗效并不乐观[12-13]。此外,氯氮平还存在粒细胞减少、代谢综合征高风险以及高剂量时降低癫痫发作阈值和过度镇静等潜在的安全性风险。因此,探究非氯氮平的有效治疗策略,包括其他非典型抗精神病药物的单药或联合治疗,是精神科医生研究的重点。
齐拉西酮是一种新型的5-HT2A受体和多巴胺D2受体拮抗剂,能抑制突触5-HT和多巴胺的再摄取,对精神分裂症的阳性与阴性症状均有效,与其他非典型抗精神病药物相比,其具有锥体外系不良反应发生率低,对血清泌乳素、血脂和血糖代谢影响小,较少引起体重增加,甚至有导致体重下降的作用特点[14]。尽管齐拉西酮存在这些药理学优势,但其具有剂量依赖性的QTc间期延长甚至诱发尖端扭转性室性心动过速(TdP)等致死性心律失常的风险,很有可能会导致精神分裂症病人猝死,这是齐拉西酮治疗安全性的主要关注点[15]。因此限制了其临床应用。当QTc间期延长达到500 ms时,发生TdP的风险将会急剧增加。QTc间期延长被认为是TdP或心源性死亡的风险指标[16]。有报道使用齐拉西酮治疗期间,出现了TdP和猝死的病例[17-18]。本研究发现,采用低剂量齐拉西酮联合低剂量舍曲林治疗TRS,可降低QTc间期延长的幅度。选择性5-HT再摄取抑制剂(SSRIs)类抗抑郁药物都具有选择性对突触前膜5-HT再摄取的强效抑制作用,增加突触间隙有效的5-HT浓度,从而促进5-HT能神经兴奋的传导能力。特别是SSRIs中舍曲林还可以作为多巴胺阻滞剂发挥治疗精神病性症状的作用,舍曲林通过阻断DA转运体(DAT),直接抑制DA再摄取来提高多巴胺功能,而且舍曲林是已知抗抑郁药物中最强效的DA再摄取抑制剂[19],为精神分裂症病人带来显著的临床获益,如精力、动机、集中注意力和焦虑抑郁情绪等多方面的改善,从而消除其阴性症状、情感症状和认知症状;舍曲林还具有结合σ1受体的独特效应,该效应能够治疗抑郁障碍病人的精神病性成分;此外,舍曲林几乎无心脏毒性,甚至有心脏保护作用。舍曲林的上述药理学特征为其用于精神分裂症的治疗提供了理论依据[20]。本研究首次将低剂量齐拉西酮与低剂量舍曲林联合用于治疗TRS病人,结果显示,低剂量舍曲林联合低剂量齐拉西酮的治疗方案更有利于消除精神分裂症病人的阴性症状、情感症状和认知症状,还表现出较低的心脏毒性。
综上所述,本研究首次使用低剂量舍曲林联合低剂量齐拉西酮治疗TRS,为TRS提供了一种新的安全有效的治疗策略,由于使用低剂量齐拉西酮和低剂量舍曲林,可降低医疗成本,减轻TRS病人的经济负担,具有重要的临床实用价值和社会经济价值。

