情绪抑制量表的汉化及信效度检验
刘丽萍,周春兰,吴艳妮,从维莲,胡明钰,李晓霞
(南方医科大学南方医院,广东 广州510515)
情绪抑制不仅影响癌症患者的心理适应, 还会影响他们的免疫、心血管和内分泌功能[1-2],导致情绪障碍,生活质量下降[3-5]。 因此,关注癌症患者的情绪调节特点, 早期对情绪抑制程度高的患者进行筛查显得尤为重要[6]。 通过文献回顾,发现可以测量情绪抑制水平的中文版量表有考陶尔德情绪控制量表、伯克利情绪表达量表、斯坦福情绪调节量表、情绪表达性量表和情绪调节量表, 但这些量表都只是以情绪抑制为其中一个维度, 不能揭示情绪抑制的本质和因素[7]。目前国内尚无可测量情绪抑制的专用量表, 因此引进情绪抑制的测评工具也是很有必要的。 由Robert Kellner 开发的情绪抑制量表(Emotional Inhibition Scale)以其良好的信效度且适用于评估个人抑制情绪的趋势及内在因素, 被广泛应用于心理学测评中。目前该量表尚无中文版本,故本研究旨在引进情绪抑制量表, 进行跨文化调试及信效度检验, 形成适用于我国国情的中文版情绪抑制量表, 为了解国内情绪抑制现状和影响因素提供科学依据。
1 对象与方法
1.1 研究对象 采用便利抽样法, 于2019 年1—5月抽取广州市的一所三级甲等医院癌症患者作为研究对象。为了更好地代表癌症人群,本研究采用分层便利抽样方法,根据2018 年最新的全球癌症数据[8],选取发病率排在前十位的癌症患者:肺癌、乳腺癌、前列腺癌、结肠癌、鼻咽癌、胃癌、肝癌、直肠癌、食道癌、子宫颈癌、样本分别从10 个科室选取。 纳入标准:(1)经病理诊断为癌症; (2)年龄>18 周岁;(3)有清晰的认知,具备完全的行为能力;(4)已签署知情同意。 排除标准:有确诊的精神疾病。
1.2 研究方法
1.2.1 研究工具
1.2.1.1 一般资料调查表 为自行设计, 内容包括年龄、性别、婚姻状况、信仰、家庭收入、教育程度、职业、疾病类型、医疗费用支付方法和近期治疗方式。
1.2.1.2 情绪抑制量表 由Robert Kellner(1986)研制,用于评估个人情绪抑制水平,解释情绪抑制行为和内在特征的唯一可靠工具[9]。 它包括4 个分量表:胆怯、言语抑制、自我控制和情感伪装,每个维度有4 个条目。 采用5 级评分制,由0 分(不会)到4 分(总是),得分越高表明内向程度、自我控制和胆怯程度越高。 其中反向计分条目为2、4、5、9、11、16。
1.2.1.3 中文版多伦多述情障碍量表-20 由多伦多大学Bagby(1994)研制[10]。2003 年经袁勇贵等[11]汉化修订,可用于衡量一个人识别、描述和表达感受的困难程度。 该量表为自评量表,有20 个条目,分为3个维度:外向思维、难以描述感受、难以识别感受。采用5 级评分制,由1 分(完全不同意) 到5 分(完全同意),分数越高则表明述情障碍程度越重。 总量表的Cronbach α 系数为0.83,重测信度为0.87。
1.2.2 量表汉化与跨文化调试 由于原作者Robert Kellner 已去世,故通过电子邮件与意大利版本修订者Laura Siri 联系,获得汉化授权。 根据Brislin 翻译原则对情绪抑制量表进行汉化和文化调适[12]。 步骤如下:(1)2 名双语医学研究生完成了情绪抑制量表正向翻译;(2)1 名留学硕士完成正译的2 个版本进行整合调试形成最终版本;(3)2 名双语专家(1 名护理教师,1 名医学研究生)对最终版本进行回译;(4)由另一名未参与前期翻译的留学硕士对回译版本进行整合调试形成最终回译版本;(5)召开专家小组会议,从概念等价、语义等价、习惯等价和经验等价的角度对以上所有的版本进行评估,形成预测试版本;(6)选择符合标准的30 例癌症患者对预测试版本进行预测试,并要求30 名参与者对条目的理解性给予反馈;(7)专家小组对所有条目进行了重新讨论和调整,直到每个条目没有实质性差异,最后确定了修订版情绪抑制量表。
1.2.3 资料收集 该调查分2 个阶段进行。 (1)从2019 年1—3 月选取样本1(n=100)完成修订版情绪抑制量表和中文版多伦多述情障碍量表-20 问卷调查,进行内部一致性分析和探索性因子分析。 (2)从2019 年4—5 月,招募样本2(n=202)参与问卷调查并进行效标关联效度评估和验证性因子分析。 3周后从2 个样本中随机选取15 例患者再次完成修订版情绪抑制量表来评估重测信度。
1.2.4 信度检验 信度可以反映量表测量结果的可靠程度。 本研究采用重测信度,折半信度Spearman-Brown 系数和一致性检验(Cronbach α 系数)测定量表内部条目的一致性。 其中重测信度包括Pearson相关系数和组内相关系数 (intraclass correlation coefficient,ICC)来体现。
1.2.5 量表的效度检验
1.2.5.1 内容效度 可以通过所有条目的内容效度指数(item-content validity index, I-CVI)和总量表的内容效度指数(scale-content validity index, S-CVI)来测量量表的内容有效性。 本研究成立了一个专家小组(4 名临床护理专家,1 名护理杂志编辑和1 名大学护理专业老师)。 其中专家纳入标准为:熟悉量表引进流程,参与过科研培训,本科及以上学历。 要求专家使用Likert 4 级评估量表对每个条目的相关性进行相应的评分,范围从1(完全不相关)到4(非常相关)。
1.2.5.2 结构效度 采用主成分分析和方差最大正交旋转法, 项目保留和因子提取的标准如下:(a)每个因子有3 个项目或以上组成;(b)因子载荷>0.40;(c)特征值>1.0;(d)删除交叉负荷>0.20 的条目[13]。
用验证性因子分析检测探索性因子分析产生的模型。 估计方法采用最大似然法。 拟合优度指数标准:标准化均方根残差(SRMR)<0.08;拟合优度指数(GFI)>0.90; 卡方统计量与自由度之比 (χ2/df)<3;Tucker-Lewis 指数(TLI)>0.90; 近似的均方根误差(RMSEA)<0.06;比较拟合指数(CFI)>0.90[14]。
1.2.5.3 效标关联效度 将修订版情绪抑制量表的得分与多伦多述情障碍量表-20 的得分进行相关性分析,评估效标关联效度。
1.2.5.4 已知组别效度 将样本按年龄、婚姻状况、信仰、家庭收入、教育程度、职业、癌症诊断时间、癌症类型、癌症分期等特征分组,比较其情绪抑制得分的情况。
1.2.6 统计学方法 采用SPSS 17.0 进行探索性因素分析和描述性统计。 验证性因子分析采用统计软件AMOS 24.0。计量资料采用(均数±标准差)进行描述,P<0.05 表示差异有统计学意义。
1.3 伦理考虑 本研究基于2013 年赫尔辛基宣言中概述的原则进行[15],并获得该案例医院医学伦理委员会的批准(批准号:NFEC-2018-049)。 所有参与者均签署了知情同意书,自愿填写。 并强调在整个研究过程中, 参与者的隐私会得到严格保密。
2 结果
在第1 阶段, 向参与者分发的107 份调查问卷中, 有2 份被丢失,5 份因一些题目未完成被排除。因此,共纳入100 份问卷,有效回收率为93.5%。 在第2 阶段,在向参与者分发的212 份调查问卷中,有4 份被丢失,6 份由于一些题目未完成被排除。 共纳入202 份问卷,有效回收率为95.3%。 此外,患者完成量表的时间范围为5~15 min。
2.1 社会人口学和临床特征 共有302 例患者参与了本研究。样本1 包括27 名女性和73 名男性,年龄22~77(58.1±10.9)岁,样本2 包括97 名女性和105 名男性,年龄20~81(51.7±12.5)岁。 样本1 有1/4 是鼻咽癌,而样本2 有1/4 是乳腺癌。 2 个样本也存在一些共同特征: 近一半样本的癌症分期为II期;大部分样本近期治疗是手术和化疗;近一半的样本家庭月收入≤3 500 元; 且近70%的样本诊断时间<1 年。
2.2 信效度检验
2.2.1 信度 总量表中Cronbach α 系数为0.717,各维度Cronbach α 系数范围分别为0.882、0.749、0.602、0.784。 对于折半信度,Spearman-Brown 系数为0.755(P<0.05)。Pearson 系数为0.855,ICC 范围为0.477~0.944,表明测量结果在不同时间内一致性良好,见表1。
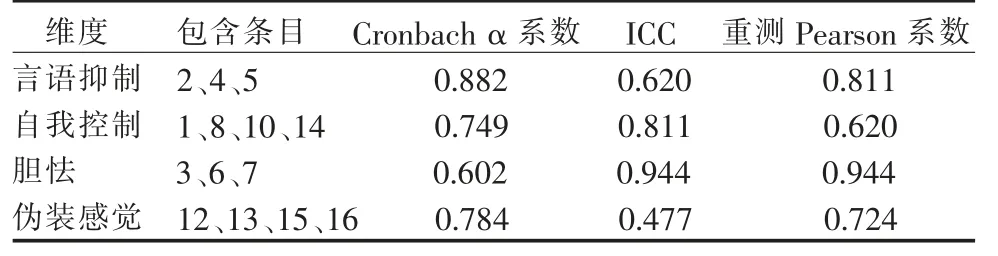
表1 中文版情绪抑制量表的信度检验
2.2.2 内容效度 S-CVI 值为0.915,I-CVI 值0.83~1.00,表明修订版情绪抑制量表内容效度良好。 专家小组降低了中英文语言结构固有差异导致错误的风险,并确定了修订版情绪抑制量表最准确,最易理解的词语。例如,第15 项“你有想过告诉别人你的感受但是抑制了吗? ”被修改为“你有没有想过告诉别人你的感受,却因为不好意思而没有说出口?”。第9 项“你是否会为自己的权利说话?”被修改为“是否会努力争取自己的权利? ”。
探索性因子分析结果显示,该量表KMO 检验值为0.983,Battlet 球形检验统计量为485.45 (χ2=485.5,df=91,P<0.001),表明适合做探索性因子分析。特征根>1.0 的有5 个因子,但项目9 因因子载荷太低被删除,而条目11 因为在这个因子只有一个条目而被删除。 最终修订版情绪抑制量表有14 个条目4 个因子 (见表2)。 根据各因子的内容特性,4个因子分别命名为:言语抑制(因子1),自我控制(因子2),胆怯(因子3),伪装感情(因子4),解释了65.58%的变异。 见表2。
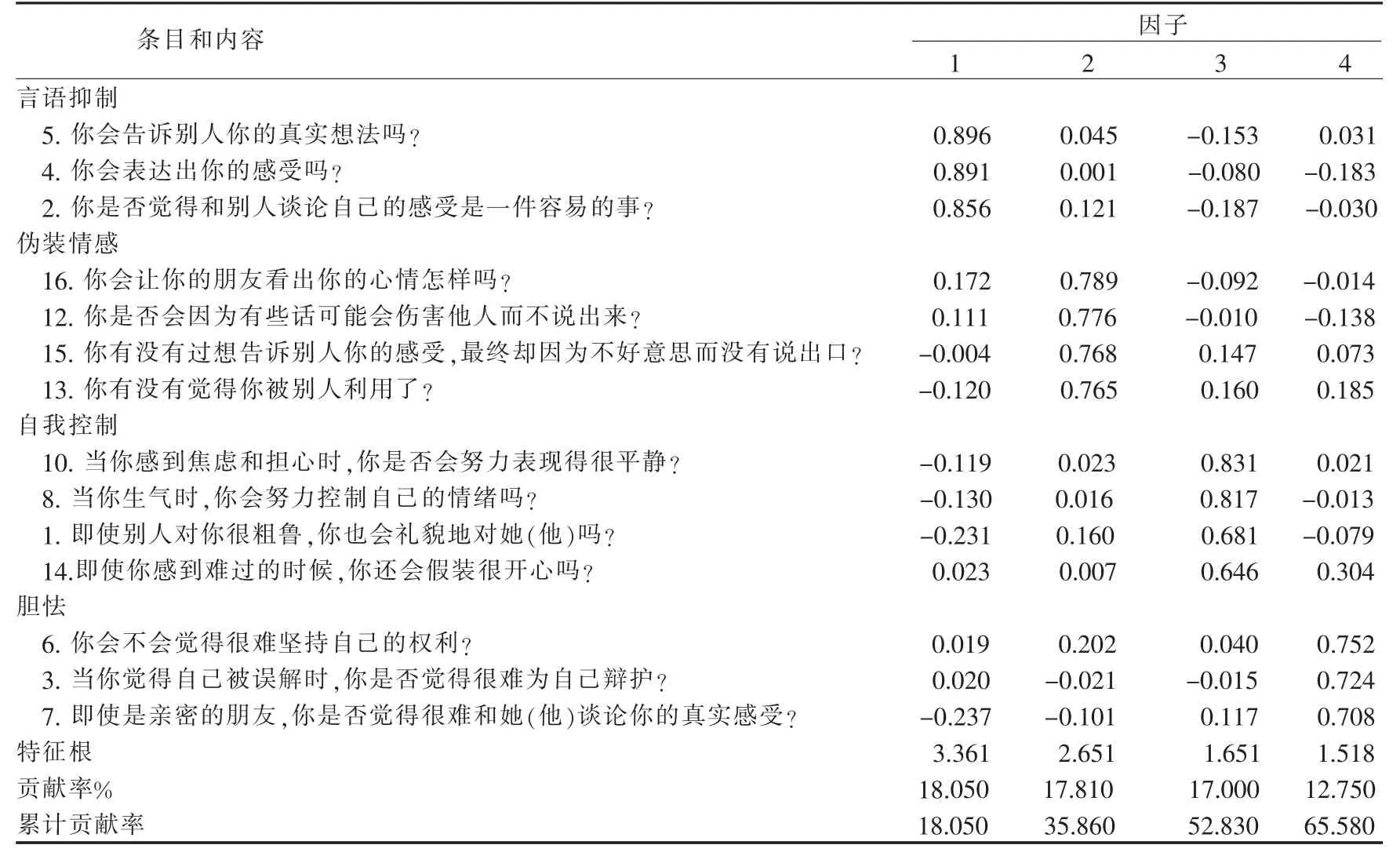
表2 探索性因子分析结果(n=100)
验证性因子分析再次验证了探索性因子分析得出的4 因子结构(见表2)。 5 个残差Cov(e4,e8);Cov(e5,e14);Cov(e7,e13);Cov(e9,e14);Cov(e10,e11)被设置为自由参数来改善模型拟合。 拟合优度指数的结果为:χ2/df=1.438,RMSEA=0.047,SMRM=0.065,TLI=0.940,CFI=0.918,IFI=0.943,表明该模型中模型拟合优度指数良好。
2.2.5 效标关联效度 虽然关联强度相对较小,但总体上中文版情绪抑制量表总得分与中文版多伦多述情障碍量表-20 总得分具有统计学意义(r=0.322,P<0.001),这一定程度上证明了其效标关联效度。
2.2.6 已知组别效度 不同癌症类型及不同癌症分期的患者, 情绪抑制得分比较差异具有统计学意义(P<0.001),详见表3。
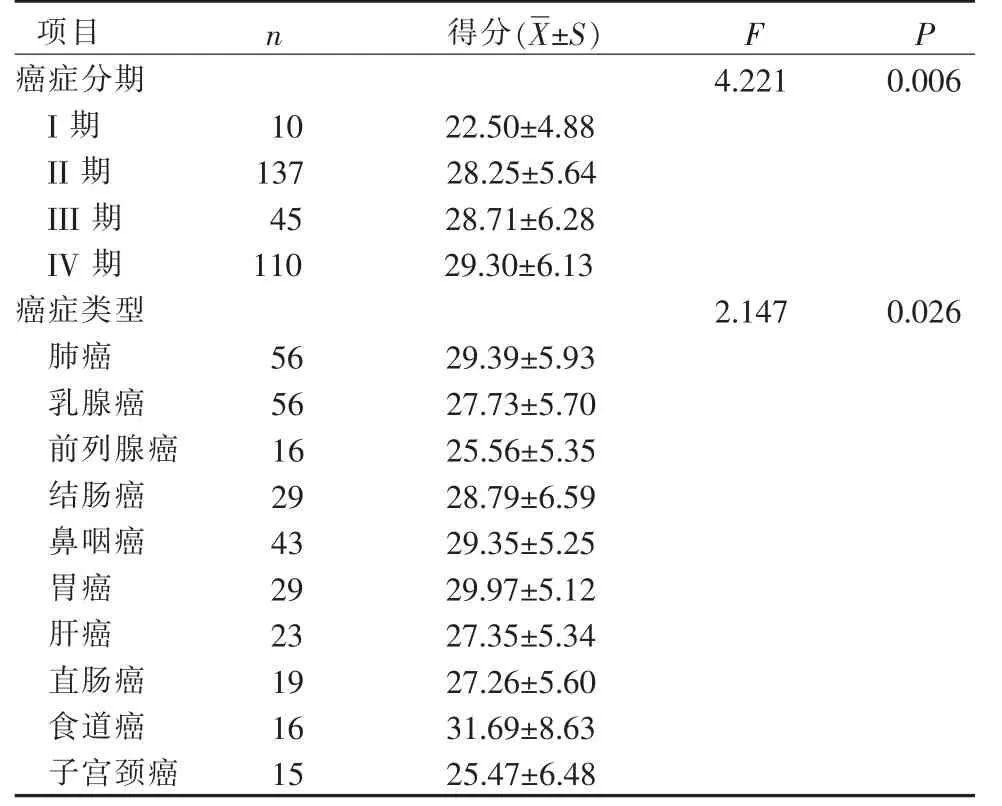
表3 不同特征癌症患者情绪抑制得分比较(n=302)
3 讨论
3.1 中文版情绪抑制量表具有较好的信度 重测信度是评价研究工具稳定程度的指标。 使用同一研究工具重复测量研究对象所得的结果一致性越高,其重测信度越高,该工具的稳定性越好。一般认为,2次测量结果的Pearson 相关系数>0.7,可认为重测信度较好,量表的稳定性高。 本研究Pearson 相关系数为0.866,ICC>0.477,说明中文版的EIS 量表具有较好的重测信度。本研究中量表总的Cronbach α 系数为0.717,4 个公因子的Cronbach α 为0.602~0.882。表明中文版情绪抑制量表具有较好的内部一致性。3.2 中文版情绪抑制量表具有较好的效度 内容效度采用CVI 作为量化测评指标,一般认为CVI 应达到0.80 以上可接受。 本研究结果(S-CVI=0.915,I-CVI=0.83~1.00) 提示量表中各条目的代表性较好,说明量表所涉及的内容可以体现情绪抑制。
因为样本之间在文化、样本、种族或某些社会因素方面存在潜在差异, 不同语言版本的结构模型常常存在差异, 故进行跨文化调试和因子分析是非常重要的。根据因素分析,修订版量表从原量表中删除了2 个条目:条目9(“你是否说出你的权利? ”)和条目11(“即使对你不好,你会说出你的想法吗?”)。最终中文版情绪抑制量表包括4 个维度:言语抑制(条目2,4,5),自我控制(条目1,8,10,14),胆怯(条目3,6,7),伪装感情(条目12,13,15,16)。 与英文版的情绪抑制量表[16]相比,因子数和名称相同,但每个因子具体条目不相同。 这些条目的转变可能是由于美国和中国患者类型,样本大小,参与者年龄,性别分布和疾病状况的差异。 14 个条目的因子载荷范围为0.602~0.882, 累计方差贡献率达65.58%(见表2),体现了良好的结构效度。
在验证性因子分析中, 由于某些条目存在相似之处,在残差之间存在5 个相关性。在验证性因子模型中, 量表条目的语义相似性是相关误差的最常见原因[17],很难避免。 但验证性因子分析模型中的拟合优度指数良好, 表明中文版情绪抑制量表具有较好的效度。
对于效标关联效度, 尽管中文版情绪抑制量表与中文版多伦多述情障碍量表-20 Pearson 系数差异有统计学意义,但这种关联相对较小,这与之前的研究一致。Grandi 等[16]的研究表明,情绪抑制与述情障碍概念类似但有差异。 述情障碍与情绪抑制量表中“言语抑制”维度呈正相关,而与情绪抑制量表中“自我控制”“胆怯”和“情感伪装”维度无关。
3.3 中文版情绪抑制量表的实用性及可行性 作为应对方式之一, 情绪抑制是癌症人格特征的核心组成部分[18]。 被诊断患有癌症并经历各种治疗可能是一种情绪上的创伤经历, 因此癌症患者将更需要释放他们的负面情绪[19]。 因此,在癌症患者心理护理中增加情绪抑制预防与干预是非常必要的。目前,国内有关情绪抑制研究很少, 故而对这方面的关注也少。国外研究发现,让倾向于情绪抑制的人释放不良情绪可以减少痛苦[20]。 而引入有效的评估工具是进行情绪抑制早期筛查和心理干预的基础。 本研究在中国癌症患者样本中验证了中文版情绪抑制量表有良好的信效度, 说明中文版情绪抑制量表可对情绪抑制程度进行初步测量, 并确定情绪困扰的早期迹象。该量表由于没有复杂的句子和计算,可以在15 min内完成,因此在临床上很容易执行,具有较好的适用性和可操作性。综上所述,中文版情绪抑制量表可作为一种简短而有效的衡量标准, 供护士和心理学家评估情绪抑制水平和情绪披露干预的效果。
3.4 局限性及未来研究方向 本研究有一些局限性。目前的样本量较小,仅限于一所三级甲等医院的癌症人群, 未来的研究需要在中国其他人群和不同地区招募更多具有代表性样本进行验证。其次,这项研究方法采用自填问卷调查,可能存在潜在的缺陷,如报告偏倚, 未来的研究可以加入客观的测评方法联合评估,例如生理测量及脑电图测量。另外由于本量表条目不具备疾病特异性, 需要更进一步的研究来测试在非癌症疾病样本或健康样本中该量表是否足够敏感。
[致谢] 本研究感谢吴金艳、李文姬、李晓瑾、邓霞、张进超、王艳芳等老师在本量表汉化及跨文化调试过程中的帮助, 陈昭越博士在统计学方法处理上的支持。
——基于体育核心期刊论文(2010—2018年)的系统分析

