非耐盐乳酸菌与米曲霉共生酿造酱油的研究
孙莉,胡文康,黄瑶,付彩霞,李冬生,徐宁*
(1.湖北工业大学 生物工程与食品学院 湖北省食品发酵工程技术研究中心,武汉 430068; 2.湖北土老憨生态农业科技股份有限公司,湖北 宜昌 443000)
酱油最早起源于我国的周朝(公元前1046年-公元前256年)[1],又称“清酱”或“酱汁”。目前传统酱油以大豆、豆粕等为原料,以面粉、小麦等作为辅料,利用微生物的分解作用,主要是米曲霉、酵母菌和乳酸菌等产生丰富的酶系将原料水解成各种氨基酸、小分子肽、单糖、寡糖、有机酸,进而在一定的温度、湿度条件下,发生一系列的生化反应,最终形成具有特殊色泽、滋味并带有浓烈酱香味的醪液[2]。在两大传统发酵方式中,高盐稀态发酵法改善了低盐固态酱油所带来的口感不佳的问题[3,4]。高盐稀态发酵工艺结合了纯菌种制曲和天然晒露发酵法的优点,所得成品酱油的酱香味浓郁,口感滋味佳。此类发酵产品深受消费者的青睐,是我国目前出口的酱油制品,在未来的酱油工艺发展过程中也将扮演不可或缺的角色[5,6]。
我国酱油酿造普遍采用单一菌种制曲,但由于发酵过程是半开放式,发酵体系实际上由多种微生物构成,参与的微生物种类繁多,发酵过程中微生物群落不断地演替变化,最终完成大分子原料的降解、转化、代谢等过程[7]。多菌种制曲是指在制曲阶段选育多种微生物混合制曲,它可以弥补单一米曲霉制曲存在的原料利用率低、风味差等问题,对酱油产量和质量的提高具有重要意义。但各种微生物生长所需的原料、温度、湿度、pH等条件存在差异,并且多种微生物之间的相互作用尚不明确,所以实际生产中尚未使用[8]。
因此,本研究通过在制曲过程中添加适量的非耐盐的乳酸菌,模拟传统酱油酿造的多微生物的群落制曲过程,研究制曲过程中乳酸菌与米曲霉共生生长对曲料酶系的影响以及后期酱油中各项生化指标的变化情况,以期为非耐盐乳酸菌具体如何影响酱油的品质变化和现代化多菌种酱油的生产应用提供理论基础。
1 材料和方法
1.1 菌种和材料
米曲霉3.042 HY-04、乳酸菌融合魏斯氏菌(Weissellaconfusa)HY-02:均保藏于湖北工业大学湖北省食品发酵工程技术研究中心;豆粕、炒小麦:由湖北土老憨生态农业科技股份有限公司提供。
1.2 酱油的制备
酱油曲制备的工艺路线,参照高盐稀态酱油的发酵工艺流程[9]。具体的曲料配方为:豆粕加一定比例的水润湿1.5~2 h左右,豆粕润水后与炒小麦按照6∶4的比例混合均匀,于115 ℃高温灭菌锅灭菌20 min,放入无菌操作室冷却至室温。接种米曲霉种曲0.5%,乳酸菌1.0 mL/100 g(每1 mL菌液含有1.0×1010CFU个乳酸菌,对照组只接种米曲霉),随后放入制曲室培养直至制曲结束,制曲温度范围为32~35 ℃。制曲时间为36~40 h,期间翻曲2次。将成熟曲料装入发酵罐中,并注入其2倍质量的18%盐水,置于35 ℃恒温发酵箱中发酵4个月。
1.3 样品的收集
收集16,20,24,28,32,36,40 h的成曲以及15,30,45,60,75,90,105,120 d酱醪发酵液样品,密封,-20 ℃冰箱保存备用。
1.4 成曲中酶活力的测定
称取2.0 g的成曲,用研磨研碎后装入干净的烧杯中,加入适量体积的缓冲液,于40 ℃水浴锅浸提1~1.5 h,此过程中不时搅拌,之后用适宜pH的缓冲液稀释定容,最后经滤纸过滤得粗酶液。
参照SB/T 10317-1999标准[10]中的方法测定曲料中的中性蛋白酶活力(pH 7.2的磷酸缓冲液)、酸性蛋白酶活力(pH 3.0的乳酸钠缓冲液)。α-淀粉酶活力的测定参考Chutmanop J等的研究方法[11,12],取稀释粗酶液与0.4%的淀粉溶液在40 ℃水浴锅预热 5 min,取酶液0.1 mL加入1 mL淀粉混合均匀于水浴40 ℃反应7.5 min(精确计时),加入1 mL碘(0.01 mol/L)混合均匀,加5 mL蒸馏水稀释,测定其在660 nm处的吸光值。纤维素酶活力的测定参照Vatanparast等的研究方法[13,14],采用DNS法。果胶酶活力的测定参照Long L H等的研究方法[15,16],测定其在540 nm处的吸光度值。β-葡萄糖苷酶的测定参考Elghonemy D H等的研究方法[17,18],采用pNPG法。
1.5 制曲过程中乳酸菌的生长变化情况
乳酸菌的数量计算采用平板计数法,用灭菌生理盐水稀释至相应倍数,吸取适量菌液均匀涂布于倒有MRS培养基的平板中,于恒温培养箱培养2~4 d,观察并记录乳酸菌菌落数。
1.6 酱油中pH的测定
取适量的醪液发酵液,用精密pH计测定。
1.7 酱油常规指标的测定
选用甲醛滴定法分析测定酱油中氨基酸态氮的含量。总氮含量的测定参考陈智慧等的研究中采用的凯氏定氮法并稍作修改[19]。参考国家标准GB/T 5009.39-2003[20],采用酸碱滴定法测定酱油中总酸的含量。还原糖含量的测定采用DNS比色法。
1.8 酱油中总黄酮和多酚类物质的测定
酱油中总黄酮含量的测定参照黄健蓉等的测定方法[21],采用比色法进行测定。总多酚含量的测定参照Hsiao W Y等的测定方法[22]。
1.9 酱油抗氧化能力的测定
DPPH自由基清除能力的测定参考Hsiao W Y等的试验方法:稀释酱油与DPPH乙醇溶液充分震荡摇匀,室温避光黑暗条件下静置30 min,测定517 nm处的吸光值。亚铁离子还原能力(FRAP)的测定参照Granato D等的研究方法[23]。预热的稀释样品在37 ℃下与预热的FRAP工作液反应4 min,测定593 nm处的吸光值。
1.10 有机酸的测定
从发酵罐中量取适量酱油样品,滤纸过滤除去酱渣,用Amberlite IR120阳离子交换树脂脱去盐分,取适量脱盐样品,于冷冻高速离心机以10000 r/mim离心30 min,取上清液用微孔滤膜过滤。有机酸的测定参照Park Y C等的方法,采用液相色谱法[24]。
2 结果与讨论
2.1 制曲过程中主要酶活力的变化
添加乳酸菌(魏斯氏菌)的实验组与对照组在制曲过程中酶活动态变化情况见图1。
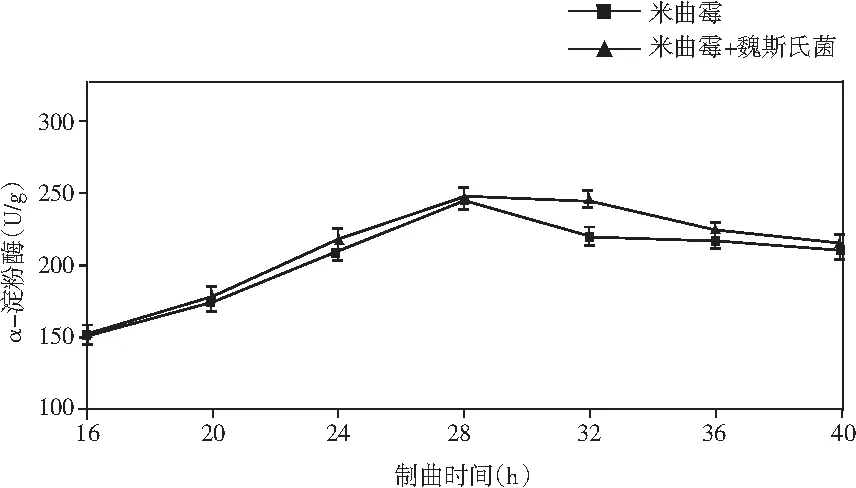
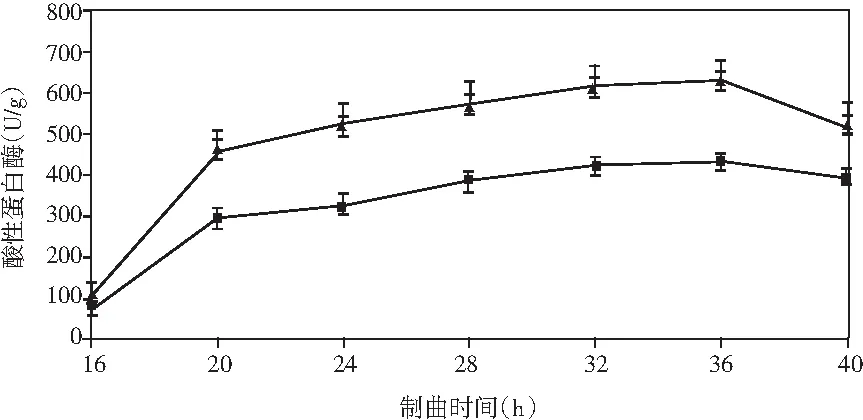
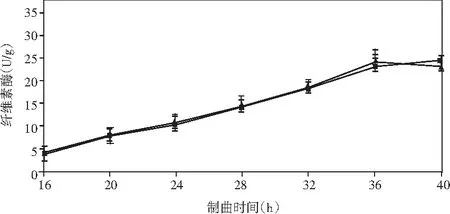
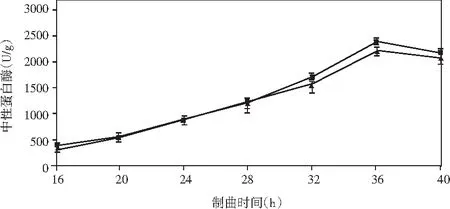
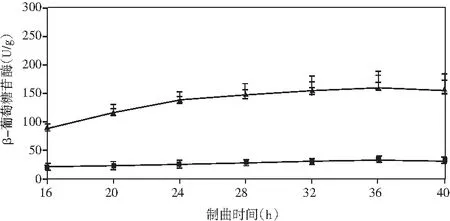
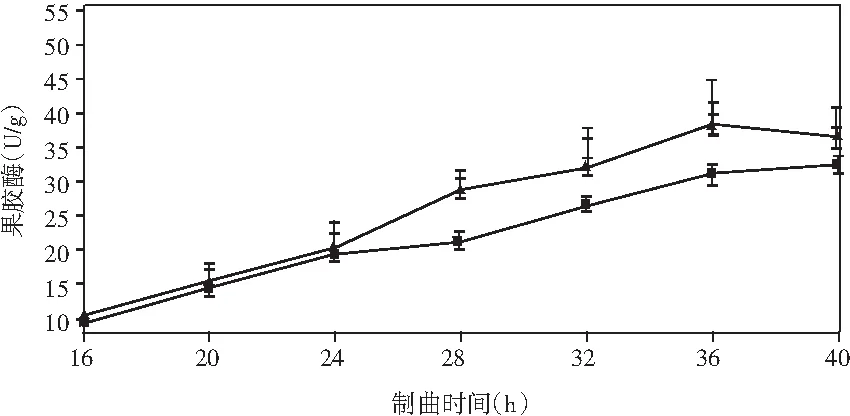
图1 制曲过程中酶活变化情况Fig.1 The changes in enzyme activity during koji making
由图1可知,在制曲36 h时,除α-淀粉酶外,其余各组酶酶活均达到最大值。实验组与对照组相比,中性蛋白酶活力稍有下降,但不显著;α-淀粉酶酶活力无明显差异;酸性蛋白酶酶活力提高了47%;β-葡萄糖苷酶酶活力提高了460%(160.47 U/g);纤维素酶酶活力提高了18%(24.43 U/g);果胶酶酶活力提高了23%(38.53 U/g)。
结果表明,制曲过程中添加乳酸菌会增强成曲曲料整体蛋白酶酶系的活力。β-葡萄糖苷酶可以分解原料中糖苷型异黄酮成游离的苷元形式,其酶活的提高可以有效改善成品酱油中游离型异黄酮苷元的含量,从而提高酱油的抗氧化活性等保健功能。果胶酶可分解果胶为半乳糖醛酸,降低酱油的黏度,进而提高出油率[25]。
2.2 制曲过程中非耐盐乳酸菌的生长情况
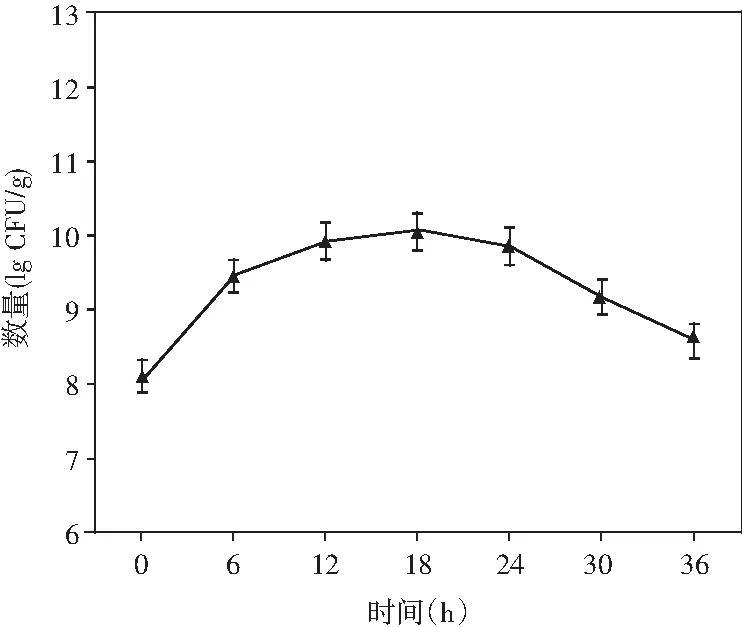
图2 制曲过程中非耐盐乳酸菌生长变化情况Fig.2 The changes in growth of non-salt-tolerant lactic acid bacteria during koji making
由图2可知,非耐盐乳酸菌在制曲过程中呈现出先增加后减少的趋势,在制曲前12 h,乳酸菌呈现快速增长的趋势,而后增长开始减缓,可能的原因是后期对于曲料的翻动,增加了整体的含氧量,稍微抑制了乳酸菌的生长。在最终制曲结束的36 h时,曲料存在乳酸菌数量为4.06×108CFU/g。
2.3 酱油发酵过程中pH的变化
酱油发酵过程中pH的变化见图3。
添加乳酸菌制曲的酱油的pH在发酵过程中呈先下降并逐渐保持稳定的趋势,在发酵的前20 d,pH下降速度较快,在60 d以后基本保持不变。在发酵的120 d时,米曲霉组的pH值维持在4.63左右;添加了乳酸菌的实验组的pH值较米曲霉的pH值减少了4.7%(pH 4.41)。
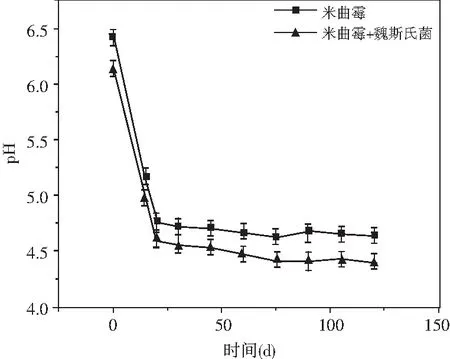
图3 酱油发酵过程中pH的变化Fig.3 Changes in pH values during soy sauce fermentation
2.4 酱油样液发酵过程中理化指标的变化
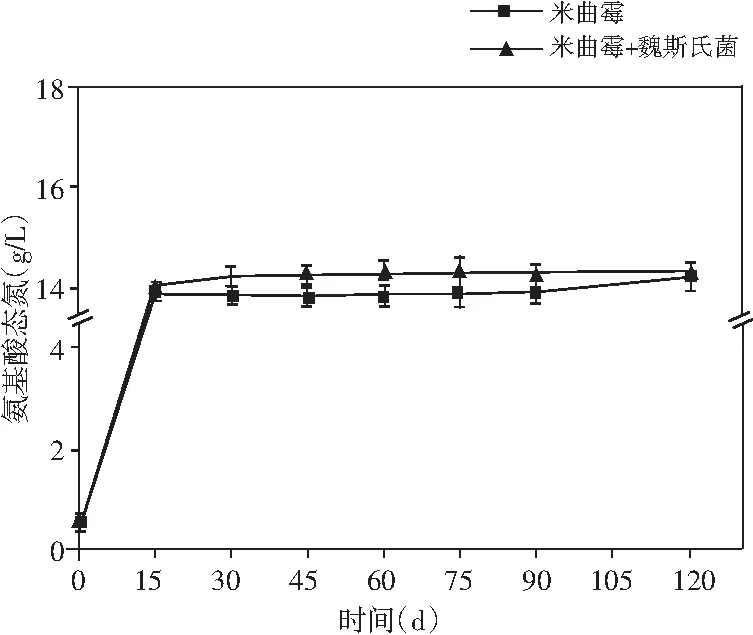
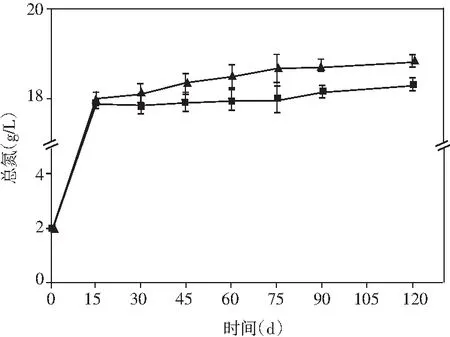
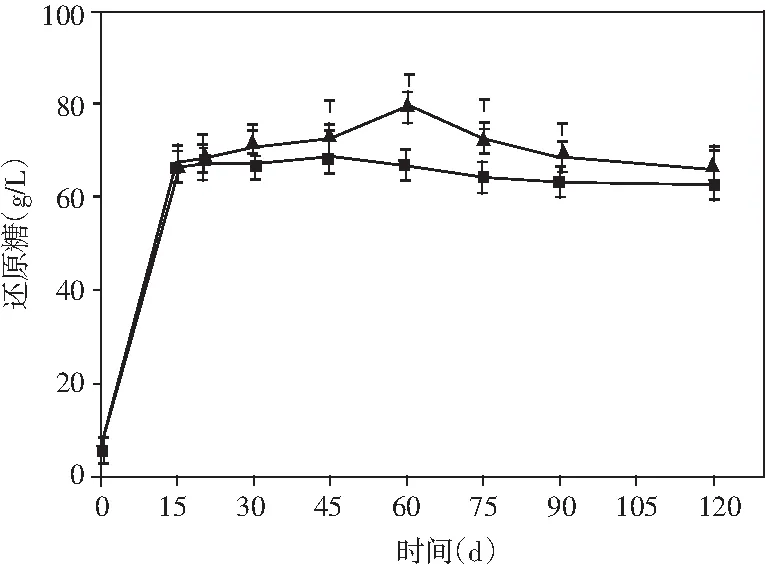
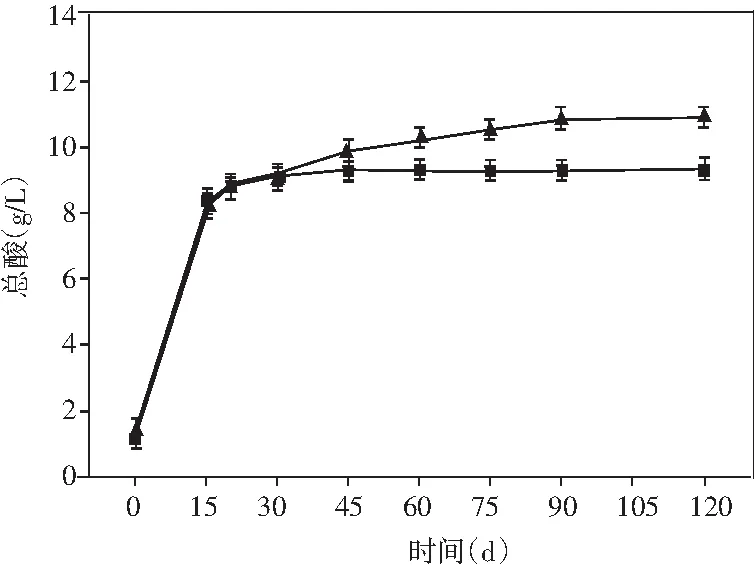
图4 酱油发酵过程中氨基酸态氮、总氮、 还原糖和总酸含量的动态变化Fig.4 Dynamic changes of amino acid nitrogen, total nitrogen, reducing sugar and total acid content during soy sauce fermentation
酱油中的氨基酸态氮、总氮、还原糖和总酸的含量都有利于酱油产生特定风味物质[26]。研究了添加乳酸菌制曲的酱油在发酵过程中上述4种物质含量的动态变化。由图4可知,氨基酸态氮、总氮和总酸的含量呈现先增加然后趋于平缓的趋势。在发酵完成时,与米曲霉酱油相比,添加了非耐盐乳酸菌的实验组氨基酸态氮、总氮均有小幅度提升,总酸的含量提升最为显著,提高了17.48%。酱油发酵过程中,在发酵的第60天,添加乳酸菌的实验组还原糖的含量达到最大(79.93 g/L),而米曲霉组的还原糖含量却在酱油发酵的第45天达到最大,最大值为65.42 g/L。还原糖含量在发酵的前期迅速增加,且实验组增加的时间高于对照组,可能是在制曲过程中得到大量的淀粉酶,以及添加乳酸菌后,纤维素酶和果胶酶活力的提高,将原料中淀粉、果胶、纤维素类物质大量分解为还原糖,后期还原糖含量的减少可能是还原糖在酱油发酵的后期参与了美拉德反应[27]。上述结果表明:在制曲过程中添加乳酸菌可有效提高酱油的品质。
2.5 酱油发酵过程中多酚类物质和抗氧化能力的动态变化
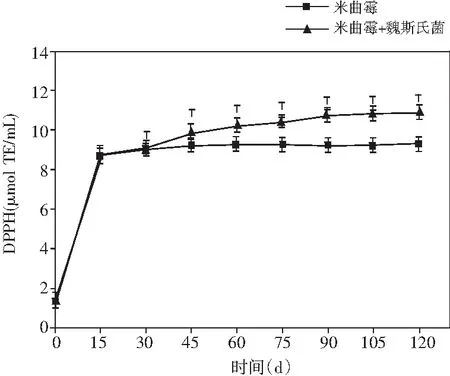
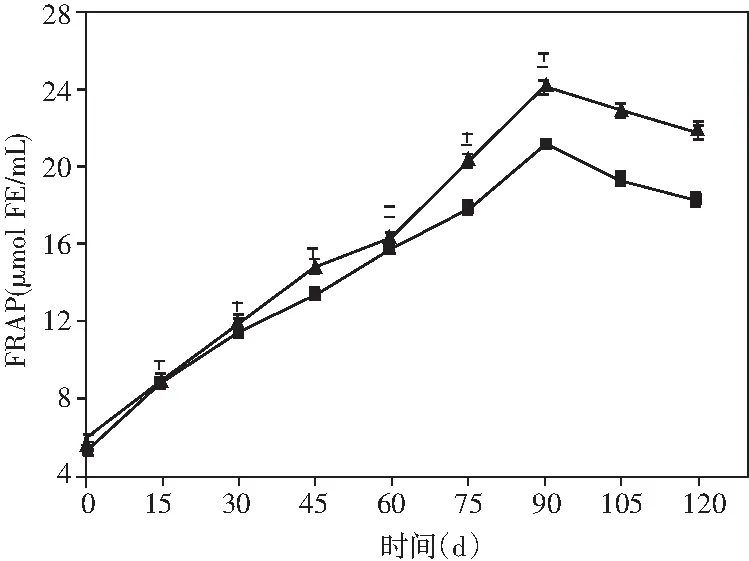
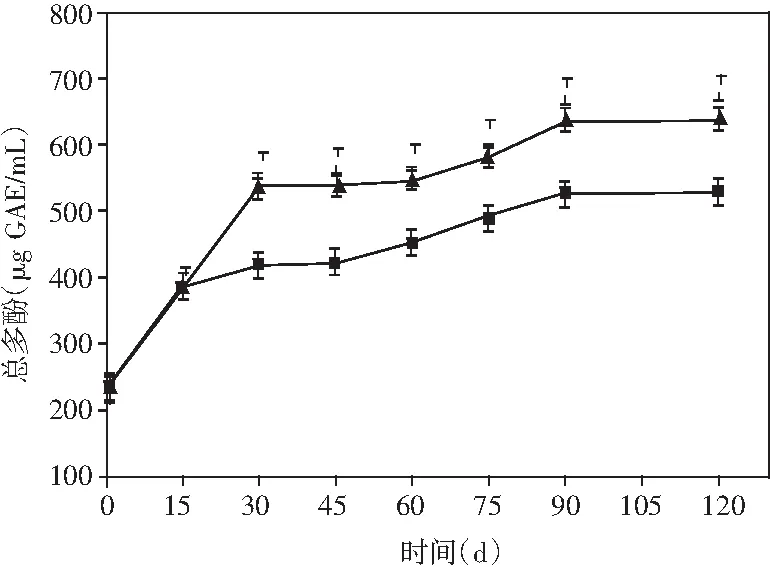
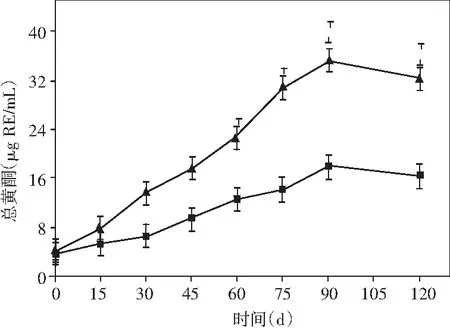
图5 酱油发酵过程中多酚类物质和抗氧化能力的动态变化Fig.5 Dynamic changes of polyphenols and antioxidant ability during soy sauce fermentation
通过总多酚和总黄酮两个指标在发酵过程中含量的变化来阐释酱油发酵中酚类物质的动态变化情况,通过DPPH和FRAP两个指标在发酵过程中含量的变化来阐释酱油发酵中抗氧化能力的动态变化情况,见图5。
由图5可知,添加乳酸菌的酱油中总多酚、总黄酮含量的变化相似,在发酵阶段呈现不断增加的变化趋势。在发酵第120天时,米曲霉组总多酚为530.65 μg GAE/mL,而添加乳酸菌组的样液中总多酚含量则有大幅度提高,较对照组提高了1.21倍,其总多酚含量为640.34 μg GAE/mL。总多酚含量的提升,可能是由于添加了乳酸菌后,使得果胶酶和纤维素酶的活性提高,有研究表明[28],此类酶会破坏酚-肽复合物,促使结合型酚类物质的释放。故添加乳酸菌可增加酱油中酚类物质的含量,从而改善酱油的功能活性。但总黄酮在发酵的第90天时,含量已经达到最大值35.21 μg RE/mL,而米曲霉组为17.89 μg RE/mL;在发酵结束的第120天时,添加乳酸菌组醪液中的总黄酮含量较米曲霉组提高了1.97倍。这说明添加了乳酸菌的双菌种酿造酱油可以提高酱油中总黄酮的含量。
酱油中DPPH自由基清除能力变化表现出不断上升的趋势,且前15 d增速较快,随后平稳增长。在发酵结束的第120天,米曲霉组的DPPH为9.27 μmol TE/mL,添加乳酸菌组酱油样液中DPPH自由基清除能力比米曲霉组提高了17.48%。
与DPPH不同,酱油酿造过程中的FRAP值则呈现出先增加后减少的趋势。在发酵后期,添加乳酸菌组酱油的FRAP值比米曲霉组提高了19.36%(21.89 μmol FE/mL)。所以,本研究的结果表明添加非耐盐乳酸菌与米曲霉共同制曲可以显著提高酱油的抗氧化能力。
2.6 酱油有机酸的含量分析
添加乳酸菌的酱油发酵中有机酸变化结果见表1。酱油中主要含有酒石酸、乳酸、乙酸、琥珀酸、柠檬酸和苹果酸6种有机酸。在酱油发酵过程中,乳酸和乙酸的含量表现出随时间增加而持续增加的趋势,而另外4种酸则呈先增加后减少的趋势。在发酵第120天,乳酸菌组与米曲霉组有机酸含量差异较小,在10%左右,说明非耐盐的乳酸菌在高盐的发酵阶段并未充分生长。
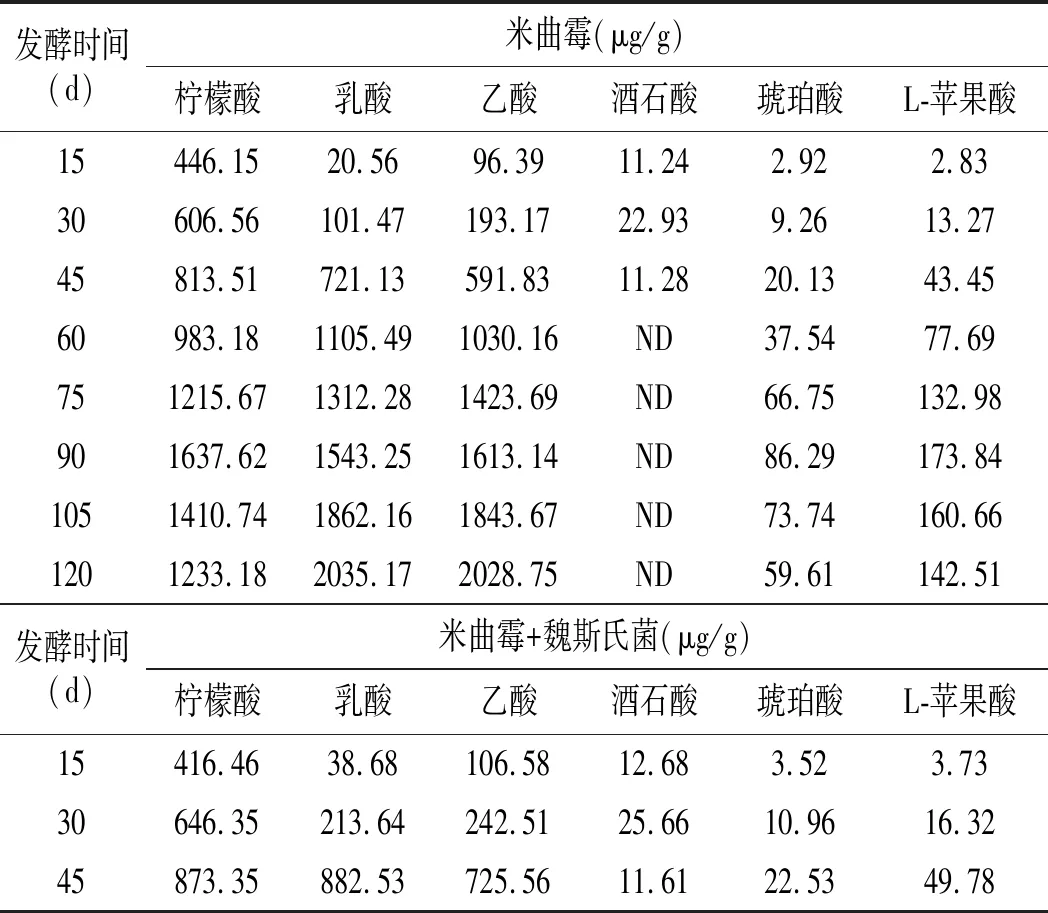
表1 酱油中主要有机酸的含量变化情况Table 1 Changes in the content of major organic acids in soy sauce
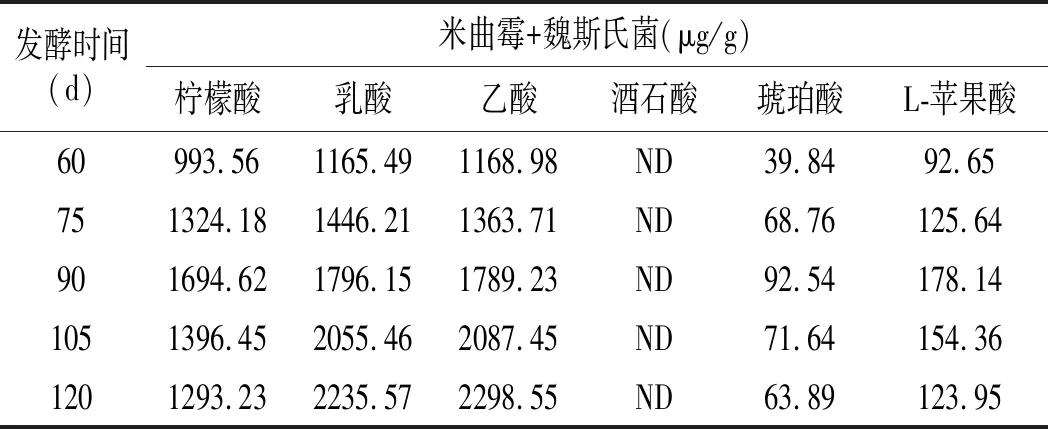
续 表
3 总结
制曲过程中酶系的丰富程度以及酶活力的大小直接决定后期酱油发酵过程中质量指标的好坏,最终影响酱油的品质。而以上结果均表明非耐盐乳酸菌和米曲霉共生制曲可有效改善酶系的丰富程度及活力大小。
在制曲过程中添加非耐盐乳酸菌后的酱油,不仅提高了酱油中酚类物质的含量及增强酱油的抗氧化活性,还增加了风味物质的种类和含量以及总游离氨基酸的含量,显著改善了酱油的风味。

