微波辅助低共熔溶剂提取桑葚果渣花青素的工艺研究
栾琳琳,卢红梅*,陈莉,吴煜樟
(1.贵州大学 酿酒与食品工程学院,贵阳 550025;2.贵州大学贵州省发酵工程 与生物制药重点实验室,贵阳 550025)
桑葚(mulberry)是桑科桑属(MorusalbaL.)多年生木本植物桑树的果实,又称桑椹、桑枣、桑果等,被国家卫生部列为首批药食同源植物,被誉为“21世纪最佳保健果品”[1],桑葚中的花青素是其主要的生物活性成分,具有丰富的营养和药用价值[2-5]。因此,从桑葚中提取花青素应用到食品及药品领域具有重要意义。传统花青素提取大都采用有机溶剂为提取剂,提取效率低,处理剂量大,且易污染环境,随着人们对环境保护意识的增强,使得绿色提取成为科研人员关注的焦点。
低共熔溶剂(DES)是继离子液体后的新一代绿色溶剂,由一定化学计量比的氢键受体和氢键供体组合而成的两组分或三组分低共熔混合物。低共熔溶剂具有挥发性低、不易燃、无毒、价格低廉、环境友好和易制备等优点而作为传统挥发性有机溶剂的替代溶剂[6]。Bakirtzi等[7]以乳酸基低共熔溶剂为提取介质,超声辅助提取希腊药用植物中的抗氧化多酚;Jeong 等[8]采用低共熔溶剂高效提取人参中的主要生物活性物质人参皂苷;Zeng等[9]首次以含水两相体系的低共熔溶剂(氯化胆碱-尿素)为介质研究用于提取牛血清白蛋白;李梅等[10]研究了利用低共熔溶剂从薏苡叶中提取总黄酮;倪玉娇等[11]以一系列低共熔溶剂为提取剂,采用超声波辅助法从沙棘籽粕中提取多酚。
目前,还没有关于低共熔溶剂提取花青素的文献报道。因此,本试验以桑葚加工副产物果渣为原料,应用微波辅助提取技术,研究不同低共熔溶剂对桑葚果渣花青素提取量的影响,并结合 Box-Behnken设计-响应面法对提取工艺进行优化,以期在最大限度下提取花青素,为桑葚花青素绿色、高效提取提供了新思路。
1 材料与方法
1.1 材料与仪器
桑葚果渣果汁加工副产物:贵州台今联合农业科技有限责任公司提供,-20 ℃冷冻保藏;氯化钾、乙酸钠:分析纯,成都金山化学试剂有限公司;盐酸:分析纯,重庆川东化工有限公司;无水乙醇、1,2-丙二醇、丙三醇:分析纯,天津市富宇精细化工有限公司;氯化胆碱:分析纯,上海源叶生物科技有限公司;葡萄糖、柠檬酸:分析纯,天津市永大化学试剂有限公司;草酸:分析纯,重庆茂业化学试剂有限公司;乳酸:分析纯,国药集团化学试剂有限公司。
ZD-2A型自动电位滴定仪 上海大普仪器有限公司;LD-3电动离心机 上海上登实验设备有限公司;101-1电热干燥箱 北京科伟永兴仪器有限公司;HH-b型数显恒温水浴锅 常州奥华仪器有限公司;FA2004N精密电子天平 上海菁海仪器有限公司;722S可见分光光度计 上海菁华科技仪器有限公司;XTP-200型高速多功能粉碎机 浙江永康市红太阳机电有限公司;XH-100A微波催化合成/萃取仪 北京祥鸽科技发展有限公司。
1.2 试验方法
1.2.1 原料预处理
取冷冻保藏的桑葚果渣于50 ℃烘箱中烘干,用粉碎机粉碎成粉末,过60~80 目筛,将其装入保鲜袋于-20 ℃避光保存备用。
1.2.2 低共熔溶剂制备
参考尚宪超等[12]的方法,低共熔溶剂由氯化胆碱与不同氢键供体(草酸、1,2-丙二醇、丙三醇、乳酸、柠檬酸、葡萄糖)按一定摩尔比混合放置于圆底烧瓶中,80 ℃恒温水浴一定时间,直至得到无色透明液体,冷却至室温后,制得低共熔溶剂。
1.2.3 提取方法
准确称取0.5 g桑葚果渣粉末于提取器中,加入一定量低共熔溶剂,混匀,一定条件下微波提取,提取液转移至离心管内,4000 r/min离心10 min,上清液即为桑葚果渣花青素粗提液。
1.2.4 单因素试验
称取0.5 g桑葚果渣粉末,分别在低共熔溶剂类型(DES-1、DES-2、DES-3、DES-4、DES-5、DES-6)、加水量(0%、20%、30%、40%、50%)、料液比(1∶20、1∶30、1∶40、1∶50、1∶60,g/mL)、微波功率(400,500,600,700,800 W)、微波温度(30,40,50,60,70 ℃)、微波时间(30,40,50,60,70 s)条件下进行单因素试验。
1.2.5 响应面优化试验
通过单因素试验的结果,以花青素提取量为考察指标,依据Box-Behnken设计原理,选择微波功率、微波温度和微波时间进行三因素三水平响应面试验,确定最优工艺参数见表1。

表1 响应面试验因素水平设计Table 1 Factors and levels of response surface experiment
1.2.6 花青素含量的测定
1.2.6.1 pH 1.0缓冲液的配制
准确称取3.725 g KCl用蒸馏水稀释并定容至250 mL;准确量取4.25 mL浓盐酸用蒸馏水定容至250 mL,将KCl溶液与HCl溶液以25∶67比例混合。用KCl溶液调pH为1.0±0.1。
1.2.6.2 pH 4.5缓冲液的配制
准确称取4.1 g CH3COONa用蒸馏水稀释并定容至250 mL,用HCl溶液调pH为4.5±0.1。
1.2.6.3 测定方法
测定过程根据Aramwit等[13]的方法稍作改动:取2.5 mL提取液,用蒸馏水定容至25 mL。移取2.5 mL样液2份,分别用pH 1.0和pH 4.5缓冲液定容至25 mL,40 ℃水浴平衡30 min,以蒸馏水代替样品做空白对照,在510 nm和700 nm处测定吸光度。
花青素含量的计算如下:
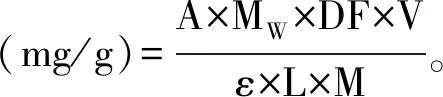
式中:A=(A510 nm-A700 nm)pH 1.0-(A510 nm-A700 nm)pH 4.5;MW为矢车菊素-3-葡萄糖苷分子量,449.2 g/mol;DF为稀释倍数;V为提取液体积,mL;ε为摩尔消光系数,26900 L/(mol·cm);L为光程,1 cm;M为原料质量,g。
1.3 数据处理与分析
采用Origin 8.6和Design-Expert V8.0.6等软件对试验数据进行处理,每个处理组进行3次平行试验。
2 结果与分析
2.1 单因素试验
2.1.1 低共熔溶剂种类对花青素提取量的影响
在固定摩尔比1∶1、料液比1∶50(g/mL)、微波功率700 W、微波温度50 ℃、微波时间40 s的条件下,考察不同低共熔溶剂种类对花青素提取量的影响,结果见图1。
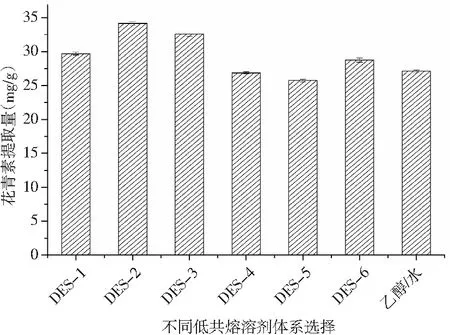
图1 提取剂对花青素提取量的影响Fig.1 Effect of extractants on yield of anthocyanins
由图1可知,6种低共熔溶剂对花青素的提取量依次为DES-2(氯化胆碱/1,2-丙二醇)>DES-3(氯化胆碱/丙三醇)>DES-1(氯化胆碱/草酸)>DES-6(氯化胆碱/葡萄糖)>DES-4(氯化胆碱/乳酸)>DES-5(氯化胆碱/柠檬酸)。其中,DES-2(氯化胆碱/1,2-丙二醇)对桑葚花青素提取量最高,达到34.17 mg/g,而DES-5(氯化胆碱/柠檬酸)对花青素提取量最低,仅有25.74 mg/g。同时,比较DES与有机溶剂(乙醇)对桑葚花青素提取量的影响,由结果可知,DES-2对桑葚花青素的提取优于传统有机溶剂。DES能提高花青素的提取量可能是由于DES的扩散力、溶解度和极性等有利于花青素的溶出[14],DES-2的极性与桑葚花青素的极性最为相近,能更好地与花青素分子接触,因此,选择DES-2作为桑葚花青素提取剂。
2.1.2 不同摩尔比例对花青素提取量的影响
在料液比1∶50(g/mL)、微波功率700 W、微波温度50 ℃、微波时间40 s的条件下,以DES-2为提取剂,含水量为40%,考察不同摩尔比例对花青素提取量的影响,结果见图2。
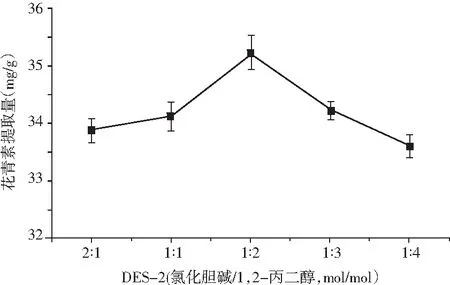
图2 摩尔比对花青素提取量的影响Fig.2 Effect of molar ratio on yield of anthocyanins
由图2可知,当DES-2摩尔比由2∶1增大到时,花青素提取量明显升高,这可能是由于随着1,2-丙二醇量增加使DES粘度降低,扩散力增强,有利于花青素溶出[15]。而随着摩尔比继续增大,花青素提取量则降低,这是由于1,2-丙二醇量增加,DES极性变小,与桑葚花青素极性差距拉大,使得花青素提取量降低,因此,选择DES-2摩尔比为1∶2。
2.1.3 加水量对花青素提取量的影响
DES具有较高的粘性,扩散力较低,难以渗入基质内部,因此需要添加一定量的水以降低DES的粘度[16]。在料液比1∶50(g/mL)、微波功率700 W、微波温度50 ℃、微波时间40 s的条件下,以摩尔比1∶2的DES-2为提取剂,考察加水量对花青素提取量的影响,结果见图3。
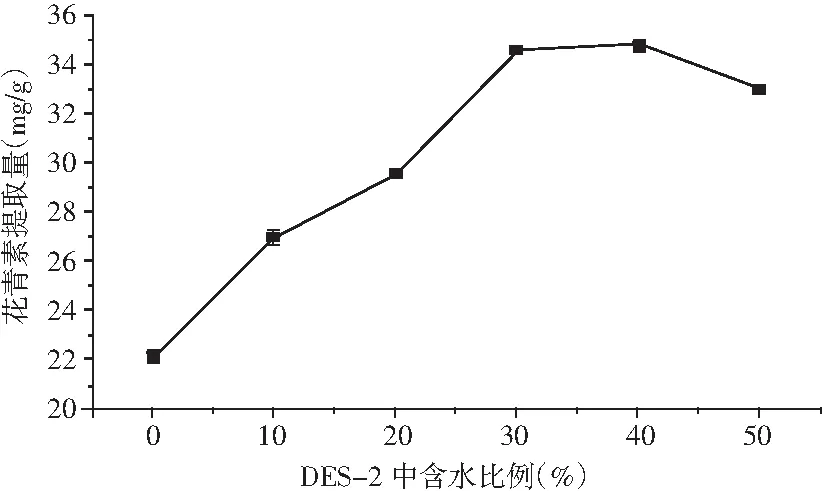
图3 低共熔溶剂(DES-2)的含水量对花青素提取量的影响Fig.3 Effect of water content in DES-2 on yield of anthocyanins
由图3可知,随着DES-2中加水量的增加,花青素提取量逐渐增加。当加水量达到30%~40%时,花青素提取量达到最大;随着加水量继续增加,花青素提取量降低。这可能是由于DES与花青素之间是氢键作用力,随着加水量的增加,减弱了这种作用力,使得花青素提取量降低[17]。因此,选择DES-2的加水量为30%~40%。
2.1.4 料液比对花青素提取量的影响
在微波功率700 W、微波温度50 ℃、微波时间40 s的条件下,以摩尔比1∶2的DES-2(含水量40%)为提取剂,考察料液比对花青素提取量的影响,结果见图4。
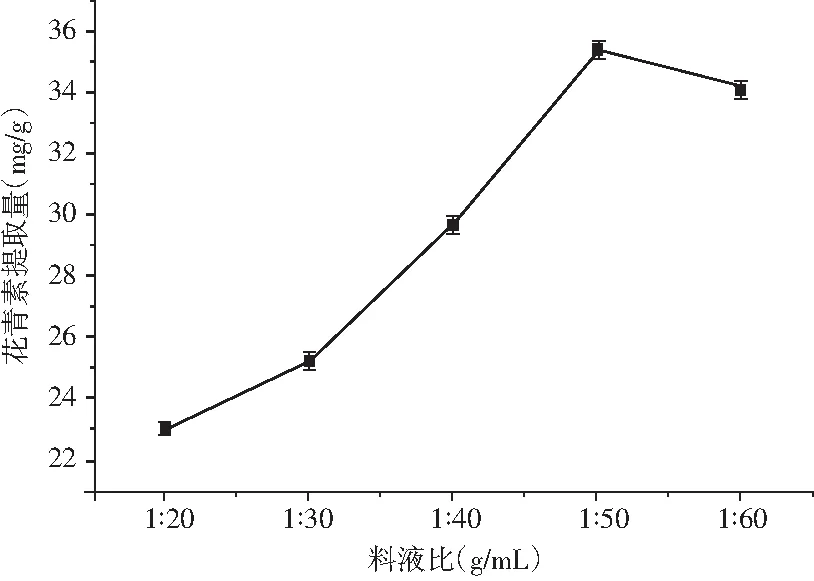
图4 料液比对花青素提取量的影响Fig.4 Effect of solid-to-liquid ratio on yield of anthocyanins
由图4可知,随着料液比的增大,花青素提取量逐渐增加。当料液比达到1∶50时花青素提取量达到最大;随着料液比继续增大,花青素提取量降低。其原因可能是随着料液比增大,桑葚细胞内外浓度差增大,有利于桑葚花青素溶出;而当料液比达到1∶60后,花青素提取量变化不大,可能是花青素溶出至饱和,没有更多花青素分离出[18]。因此,微波辅助低共熔溶剂提取花青素的最佳料液比为1∶50。
2.1.5 微波功率对花青素提取量的影响
在料液比1∶50、微波温度50 ℃、微波时间40 s的条件下,以摩尔比1∶2的DES-2(含水量40%)为提取剂,考察微波功率对花青素提取量的影响,结果见图5。
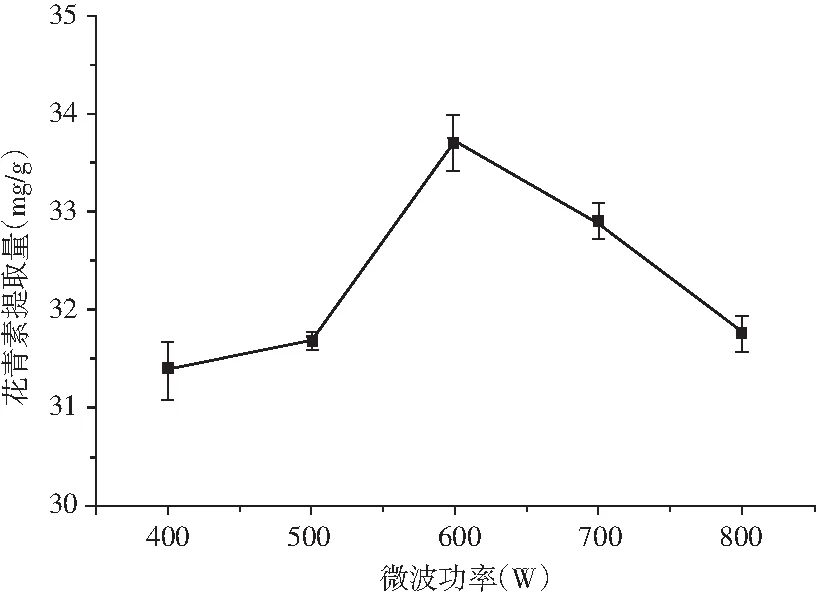
图5 微波功率对花青素提取量的影响Fig.5 Effect of microwave power on yield of anthocyanins
由图5可知,花青素提取量随着微波功率的增大呈先上升后下降的趋势。在微波功率小于600 W时,桑葚花青素提取量随着微波功率增大而提高,当微波功率达到600 W时花青素提取量达到最大;当微波功率大于600 W时,花青素提取量降低。其原因可能是微波的辐射作用穿透桑葚细胞,使得细胞壁破裂,有利于桑葚花青素的溶出,当微波功率过大时,产生剧烈震动,使得花青素降解,提取量降低[19]。因此,微波辅助低共熔溶剂提取花青素最适功率为600 W。
2.1.6 微波温度对花青素提取量的影响
在料液比1∶50、微波功率600 W、微波时间40 s的条件下,以摩尔比1∶2的DES-2(含水量40%)为提取剂,考察微波温度对花青素提取量的影响,结果见图6。
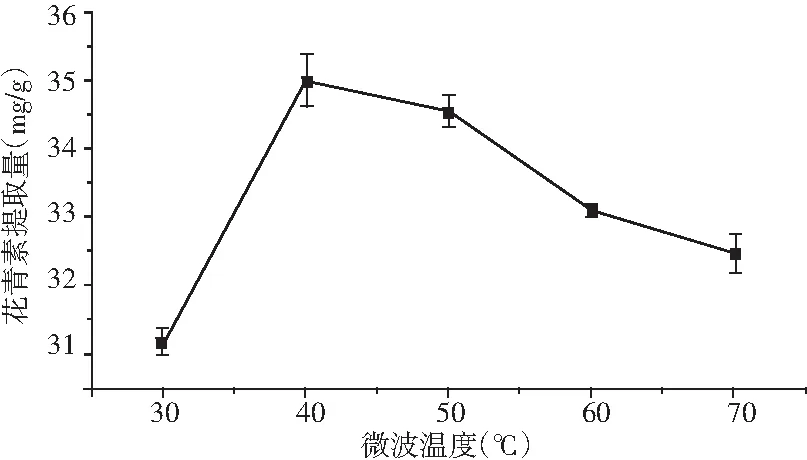
图6 微波温度对花青素提取量的影响Fig.6 Effect of microwave temperature on yield of anthocyanins
由图6可知,桑葚花青素提取量随着提取温度的升高而增大,温度升至40 ℃时,桑葚花青素提取量最高;随着温度进一步升高,桑葚花青素提取量开始下降。其原因可能是随着温度的升高,桑葚果渣粉在溶剂中的溶解和扩散能力增加,有利于花青素的溶出[20];当提取温度过高时,高温导致热敏性的花青素降解,花青素提取量下降。因此,微波辅助低共熔溶剂提取花青素的最适温度为40 ℃。
2.1.7 微波时间对花青素提取量的影响
在料液比1∶50、微波功率600 W、微波温度40 ℃的条件下,以摩尔比1∶2的DES-2(含水量40%)为提取剂,考察微波时间对花青素提取量的影响,结果见图7。
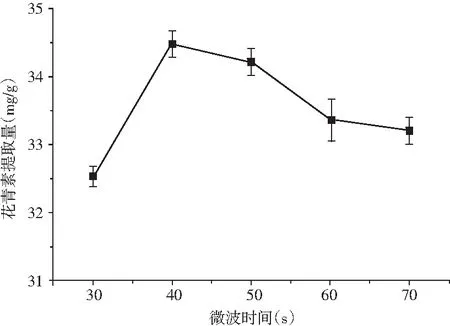
图7 微波时间对花青素提取量的影响Fig.7 Effect of microwave time on yield of anthocyanins
由图7可知,随着提取时间的延长,花青素提取量逐渐增加。当提取时间为40 s时,花青素提取量达到最大;随着提取时间继续延长,花青素提取量降低。其原因可能是随着提取时间延长,花青素不断溶出;而提取时间过长,导致花青素降解。因此,微波辅助低共熔溶剂提取花青素的最佳时间为40 s。
2.2 响应面优化试验
2.2.1 响应面试验结果及方差分析
微波辅助低共熔溶剂提取花青素响应面试验结果见表2,方差分析结果见表3。
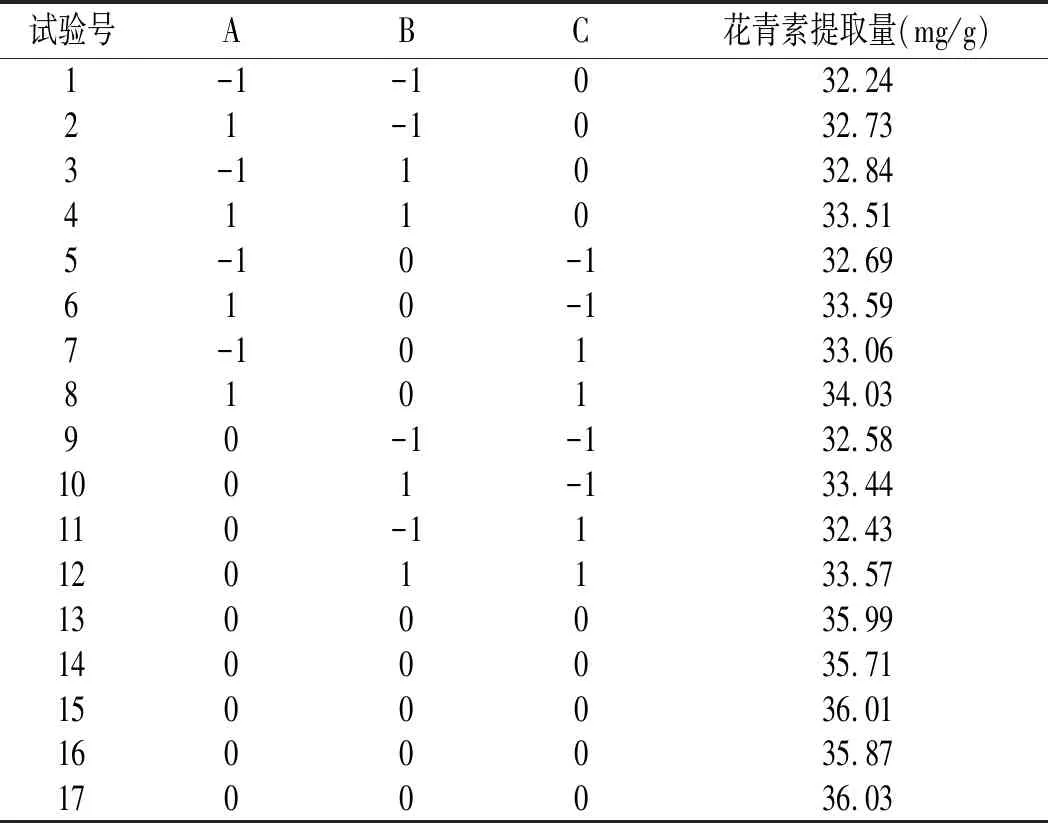
表2 响应面设计方案及结果Table 2 Design and results of response surface experiment
采用Design-Expert V8.0.6软件对数据进行回归分析,得到回归方程的方差分析表(见表2),进行非线性回归二次多项式拟合,得到二次回归方程:
Y=-62.07+0.17A+1.40B+0.93C-0.02B2-0.01C2。
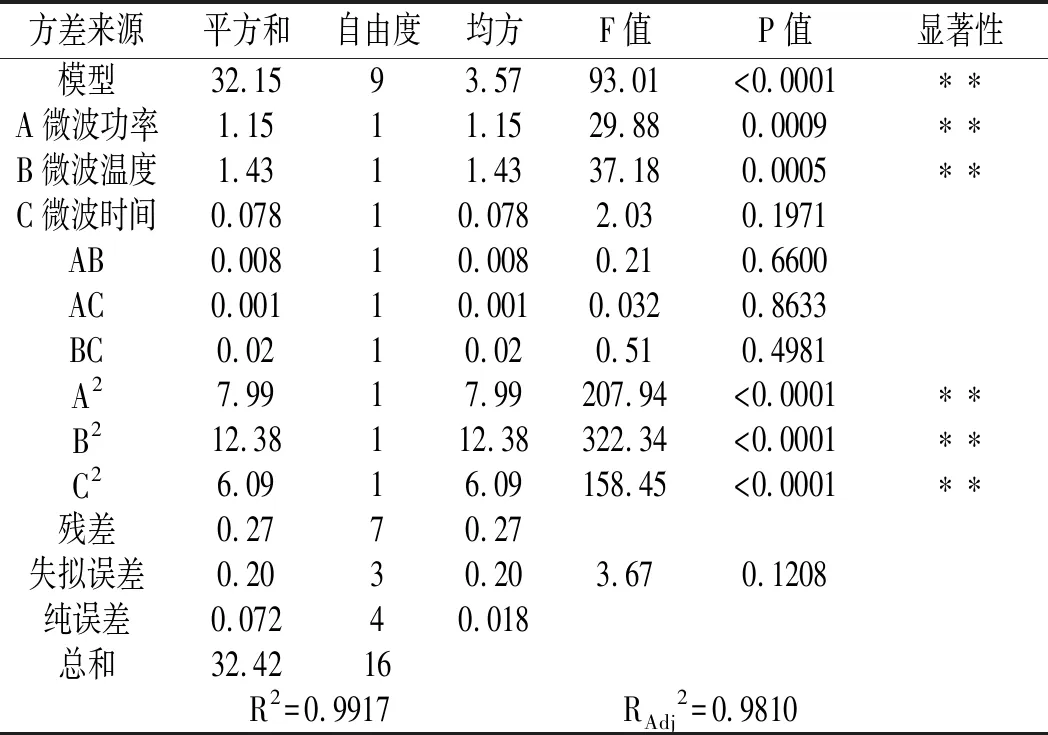
表3 回归方程的方差分析Table 3 Analysis of variance of regression equation
注:“*”代表0.05显著水平;“**”代表0.01显著水平。
由表3可知,回归方差分析显著性检验表明,回归模型极显著(P<0.0001),失拟项不显著(P=0.1208>0.05),说明建立的模型是可靠的。相关系数R2=0.9917,表明响应变量与响应值的线性关系显著,模型拟合度较好,可用来预测桑葚花青素的提取量。
由方差分析结果可知,一次项A,B极显著(P<0.001),交互项AB、AC、BC均不显著(P>0.05),A2、B2、C2均极显著(P<0.0001),说明响应变量与响应值之间不是简单的线性关系。各响应变量对桑葚花青素提取量影响大小顺序为:微波温度>微波功率>微波时间。
2.2.2 响应面分析
以响应曲面和等高线图可以直观地看出各因素间的交互作用对花青素提取量的影响,交互作用图和等高线图见图8。
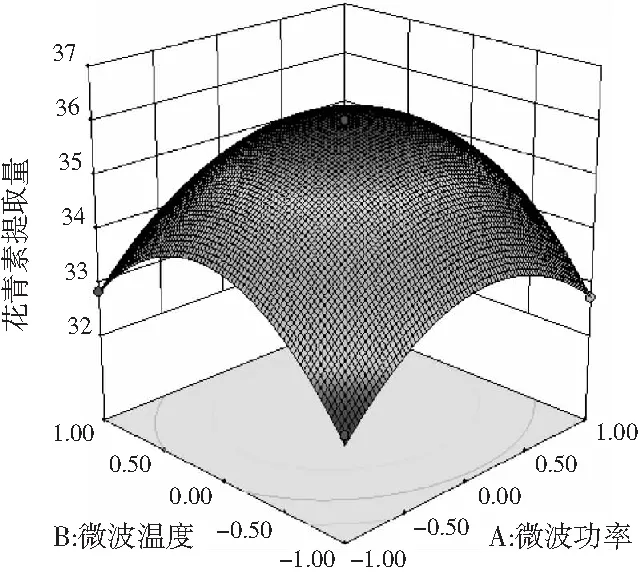
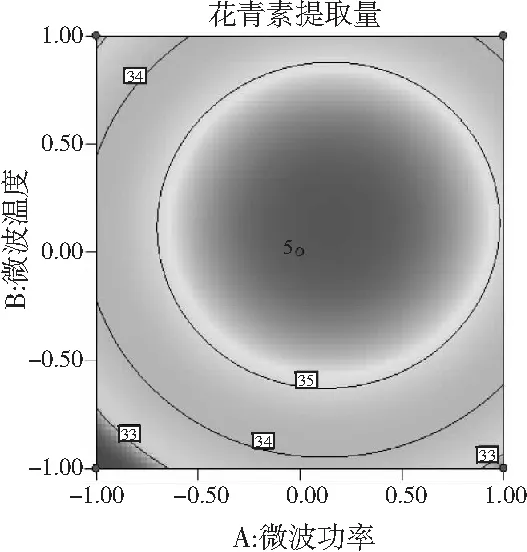
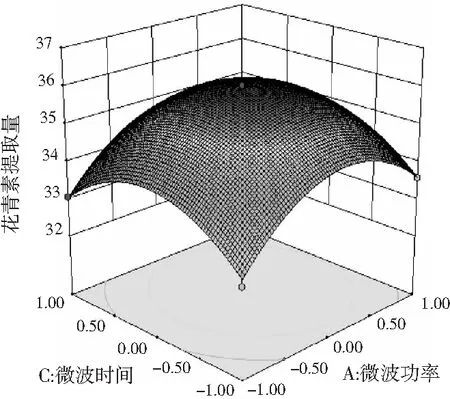
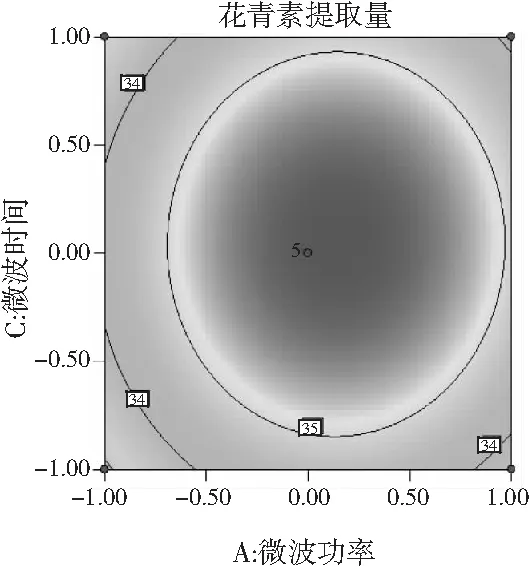
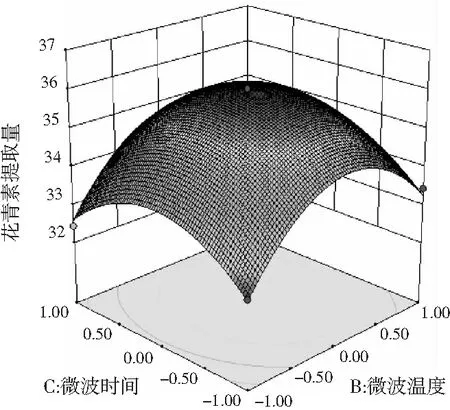
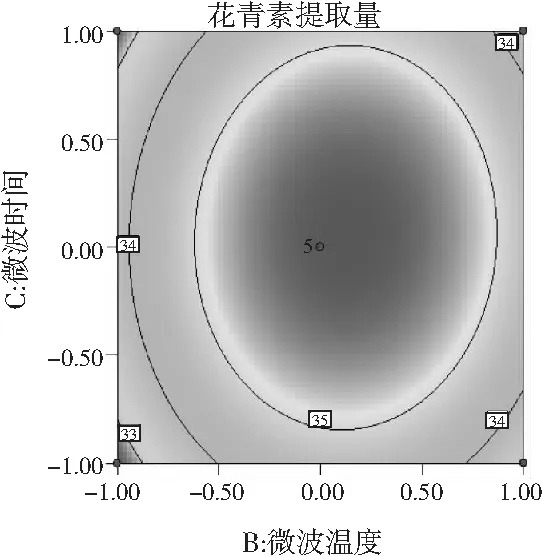
图8 两因素交互作用对花青素提取量影响的 响应面和等高线图Fig.8 Response surface and contour plots of the effect of interaction of two factors on the yield of anthocyanins
在响应面图中,曲面越陡,说明两因素交互作用越显著;等高线的形状可反映出交互作用的强弱,椭圆形表示两因素交互作用显著,而圆形则与之相反。由可知,微波功率(A)与微波温度(B)、微波功率(A)与微波时间(C)及微波温度(B)与微波时间(C)三组交互作用的等高线不密集,接近圆形,因此,交互作用AB、AC、BC对桑葚花青素提取量影响不显著。
2.2.3 验证试验
根据Box-Behnken试验得到结果和回归方程,预测试验范围内桑葚果渣花青素的提取最佳工艺条件为:微波功率614.05 W,微波温度41.26 ℃,微波时间 40.46 s,在此条件下花青素提取量为36.05 mg/g。考虑到仪器的参数限制、试验的可操作性及成本等,将最优工艺条件修正为:微波功率600 W,微波温度40 ℃,微波时间40 s,在此条件下,花青素提取量的试验验证值为35.97 mg/g,与理论值接近,说明本研究优化得到的桑葚果渣花青素提取工艺参数是可靠的,可拟合实际提取。
3 结论
本研究以桑葚果渣粉为原料,利用新型绿色的低共熔溶剂作为提取溶剂,以微波辅助手段对桑葚果渣中花青素进行高效快速提取。发现由氯化胆碱/1,2-丙二醇(摩尔比1∶2,含水量40%)组成的溶剂最适合花青素提取,比传统乙醇提取法提取含量更高,且环保节能,可用于花青素类物质的提取,且为其他生物活性物质的提取提供了新思路。然而关于低共熔溶剂的后续分离问题还有待进一步探讨,或可很据产物的应用属性,选择合适的低共熔溶剂,将提取液作为产品直接应用。

