藏悠游胶囊安全性毒理学评价及提高缺氧耐受力功能研究
张 娟,李水仙,王春芳,赵 岩,祝清芬
(山东省食品药品检验研究院,山东 济南 250101)
藏悠游胶囊是以葛根冻干粉、桔梗提取物、茯苓提取物、川芎提取物为主要原料制成的保健食品。《神农本草经》云:葛根“主消渴,身大热,呕吐,诸痹,起阴气,解诸毒”[1]。《中国药典》一部:桔梗止咳祛痰,用于痰浊阻肺所致的咳嗽痰多[2]。《世补斋医书》中记载:“茯苓一味,为治痰主药。痰之本,水也,茯苓可以行水;痰之动,湿也,茯苓又可以行湿”。《本草汇言》曰:“川芎,上行头目,下调经水,中开郁结,血中气药。味辛性阳,气善走窜而无阴凝黏滞之态。虽入血分,又能去一切风,调一切气”[1]。本研究按照《食品安全性毒理学评价程序》GB15193.1-2014的要求及其药理活性,对藏悠游胶囊进行安全性毒理学评价及提高缺氧耐受力功能研究,为其作为保健食品的食用安全性及功效提供实验依据。
1 仪器与试药
1.1 仪器
BP 211D电子天平(德国Sartorius公司);高压蒸汽灭菌器(日本SANYO公司);隔水式恒温培养箱,Stuart温控摇床培养箱(英国Stuart公司);BSC-1360ⅡA2生物安全柜(北京中联哈尔);AL204电子天平(Mettler);全自动生化分析仪(日立);ADVIA®2120i血液分析仪(西门子);ASP200s全自动全封闭脱水机,EG1150 H & C 包埋机,RM2245半自动轮转式切片机,HI1210摊片机,HI1220烤片机,XL全自动染色机,CV5030 全自动封片机(Leica);BX51生物显微镜(Olympus)。
1.2 受试物
藏悠游胶囊,规格:360 mg/粒,36粒/瓶,内容物为棕黄色,由某保健品有限公司生产。食用量为每日3次,每次3粒(360 mg/粒);保存条件:置阴凉干燥处,避免阳光直照。
1.3 试剂
哺乳动物微粒体酶(S9),批号:3516,诱导剂及动物品种:多氯联苯(Aroclor 1254)诱导雄性SD大鼠(上海宝录);敌克松(Dexon,批号:10112926,上海晶纯);注射用丝裂霉素(MMC,批号:131101,浙江海正药业);2-氨基芴(批号:13152,上海晶纯);1, 8-二羟基蒽醌(批号:WXBB7902V,美国Sigma-Aldrich公司);环磷酰胺(批号:SLBG4216V,美国Sigma-Aldrich公司);钠石灰[批号:20031220,中国医药(集团)上海化学试剂公司];亚硝酸钠(批号:C1305006,阿拉丁公司)。
1.4 试验动物及菌株
SPF级ICR小鼠,SPF级SD大鼠,均购自济南朋悦实验动物繁育有限公司,实验动物生产许可证号:SCXK(鲁)2014 0007。饲养条件:SPF级动物实验室,实验室使用许可证号:SYXK(鲁)2018 0013。温度:20~25 ℃,日温差≤3 ℃,湿度:40 %~70 %,换气次数:≥10次/h。照明时间:12 h 明暗交替。SPF大小鼠生长繁殖饲料(北京科澳协力饲料有限公司),饲料生产许可证号:京饲证(2014)06054;实验动物(饲料)生产许可证号:SCXK(京)2014-0010。鼠伤寒沙门菌TA97a,TA98,TA100,TA102(上海宝录)。
2 方法
2.1 急性毒性试验
小鼠检疫合格后,取试验用小鼠20只,雌雄各半,体重,雄性20.0~22.0 g,雌性18.8~21.4 g。采用最大耐受剂量(MTD)法进行试验。禁食不禁水16 h后,称取样品粉末25.0 g,充分研磨,加0.5 %羧甲基纤维素钠溶液至25 ml,制成1.0 g/ml的混悬液,经口灌胃给予浓度为1.0 g/ml的受试物20 ml/kg BW。连续观察14 d,记录动物的中毒表现及死亡情况,试验结束后进行剖检并记录大体解剖结果。根据急性毒性剂量分级标准评价受试物的急性毒性强弱。
2.2 Ames试验
实验采用平板掺入法。受试物分为5000,1000,200,40,8 μg/皿5个剂量组。称取1.25 g藏悠游胶囊内容物,加灭菌注射用水至25 ml,混匀,制成5 %的混悬液(高剂量),0.103 MPa条件下灭菌20 min。将冷冻保存的试验菌株TA97a,TA98,TA100,TA102分别接种于营养肉汤培养基10 ml,37 ℃振荡(100次/min)培养10 h。将含0.5 mmol/L组氨酸-0.5 mmol/L生物素的顶层培养基2.0 ml分装于试管中,50 ℃水浴中保温,然后每管依次加入试验菌株增菌液0.1 ml,受试物溶液0.1 ml和S9混合液0.5 ml(需代谢活化时),充分混匀,迅速倾倒于底层琼脂平板上,转动平板,使之分布均匀。水平放置,待冷凝固化后,倒置于37 ℃培养箱里孵育48 h,计数每皿回变菌落数。在加与不加S9混合液的条件下,受试物每个剂量均做3个平行板,同时设空白对照组(自发回变组)、溶媒对照组(灭菌注射用水)和阳性对照组。
2.3 小鼠骨髓细胞微核试验
取试验用小鼠50只,雄性小鼠25.1~28.1 g,雌性小鼠25.0~28.7 g,随机区组法分为5组,每组10只,雌雄各半。试验设置受试物低、中、高剂量(2.5,5,10 g/kg BW)组、溶媒(0.5 %羧甲基纤维素钠溶液)对照组和阳性(环磷酰胺40 mg/kg BW)对照组,各组小鼠均经口灌胃给予,采用30 h两次给予法,即两次给予间隔24 h,第二次给予后6 h取材。首次给予时称量动物体重并记录。颈椎脱臼法处死小鼠,取胸骨,用止血钳挤出骨髓液与载玻片一端的胎牛血清混匀,常规涂片。空气干燥后,用甲醇固定10 min,将固定好的涂片放入Giemsa应用液中,染色10 min,用水轻轻冲洗,晾干。光学显微镜下,观察200个嗜多染红细胞(PCE),同时计数正染红细胞(NCE),计算PCE/NCE比值,每只动物计数1000个嗜多染红细胞。观察含有微核的嗜多染红细胞数,微核率以千分率表示。
2.4 小鼠精子畸形试验
取试验用小鼠25只,雄性,体重25.3~28.0 g,随机区组法分为5组,每组5只。试验设置受试物低、中、高剂量(2.5,5,10 g/kg BW)组、溶媒(0.5 %羧甲基纤维素钠溶液)对照组和阳性(环磷酰胺40 mg/kg BW)对照组。首次给予受试物后的第35天,颈椎脱臼法处死小鼠,取出两侧附睾,放入盛有约1 ml生理盐水的小烧杯中,用眼科剪纵向剪1~2刀,静止5 min,轻轻摇动。用4层擦镜纸过滤,滤液涂片。空气干燥后,用甲醇固定5 min,晾干后用1 %伊红染色1 h,用水轻轻冲洗,干燥。在低倍镜下找到背景清晰、精子重叠较少的部位,用高倍镜检查精子的形态。精子畸形按无钩、香蕉形、胖头、无定形、双头、双尾、尾折叠进行记录。每只动物检查1000个精子。记录畸变的类型和数量,计算精子畸形率。
2.5 30 d喂养试验
动物检疫合格后,取SD大鼠80只,雄性体重68.8~84.3 g、雌性体重65.1~79.6 g,雌雄分别随机分为4组,每组20只,雌雄各半。设低、中、高3个剂量组,剂量分别为1.35,2.7,5.4 g/kg BW(分别相当于人可能摄入量的25倍、50倍、100倍),大鼠掺入饲料量按10 g/100g BW计,掺入比例分别为1.35 %,2.7 %,5.4 %。采用逐级放大法将受试物掺入饲料中,见表1。对照组动物给予普通饲料。单笼饲养,自由饮食,连续喂养30 d。每周称一次体重和两次摄食量,计算每周及总的食物利用率。第31天在禁食16 h后,称取禁食动物体重(空腹体重)后,戊巴比妥钠麻醉,经腹主动脉取血,进行血常规和血液生化测定,解剖动物并取材进行病理检查。
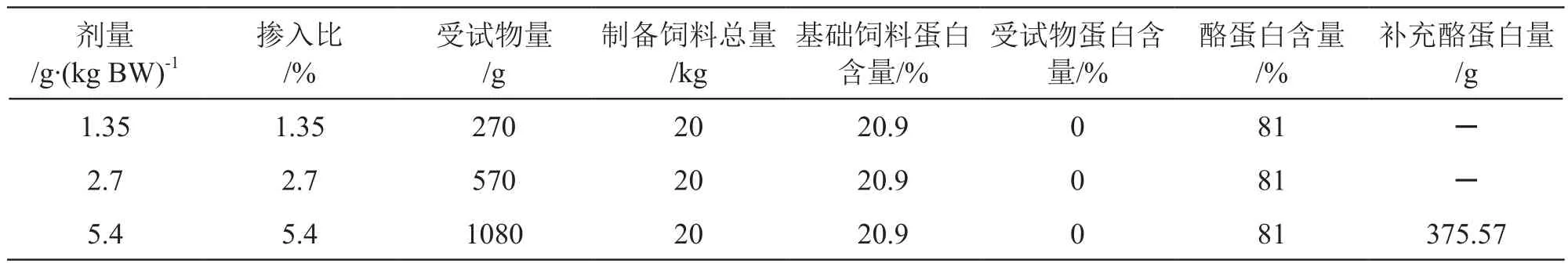
表1 受试物掺入饲料法饲料制备表
2.6 提高缺氧耐受力功能试验
2.6.1 分组及受试物给予方式 取小鼠120只,雄性,体重18~22 g,按体重随机分为3组,分别进行常压耐缺氧实验、亚硝酸钠中毒存活实验、急性脑缺血性缺氧实验。每组40只,各分为溶媒对照组和受试物低、中、高剂量组,每组10只。低、中、高剂量分别为270,540,1620 mg/kg BW,相当于人体推荐量的5倍、10倍、30倍,用0.5 %的羧甲基纤维素钠溶液配制受试物。灌胃体积20 ml/kg BW,低、中、高剂量组的受试物浓度分别为13.5,81 mg/ml。同时设溶媒对照组,灌胃给予同等体积的0.5 %羧甲基纤维素钠溶液。每天灌胃1次,连续给予30 d后,开始测定各项缺氧指标。
2.6.2 常压耐缺氧实验 末次灌胃后1 h,将各组小鼠分别放入盛有5 g钠石灰的250 ml磨口瓶内,每瓶1只,用凡士林封瓶口,盖严,使之不漏气,立即计时,以呼吸停止为指标,观察小鼠因缺氧而死亡的时间。
2.6.3 亚硝酸钠中毒存活实验 末次灌胃后1 h,各组小鼠腹腔注射240 mg/kg BW的亚硝酸钠,注射剂量0.1 ml/10 g BW,立即计时,记录动物存活时间。
2.6.4 急性脑缺血性缺氧实验 末次灌胃后1 h,各组小鼠自颈部逐只断头,立即按秒表记录小鼠断头后至张口喘气停止时间。
2.7 数据统计处理[4]
数据采用SPSS19.0统计软件进行分析,以±s表示,微核率和精子畸形率使用χ2检验进行分析,其他各指标均使用单因素方差分析(ANOVA)进行分析。
3 结果与分析
3.1 急性毒性试验结果
小鼠一日内经口灌胃给予受试物20.0 g/kg BW,结果显示,小鼠饮食活动正常,生长良好,未见明显中毒表现及死亡情况,大体剖解未见明显的异常表现,该受试物对两种性别小鼠的MTD均大于20.0 g/kg BW。根据急性毒性分级标准,该受试物属无毒级保健食品,结果见表2。

表2 藏悠游胶囊小鼠急性毒性试验结果
3.2 Ames试验结果
两次试验中受试物各剂量组在加和不加S9条件下各菌株回变菌落数均未超过自发回变菌落数的2倍,各剂量组间亦无剂量反应关系,表明在加与不加S9条件下,受试物对鼠伤寒沙门氏菌TA97a、TA98、TA100、TA102 4株菌株均未出现遗传毒性。结果见表3、表4。
3.3 骨髓微核试验结果
受试物各剂量组PCE/NCE比值不少于溶媒对照组的20 %,表明受试物对小鼠骨髓细胞未见明显毒性。受试物各剂量组微核率与溶媒对照组比较差异无统计学意义(P>0.05),环磷酰胺阳性对照组与溶媒对照组比较差异有统计学意义(P<0.01),表明受试物无致小鼠骨髓嗜多染红细胞微核作用,小鼠骨髓微核试验结果为阴性,结果见表5。
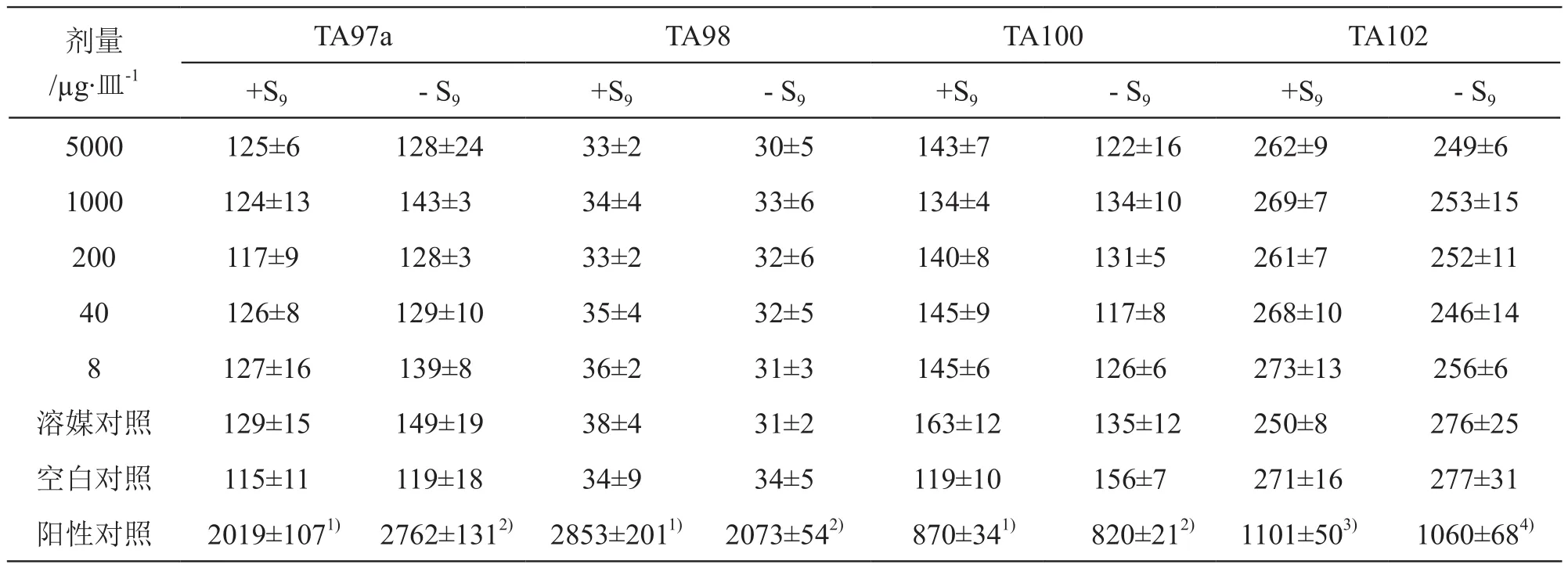
表3 Ames试验结果(第1次试验)

表4 Ames试验结果(第2次试验)

表5 小鼠骨髓细胞微核试验结果
3.4 小鼠精子畸形试验结果
受试物各剂量组小鼠精子畸形率与溶媒对照组比较差异无统计学意义(P>0.05),环磷酰胺阳性对照组与溶媒对照组比较差异有统计学意义(P<0.01)。结果表明,受试物对小鼠精子畸形试验结果为阴性,结果见表6。
3.5 30 d喂养试验结果
3.5.1 对大鼠体重、摄食量及食物利用率的影响
3.5.1.1 对大鼠体重的影响 雌性动物高剂量组第3周和第4周体重、体重增重、总增重低于对照组,差异有统计学意义(P<0.01,P<0.05),结果见表7,表8。

表8 藏悠游胶囊对大鼠每周增重及总增重的影响(n=10)
3.5.1.2 对大鼠摄食量的影响 受试物各剂量组大鼠给药期间各周摄食量与对照组差异均无统计学意义(P>0.05)。结果表明,受试物对大鼠各周摄食量无影响。结果见表9。
3.5.1.3 对大鼠食物利用率的影响 雄性动物高剂量组第4周食物利用率和总食物利用率低于对照组,差异有统计学意义(P<0.05)。雌性动物中剂量组第3周食物利用率和总食物利用率,高剂量组第3周和第4周食物利用率、总食物利用率低于对照组,差异有统计学意义(P<0.01,P<0.05),结果见表10。
受试物对动物体重和食物利用率的影响可能与受试物主要成分的功效有关,本品主要成分为葛根提取物、桔梗提取物、茯苓提取物、川芎提取物,据文献报道葛根具有降血脂的作用[5],桔梗具有降血脂和抗肥胖的作用[6-7],茯苓具有利尿作用[8-9]。
3.5.2 对大鼠血液学指标的影响 与对照组比较,雄性动物低剂量组中性粒细胞百分比升高,淋巴细胞百分比降低,差异有统计学意义(P<0.01),但上述检测指标均在正常值范围内,不认为存在生物学意义。其他各剂量组动物各血液生化学指标与对照组比较差异均无统计学意义(P>0.05)。结果见表11。
3.5.3 对大鼠血清生化学指标的影响 雄性动物中剂量组总蛋白、血清白蛋白高于对照组,差异有统计学意义(P<0.05);雌性动物低剂量组谷草转氨酶高于对照组,差异有统计学意义(P<0.05),但均在正常值范围内,不认为存在生物学意义。其他各剂量组各血清生化指标与对照组差异均无统计学意义(P>0.05)。结果见表12。
3.5.4 病理学大体解剖观察检查 各剂量组大鼠肝脏、肾脏、脾脏、胃肠、睾丸和卵巢大体解剖检查均未见异常,各脏器组织病理学检查未发现与受试物相关的组织病理学改变。雌雄动物各剂量组脏器湿重及脏器系数与对照组比较,差异均无统计学意义(P>0.05)。结果见表13、表14。
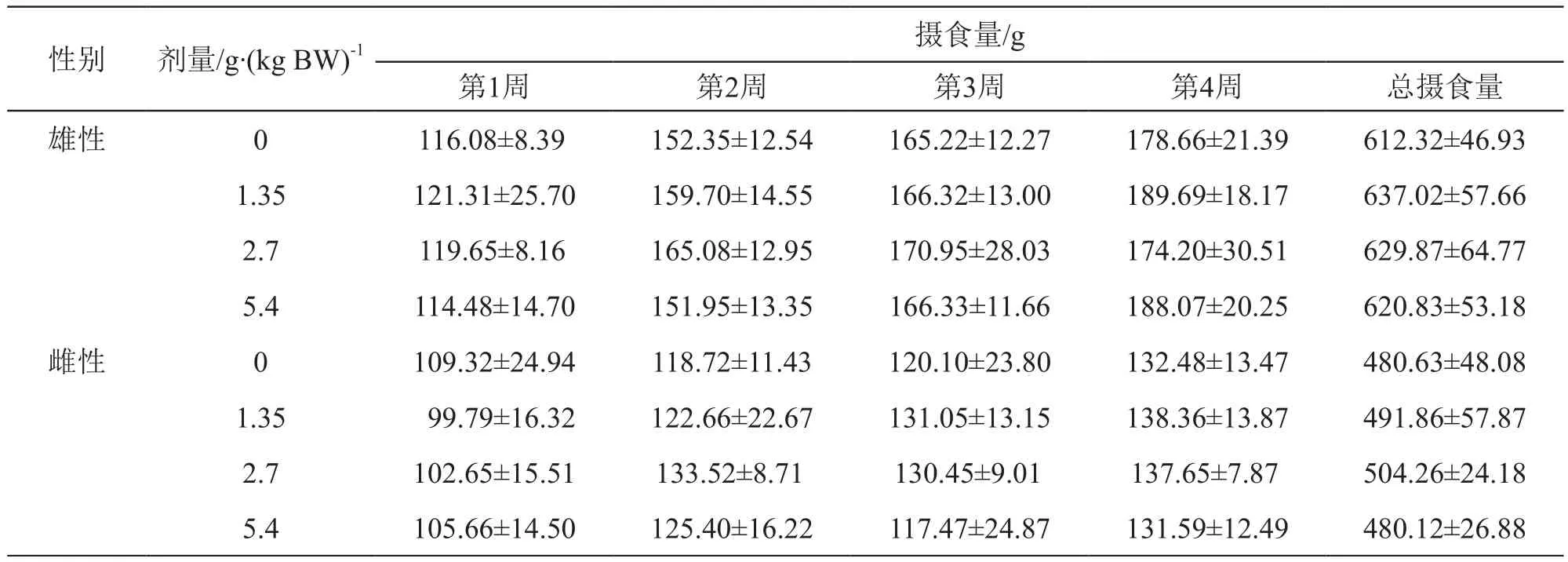
表9 藏悠游胶囊对大鼠每周摄食量的影响(n=10)

表10 藏悠游胶囊对大鼠每周及总的食物利用率的影响(n=10)

表11 藏悠游胶囊对大鼠血液学指标的影响(n=10)
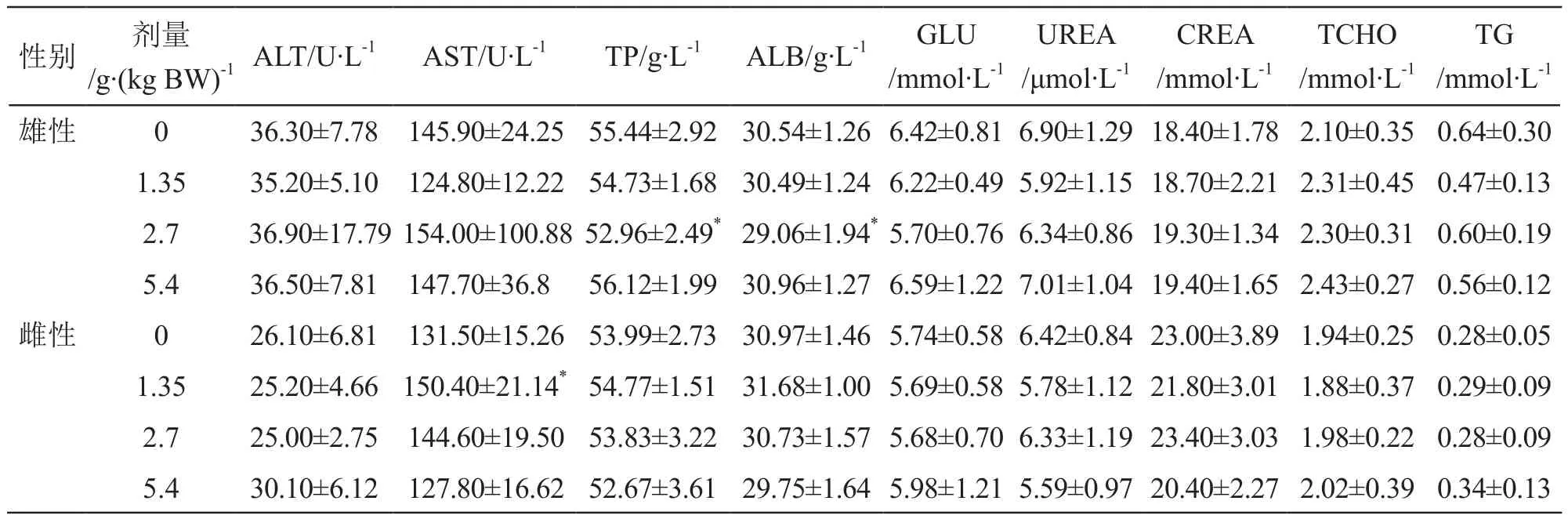
表12 藏悠游胶囊对大鼠血清生化学指标的影响(n=10)
3.6 提高缺氧耐受力功能试验结果
3.6.1 臧悠游胶囊对小鼠常压耐缺氧存活时间的影响 结果见表15。由表15可见,经口给予小鼠不同剂量的藏悠游胶囊30 d,各剂量组与溶媒对照组比较,存活时间明显延长,差异均有统计学意义(P<0.05,P<0.01)。
3.6.2 高反灵牌藏悠游胶囊对小鼠亚硝酸钠中毒存活时间的影响 结果见表16。由表16可见,经口给予小鼠不同剂量的高反灵牌藏悠游胶囊30 d,各剂量组与溶媒对照组比较,中剂量组存活时间延长,且差异有统计学意义(P<0.01),即藏悠游胶囊小鼠亚硝酸钠中毒存活实验结果阳性。
3.6.3 藏悠游胶囊对小鼠急性脑缺血性缺氧喘气时间的影响 结果见表17。由表17可见,经口给予小鼠不同剂量的藏悠游胶囊30 d,各剂量组与溶媒对照组比较,喘气时间均延长,差异均有统计学意义(P<0.01)。
4 结论
本研究采用小鼠急性毒性试验、Ames试验、骨髓细胞微核试验、小鼠精子畸形试验、30 d喂养试验5个方面对藏悠游胶囊进行安全毒理学评价,采用常压耐缺氧实验、亚硝酸钠中毒存活实验、急性脑缺血性缺氧实验研究其提高缺氧耐受力的功能。安全毒理学评价结果显示,两种性别小鼠MTD均大于20.0 g/kg BW,该受试物属无毒级,Ames试验、骨髓细胞微核试验、小鼠精子畸形试验3项遗传毒性试验结果均为阴性,30 d喂养未见明显毒性作用。常压耐缺氧实验中,各剂量组均能延长小鼠常压耐缺氧存活时间;亚硝酸钠中毒存活实验中,中剂量组能延长小鼠存活时间;急性脑缺血性缺氧实验中,各剂量组均能延长小鼠的喘气时间,3项试验均为阳性。根据《食品安全性毒理学评价程序》GB15193.1-2014[3],藏悠游胶囊未见明显毒性作用且具有提高缺氧耐受力功能的作用。

表13 藏悠游胶囊对大鼠脏器湿重的影响(n=10)

表14 藏悠游胶囊对大鼠脏器系数的影响(n=10)
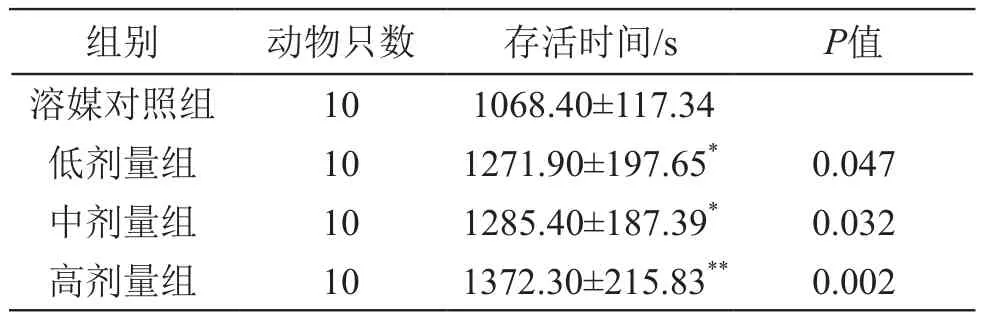
表15 高反灵牌藏悠游胶囊对小鼠常压耐缺氧存活时间的影响

表16 藏悠游胶囊对小鼠亚硝酸钠中毒存活时间的影响
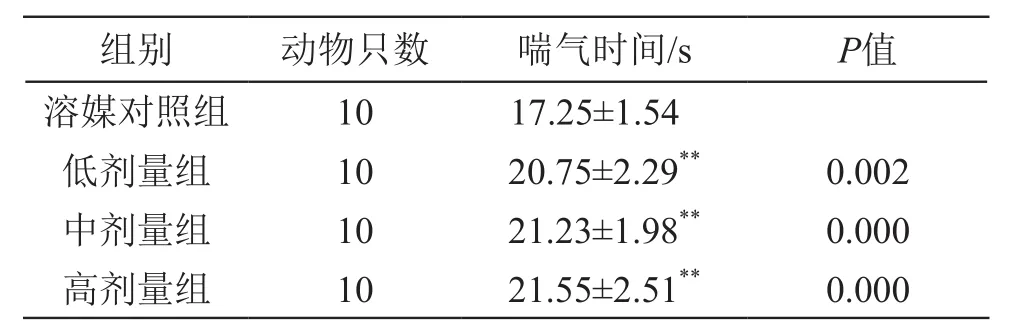
表17 藏悠游胶囊对小鼠急性脑缺血性缺氧喘气时间的影响

