救必应化学成分的分离与鉴定
陈曼钿,柳新然,张 琳,李 玲,李百柠,陈丽亚,陈 苗,陈 刚,李 宁
(沈阳药科大学 中药学院,辽宁 沈阳 110016)
救必应(Ilex rotundaThunb.)又称山冬青、熊胆木、白木香等,为冬青科(Aquifoliaceae)冬青属植物铁冬青的干燥树皮或根皮。广泛分布于东亚地区(中国、日本、韩国及越南等)[1],在我国主要分布于安徽、江苏、福建、广东、广西、云南、台湾等地[2],为华南地区常用中草药。救必应味苦,性寒,归肺、肝、大肠经,有泻火解毒、清热利湿、行气止痛、凉血止血等功效,民间主要用于治疗感冒发热、咽喉肿痛、暑湿泄泻、急性胃肠炎,风湿痹痛等;外用治跌打损伤、烧烫伤、痈疖疮疡、外伤出血等[3]。因其治疗跌打损伤、烧烫伤的效果显著,故美其名为救必应[4]。现代药理学研究表明,救必应具有抗心律失常、降低冠脉流量、提高耐缺氧能力、降压、止血、抗炎、抑菌及抗肿瘤等药理作用。临床上救必应常应用于治疗胃肠道消化系统疾病、心血管疾病、以及多种感染性疾病[5]。本实验对救必应95 %乙醇提取物的乙酸乙酯层的化学成分进行分离与纯化,并根据理化性质、波谱数据鉴定化合物结构。共分离得到6个化合物,分别鉴定为3, 4-dihydroxy-acetophenone(1)、threo-8S-7-methoxysyringylglycerol(2)、2, 3-dihydroxy-1-(4-hydroxy-3, 5-dimethoxyphenyl)-1-propanone(3)、caffeic acid (1-hydroxyl-4-O-β-D-glucopyranosylprenyl)-ester(4)、长梗冬青苷(pedunculoside,5)、rotungenoside(6)、救必应酸(rotundic acid,7)、rotungenic acid(8),其中化合物1~4为首次从冬青属植物分得。
1 仪器与试药
1.1 仪器
Bruker-ARX-400型,Bruker-AV-600型核磁共振波谱仪(TMS内标,瑞士Bruker);microTOFQ Bruker质谱仪(瑞士Bruker);Shimadzu LC-6AD 高效液相色谱仪(SPD-20A UV-VIS型紫外检测器,RID-10A型示差检测器,日本Shimadzu公司)。分析型色谱柱:Unitary C18(250 mm×4.6 mm,5 μm)色谱柱;YMC C18(10 mm×250 mm,5 μm)半制备型色谱柱;YMC C18(20 mm×250 mm,5 μm)制备型色谱柱; 341MC型旋光仪(Perkin-Elmer);JASCO pu-2080高效液相仪(日本Jasco公司);柱色谱硅胶(200~300目),薄层色谱硅胶GF(10~40 μm,青岛海洋化工厂);Sephadex LH-20(瑞典Amersham Pharmacia Biotech AB);ODS(50 μm,日本YMC公司)。
1.2 试药
救必应饮片由广州中医药大学提供,经沈阳药科大学潘英妮副教授鉴定为救必应 (Ilex rotunda Thunb.)的干燥树皮。石油醚,二氯甲烷,乙酸乙酯,正丁醇,甲醇,均为分析纯(山东禹王实业有限公司化工分公司);甲醇(色谱纯,山东禹王实业有限公司化工分公司);乙腈(色谱纯,Sigma);甲酸(色谱纯,沈阳试剂一厂)。
2 提取与分离
救必应乙酸乙酯提取物经硅胶吸附柱色谱分离,二氯甲烷-甲醇梯度洗脱。同时用制备薄层色谱、ODS柱色谱、重结晶及制备型高效液相色谱(HPLC)等方法进行分离纯化,得到化合物1(42.7 mg),2(2.8 mg),3(6.0 mg),4(15.2 mg),5(61.6 g),6(50.0 mg),7(7.0 g),8(7.0 mg)。并通过理化性质和波谱学特征确定其结构。化合物1~8的化学结构见图1。
3 结构鉴定
化合物1:白色针晶(甲醇)。1H-NMR(600 MHz,CD3OD)给出3个芳香质子信号δ 7.41(2H,m,H-2,6),6.82(1H,d,J=8.0 Hz,H-5)和一个甲基信号δ 2.48(3H,s,8-CH3)。13C-NMR(150 MHz,CD3OD)给出了1个羰基碳信号δ 199.8(C=O),6个芳香碳信号δ 130.8(C-1),116.2(C-2),146.5(C-3),152.4(C-4),115.9(C-5),123.6(C-6),和1个甲基信号26.3(C-8)。将以上数据与文献[6]比较,鉴定化合物1为3, 4-二羟基苯乙酮(3, 4-dihydroxy-acetophenone)。
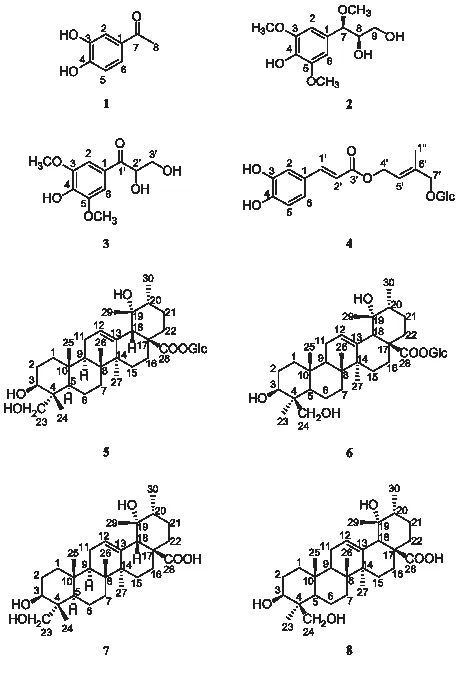
图1 化合物1~8的化学结构式
化合物2:无色油状物(甲醇)。1H-NMR(600 MHz,DMSO-d6)给出了2个芳香质子信号δ 6.51(2H,s,H-2,6)和3个甲氧基信号δ 3.73(6H,s,3,5-OCH3),3.13(3H,s,7-OCH3),此外还有2个次甲级和1对亚甲基信号δ 3.99(1H,d,J=6.0 Hz,H-7),3.48(1H,m,H-8),3.23(1H,dd,J=10.8,4.0 Hz,H-9a),3.09 (1H,dd,J=10.8,6.1 Hz,H-9b)。13C-NMR(150 MHz,DMSO-d6)共给出了12个碳信号δ 129.5(C-1),104.7(C-2,6),147.7(C-3,5),134.8(C-4),84.1(C-7),75.1(C-8),62.5(C-9),55.9(3,5-OCH3),56.3(7-OCH3)。与文献[7]对比分析,鉴定化合物2为thero-8S-7-methoxysyringylglycerol。
化合物3:白色无定形粉末(甲醇)。1H-NMR(400 MHz,CD3OD)中δ 7.34 (2H,s,H-2,6)为芳香质子信号,δ 5.14(1H,dd,J=5.0,4.0 Hz,H-2’),3.87 (1H,dd,J=11.6,4.0 Hz,H-3’a),3.75(1H,dd,J=11.6,5.0 Hz,H-3’b)为连氧氢信号,δ 3.91(6H,s,2 × OCH3)为2个甲氧基信号。13C-NMR(100 MHz,CD3OD)给出碳信号δ 126.7(C-1),107.7(C-2,6),149.1(C-3,5),199.7(C-1’),75.5(C-2’),66.2(C-3’),56.9(2 × OCH3)。对比文献[8],鉴定化合物3为2, 3-dihydroxy-1-(4-hydroxy-3, 5-dimethoxyphenyl)-1-propanone。
化合物4:白色粉末(甲醇)。1H-NMR(400 MHz,CD3OD)中给出一组芳香质子信号:δ 7.05(1H,d,J=1.8 Hz,H-2),6.96(1H,dd,J=8.2,1.8 Hz,H-6),6.78 (1H,d,J=8.2 Hz,H-5),组成ABX自旋耦合系统,提示结构中存在1,3, 4三取代苯环;3个不饱和双键信号:δ 7.57(1H,d,J=15.9 Hz,H-1’),6.28(1H,d,J=15.9 Hz,H-2’),5.71(1H,br.t,J=6.9 Hz,H-5’);2个亚甲基信号:δ 4.61(2H,br.s,H-4’),4.45(1H,d,J=12.0 Hz,H-7’a),4.28(1H,d,J=12.0 Hz,H-7’b);1个甲基信号:δ 1.76(3H,s,H-1’’);以及一个糖端基质子信号:δ 4.32(1H,d,J=7.0 Hz,Glc-H-1)。13C-NMR(100 MHz,CD3OD)谱中给出20个碳信号,其中一个酯羰基信号δ 168.9(C-3’);10个不饱和碳信号δ 127.7(C-1),114.9(C-2),146.8(C-3),149.7(C-4),116.5(C-5),123.0(C-6),147.2(C-1’),115.2(C-2’),125.0(C-5’),135.9(C-6’);一组葡萄糖碳信号δ 103.3(Glc-1),75.1(Glc-2),78.0 (Glc-3),71.7(Glc-4),78.1(Glc-5),62.8(Glc-6);2个连氧亚甲基碳信号δ 66.1(C-4’),69.7(C-7’) 和1个甲基信号δ 14.2(C-1’’)。综合以上数据,查询文献[9],鉴定化合物4为caffeic acid(1-hydroxyl-4-O-β-D-glucopyranosylprenyl)-ester。
化合物5:无色针晶(甲醇)。1H-NMR(400 MHz,pyridine-d5):δ 6.30(1H,d,J=7.6 Hz,Glc-H-1),5.59(1H,br.s,H-12),1.66(3H,s,29-CH3),1.42(3H,s,24-CH3),1.24(3H,s,26-CH3),1.08(3H,s,27-CH3),1.05(3H,s,25-CH3),1.09(3H,d,J=6.5 Hz,30-CH3)。13C-NMR(100 MHz,pyridine-d5)给出36个碳信号,其中30个为三萜母核碳信号δ 39.6(C-1),27.4(C-2),73.8(C-3),43.3(C-4),49.5(C-5),19.3(C-6),33.6(C-7),41.2(C-8),48.0(C-9),37.9(C-10),24.7(C-11),129.7(C-12),139.6(C-13),42.7(C-14),29.7(C-15),26.5(C-16),49.1(C-17),55.0(C-18),73.6(C-19),42.9(C-20),27.1(C-21),38.3(C-22),67.5(C-23),12.7(C-24),17.6(C-25),16.6(C-26),24.7(C-27),177.3 (C-28),27.2(C-29),16.3(C-30),剩余6个为葡萄糖信号δ 95.8(Glc-1),74.0 (Glc-2),78.6(Glc-3),71.1(Glc-4),78.3(Glc-5),62.4(Glc-6)。查阅文献[10]对比以上数据,鉴定化合物5为长梗冬青苷(pedunculoside)。
化合物6:白色无定形粉末(甲醇)。与化合物5相似,13C-NMR(100 MHz,pyridine-d5)同样给出36个碳信号,30个为三萜母核碳信号δ 39.2(C-1),28.8(C-2),80.6(C-3),43.5(C-4),56.8(C-5),19.6(C-6),34.2(C-7),40.9(C-8),48.2(C-9),37.4(C-10),24.6(C-11),128.6(C-12),139.6(C-13),42.5(C-14),29.6(C-15),26.4(C-16),49.0(C-17),54.8(C-18),73.0(C-19),42.4(C-20),27.0(C-21),38.0(C-22),23.9(C-23),64.9(C-24),16.5(C-25),17.6(C-26),24.9(C-27),177.3(C-28),27.4(C-29),17.0(C-30),及6个葡萄糖信号δ 96.2 (Glc-1),74.4(Glc-2),79.6(Glc-3),71.5(Glc-4),79.3(Glc-5),62.8(Glc-6)。综合比较可发现,化合物5和6为同分异构体,二者的区别仅仅在于23,24位羟基的位置,根据相关报道[108]:当24位为-OH时,对应的13C-NMR化学位移值分别为δ 23.5(C-23)/64.5(C-24);当23位为-OH时,其对应的13C-NMR化学位移值分别为δ 67.9(C-23)/12.8(C-24)。因此将以上数据与文献[11]比较,鉴定化合物6为rotungenoside(ilexoside XXXV)。
化合物7:无色针晶(甲醇)。1H-NMR(400 MHz,pyridine-d5) 给出一个不饱和双键氢信号δ 5.64(1H,br.s,H-12),和6个甲基信号δ1.71(3H,s,29-CH3),1.46(3H,s,24-CH3),1.15(3H,s,26-CH3),1.14(3H,d,J=6.7 Hz,30-CH3),1.08(3H,s,27-CH3),1.02(3H,s,25-CH3)。13C-NMR(100 MHz,pyridine-d5) 给出30个碳信号,δ 39.2 (C-1),28.0 (C-2),73.9(C-3),43.2(C-4),49.0(C-5),19.1(C-6),33.6(C-7),40.7(C-8),48.1(C-9),37.5(C-10),24.4(C-11),128.4(C-12),140.3(C-13),42.4(C-14),29.6(C-15),26.7(C-16),48.6(C-17),54.9(C-18),73.0(C-19),42.7(C-20),27.3(C-21),38.8(C-22),68.4(C-23),13.4(C-24),17.6(C-25),17.1(C-26),25.0(C-27),181.0(C-28),27.4 (C-29),16.3(C-30)。对比NMR数据并查阅文献[12]发现该化合物为长梗冬青苷的苷元,因此鉴定化合物7为救必应酸(rotundic acid)。
化合物8:白色无定形粉末(甲醇)。13C-NMR(100 MHz,pyridine-d5):δ 39.1 (C-1),28.8(C-2),80.6(C-3),43.6(C-4),56.8(C-5),19.6(C-6),34.3(C-7),40.8(C-8),48.2(C-9),37.5(C-10),24.6(C-11),128.3(C-12),140.4(C-13),42.5(C-14),29.7(C-15),26.8(C-16),48.7(C-17),55.0(C-18),73.1(C-19),42.8(C-20),27.3(C-21),38.9(C-22),24.0(C-23),65.0(C-24),16.4(C-25),17.5(C-26),25.0(C-27),181.0(C-28),27.5(C-29),17.2(C-30),以上数据与化合物7基本一致,同样是23,24位羟基的位置不同。查阅文献[13]比较后,鉴定化合物8为救必应酸的同分异构体rotungenic acid。

