钛基体化学镀锡工艺*
贾 旭,程晓梅,张 圳,冯 佳,郭爱红
(华北理工大学,河北 唐山 063210)
目前有关化学镀制备DSA(尺寸稳定阳极)的研究比较少,DSA大多应用电沉积或热涂覆等方法制备,这两种方法制备的涂层不够均匀,焙烧时易产生裂痕,使涂层脱落,从而使钛基底氧化影响而催化活性[1-2]。采用化学镀法制备的涂层匀称,不易产生缝隙[3]。如果采用化学镀金属涂层结合焙烧法制备氧化物阳极,所得具有电极不易产生裂痕、使用寿命长等优点。以往的化学镀锡都是以铜为基体,在钛基体上化学镀锡的研究几乎没有。所以本实验重点是在探讨化学镀钛基体预处理方法和最佳镀液配方。
是由于钛金属具有好的耐蚀性、热稳定性和比强度高等特点,DSA多以钛为基体[4-7]。但钛与氧有很强的亲和力,表面有一层致密的钛氧化膜,虽然通过酸碱预处理可以去除原始氧化膜,但一经水洗就又重新形成氧化膜[8]。所以,钛基体化学镀必须采用特殊的预处理工艺,如在钛基体表面镀上一层有催化活性又廉价易得的金属铜、铁、锌等[9]。王福生[10]在塑料上植入钯离子作敏化活化处理,以诱发化学镀[11]。王永峰[12]在Al2O3表面先化学镀铜再化学镀锡。本实验基于现有的文献总结,先探究了钛基体的不同前处理方法,以选择最佳预处理方案,并通过单因素和正交实验探究钛基体化学镀锡最佳工艺条件,为后续焙烧制得DSA奠定基础。
1 实 验
1.1 仪器与药品
主要仪器:S-4800场发射扫描电子显微镜;Agilent 7500A电感耦合等离子体质谱仪(ICP);CHI660E电化学工作站;WYI-3020D直流电源等。
主要试剂:甲基磺酸、甲基磺酸锡、乙二胺四乙酸、柠檬酸、酒石酸、氨基磺酸、硫脲、对苯二酚、抗坏血酸、磷酸、盐酸、硝酸、硫酸、乙酸、碳酸钠、氢氧化钠、氯化钠等,以上试剂均为分析纯。
1.2 工艺流程
4 cm×6 cm×0.1 mm的钛片为基体,其实验流程为:超声碱洗除油(80 ℃在NaOH 32 g/L,Na2CO320 g/L溶液中超声25 min)→去离子水冲洗→活化(常温下1:1盐酸溶液中酸洗10 min)→去离子水冲洗→中间层制备→化学镀锡→去离子水冲洗。
1.3 预处理及化学镀配方与工艺
普通酸碱预处理:碱洗(NaCO332 g/L,NaOH 20 g/L,处理温度80 ℃,超声25 min),酸洗(1:1 HCl,15 min)。
氯化钯活化-敏化:经普通酸碱预处理后的钛片,浸入敏化液中,敏化(SnCl240 g/L,HCl 100 mL/L,室温,1~2 min),活化(BaCl20.8 g/L,SnCl250 g/L,HCl 300 mL/L,40 ℃,10 min)。
电镀铜:焦磷酸钾 300 g/L,焦磷酸铜 50 g/L,磷酸氢二钾 40 g/L,酒石酸钾钠 40 g/L,香草醛 1 g/L,植酸 2 g/L,柠檬酸2 g/L。
浸锌法:酸洗(70% HNO3275 mL/L,40% HF 225 mL/L,30 s),浸锌(Na2Cr2O7100 g/L,40% HF 65 mL/L,ZnSO412 g/L,90 ℃,4 min),二次酸洗(HNO3275 mL/L,HF 225 mL/L,50 s),二次浸锌(工艺同上,6 min)。
化学镀锡:甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲90 g/L,络合剂5 g/L,次磷酸钠15 g/L,抗氧化剂2 g/L,镀液温度65 ℃,沉积15 min,pH 1.02。
1.4 镀层性能性表征
表征镀液抗氧化性能:将镀液在室温下静置,记录镀液出现变色、浑浊现象经历的时间,时间越长,镀液稳定性越好。
从镀件剪下1 cm2的试样,溶于王水溶液,采用Agilent 7500A电感耦合等离子体质谱仪(ICP)测定锡离子浓度,后结合锡金属密度计算镀层厚度。最简式为:
式中:h为镀层厚度,cm
c为锡离子浓度,mg/L
锡金属密度为7.28 g/cm2
用S-4800场发射扫描电子显微镜(SEM)观察表面晶核排列和分布情况。

表1 锡镀层表面形貌评价标准
采用上海辰华CHI660E电化学工作站,参比电极为饱和甘汞电极、辅助电极为铂电极、工作电极的有效面积为2 cm2,通过测定试样在3.5% NaCl溶液中的Tafel曲线来表征耐蚀性,扫描速率为10 mv/s,并采用电化学工作站自带软件拟合得到腐蚀电流密度,通常情况下电流密度越小耐蚀性越好。
采用划格法测定镀层的结合力,镀层无碎屑或起皮现象说明结合力较好。

表2 结合力评价标准
2 结果与讨论
2.1 中间层制备工艺的选择
钛基体预处理方法主要有普通酸碱预处理、氯化钯活化-敏化[11]、电镀铜[13]和浸锌[14]4种,将预处理后的基体浸入基础化学镀液(甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲90 g/L,配位剂5 g/L,次磷酸钠15 g/L,抗氧化剂2 g/L)中,比较镀件镀层厚度,选出效果最佳预处理方案。
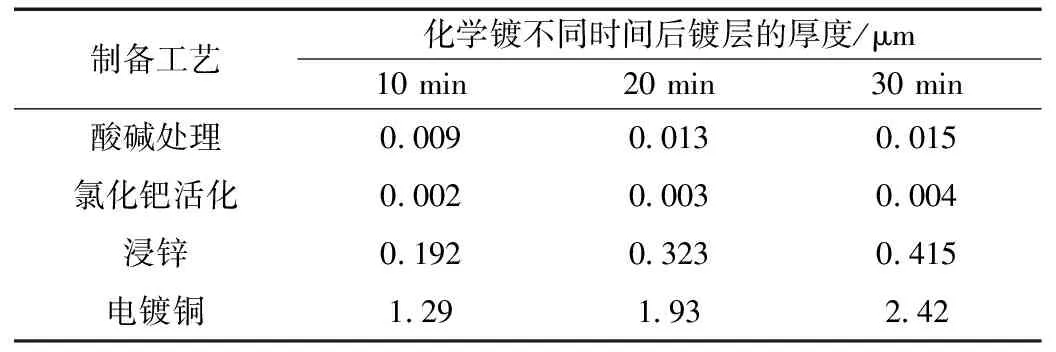
表3 不同预处理的锡镀层厚度
从表3可知,酸碱处理、氯化钯活化或浸锌后再化学镀所得锡镀层都极薄,说明其在钛基体上无明显作用。而经电镀铜处理后再化学镀锡所得镀层较厚,说明电镀铜预处理的效果好,因此选择电镀铜作为预处理方式。
2.2 化学镀锡镀液成分的确定
2.2.1 配位剂的确定
分别选取柠檬酸、酒石酸、EDTA作为配位剂对钛基体进行化学镀锡,其他镀液成份为:甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲90 g/L,次磷酸钠15 g/L,配位剂5 g/L,抗氧化剂2 g/L。测定得到的镀层厚度、耐腐性和结合力,结果如表4所示。

表4 采用不同物质作为配位剂时所得镀层的厚度和结合力
由表4可知,当EDTA作络合剂时镀层厚度最大为1.83 μm,用酒石酸作络合剂时镀层厚度最小为1.34 μm;经划格法测得结合力均较好。EDTA与Sn2+配位数为1,稳定常数为1023.1,说明EDTA络合能力强;EDTA络合Sn2+后,溶液中Sn2+浓度低,次磷酸钠对Sn2+的还原能力增强,使溶液中Sn2+被还原成Sn在钛基体上沉积,形成较厚的镀层。腐蚀电流密度EDTA<柠檬酸<酒石酸,EDTA作络合剂得到的镀层耐腐蚀性最好。综上所述,选用EDTA作为化学镀液络合剂。
2.2.2 抗氧化剂种类的确定
在镀液Sn2+易氧化成Sn4+,继而水解成锡酸,锡酸与Sn2+、有机物等形成胶团结构,使溶液颜色和性质发生变化[10],在镀液中加入抗氧化剂可获得长期稳定的镀液[11]。选取抗氧化性较好的三种抗氧化剂:对苯二酚、异烟酸、抗坏血酸[12],其他镀液成份为:甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲90 g/L,次磷酸钠15 g/L,配位剂5 g/L,抗氧化剂2 g/L。测定镀层厚度、耐腐性、结合力,并放置考察镀液的稳定性,得到最佳抗氧剂。结果如表5所示。
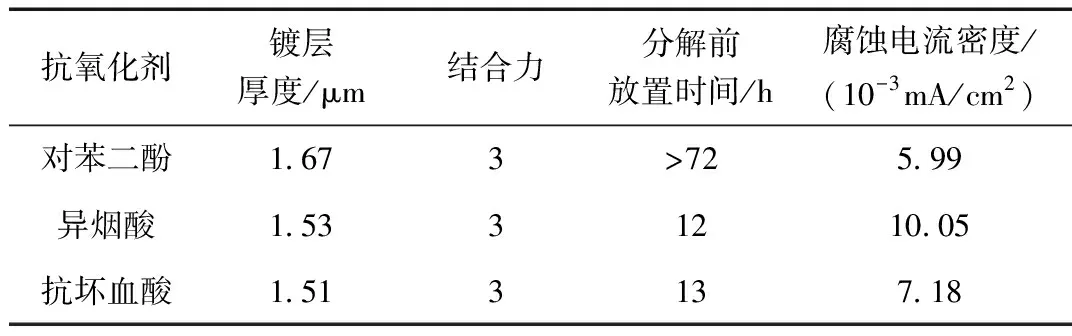
表5 添加不同抗氧化剂对镀层厚度和结合力影响
由表5可知,用对苯二酚作抗氧化剂时镀层厚度稍大为1.67 μm,抗坏血酸作抗氧化剂时镀层厚度稍小为1.51 μm;三者作为抗氧化剂时结合力均较好。经放置,添加对苯二酚的镀液分解前放置时间最长。腐蚀电流密度从小到大依次为对苯二酚<异烟酸<抗坏血酸,耐腐蚀性最好的是用对苯二酚作抗氧化剂得到的镀层。因此,选用对苯二酚作化学镀液抗氧化剂。
2.3 化学镀锡镀液成分浓度的确定
2.3.1 硫脲浓度对镀层性能的影响
所用镀液成分为甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲90 g/L,次磷酸钠15 g/L,EDTA 5 g/L,对苯二酚2 g/L。
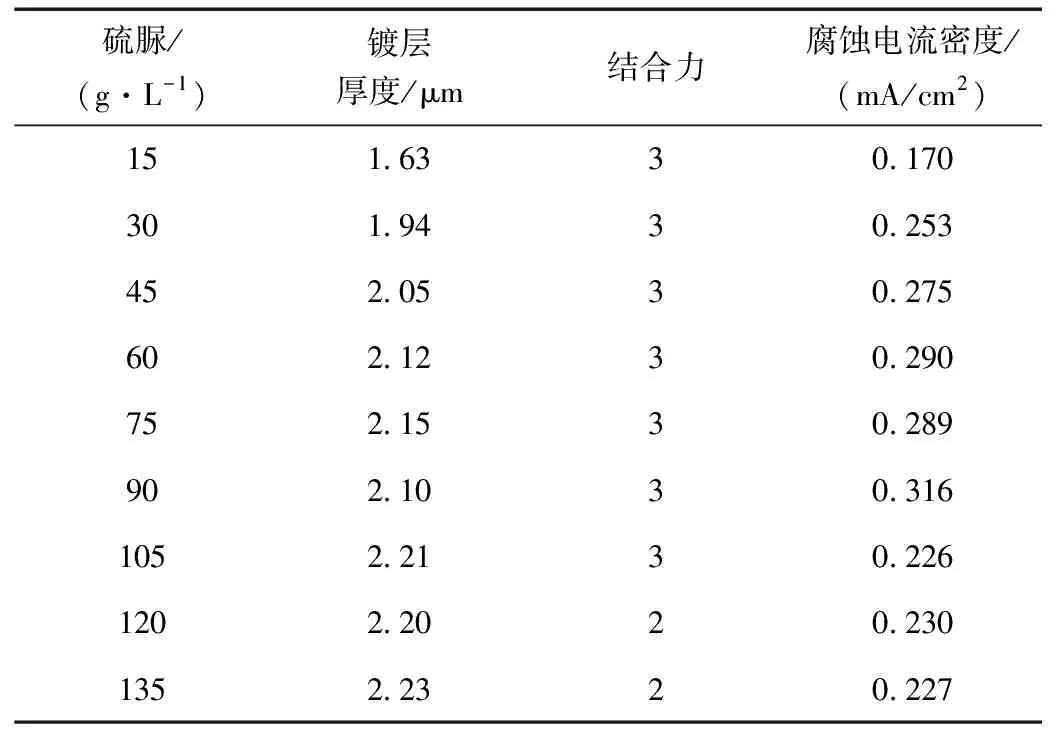
表6 硫脲浓度对镀层厚度和结合力影响
从表6可知,随硫脲质量浓度的增大,镀层厚度总体呈现先增大后平稳的变化趋势。硫脲质量浓度为15 g/L时,腐蚀电流密度最小,此时镀层薄,但表面致密性好。硫脲浓度从30 g/L 到90 g/L时,硫脲浓度越大,对铜的腐蚀作用越大,腐蚀电流密度越大。当硫脲投加量为105 g/L时,电流密度突降,此时硫脲对铜的腐蚀作用也达极限,但厚度增加,镀层耐蚀性变好。
不同浓度下硫脲的镀层表面形貌如图1所示:硫脲浓度较低时,镀层形貌较平整均匀;随着硫脲浓度的增大,锡的沉积速度加快,镀层形貌越来越粗糙、不均匀。选择厚度尽量厚,耐腐蚀性好的镀层,综合考虑选择硫脲最佳投加量为105 g/L。
新时代乡村振兴战略导向必然带来城乡经济结构、城乡关系等方面的全新变化。实施乡村振兴战略要适应新时代新的要求新的发展新的变化,从解决当前“三农”问题中的突出矛盾入手,在分析矛盾中厘清思路、在解决矛盾中推动振兴。

图1 不同硫脲浓度所得镀层SEM图
2.3.2 对苯二酚抗氧化剂浓度对镀层性能的影响
所用镀液成分为甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲105 g/L,次磷酸钠15 g/L,EDTA 5 g/L。对苯二酚浓度对镀层性能影响如表7所示。
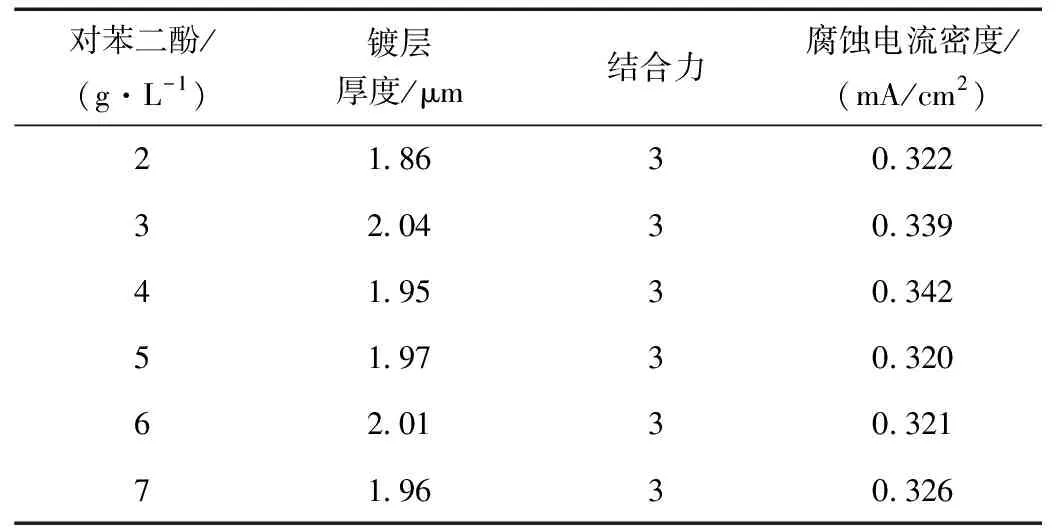
表7 对苯二酚浓度对镀层厚度和结合力影响
不同浓度对苯二酚得到镀层的表面形貌如图2所示。镀层厚度随对苯二酚浓度上下浮动;划格法测试镀层结合力均较好。静置实验证明,对比无抗氧化剂加入,镀液稳定性都有提高,可以维持3天不分解。各腐蚀电流密度值相差不大。图2中看出,镀层表面的锡晶粒大小与致密性无明显变化,说明对苯二酚的加入量不影响镀层表面形貌。加入少量对苯二酚即可起到抗氧化的作用,综上所述,确定其加入量为2 g/L。

图2 不同EDTA浓度所得镀层SEM图像
2.3.3 甲基磺酸浓度对镀层性能的影响
甲基磺酸浓度对镀层性能影响如表8所示。所用镀液成分为甲基磺酸锡12 g/L,甲基磺酸50 mL/L,硫脲105 g/L,次磷酸钠15 g/L,EDTA 5 g/L,对苯二酚2 g/L。
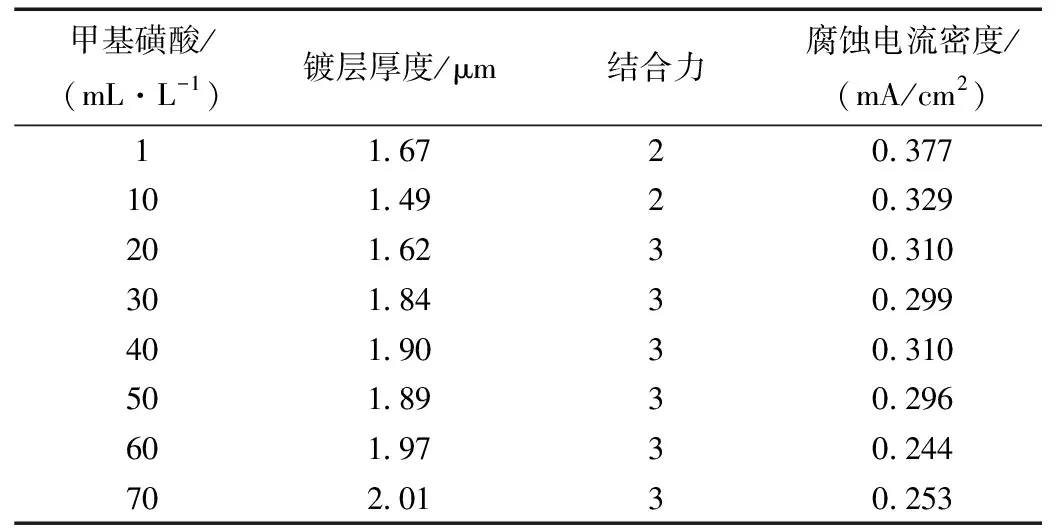
表8 甲基磺酸浓度对镀层厚度和结合力影响
镀层厚度随甲基磺酸浓度的增大呈平稳上升趋势,当酸介质投入达到一定浓度后镀速减慢,镀层厚度增速减缓。静置实验证明,甲基磺酸浓度小时镀液不稳定,很快发生分解。当甲基磺酸浓度为50 mL/L以上时,镀液变稳定,可以维持三天不分解。甲基磺酸添加量为0和10 mL/L时腐蚀电流密度较大,此时镀层结合力不好,镀液分解最快,其他添加量下腐蚀电流密度呈小范围内上下浮动。
不同甲基磺酸投加量的镀层表面形貌如图3所示。

图3 不同甲基磺酸浓度所得镀层SEM图像
从图3中可以看出,在甲基磺酸添加量为10 mL/L时,镀层晶粒分布不均,并且肉眼均可观察到镀液甲基磺酸浓度低时镀层表面发灰发花。随着浓度增大,锡晶粒分布越来越均匀,晶粒之间孔隙减少,镀层表面逐渐呈现亚光白色。综合镀层厚度,镀速,表面形貌及腐蚀性分析,确定甲基磺酸最佳投加量为60 mL/L。
2.3.4 次磷酸钠浓度对镀层性能的影响
次磷酸钠浓度对镀层性能影响如表9所示。所用镀液成分为甲基磺酸锡12 g/L,甲基磺酸60 mL/L,硫脲105 g/L,EDTA 5 g/L,对苯二酚2 g/L。
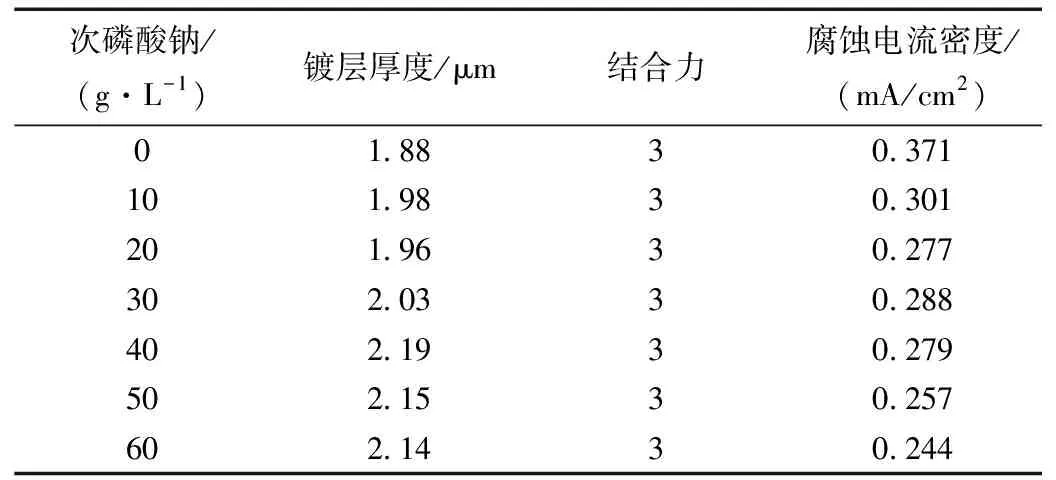
表9 次磷酸钠浓度对镀层厚度和结合力影响
从表9中得知,随次磷酸钠浓度增大,镀层厚度先上升后稍有下降,这是因为次磷酸钠浓度增加,锡离子被还原的速度加快,但当其浓度过大时,容易使Sn2+在溶液中被还原,而不是在基体表面。腐蚀电流密度变化幅度不大,但随着次磷酸钠加入量增多,镀层增厚,腐蚀电流密度呈递减趋势。不同次磷酸钠加量的镀层表面形貌如图4所示。

图4 不同次磷酸钠浓度所得镀层SEM图像
随次磷酸钠浓度增加,镀层微观表面晶粒越来越多,但颗粒越来越不均匀,且有堆积现象。这是由于次磷酸钠加入量的增加,被催化的锡离子增多,且速度加快,造成表面晶粒不能整齐排列。结合镀层耐腐蚀性、厚度和节约成本综合考虑,选择次磷酸钠最佳投加量为30 g/L。
2.3.5 EDTA络合剂浓度对镀层性能的影响
EDTA浓度对镀层性能影响如表10所示。所用镀液成分为甲基磺酸锡12 g/L,甲基磺酸60 mL/L,硫脲105 g/L,次磷酸钠30 g/L,对苯二酚2 g/L。
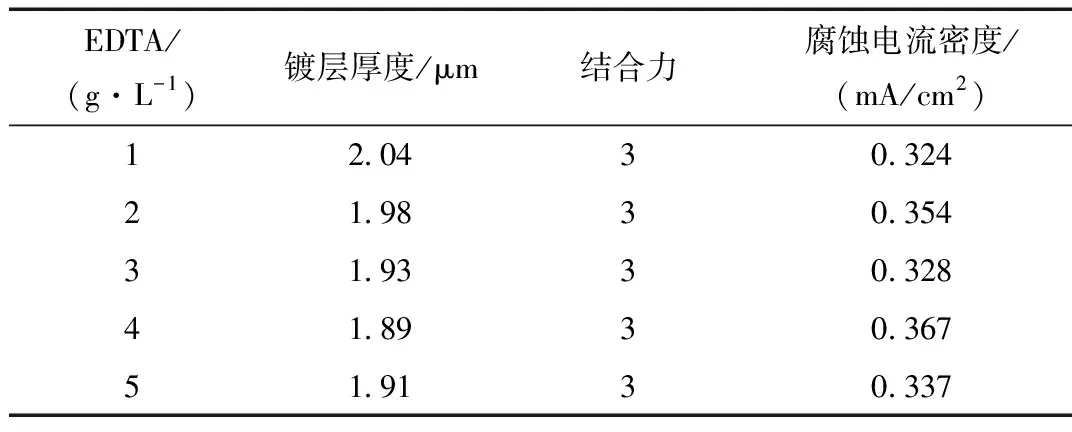
表10 EDTA浓度对镀层厚度和结合力影响
从表10可知,镀层厚度随EDTA加入量的增大呈而下降,是因为其浓度增大,被络合的Sn2+增多,游离的Sn2+减少,沉积速率减慢,相同时间内所得镀层较薄。电流密度在EDTA浓度为1 g/L时最小,在4 g/L时最大,其余投加浓度所得镀层的电流密度在小范围内上下浮动。随着镀液中EDTA浓度的增大,锡的沉积速度减慢,镀层晶粒均匀、规整。1 g/L时虽然微观形貌不是最好,但厚度最大,表现出的耐蚀性也最佳,从成本看也最低,综合考虑,选择EDTA最佳投加量为1 g/L。

图5 不同EDTA浓度所得镀层SEM图像
2.4 正交实验
通过单因素实验所得最佳条件基础上,通过5因素4水平的正交实验,研究了化学镀锡液EDTA、硫脲、对苯二酚、次磷酸钠和甲基磺酸五种因素对厚度、结合力、耐腐蚀性和表面形貌的影响,所测结果如表11、表12所示。
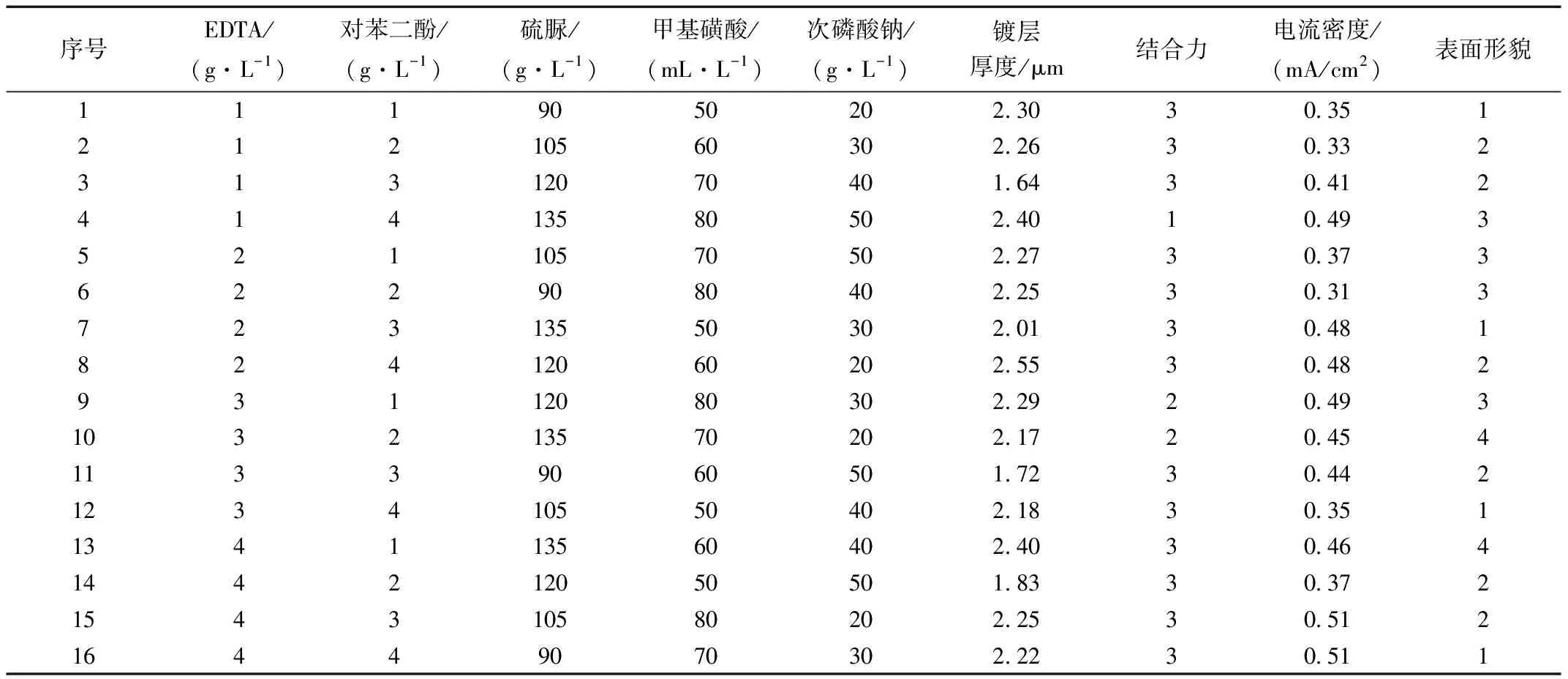
表11 正交实验
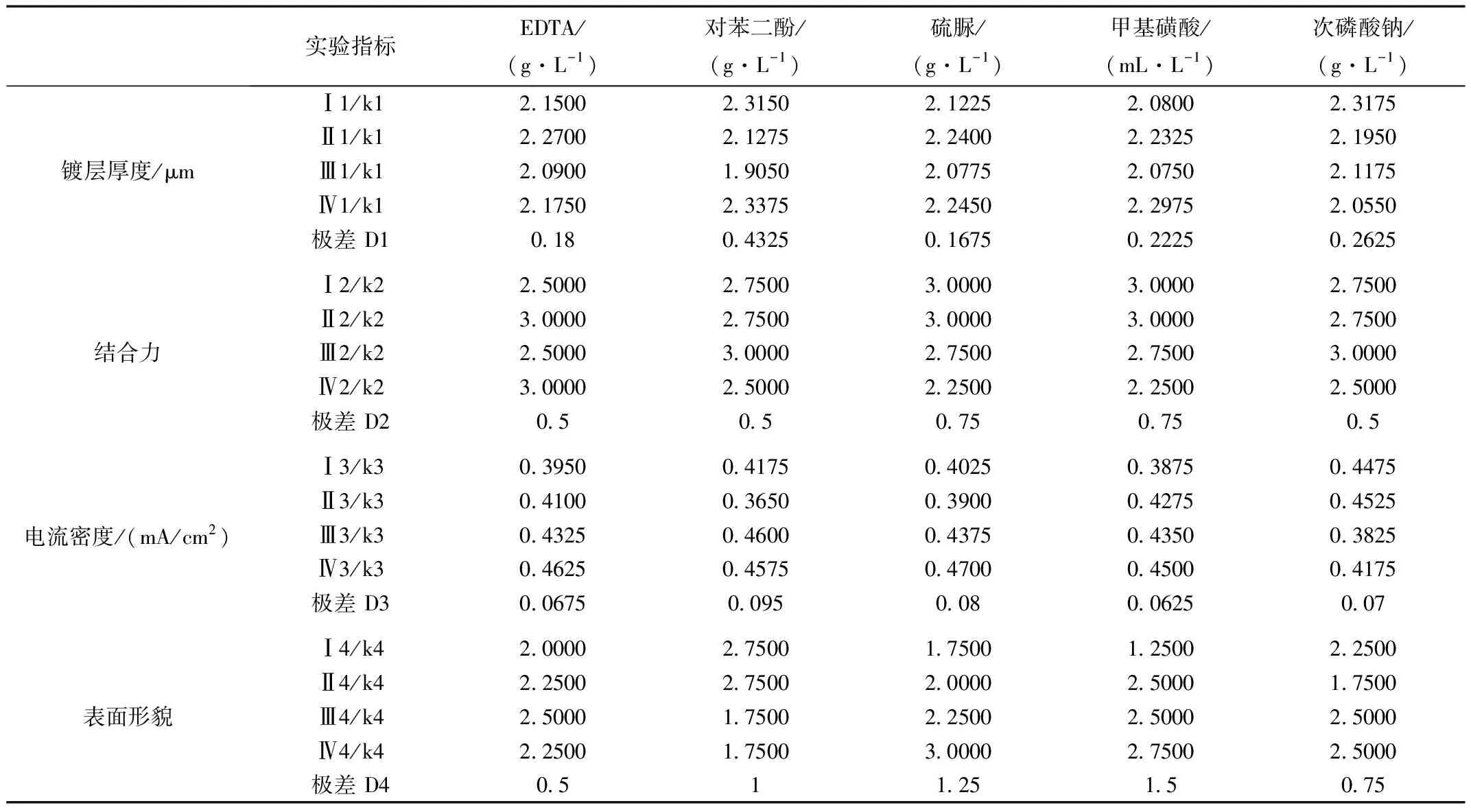
表12 镀锡液正交实验极差分析结果
说明:(1)Ij代表第 j 列“1”水平所对应的实验指标的数值之和;Ⅱj代表第 j 列“2”水平所对应的实验指标的数值之和;Ⅲj代表第 j 列“3”水平所对应的实验指标的数值之和;Ⅳj代表第 j 列“4”水平所对应的实验指标的数值之和;(2)kj代表第 j 列同一水平出现的次数;(3)Dj代表第 j 列各水平对应的实验指标平均值中的最大值减最小值。
由表12可以看出,在选取单因素最佳条件附近的四水平,对镀锡层厚度影响最大的因素是对苯二酚的浓度,影响最小的是硫脲的浓度;对表面形貌影响最大的是甲基磺酸的浓度,影响最小的是EDTA的浓度;对结合力影响最大的是硫脲和甲基磺酸的浓度,其次是对苯二酚、次磷酸钠和EDTA的浓度。对腐蚀电流影响最大的是对苯二酚的浓度,影响最小的是甲基磺酸的浓度。由此得出优化方案为:12 g/L甲基磺酸锡,60 mL/L甲基磺酸,105 g/L硫脲,2 g/L EDTA,40 g/L次磷酸钠,3 g/L对苯二酚,镀液温度65 ℃,沉积25 min。
3 结 论
(1)得到一种钛基体化学镀锡液,经正交实验优化方案得到的最佳配方为12 g/L甲基磺酸锡,60 mL/L甲基磺酸,105 g/L硫脲,2 g/L EDTA,40 g/L次磷酸钠,3 g/L对苯二酚。
(2)该配方结合电镀铜层特殊预处理方法,可在钛基体上得到厚度为2.18 μm的镀层,镀层耐蚀,结合力较好,表面结晶均匀致密,且此工艺条件下的镀液稳定,可为后续结合焙烧实验制得DSA电极提供条件。

