合并多种抗体阳性自身免疫性脑炎临床分析
王小俊 王梦涵 余 列 彭 涛 胡文涛 孙桂芳 刘 宇 刘艳茹 卢 宏
郑州大学第一附属医院神经内科,河南 郑州 450052
自身免疫性脑炎(autoimmune encephalitis,AE)是指一类由于血清和(或)脑脊液存在针对自身抗原的阳性抗体,进而对中枢神经系统产生异常免疫反应的一系列症状的脑炎综合征。通常急性或亚急性起病(≤3个月),根据阳性抗体的不同被分为很多亚型,每个亚型有各自的临床特点,影像学检查及肿瘤合并率也不尽相同。共同的临床表现主要有精神行为异常、认知障碍、近记忆力下降、癫痫发作、言语障碍、不自主运动、意识水平下降或昏迷、自主神经功能障碍等。主要诊断方法是血和脑脊液存在相关的抗神经元阳性抗体。目前最公认的自身免疫性脑炎的分类方法是根据抗体类型,大致分为两大类:抗神经元细胞内抗原抗体相关AE(即经典的副肿瘤性性脑炎)和抗神经元细胞表面或突触蛋白抗原抗体相关AE(新型AE)。单个抗神经元抗体阳性的自身免疫性脑炎已经得到广大医学研究者的关注及研究,近10 a来已有大量的自身免疫性脑炎被诊断和报道,临床意义基本明确,但合并多个抗神经元抗体阳性的自身免疫性脑炎并不多见,近几年虽有陆陆续续的报道,但其临床意义及发生机制尚不明确。本文通过回顾2015-01-2019-05在郑州大学第一附属医院确诊的合并多种抗神经元抗体阳性的自身免疫性脑炎病例,分析讨论其临床意义,以提高临床中对该类疾病的认识。
1 对象与方法
1.1对象收集郑州大学第一附属医院2015-01-2019-05确诊为自身免疫性脑炎患者255例,其中合并双抗体阳性者7例。均符合2016年GRAUS等[1]提出的AE诊断标准。
1.2方法收集7例患者的临床表现、实验室检查及影像学检查结果,分析治疗效果及预后。所有患者均行血和脑脊液AE抗体检测,采用间接免疫荧光法检测自身免疫脑炎抗体,包括抗NMDAR抗体、抗LGI1受体、抗GABABR抗体、抗AMPA1受体、抗AMPA2受体、抗CASPR2受体;采用间接免疫荧光法检测副肿瘤相关抗体(抗-Hu、抗-Ri、抗-Yo、抗CV2、抗Ma2、抗Amphiphsin)。AE相关抗体均由郑州大学第一附属医院我院神经内科实验室进行检测并报告。均于2019-05进行电话随访。
2 结果
2.17例AE患者抗体检测结果4例抗NMDAR抗体阳性患者分别合并抗LGI1抗体(2例)、抗-Ma2、抗-Yo抗体阳性,2例抗GABABR脑炎分别合并抗Hu、抗amphiphsin阳性,1例抗LGI1脑炎合并抗Hu阳性。均未见其他抗自身抗体阳性。见表1。
2.2合并多种抗体阳性AE患者的临床特点7例患者中男2例,女5例,男女比例为1:2.5,平均发病年龄61.8岁(43~84岁)。均为急性或亚急性起病。5例好转,2例死亡。
7例患者临床表现多样,症状由轻至重不同。首发症状依次为癫痫发作(4/7)、精神行为异常(2/7)、记忆力下降(1/7)。2例合并肿瘤(小细胞肺癌和子宫肌瘤),2例高度怀疑合并肿瘤,未证实。颅脑MRI出现责任病灶者5例,脑脊液检查细胞数及蛋白增高者4例,寡克隆带电泳阳性者1例。6例免疫治疗[激素和(或)静脉注射免疫球蛋白(IVIG)]均有效好转,1例对症治疗后好转,3例复发。具体如下:4例抗NMDAR脑炎患者分别合并抗LGI1抗体(例2、例6)、抗-Ma2抗体(例4)及抗-Yo抗体阳性(例7)。主要临床表现为近事记忆力下降(4/4)、癫痫发作(3/4)、精神行为异常(2/4)、意识水平下降(2/4)、不自主运动(2/4)、认知障碍(1/4)。2例患者可见头MRI不同部位病灶,其中例4受累部位较广泛;例7因左额叶病灶曾误诊为脑肿瘤,后经我院确诊为AE,给予免疫治疗后额叶病灶较前明显缩小(图1)。脑脊液细胞数及蛋白较高者仅2例,寡克隆带电泳均阴性。1例合并子宫肌瘤。其中3例均给予一线免疫治疗后症状好转未再复发,例4症状较轻,给予对症治疗后好转无复发。
2例抗GABABR脑炎患者分别合并抗Hu抗体(例3)、抗amphiphsin阳性(例5)。1例合并小细胞肺癌,1例高度怀疑肺癌。二者脑炎症状复杂多样,并发症较多,病情较重,主要脑炎表现有癫痫发作、记忆力下降、精神及认知障碍、言语不清、意识模糊及自主神经功能障碍。头MRI均表现双侧海马及颞叶内侧病灶(图2),脑脊液细胞数及蛋白均明显增高,例5寡克隆带阳性,脑电图左侧弥散异常。二者分别给予IVIG和激素免疫治疗,例5同时抗肿瘤治疗(化疗),病情仍反复,最终均死亡,未尸检。例1为抗LGI1合并抗Hu抗体阳性AE,临床表现以认知障碍、命名性失语及记忆力下降为主,合并感觉性周围神经病变。脑脊液无异常改变,脑MRI左侧额颞顶枕叶病灶,脑电图左侧局限性异常,未发现肿瘤征象,结合查体及辅助检查已排除脑卒中。接受激素治疗后好转,随访时仅有间断性失语。见表2、3。

表1 7例患者抗体检测结果
注:NMDAR:N-甲基-D-天冬氨酸受体;LGIl:富亮氨酸胶质瘤失活蛋白l;GABABR:γ-氨基丁酸B型受体;Amphiphsin:两性蛋白
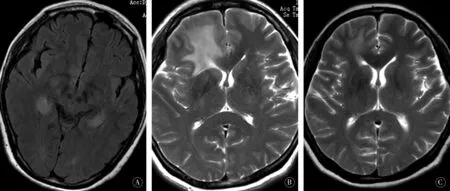
图1 例7颅脑MRI/T2-FLAIR A:治疗前:双侧海马区、颞叶内侧高信号;B:对症治疗后:双海马及颞叶内侧病灶基本消失,右侧额叶新发片状高信号,已排除肿瘤,考虑炎性复发;C:免疫治疗后:右侧额叶病灶较前明显缩小Figure 1 Case 7 MRI/T2-FLAIR of craniocerebral brain A:Before treatment,bilateral hippocampus and medial temporal lobe hyperintensity;B:After symptomatic treatment,bilateral hippocampus and medial temporal lobe lesions basically disappeared,and the right frontal lobe has a new high signal,the tumor has been excluded,consider the inflammatory recurrence;C:After immunotherapy,the right frontal lobe lesions are significantly reduced
3 讨论
自身免疫性脑炎泛指一类由自身免疫机制介导的脑炎。通常急性或亚急性起病(≤3个月),累及边缘系统者称边缘性脑炎,合并肿瘤者称副肿瘤相关性脑炎[2]。共同的临床表现主要有精神行为异常、认知障碍、近记忆力下降、癫痫发作、言语障碍、不自主运动、意识水平下降或昏迷、自主神经功能障碍等[3-5]。AE诊断的核心依据主要是血和/或脑脊液抗AE抗体阳性,但目前临床中检出的大多是单抗体阳性,仅少数同一患者中可检出两种或以上的阳性抗体(1.88%)[1,6-7]。HOFTBERGER等[8]发现20 例抗GABABR抗体脑炎中有 7 例合并其他抗体;王颖等[9]报道了1例抗CASPR2合并抗LGI1阳性的年轻患者;韩爽等[10]报道了抗GABABR合并抗NMDAR阳性AE患者1例。

表3 7例患者影像学特点、治疗与转归
注:IVIG:静脉注射丙种球蛋白
本研究显示,多重抗体阳性AE的发生率为2.7%(7/255),其中以抗NMDAR抗体居多(4/7),其次是抗LGI1(3/7)和GABABR抗体(2/7),与单抗体阳性AE的发生频率较类似[6,11],但不能排除受样本量的影响,需大样本证实。且绝大多数合并副肿瘤性相关抗体(5/7),与单抗体阳性AE相比,病变累及范围更广泛,中枢、周围神经系统、自主神经系统及言语、运动功能等均有不同程度的受累,症状更不典型,极易引起误诊或漏诊。抗体类型的叠加可能导致AE症候群的叠加,而具有致病性的抗神经元细胞表面或突触抗体之间的叠加似乎引起的症状更重,合并副肿瘤性抗体时提示潜在的肿瘤相关性更大。双侧颞叶内侧受累被认为是AE的一个典型标志,但我们观察到合并多抗体阳性AE患者脑MRI大多不典型,病灶分布更广泛,尤其单侧病灶易与脑卒中、脑肿瘤混淆,可结合病史体征及磁共振波谱分析或灰白质差异性分析协助AE的诊断[12-14]。
本文还发现少数AE合并神经系统以外的其他自身免疫性抗体(26/255),如抗NMDAR抗体合并甲状腺抗体,或合并结缔组织病,既往有类似报道[15-16],均与自身免疫发生有关,但具体的产生机制及二者发生发展关系尚不明确,在疾病初期可能仅表现其中一种免疫病(如桥本脑病或干燥综合征),应注意随访观察是否发生演变出现自免脑炎,有一定的指导意义,有待进一步的大数据研究及观察。
本研究发现1例合并子宫肌瘤(例7),目前未见相关报道明确子宫肌瘤与AE的相关性,但有报道称抗Yo抗体阳性者合并妇科肿瘤或乳腺癌的比例占90%[17]。另有研究发现,抗NMDAR脑炎中94%为卵巢畸胎瘤,其余6%为卵巢外肿瘤,包括肺、乳腺、睾丸、子宫、胸腺和胰腺肿瘤[18],因此可认为该患者发生子宫肌瘤与上述两种抗体相关性较大,并非独立存在。据报道,肿瘤阴性及未应用二线免疫治疗的AE易复发[19-22],该类患者在确诊前仅给予对症治疗,复发后病灶范围较前增大,给予一线免疫治疗后好转未复发,考虑例7复发的影响因素可能与抗体叠加、合并肿瘤、未给予免疫治疗等相关。7例患者中共3例出现复发(3/7),仍需大量样本进一步验证复发率及影响因素是否与单抗体阳性AE有关。
本报道中7例患者具体治疗方案虽有差异,但经一线免疫治疗及对症治疗后好转率达71.4%(5/7),随访时患者的神经功能恢复情况采用改良Rankin评分(mRS)评估(mRS≤2分被定义为神经恢复良好功能状态)[2],其中5例患者mRS均≤2分,提示其功能恢复良好,免疫治疗有效。因此,针对多重抗体阳性AE者,临床表现虽复杂多样,仍然可采用常规AE的治疗原则,合并肿瘤者及早行肿瘤切除或其他抗肿瘤治疗,同时给予一线免疫治疗(糖皮质激素、IVIG和血浆置换),效差时可给予二线免疫治疗(利妥昔单抗、静脉用环磷酰胺),抗癫痫和精神障碍等对症治疗也是必要的。目前没有专门针对AE患者神经预后的评估量表,但临床中可采用改良Rankin评分(mRS)进行评估[23]。
因此,AE患者同时出现多种抗体阳性(抗神经元抗体或其他系统自身抗体)并非偶然,可能与患者本身存在自身免疫性有关,但引起这种现象发生的具体机制尚不能明确,仍需大量的临床观察总结及病理研究。抗体的叠加不仅体现在临床症状的叠加,其合并的肿瘤类型可能会更广泛,更边缘化。
合并多种抗体阳性的自身免疫性脑炎虽不多见,但具有一定的临床意义,可提示患癌率的增加及潜在合并的肿瘤类型,提高肿瘤筛查。因临床表现更加复杂多样,影像表现更不典型,增加了诊断、鉴别诊断及治疗的难度,可能会加重病情、增加复发率及病死率,定期复查随诊意义重大。本文报道的病例数较少,且为回顾性分析,具有一定的局限性,并不能全面概括这种现象的发生机制及意义,仍需进一步深入研究。

