培美曲塞或多西他赛联合卡铂治疗吉非替尼耐药的晚期肺腺癌患者的疗效
亓妍文,LALLOO M.B.IBRAHIM,王丽萍
1)郑州大学第一附属医院肿瘤中心 郑州450052 2)郑州大学第一附属医院生物细胞治疗中心 郑州450052
据2018年全球癌症统计,肺癌是最常见的癌症类型,占所有癌症现患病例的11.6%,是癌症死亡的主要原因,占癌症死亡总数的18.4%[1]。在我国肺癌亦是最常见的恶性肿瘤之一,它的发病率和死亡率迅速上升,已成为我国首要的癌症死因[2]。对2005年至2014年间我国8个省份7 184例原发性肺癌的研究[3]发现,肺腺癌患者的比例显著上升(从36.4%上升至53.5%),肺鳞癌患者的比例显著下降(从45.4%下降至34.4%)。研究[4]发现EGFR基因在晚期肺腺癌中的突变率为51.0%,EGFR突变阳性的肺腺癌患者口服靶向药物治疗,有效率高达80%,无进展生存期达10~14个月[5-6]。靶向药物如吉非替尼治疗失败后,对晚期肺腺癌通常进行化疗,在化疗的选择上既要考虑到疗效,也要考虑到药物的毒副作用。为进一步研究吉非替尼耐药的晚期肺腺癌患者化疗的疗效和安全性,本研究收集了郑州大学第一附属医院收治的、分别使用培美曲塞或多西他赛联合卡铂治疗的吉非替尼耐药的晚期肺腺癌患者的临床资料,比较了这两种化疗方案的疗效和安全性。
1 对象与方法
1.1研究对象选取2015年4月至2018年9月郑州大学第一附属医院收治的、病理诊断明确、病历资料完整、临床分期为Ⅲ~Ⅳ期、吉非替尼耐药的晚期肺腺癌患者,此前均未进行过化疗。患者均至少有一个CT可测量病灶,ECOG评分0~2分,预计生存期≥3个月,KPS评分≥60分。按上述标准共纳入56例,28例在吉非替尼治疗失败后采用多西他赛联合卡铂化疗方案(多西他赛组),28例在吉非替尼治疗失败后采用培美曲塞联合卡铂化疗方案(培美曲塞组)。多西他赛组患者32~69(54.7±8.5)岁,培美曲塞组患者42~77(57.9±9.4)岁。2组患者在性别、>60岁患者比例、吸烟史、EGFR突变类型、临床分期和ECOG评分等方面差异均无统计学意义,见表1。
1.2治疗方法多西他赛组:多西他赛75 mg/m2静脉滴注,第1天;卡铂400 mg/m2静脉滴注,第2天;在开始化疗之前均给予地塞米松预处理。21 d为1个周期。培美曲塞组:培美曲塞500 mg/m2静脉滴注,第1天;卡铂400 mg/m2静脉滴注,第2天;在开始化疗之前给予地塞米松、叶酸、维生素B12预处理。21 d为1个周期。所有患者每个化疗周期前均行血常规、肝肾功能、心功能等常规检查,以排除化疗禁忌证,并在化疗前常规应用保护胃黏膜、预防性止吐、抗过敏药物,有骨转移者每月给予唑来磷酸4 mg静脉滴注。化疗中出现骨髓抑制、消化道症状时对症处理。每治疗2个周期行影像学检查(CT、彩超,有骨转移者行骨扫描,有脑转移者行头颅MRI)评价疗效。
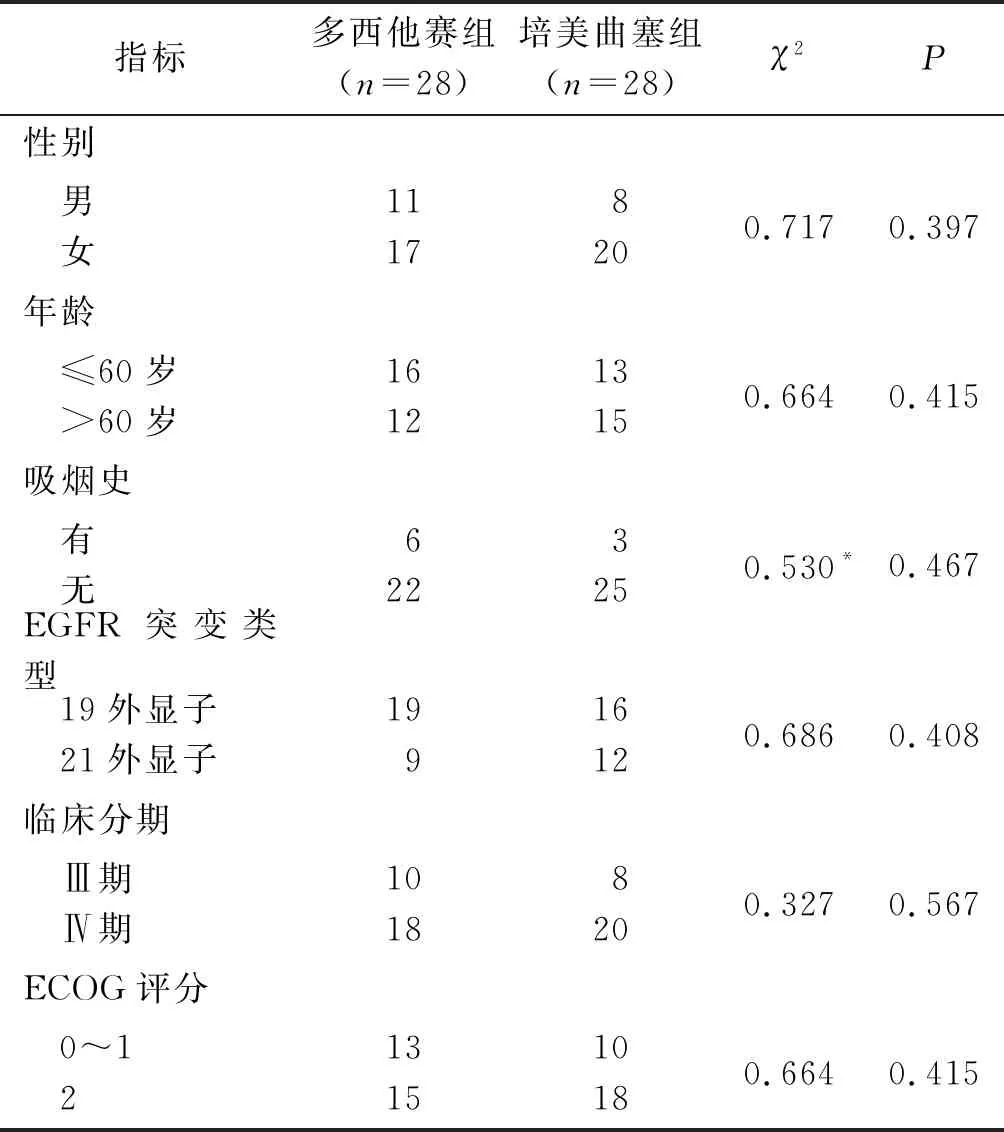
表1 2组患者一般资料的比较 例
*:校正χ2检验
1.3疗效评价2个周期化疗后根据实体瘤疗效评价标准(RECIST 1.1)评定近期疗效,分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、疾病进展(PD),治疗有效率(RR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。无进展生存时间(PFS)为自治疗开始到患者肿瘤病灶出现进展的时间,总生存时间(OS)为自治疗开始到任何原因致患者死亡的时间。不良反应采取WHO化疗毒副作用分级标准( 0~Ⅳ级)进行评价,Ⅲ、Ⅳ度不良反应为重度不良反应。疗效评价为CR、PR、SD的患者可继续原方案化疗,疗效评价为PD的患者则终止该方案化疗。对疗效评价为CR、PR及SD的患者进行随访,截止时间为2019年1月,随访期间无失访病例。
1.4统计学处理采用SPSS 22.0处理数据。采用χ2检验比较2组患者的一般资料及重度不良反应发生情况,采用秩和检验比较2组患者近期疗效,采用Kaplan-Meier法绘制生存曲线并行log-rank检验。检验水准α=0.05。
2 结果
2.1近期疗效比较2组均无CR患者。多西他赛组PR 9例,SD 12例,PD 7例,培美曲塞组PR 6例,
SD 17例,PD 5例,2组近期疗效相比,差异无统计学意义(Z=1.409,P=0.159)。多西他赛组和培美曲塞组的RR分别为32.1%和21.4%,差异无统计学意义(χ2=0.820,P=0.365),DCR分别为75.0%和82.1%,差异无统计学意义(χ2=0.641,P=0.423)。
2.2远期疗效比较2组PFS生存曲线差异无统计学意义(χ2=1.696,P=0.193),见图1。培美曲塞组中位PFS为5.50个月,95%CI为3.69~7.32个月,多西他赛组中位PFS为4.20个月,95%CI为2.26~6.15个月。2组OS生存曲线差异无统计学意义(χ2=0.804,P=0.370),见图2。培美曲塞组中位OS为10.40个月,95%CI为6.77~14.03个月,多西他赛组中位OS为9.40个月,95%CI为7.20~11.60个月。
2.3不良反应2组患者常见的不良反应为白细胞减少、中性粒细胞减少、血红蛋白减少、血小板减少、恶心呕吐、便秘、疼痛等。培美曲塞组Ⅲ、Ⅳ度白细胞减少、中性粒细胞减少、血小板减少、恶心呕吐的发生率低于多西他赛组,其他差异无统计学意义(表2)。
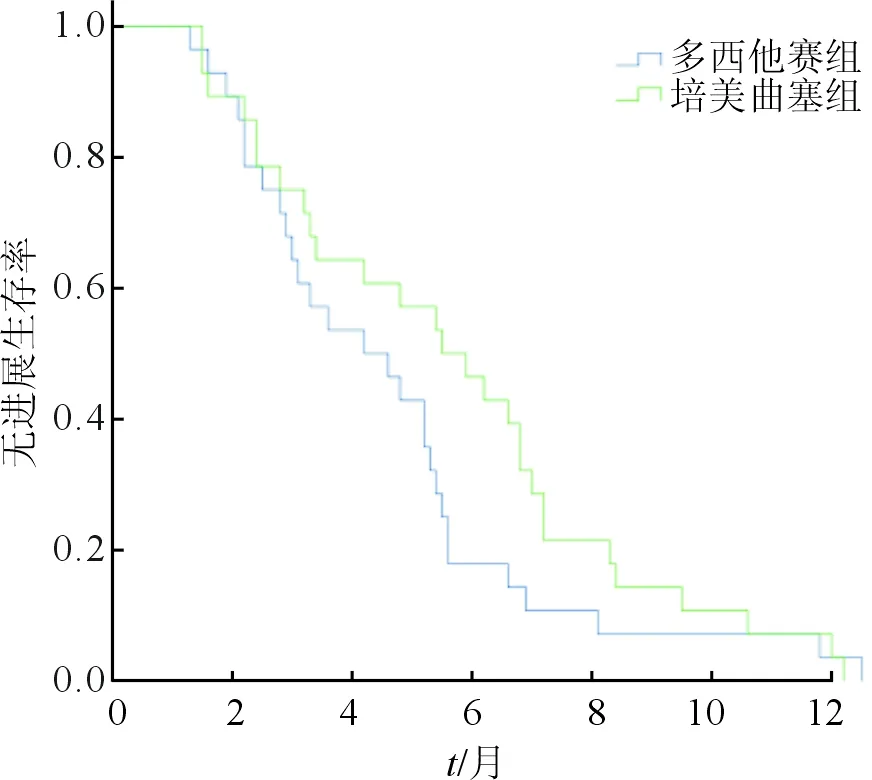
图1 2组晚期肺腺癌患者PFS生存曲线
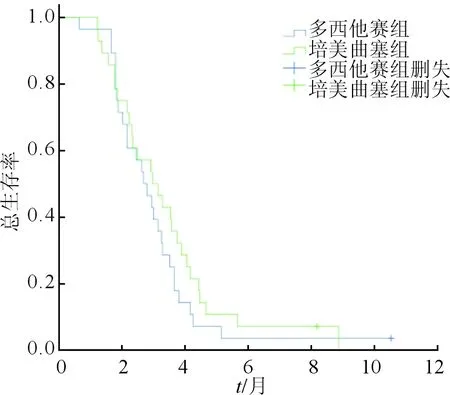
图2 2组晚期肺腺癌患者OS生存曲线
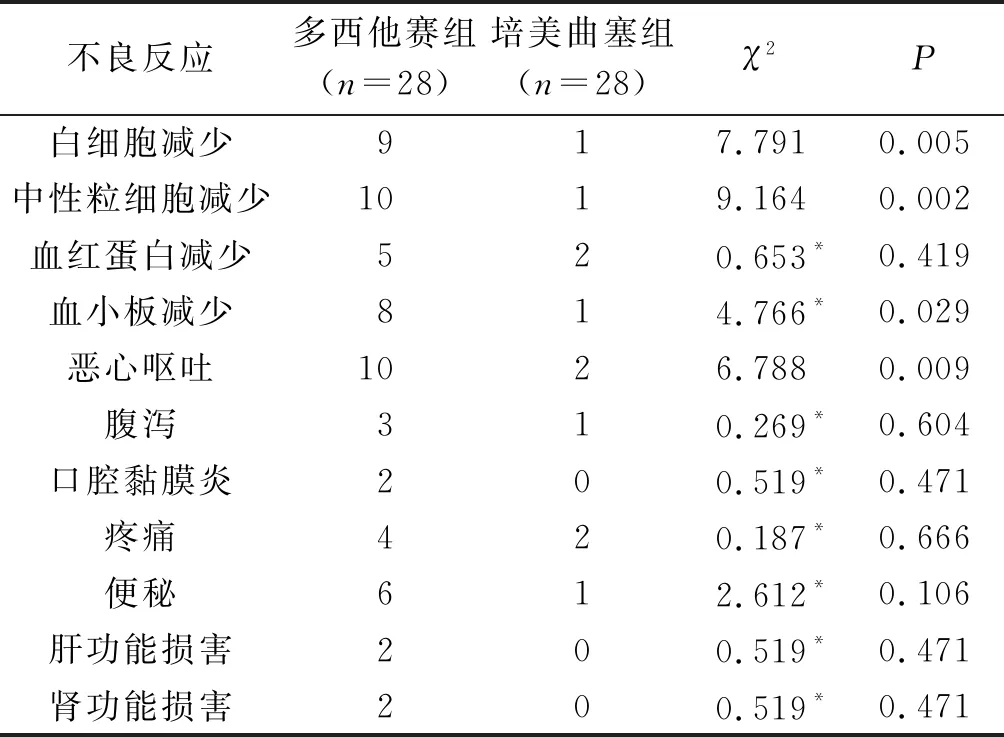
表2 2组患者重度不良反应发生情况的比较 例
*:校正χ2检验
3 讨论
肺腺癌早期常无明显的临床症状,多数患者发现时已处于ⅢB期~Ⅳ期,失去了手术根治的机会,部分患者已出现远处转移,预后较差,因此如何更好地提高晚期肺腺癌患者的生存质量、延长生存时间是一个亟待解决的问题。随着肺腺癌基因突变类型的挖掘和分子靶向药物的研发,肺腺癌的治疗已达到基因亚型指导下个体化用药的新阶段,其中最常用的是表皮生长因子受体酪氨酸激酶抑制剂,代表药物是吉非替尼。靶向药物具有定位精准、服用方便和毒副作用小的优点,但也容易发生耐药。在靶向药物治疗失败后,临床对于晚期肺腺癌患者采取的治疗方法主要是化疗。
培美曲塞是一种新型多靶点叶酸拮抗剂,能同时阻断胸苷酸合成酶、二氢叶酸还原酶和甘氨酸核糖核苷甲酰基转移酶等多种叶酸代谢所必需的酶,可使肿瘤细胞的嘌呤和嘧啶合成受阻,进而影响细胞DNA和RNA的合成,最终使肿瘤细胞的增殖停滞,因而具有抗肿瘤作用[7]。研究[8-9]表明非小细胞肺癌患者对单药培美曲塞维持治疗耐受性较好,除了食欲略有减退外,生存质量基本不受影响;该治疗方案能显著延缓疼痛和咯血的恶化,减少支持性护理,且能延长患者的PFS和OS。多西他赛是一种半合成的紫杉醇类药物,通过促进微管蛋白聚合成稳定的微管并抑制微管解聚,破坏细胞的有丝分裂,从而起到抗肿瘤作用[10-11]。研究[12]表明多西他赛治疗能显著延长非小细胞肺癌患者的生存期。
有研究[13-14]发现培美曲塞或多西他赛治疗非小细胞肺癌患者的疗效相近。张敬伟等[15]对EGFR基因突变的非小细胞肺癌靶向治疗失败的患者,分别进行最佳支持治疗、单药化疗(多西他赛或培美曲塞)和多西他赛或培美曲塞联合铂类化疗,结果发现联合化疗组的中位PFS和OS较最佳支持治疗、培美曲塞单药化疗或多西他赛单药化疗延长,可见联合化疗的效果要优于单药化疗。本研究结果显示,多西他赛联合卡铂和培美曲塞联合卡铂治疗晚期肺腺癌的近远期疗效相当,前者的中位PFS和OS分别为4.20和9.40个月,后者为5.50和10.40个月。该研究结果与一项随机多中心平行开放的临床试验[16]结果一致。文献[16]的结果还显示,培美曲塞的毒副作用相对较轻,能降低骨髓抑制和消化道不良反应的发生。本研究中,2组常见的不良反应均为胃肠道反应和血液学毒性,但培美曲塞组Ⅲ~Ⅳ度白细胞减少、中性粒细胞减少、血小板减少、恶心呕吐的发生率均低于多西他赛组,因此认为培美曲塞联合卡铂治疗晚期肺腺癌疗效好,安全性相对较高,不良反应相对轻微,患者更易于接受。

